1 . 在抗击新冠肺炎疫情的战役中,84消毒液发挥着重要作用。实验小组对其进行研究。
【查阅资料】
①84消毒液的有效成分为次氯酸钠(NaClO),有效含氯量5.5%-6.5%;NaClO溶液呈碱性。
②消毒杀菌的原理是使菌体蛋白质变性,变性程度越大,消毒液消毒杀菌效果越好。鸡蛋清中的蛋白质发生变性反应时变为白色固体物质。
②ORP指84消毒液的漂白能力,ORP数值越大,84消毒液的漂白能力越强。
Ⅰ.制备84消毒液的有效成分NaClO
工业上能以食盐为原料制得次氯酸钠,其工业流程如图所示:
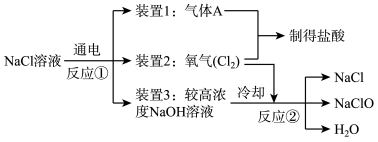
(1)装置1必须保证气密性良好并在其周围严禁明火,其原因是___ 。
(2)写出反应②的化学方程式___ 。
Ⅱ.探究84消毒液
实验1:在鸡蛋清中加入不同浓度的消毒液,静置15min现象如表:
实验2:探究84消毒液漂白性的影响因素:
【解释与结论】
(3)实验1的目的是___ 。
(4)实验2得出影响84消毒液失效的因素是___ 。
【反思与评价】
(5)生活中,84消毒液不能与洁厕灵(主要成分是盐酸)混合使用的原因是___ 。
Ⅲ.定量检测某品牌84消毒液中NaClO含量
依据原理:2HCl(浓)+NaClO═NaCl+Cl2↑+H2O
已知:①氯气的密度为3.17g/L;
②氯气可溶于水,且会与水反应,但基本不溶于饱和食盐水。
③氯化氢气体极易溶于水。
实验探究:测“84消毒液”样品中NaClO的质量分数。(不考虑消毒液中NaClO以外的物质与浓盐酸反应)
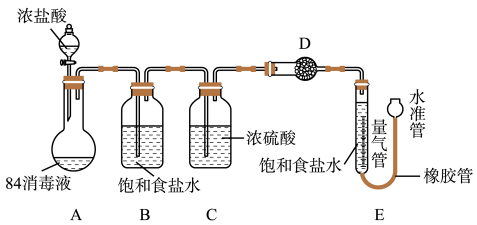
实验过程:
①连接装置并检查气密性;②准确称量10g“84消毒液”样品;③装药品,调节量气装置两边液面相平,读数;④加入浓盐酸,当不再有气体生成;⑤冷却到室温;⑥,读取量气管数值224mL。
(6)补全步骤⑥中的操作___ 。
(7)装置B的作用是___ ,D中的试剂是___ (填字母序号)。
a.碱石灰
b.浓硫酸
c.硫酸铜
(8)若其它操作均正确,仅因下列因素可使样品中NaClO的质量分数的测定结果偏小的是___ (填字母序号)。
a.反应前量气管水面到0刻度处,反应后仰视读数
b.装置A中仍有气泡就停止实验进行测量气体的体积
c.量气管中的食盐水不饱和
【查阅资料】
①84消毒液的有效成分为次氯酸钠(NaClO),有效含氯量5.5%-6.5%;NaClO溶液呈碱性。
②消毒杀菌的原理是使菌体蛋白质变性,变性程度越大,消毒液消毒杀菌效果越好。鸡蛋清中的蛋白质发生变性反应时变为白色固体物质。
②ORP指84消毒液的漂白能力,ORP数值越大,84消毒液的漂白能力越强。
Ⅰ.制备84消毒液的有效成分NaClO
工业上能以食盐为原料制得次氯酸钠,其工业流程如图所示:

(1)装置1必须保证气密性良好并在其周围严禁明火,其原因是
(2)写出反应②的化学方程式
Ⅱ.探究84消毒液
实验1:在鸡蛋清中加入不同浓度的消毒液,静置15min现象如表:
| 序号 | 1-1 | 1-2 | 1-3 | 1-4 |
| 实验操作 | 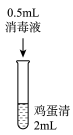 | 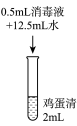 | 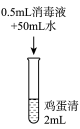 |  |
| 实验现象 | 实验液体表面产生大量气泡,无其他现象 | 液体中产生大量白色固体 | 液体中产生少量白色固体 | 液体中产生极少量白色固体 |
| 序号 | 2-1 | 2-2 |
| 实验操作 | 取烧杯倒入30mL浓度为1:100的84消毒液,将烧杯放置在距离光源10cm处进行光照,测量ORP变化 | 取四个烧杯,分别倒入30mL浓度为1:100的84消毒液,并置于20℃、30℃、40℃、50℃水溶中加热,测量ORP变化 |
| 测量数据 | 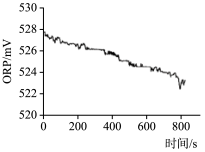 | 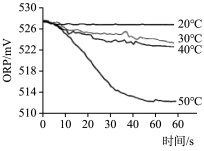 |
(3)实验1的目的是
(4)实验2得出影响84消毒液失效的因素是
【反思与评价】
(5)生活中,84消毒液不能与洁厕灵(主要成分是盐酸)混合使用的原因是
Ⅲ.定量检测某品牌84消毒液中NaClO含量
依据原理:2HCl(浓)+NaClO═NaCl+Cl2↑+H2O
已知:①氯气的密度为3.17g/L;
②氯气可溶于水,且会与水反应,但基本不溶于饱和食盐水。
③氯化氢气体极易溶于水。
实验探究:测“84消毒液”样品中NaClO的质量分数。(不考虑消毒液中NaClO以外的物质与浓盐酸反应)

实验过程:
①连接装置并检查气密性;②准确称量10g“84消毒液”样品;③装药品,调节量气装置两边液面相平,读数;④加入浓盐酸,当不再有气体生成;⑤冷却到室温;⑥,读取量气管数值224mL。
(6)补全步骤⑥中的操作
(7)装置B的作用是
a.碱石灰
b.浓硫酸
c.硫酸铜
(8)若其它操作均正确,仅因下列因素可使样品中NaClO的质量分数的测定结果偏小的是
a.反应前量气管水面到0刻度处,反应后仰视读数
b.装置A中仍有气泡就停止实验进行测量气体的体积
c.量气管中的食盐水不饱和
您最近一年使用:0次
名校
解题方法
2 . 氮化钙有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域。某化学兴趣小组设计制备氮化钙并测定其纯度的实验如下:
已知:氮化钙(Ca3N2)是一种棕色粉末,遇水会发生水解,生成氢氧化钙并放出氨。
I.氮化钙的制备(如图):

(1)仪器a的名称是_______ 。
(2)装置A中每生成标准状况下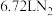 ,转移的电子数为
,转移的电子数为_______ 。
(3)装置C的作用是吸收氧气,则C中发生反应的离子方程式为_______ 。
(4)设计实验证明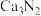 中混有钙单质,写出实验操作及现象:
中混有钙单质,写出实验操作及现象:_______ 。
II.测定氮化钙的纯度:
(5)甲同学称取mg反应后的固体,加入足量的碳酸钠溶液充分反应,过滤、洗涤、干燥得ng沉淀,通过数据m、n即可求得氮化钙的质量分数。
甲同学的方案是否合理?_______ (填“是”或“否”),理由是_______ 。
(6)乙同学的方案如下:
取氮化钙样品24g,按图所示装置进行实验,发现B装置增重5.1g。
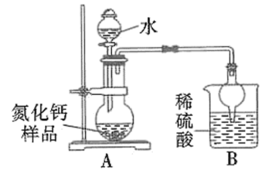
①该样品中氮化钙的质量分数为_______ 。
②导致该样品中氮化钙含量测定结果偏低的可能原因是_______ 。
已知:氮化钙(Ca3N2)是一种棕色粉末,遇水会发生水解,生成氢氧化钙并放出氨。
I.氮化钙的制备(如图):

(1)仪器a的名称是
(2)装置A中每生成标准状况下
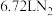 ,转移的电子数为
,转移的电子数为(3)装置C的作用是吸收氧气,则C中发生反应的离子方程式为
(4)设计实验证明
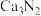 中混有钙单质,写出实验操作及现象:
中混有钙单质,写出实验操作及现象:II.测定氮化钙的纯度:
(5)甲同学称取mg反应后的固体,加入足量的碳酸钠溶液充分反应,过滤、洗涤、干燥得ng沉淀,通过数据m、n即可求得氮化钙的质量分数。
甲同学的方案是否合理?
(6)乙同学的方案如下:
取氮化钙样品24g,按图所示装置进行实验,发现B装置增重5.1g。

①该样品中氮化钙的质量分数为
②导致该样品中氮化钙含量测定结果偏低的可能原因是
您最近一年使用:0次
2021-09-16更新
|
255次组卷
|
3卷引用:内蒙古海拉尔第二中学2021-2022学年高三上学期第一次阶段考化学试题
3 . 如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
(1)该浓盐酸中HCl的物质的量浓度为________________ mol.L-1。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是_______________(填字母)。
(3)某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.400mol.L-1的稀盐酸。
①该学生需要量取_______________ mL上述浓盐酸进行配制。
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在括号内填A表示“偏大”、填B表示“偏小”、填C表示“无影响”)。
a.用量筒量取浓盐酸时俯视观察凹液面________
b定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水________
(4)①假设该同学成功配制了0.400mol.L-1的盐酸,他又用该盐酸中和含0.4gNaOH的NaOH溶液,则该同学需取_______________ mL盐酸。
②假设该同学用新配制的盐酸中和含0.4 g NaOH的NaOH溶液,发现比①中所求体积偏小,则可能的原因是_______________ 。(填字母)
A.浓盐酸挥发,浓度不足
B.配制溶液时,未洗涤烧杯
C.配制溶液时,俯视容量瓶刻度线
D.加水时超过刻度线,用胶头滴管吸出
| 盐酸 分子式:HCl 相对分子质量:36.5 密度:1.19g.cm-3 HCl的质量分数:36.5% |
(1)该浓盐酸中HCl的物质的量浓度为
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是_______________(填字母)。
| A.溶液中HCl的物质的量 | B.溶液的物质的量浓度 |
| C.溶液中Cl-的数目 | D.溶液的密度 |
(3)某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.400mol.L-1的稀盐酸。
①该学生需要量取
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在括号内填A表示“偏大”、填B表示“偏小”、填C表示“无影响”)。
a.用量筒量取浓盐酸时俯视观察凹液面
b定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
(4)①假设该同学成功配制了0.400mol.L-1的盐酸,他又用该盐酸中和含0.4gNaOH的NaOH溶液,则该同学需取
②假设该同学用新配制的盐酸中和含0.4 g NaOH的NaOH溶液,发现比①中所求体积偏小,则可能的原因是
A.浓盐酸挥发,浓度不足
B.配制溶液时,未洗涤烧杯
C.配制溶液时,俯视容量瓶刻度线
D.加水时超过刻度线,用胶头滴管吸出
您最近一年使用:0次
2024-01-07更新
|
20次组卷
|
2卷引用:内蒙古自治区赤峰四中2021-2022学年高一上学期第一次月考化学试题
4 . 将下列物质:①0.78gNa2O2、②0.62gNa2O、③0.23g金属钠、④0.4gNaOH,分别加入盛有100mL蒸馏水的四个烧杯中,待固体完全溶解,则烧杯中溶液的质量分数的大小顺序是
| A.①>②>③>④ | B.①>②>④>③ |
| C.①=②>③>④ | D.①=②>③=④ |
您最近一年使用:0次
解题方法
5 . 84消毒液是一种以NaClO为主的高效消毒剂,被广泛用于宾馆、旅游、医院、食品加工行业、家庭等的卫生消毒,某84消毒液瓶体部分标签如图所示,该84消毒液通常稀释100倍(体积之比)后使用,请回答下列问题:
(1)某同学量取100mL此84消毒液,按说明要求稀释后用于消毒,则稀释后的溶液中c(NaClO)=_______ mol·L-1。
(2)某化学实验小组欲用NaClO固体配制含25%NaClO的消毒液480mL。
①计算配制此溶液需称取NaClO固体的质量为_______ g。
②如图所示的仪器中配制溶液需要使用的是_______ (填字母),还缺少的玻璃仪器是_______ 。

(3)配制时,一般可分为以下几个步骤:①称量②计算③溶解④摇匀⑤移液⑥洗涤⑦定容⑧冷却。正确的操作顺序是_______
(4)若实验遇下列情况,导致所配溶液的物质的量浓度偏高的是_______(填字母)。
| 84消毒液 【有效成分】NaClO 【规格】1000mL 【质量分数】25% 【密度】1.192g·cm-3 【使用方法】稀释100倍(体积比)后使用 |
(2)某化学实验小组欲用NaClO固体配制含25%NaClO的消毒液480mL。
①计算配制此溶液需称取NaClO固体的质量为
②如图所示的仪器中配制溶液需要使用的是

(3)配制时,一般可分为以下几个步骤:①称量②计算③溶解④摇匀⑤移液⑥洗涤⑦定容⑧冷却。正确的操作顺序是
(4)若实验遇下列情况,导致所配溶液的物质的量浓度偏高的是_______(填字母)。
| A.定容时俯视刻度线 | B.转移前,容量瓶内有蒸馏水 |
| C.未冷却至室温就转移定容 | D.定容时水加多了用胶头滴管吸出 |
您最近一年使用:0次
名校
解题方法
6 . 掌握仪器的名称、组装及使用方法是中学化学实验的基础,如图为两套实验装置。
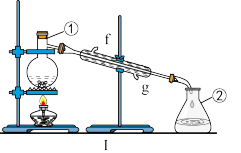
(1)写出仪器的名称:①_______ 。
(2)若利用装置Ⅰ分离四氯化碳和酒精的混合物,还缺少的仪器有_______ 。
(3)某校环保兴趣小组在处理污水样品时,需用质量分数为37%、密度为1.19 g/cm3的浓盐酸配制成250 mL 0.1 mol/L的稀盐酸。装置Ⅱ是某同学转移溶液的示意图,图Ⅱ中的错误是_______ 。
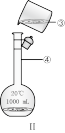
①盛放浓盐酸的试剂瓶标签上应印有图中警示标识中的_______ 。(填序号)。
A. B.
B.  C.
C. D.
D.
②在如图所示仪器中,配制上述溶液不需要的是_______ (填图中相应仪器的序号)。
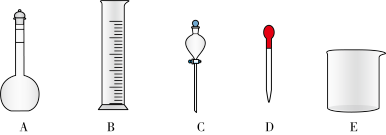
③根据计算,本实验需要量取浓盐酸的体积为_______ mL,本实验应使用的量筒_______ (填序号)。
A.10ml B.100ml C.250ml D.500ml
④在容量瓶的使用方法中,下列操作正确的是_____ (填序号)。
A.使用容量瓶前检查是否漏水
B.容量瓶用水洗净后,再用配好的稀HCl溶液润洗
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加水至接近刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线
D.配制溶液时,若试样是液体,用量筒取试样后直接倒入容量瓶中,缓慢加水至接近刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住容量瓶底部,反复倒转多次,摇匀
⑤假设配制时其他操作均正确,只出现以下某一情况,试判断对所配制的溶液浓度的影响(相比于要求的值,即0.1 mol/L,填“偏高”“偏低”或“无影响”)。
A.容量瓶中有少量蒸馏水:_______ ;
B.稀释浓盐酸时,没有冷却就立即转移到容量瓶中:_______ ;
C.配制的溶液装入洁净的但有少量蒸馏水的试剂瓶中:_______ ;
D.定容时俯视:_______ 。

(1)写出仪器的名称:①
(2)若利用装置Ⅰ分离四氯化碳和酒精的混合物,还缺少的仪器有
(3)某校环保兴趣小组在处理污水样品时,需用质量分数为37%、密度为1.19 g/cm3的浓盐酸配制成250 mL 0.1 mol/L的稀盐酸。装置Ⅱ是某同学转移溶液的示意图,图Ⅱ中的错误是

①盛放浓盐酸的试剂瓶标签上应印有图中警示标识中的
A.
 B.
B.  C.
C. D.
D.
②在如图所示仪器中,配制上述溶液不需要的是

③根据计算,本实验需要量取浓盐酸的体积为
A.10ml B.100ml C.250ml D.500ml
④在容量瓶的使用方法中,下列操作正确的是
A.使用容量瓶前检查是否漏水
B.容量瓶用水洗净后,再用配好的稀HCl溶液润洗
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加水至接近刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线
D.配制溶液时,若试样是液体,用量筒取试样后直接倒入容量瓶中,缓慢加水至接近刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住容量瓶底部,反复倒转多次,摇匀
⑤假设配制时其他操作均正确,只出现以下某一情况,试判断对所配制的溶液浓度的影响(相比于要求的值,即0.1 mol/L,填“偏高”“偏低”或“无影响”)。
A.容量瓶中有少量蒸馏水:
B.稀释浓盐酸时,没有冷却就立即转移到容量瓶中:
C.配制的溶液装入洁净的但有少量蒸馏水的试剂瓶中:
D.定容时俯视:
您最近一年使用:0次
2022-07-20更新
|
106次组卷
|
2卷引用:内蒙古包头市第四中学2021-2022学年高一上学期期中考试化学试题
名校
7 . I.某学习小组用如图所示装置测定铝镁合金中铝的质量分数和铝的相对原子质量。
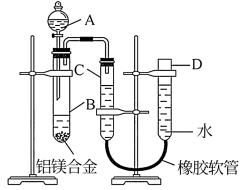
(1)A中试剂为___________ 。
(2)实验前,先将铝镁合金在稀酸中浸泡片刻,其目的是___________ 。
(3)B中发生反应的化学方程式为___________ 。
(4)若实验用的铝镁合金的质量为ag,测得氢气体积为bmL(已换算为标准状况),B中剩余固体的质量为cg,则铝的相对原子质量为___________ 。
(5)实验过程中,若未洗涤过滤所得的不溶物,则测得铝的质量分数将___________ (填“偏大”“偏小”或“不受影响”)。
II.某同学设计了如图装置(气密性已检查,部分夹持装置已省略)用于制备Fe(OH)2白色沉淀。

请回答下列问题。
(6)仪器1的名称是___________ 。装置5的作用是___________ 。
(7)实验开始时,关闭K2,打开K1,反应一段时间后,再打开K2,关闭K1,发现3中溶液不能进入4中。请为装置作一处改进,使3中溶液能进入4中:___________ 。
(8)装置改进后,将3中反应后的溶液压入4中,在4中析出了灰绿色沉淀。从实验操作过程分析没有产生白色沉淀的原因:___________ 。

(1)A中试剂为
(2)实验前,先将铝镁合金在稀酸中浸泡片刻,其目的是
(3)B中发生反应的化学方程式为
(4)若实验用的铝镁合金的质量为ag,测得氢气体积为bmL(已换算为标准状况),B中剩余固体的质量为cg,则铝的相对原子质量为
(5)实验过程中,若未洗涤过滤所得的不溶物,则测得铝的质量分数将
II.某同学设计了如图装置(气密性已检查,部分夹持装置已省略)用于制备Fe(OH)2白色沉淀。

请回答下列问题。
(6)仪器1的名称是
(7)实验开始时,关闭K2,打开K1,反应一段时间后,再打开K2,关闭K1,发现3中溶液不能进入4中。请为装置作一处改进,使3中溶液能进入4中:
(8)装置改进后,将3中反应后的溶液压入4中,在4中析出了灰绿色沉淀。从实验操作过程分析没有产生白色沉淀的原因:
您最近一年使用:0次
解题方法
8 . 氧化还原反应在生产、生活中具有广泛的用途,贯穿古今。
(1)水是人体的重要组成部分,是人体中含量最多的一种物质,而“四种基本反应类型与氧化还原反应的关系”也可用下图表达。
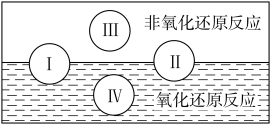
试写出有水参加的符合反应类型IV的一个离子反应方程式:________________ ,其中水为_____________ 剂;
(2)氯化铵常用于焊接。如在焊接铜器时用过量的浓氯化铵溶液除去铜器表面的氧化铜以便焊接,其反应为: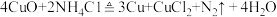
①该反应中,被氧化的元素是_____________ (填元素名称),氧化剂是_____________ (填化学式);
②往反应后的热溶液中加入过量澄清的石灰水,发现有气泡产生,写出该现象的离子方程式:_____________ ;
(3)铝热法是铝与某些金属氧化物反应获得高熔点金属单质的方法。工业上可用于制造无碳或低碳铁合金。铝粉和赤铁矿发生铝热反应的化学方程式为:
若反应中消耗了0.2 mol Al,生成Fe的物质的量为____________ mol,转移电子的物质的量为____________ mol。
(1)水是人体的重要组成部分,是人体中含量最多的一种物质,而“四种基本反应类型与氧化还原反应的关系”也可用下图表达。

试写出有水参加的符合反应类型IV的一个离子反应方程式:
(2)氯化铵常用于焊接。如在焊接铜器时用过量的浓氯化铵溶液除去铜器表面的氧化铜以便焊接,其反应为:
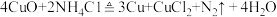
①该反应中,被氧化的元素是
②往反应后的热溶液中加入过量澄清的石灰水,发现有气泡产生,写出该现象的离子方程式:
(3)铝热法是铝与某些金属氧化物反应获得高熔点金属单质的方法。工业上可用于制造无碳或低碳铁合金。铝粉和赤铁矿发生铝热反应的化学方程式为:

若反应中消耗了0.2 mol Al,生成Fe的物质的量为
您最近一年使用:0次
名校
9 . 把5.1g镁铝合金的粉末放入过量的稀盐酸中,得到5.6L氢气(标准状况下)。试计算:
(1)该合金中铝的质量分数(保留一位小数)______
(2)该合金中镁和铝的物质的量之比为______
(1)该合金中铝的质量分数(保留一位小数)
(2)该合金中镁和铝的物质的量之比为
您最近一年使用:0次
2021-11-05更新
|
1051次组卷
|
10卷引用:内蒙古赤峰学院附属中学2020-2021学年高一上学期期末考试化学试题
内蒙古赤峰学院附属中学2020-2021学年高一上学期期末考试化学试题甘肃省兰州市第四片区2020-2021学年高一上学期期末考试化学试题福建省建瓯市芝华中学2020-2021学年高一下学期第一阶段考试化学试题上海实验高中2021-2022学年高一上学期第一次测试化学试题人教2019版必修第一册第三章 铁 金属材料复习与提高苏教2020版化学必修第二册专题9第三单元 金属材料的性能及应用课后习题上海市实验学校2021-2022学年高一上学期第一次测试化学试题云南民族大学附属中学2017-2018学年高一下学期期中考试化学试题广西钦州市第四中学2022-2023学年高一上学期11月份考试化学试题甘肃省兰州新华互联网学校2023-2024学年高一上学期期末考题化学试卷
解题方法
10 . 某厂为了测定一批Cu-Mg样品中铜的质量分数,取用10g样品,把200g稀盐酸分4次加入样品中(样品中除Cu-Mg外,其余的成分既不与盐酸反应,也不溶于水),充分反应后经过滤、干燥等操作,最后称量,得实验数据如表:
(1)该样品中铜的质量分数是___ 。
(2)计算该稀盐酸的溶质质量分数(写出计算过程,结果精确到0.1%)___ 。
| 稀盐酸的用量 | 第一次加入50g | 第二次加入50g | 第三次加入50g | 第四次加入50g |
| 剩余固体的质量 | 8.8g | 7.6g | 6.4g | 6.4g |
(2)计算该稀盐酸的溶质质量分数(写出计算过程,结果精确到0.1%)
您最近一年使用:0次



