名校
解题方法
1 . 如图是部分短周期元素化合价与原子序数的关系图,下列说法错误的是
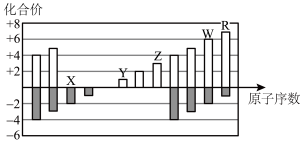

| A.由图可知并不是所有的元素的化合价都具有负价和正价 |
| B.原子半径最大的是Y |
| C.简单氢化物的稳定性:R>W |
| D.R的氧化物对应的水化物为强酸 |
您最近一年使用:0次
2024-03-09更新
|
227次组卷
|
2卷引用:广东省高州市某校2023-2024学年高一上学期期末模拟化学试题
名校
解题方法
2 . 化学与生产、生活密切相关,下列有关说法正确的是
| A.纯碱是用于治疗胃酸过多的一种药物 |
| B.工业上用氯气与冷的石灰乳反应可制得漂白粉 |
| C.食品包装袋中的小包铁粉用作干燥剂 |
| D.合金的特点是硬度比各成分金属小,熔点比各成分金属高 |
您最近一年使用:0次
2024-02-27更新
|
98次组卷
|
2卷引用:广东省高州市某校2023-2024学年高一上学期期末模拟化学试题
名校
3 . 学以致用是学习化学的动力和源泉,掌握化学知识有助于我们更好地认识世界。回答下列问题:
(1)云、雾属于胶体,鉴别胶体和溶液的方法是______ ,胶体和溶液的本质区别是_______ 。
(2)生铁是______ (填“混合物”或“化合物”)。通常合金的熔点_____ (填“高于”或“低于”)其组成单质的熔点。
(3)ClO2是一种新型含氯消毒剂,已经用于自来水消毒。实验室可通过以下反应制得: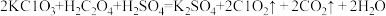 。产生1molC1O2时,转移电子的物质的量为
。产生1molC1O2时,转移电子的物质的量为______ mol;该反应中的还原剂是______ (填化学式)。
(4)在标准状况下,由CO2和CO组成的混合气体的密度是H2的19倍,则两者体积比V(CO2):V(CO)=____ 。
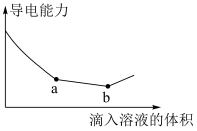
(5)Ba(OH)2溶液中滴入浓度相等的NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。从开始到a点总的离子方程式是______ ,从a点到b点反应的离子方程式是______ ,解释b点之后导电能力上升的原因:______ 。
(1)云、雾属于胶体,鉴别胶体和溶液的方法是
(2)生铁是
(3)ClO2是一种新型含氯消毒剂,已经用于自来水消毒。实验室可通过以下反应制得:
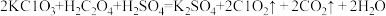 。产生1molC1O2时,转移电子的物质的量为
。产生1molC1O2时,转移电子的物质的量为(4)在标准状况下,由CO2和CO组成的混合气体的密度是H2的19倍,则两者体积比V(CO2):V(CO)=
(5)Ba(OH)2溶液中滴入浓度相等的NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。从开始到a点总的离子方程式是
您最近一年使用:0次
2024-01-28更新
|
109次组卷
|
4卷引用:广东省高州市某校2023-2024学年高一上学期期末模拟化学试题
名校
4 . 锂电池是目前应用广泛的新型电池,一种回收钴酸锂废旧电池(主要成分为LiCoO2,同时含有少量Fe、Al、C单质)的流程如下图所示。
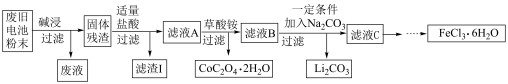
已知:Fe3+能与C2O 结合成[Fe(C2O4)3]3-,[Fe(C2O4)3]3-在强酸性环境下重新转化为Fe3+
结合成[Fe(C2O4)3]3-,[Fe(C2O4)3]3-在强酸性环境下重新转化为Fe3+
请回答下列问题:
(1)由滤液A制取CoC2O4·2H2O的过程发生的___________ (填“是”或“不是”)氧化还原反应,CoC2O4·2H2O中C的化合价为___________ ,滤渣I的主要成份为___________ 。
(2)用过量的NaOH溶液进行“碱浸”,“碱浸”的目的是___________ 。
写出该过程发生的化学反应方程式___________ 。
(3)加入适量盐酸,LiCoO2溶解后生成的Co3+能将Fe2+氧化为Fe3+,请写出该反应的离子方程式___________ 。
(4)请设计实验方案检验滤液C中的Cl-。___________
(5)高铁酸钠(Na2FeO4 ,其中铁为+6价)是一种高效多功能水处理剂。工业上用次氯酸钠和氯化铁为原料来制取高铁酸钠,该反应的离子方程式为:_________
___________ClO- +___________Fe3++___________=___________FeO +___________Cl- +___________H2O,请配平该方程式。
+___________Cl- +___________H2O,请配平该方程式。

已知:Fe3+能与C2O
 结合成[Fe(C2O4)3]3-,[Fe(C2O4)3]3-在强酸性环境下重新转化为Fe3+
结合成[Fe(C2O4)3]3-,[Fe(C2O4)3]3-在强酸性环境下重新转化为Fe3+请回答下列问题:
(1)由滤液A制取CoC2O4·2H2O的过程发生的
(2)用过量的NaOH溶液进行“碱浸”,“碱浸”的目的是
写出该过程发生的化学反应方程式
(3)加入适量盐酸,LiCoO2溶解后生成的Co3+能将Fe2+氧化为Fe3+,请写出该反应的离子方程式
(4)请设计实验方案检验滤液C中的Cl-。
(5)高铁酸钠(Na2FeO4 ,其中铁为+6价)是一种高效多功能水处理剂。工业上用次氯酸钠和氯化铁为原料来制取高铁酸钠,该反应的离子方程式为:
___________ClO- +___________Fe3++___________=___________FeO
 +___________Cl- +___________H2O,请配平该方程式。
+___________Cl- +___________H2O,请配平该方程式。
您最近一年使用:0次
2024-01-16更新
|
257次组卷
|
3卷引用:广东省茂名市七校2023-2024学年高一上学期12月联考化学试题
5 . A~G为中学化学中常见的物质,转化关系如图所示,反应①为常温下的反应,A、C、D中均含有氯元素,且A中氯元素的化合价介于C和D中氯元素的化合价之间,C是常用的调味剂。E在常温下为无色无味的液体,F是淡黄色固体,G为常见的无色气体。请据图回答下列问题:
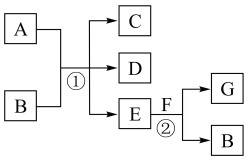
(1)B的化学式___________ ,它的摩尔质量为___________ 。
(2)标况下,等质量的A和G,其分子数之比为:___________ 。
(3)D在水溶液中的电离方程式为___________ 。
(4)F中阴阳离子个数比为:___________ , F可用于呼吸面具和潜水艇中,作为供氧剂,请分析原因___________ 。
(5)请写出反应①的离子反应方程式___________ 。
(6)将B的溶液滴入FeCl2溶液中,先产生白色絮状沉淀,沉淀迅速变为灰绿色,最终变为红褐色,该过程中发生的氧化还原反应的化学方程式为___________ 。

(1)B的化学式
(2)标况下,等质量的A和G,其分子数之比为:
(3)D在水溶液中的电离方程式为
(4)F中阴阳离子个数比为:
(5)请写出反应①的离子反应方程式
(6)将B的溶液滴入FeCl2溶液中,先产生白色絮状沉淀,沉淀迅速变为灰绿色,最终变为红褐色,该过程中发生的氧化还原反应的化学方程式为
您最近一年使用:0次
2024-01-16更新
|
73次组卷
|
2卷引用:广东省茂名市七校2023-2024学年高一上学期12月联考化学试题
6 . 1943年我国化学工程专家侯德榜发明了侯氏制碱法,又称联合制碱法,为我国化工事业的发展做出了卓越贡献。其部分工艺流程如下:
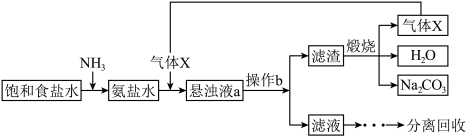
| A.调换气体X与NH3的加入顺序,对产品的产率没有影响 |
| B.操作b为过滤,需要用到的玻璃仪器有:长颈漏斗、烧杯、玻璃棒 |
| C.悬浊液a中的不溶物主要是NaHCO3 |
| D.滤液中只有NH4Cl,可直接做氮肥 |
您最近一年使用:0次
2024-01-16更新
|
149次组卷
|
3卷引用:广东省茂名市七校2023-2024学年高一上学期12月联考化学试题
名校
解题方法
7 . 几种短周期主族元素的原子半径及化合价见下表,下列说法正确的是
| 元素代号 | A | B | C | D | E | F |
| 化合价 | -2 | +4.-4 | -1 | +5.-3 | +3 | +1 |
| 原子半径/nm | 0.074 | 0.077 | 0.099 | 0.110 | 0.143 | 0.186 |
| A.A元素为氧元素,F元素为钾元素 |
| B.A元素与F元素形成的化合物中只含有共价键 |
| C.C、D的简单离子半径由大到小的顺序是C>D |
D.由上表信息可推测氮元素的原子半径:0.074nm 0.077nm 0.077nm |
您最近一年使用:0次
2024-01-13更新
|
266次组卷
|
5卷引用:广东省高州市某校2023-2024学年高一上学期期末模拟化学试题
解题方法
8 . 下列离子方程式中正确的是
A.将稀硫酸滴在铁片上: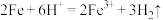 |
B.将氢氧化钡溶液与稀硫酸混合: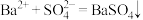 |
C.向氢氧化铜中加入稀硫酸: |
D.钠和水反应: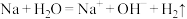 |
您最近一年使用:0次
2023-11-10更新
|
495次组卷
|
9卷引用:广东省茂名市七迳中学2023-2024学年高一上学期期中考试化学试卷
广东省茂名市七迳中学2023-2024学年高一上学期期中考试化学试卷四川省雅安市2023-2024学年高一上学期期中考试化学试题山西省部分学校2023-2024学年高一上学期11月期中联合考试化学试题广东省湛江市2023-2024学年高一上学期11月期中考试化学试题四川省名校联考2023-2024学年高一上学期11月期中考试化学试题辽宁省铁岭市一般高中协作校2023-2024学年高三上学期期中考试化学试题辽宁省葫芦岛市协作校2023-2024学年高一上学期第二次考试化学试题广东省深圳市龙华区2023-2024学年高一上学期1月期末联考化学试题四川省眉山北外附属东坡外国语学校2023-2024学年高一下学期开学化学试题
名校
解题方法
9 . 下列表示氧化还原反应中电子转移的方向和数目正确的是
A.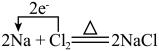 | B.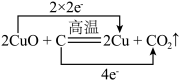 |
C.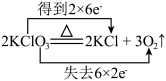 | D.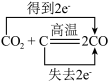 |
您最近一年使用:0次
2023-10-19更新
|
253次组卷
|
44卷引用:广东省茂名市化州市第一中学2023-2024学年高一上学期期中测评化学试题
广东省茂名市化州市第一中学2023-2024学年高一上学期期中测评化学试题四川省南充市西华师范大学附属中学2022-2023学年高一上学期期末考试化学试题湖南省永州市第一中学2022-2023学年高一上学期期末阶段性考试化学试题新疆巴音郭楞蒙古自治州第二中学2022-2023学年高一上学期期末考试化学试题黑龙江省哈尔滨市第三中学校 2023-2024 学年高一上学期第一次验收考试化学试题陕西省西安中学2023-2024学年高一上学期第一次月考化学试题四川省德阳市什邡中学2023-2024学年高一上学期10月月考(平行实验班)化学试题浙江省宁波三锋教研联盟2023-2024学年高一上学期期中联考化学试题甘肃省天水市2023-2024学年高一上学期10月份化学竞赛试卷 广东省江门市江海区外海中学2023-2024学年高一上学期期中考试化学试题重庆市复旦中学2020-2021学度高一上学期第一次段考化学试题四川省南充市2020-2021学年高一上学期期末考试化学试题贵州省贵阳市清镇养正学校2020-2021学年高一上学期期中考试化学试题四川省成都邛崃市高埂中学2020-2021学年高一下学期开学考试化学试题河北省藁城新冀明中学2020-2021学年高一上学期10月月考化学试题四川省广安市武胜烈面中学校2020-2021学年高一下学期开学考试化学试题河南省洛阳市第一高级中学2021-2022学年高一上学期9月月考化学试题山西省芮城中学2021-2022学年高一上学期阶段性月考化学试题新疆阿勒泰地区第二高级中学2021-2022学年高一上学期10月月考化学试题黑龙江省明水县第一中学2021-2022学年上学期高一10月月考化学试题四川省内江市第一中学2021-2022学年高一上学期期中考试化学试题重庆复旦中学2021-2022学年高一上学期期中考试化学试题天津市西青区杨柳青第一中学2021-2022年高一上学期期中考试化学试题黑龙江省哈尔滨市第三十二中学校2021-2022学年高一上学期期中考试化学试题四川省资阳市2021-2022学年高一上学期期末考试化学试题重庆市清华中学校2021—2022学年高一上学期10月月考化学试题重庆市实验中学2021-2022学年高一上学期10月月考化学试题辽宁师范大学附属中学2021-2022学年高一上学期10月月考化学试题吉林省长春市第二十九中学2021-2022学年高一上学期第二学程考试化学(理)试题河南省濮阳市第一高级中学2021-2022学年高一上学期第二次质量检测化学试题(已下线)1.3.1 氧化还原反应概念与电子转移-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)广东省惠州市惠州中学2021-2022学年高一上学期期中考试化学试题云南省罗平县第二中学2021-2022学年高一上学期期中考试化学试题天津市西青区杨柳青一中2022-2023学年高一上学期线上学习效果反馈化学试题新疆乌鲁木齐市第八中学2022-2023学年高一上学期期中考试化学试题黑龙江省佳木斯市第十二中学2022-2023学年高一上学期期中考试化学试题黑龙江省哈尔滨市第一六二中学校2022-2023学年高一上学期第一次月考化学试题黑龙江省虎林市高级中学2022-2023学年高一上学期期中考试化学试题云南省泸水市怒江新城新时代中学2022-2023学年高一上学期期中考试化学试题海南省海口市第一中学2022-2023学年高一上学期期中考试化学试题广东省广州市第八十六中学2022-2023学年高一上学期期中考试化学试题广东省佛山市禅城实验高级中学2022-2023学年高一上学期期中考试化学试题浙江省台州市八校联盟2022-2023学年高一上学期11月期中联考化学试题天津市实验中学滨海学校2022-2023学年高一上学期期中质量调查化学试题
10 . 实验小组为探究金属元素金属性的递变规律进行实验,主要实验包括:
①分别加热 、
、 单质观察现象;
单质观察现象;
②镁条、 单质分别与水反应;
单质分别与水反应;
③分别配制浓度均为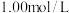 的
的 溶液和
溶液和 溶液,滴定观察现象。
溶液,滴定观察现象。
上述操作中,不需要用到的仪器为( )
①分别加热
 、
、 单质观察现象;
单质观察现象;②镁条、
 单质分别与水反应;
单质分别与水反应;③分别配制浓度均为
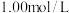 的
的 溶液和
溶液和 溶液,滴定观察现象。
溶液,滴定观察现象。上述操作中,不需要用到的仪器为( )
A. | B. | C. | D. |
您最近一年使用:0次



