名校
解题方法
1 . A、B、C、D、E为中学化学常见的单质或化合物,相互转化关系如图所示。

(1)若A是能使湿润的红色石蕊试纸变蓝的气体;C、D均为空气的主要成分;E是一种有毒气体能与血红蛋白结合,反应Ⅱ在三元催化器催化作用下常用于汽车尾气的转化。
①写出反应I的化学方程式__ 。
②写出Ⅲ在高温下反应的化学方程式__ 。
(2)若A是淡黄色化合物;常温下D是无色气体;C是一种常见的碱,含有的阴、阳离子均为10电子粒子。
①写出反应Ⅰ的化学方程式___ 。
②写出反应Ⅲ的化学方程式___ 。
(3)若A是酸,D是一种常见金属,E是一种常见的非金属单质。
①写出反应Ⅱ的离子方程式___ 。
②检验B中含有少量C的方法是:取少量溶液加入__ (填序号)后观察现象。
A.NaOH溶液 B.KSCN溶液 C.酸性KMnO4溶液 D.淀粉—KI溶液

(1)若A是能使湿润的红色石蕊试纸变蓝的气体;C、D均为空气的主要成分;E是一种有毒气体能与血红蛋白结合,反应Ⅱ在三元催化器催化作用下常用于汽车尾气的转化。
①写出反应I的化学方程式
②写出Ⅲ在高温下反应的化学方程式
(2)若A是淡黄色化合物;常温下D是无色气体;C是一种常见的碱,含有的阴、阳离子均为10电子粒子。
①写出反应Ⅰ的化学方程式
②写出反应Ⅲ的化学方程式
(3)若A是酸,D是一种常见金属,E是一种常见的非金属单质。
①写出反应Ⅱ的离子方程式
②检验B中含有少量C的方法是:取少量溶液加入
A.NaOH溶液 B.KSCN溶液 C.酸性KMnO4溶液 D.淀粉—KI溶液
您最近一年使用:0次
2021-05-01更新
|
608次组卷
|
2卷引用:天津市第一中学2020-2021学年高一下学期期中考试化学试题
名校
解题方法
2 . 向200mL1.5mol·L-lFeBr2溶液中逐渐通入Cl2,其中n(Fe2+)、n(Br-)随通入Cl2的物质的量n(Cl2)变化如图所示,下列说法错误的是


| A.①代表Fe2+,②代表Br- |
| B.还原性强弱:Fe2+>Br- |
| C.n(Cl2)=0.35mol时,溶液中c(Fe3+)=c(Br-) |
| D.n(Cl2)=0.45mol时,总的离子方程式为:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
您最近一年使用:0次
2021-02-06更新
|
812次组卷
|
2卷引用:天津市崇化中学2022-2023学年高三上学期期末检测化学试题
解题方法
3 . 绿矾是含有一定量结晶水的硫酸亚铁,在工农业生产中具有重要的用途。某化学兴趣小组对绿矾的一些性质进行探究。回答下列问题:
(1)在试管中加入少量绿矾样品,加水溶解,滴加 溶液,溶液颜色无明显变化。再向试管中通入空气,产生的现象是
溶液,溶液颜色无明显变化。再向试管中通入空气,产生的现象是______ 。
(2)为测定绿矾中结晶水含量,将带有两端开关K1和K2的石英玻璃管(设为装置A)称重,记为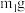 。将样品装入石英玻璃管中,再次将装置A称重,记为
。将样品装入石英玻璃管中,再次将装置A称重,记为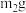 。按下图连接好装置进行实验。
。按下图连接好装置进行实验。
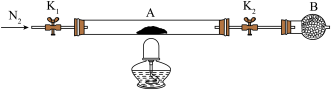
①仪器B的名称是________________ 。
②实验操作步骤:a.打开K1和K2,缓缓通入N2→b.点燃酒精灯,加热→c.熄灭酒精灯→d.→e.关闭 和
和 →f.称量A。d的操作为
→f.称量A。d的操作为________________ 。
③重复②的操作步骤,直至A恒重,记为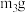 ,根据实验记录,计算绿矾化学式中结晶水数目
,根据实验记录,计算绿矾化学式中结晶水数目
________________ (列式表示)。若实验时将a、b的操作次序颠倒,则使x________ (填“偏大”“偏小”或“无影响”)。
(3)为探究硫酸亚铁的分解产物,将(2)中已恒重的装置A接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。
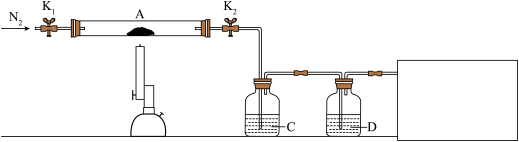
已知:装置C用于检验和吸收分解得到的气体产物之一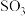 .
.
①C/D中的溶液依次为________ (填标号)。
a、品红 b. c.
c. d.
d. e.浓
e.浓
C、D中有气泡冒出,并可观察到的现象分别为________ 、________ 。
②写出硫酸亚铁高温分解反应的化学方程式:________________________ 。
③在方框中画出尾气吸收装置并注明所用试剂。_________
(1)在试管中加入少量绿矾样品,加水溶解,滴加
 溶液,溶液颜色无明显变化。再向试管中通入空气,产生的现象是
溶液,溶液颜色无明显变化。再向试管中通入空气,产生的现象是(2)为测定绿矾中结晶水含量,将带有两端开关K1和K2的石英玻璃管(设为装置A)称重,记为
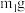 。将样品装入石英玻璃管中,再次将装置A称重,记为
。将样品装入石英玻璃管中,再次将装置A称重,记为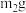 。按下图连接好装置进行实验。
。按下图连接好装置进行实验。
①仪器B的名称是
②实验操作步骤:a.打开K1和K2,缓缓通入N2→b.点燃酒精灯,加热→c.熄灭酒精灯→d.→e.关闭
 和
和 →f.称量A。d的操作为
→f.称量A。d的操作为③重复②的操作步骤,直至A恒重,记为
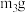 ,根据实验记录,计算绿矾化学式中结晶水数目
,根据实验记录,计算绿矾化学式中结晶水数目
(3)为探究硫酸亚铁的分解产物,将(2)中已恒重的装置A接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。

已知:装置C用于检验和吸收分解得到的气体产物之一
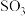 .
.①C/D中的溶液依次为
a、品红 b.
 c.
c. d.
d. e.浓
e.浓
C、D中有气泡冒出,并可观察到的现象分别为
②写出硫酸亚铁高温分解反应的化学方程式:
③在方框中画出尾气吸收装置并注明所用试剂。
您最近一年使用:0次
4 . (一)某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 mol/L 的溶液。在FeCl2溶液中需加入少量铁屑,其目的是__________________________ 。
(2)甲组同学取2mLFeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为_______________ 。
(3)乙组同学认为甲组的实验不够严谨,该组同学在2mLFeCl2溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是_____________ 。
(二)工业上用赤铁矿(含Fe2O3、FeO,也含有Al2O3、MnO2、CuO、SiO2等)制备绿矾FeSO4·7H2O的流程如下:

(4)氢氧化钠溶液加入赤铁矿中发生反应的离子方程式为____________ ;_________________ 。
(5)向滤渣Ⅰ中加入过量的试剂a为___________ ,过量的试剂b投入到滤液Ⅱ发生的所有反应的离子方程式为______________ ;_________________ ;________________ 。
(6)实验室中操作①②③的名称为_________________________ 。
(7)操作④隔绝空气的目的是_______________________________________________ 。
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 mol/L 的溶液。在FeCl2溶液中需加入少量铁屑,其目的是
(2)甲组同学取2mLFeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为
(3)乙组同学认为甲组的实验不够严谨,该组同学在2mLFeCl2溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是
(二)工业上用赤铁矿(含Fe2O3、FeO,也含有Al2O3、MnO2、CuO、SiO2等)制备绿矾FeSO4·7H2O的流程如下:

(4)氢氧化钠溶液加入赤铁矿中发生反应的离子方程式为
(5)向滤渣Ⅰ中加入过量的试剂a为
(6)实验室中操作①②③的名称为
(7)操作④隔绝空气的目的是
您最近一年使用:0次



