1 . 用富含铁元素的食品,可以补充人体所需的铁元素。某班级研究性学习小组对菠菜中的铁元素展开了检测,实验如下:

(1)下列图示装置或操作合理的是________ 。
(2)写出试剂B的化学式___________ 。
(3)试剂C若为双氧水,请写出该反应的离子方程式:___________ ;该实验证明菠菜中含有的铁元素为_____ 价。
(4)其中一名同学在研究过程中向滤液A中先加入氯水,再加入试剂B,也看到溶液变红,由此也得出和其他同学一样的结论。他的做法是否正确?______ ,原因是什么?___________ 。
(5)另取少量滤液 ,向其中加入少量NaOH溶液,观察到的现象是
,向其中加入少量NaOH溶液,观察到的现象是________ ;原因是___________ 、________ (用离子方程式解释)。

(1)下列图示装置或操作合理的是
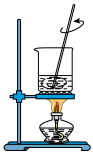 | 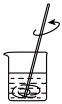 | 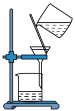 |  |
| A.灼烧 | B.溶解 | C.过滤 | D.检测菠菜液中的铁元素 |
(2)写出试剂B的化学式
(3)试剂C若为双氧水,请写出该反应的离子方程式:
(4)其中一名同学在研究过程中向滤液A中先加入氯水,再加入试剂B,也看到溶液变红,由此也得出和其他同学一样的结论。他的做法是否正确?
(5)另取少量滤液
 ,向其中加入少量NaOH溶液,观察到的现象是
,向其中加入少量NaOH溶液,观察到的现象是
您最近一年使用:0次
名校
2 . 某酸性溶液中可能含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 和
和 。某同学为了确认其成分,设计并完成了如图实验。下列叙述正确的是
。某同学为了确认其成分,设计并完成了如图实验。下列叙述正确的是

 、
、 、
、 、
、 、
、 、
、 、
、 、
、 和
和 。某同学为了确认其成分,设计并完成了如图实验。下列叙述正确的是
。某同学为了确认其成分,设计并完成了如图实验。下列叙述正确的是
A.反应①发生反应的离子方程式为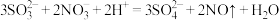 |
B.溶液中至少有6种离子大量存在,其中 一定存在,且 一定存在,且 |
C.溶液中可能含有 ,一定含有 ,一定含有 ,可取少量原溶液加入 ,可取少量原溶液加入 溶液检验 溶液检验 |
D. 、 、 、 、 一定存在, 一定存在, 、 、 一定不存在 一定不存在 |
您最近一年使用:0次
2022-11-17更新
|
1333次组卷
|
10卷引用:宁夏石嘴山市平罗中学2022-2023学年高三上学期期中考试(重点班)化学试题
宁夏石嘴山市平罗中学2022-2023学年高三上学期期中考试(重点班)化学试题百师联盟2023届高三上学期一轮复习联考(全国卷)化学试题辽宁省葫芦岛市四校2022-2023学年高三上学期期中联考化学试题(已下线)专题03 离子反应方程式和离子共存(测)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)专题三 离子反应-实战高考·二轮复习核心突破(已下线)专题卷06 离子共存与离子推断-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)河北省石家庄市正定中学2022- 2023学年高二下学期期末考试化学试题江西省百师联盟2024届高三上学期一轮复习联考化学试题江西省百师联盟2024届高三上学期9月复习联考化学试题黑龙江省海伦市第一中学2022-2023学年高三上学期1月期末考试化学试题
名校
解题方法
3 . 溶液A中存在Ba2+、Fe2+、Al3+、Fe3+、Cu2+、 、
、 、Cl-、
、Cl-、 、
、 中的五种离子,浓度均为0.01mol·L-1,溶液体积为1L。对溶液A进行以下实验,整个过程如图所示(部分产物省略),溶液B与溶液A中所含阴离子种类相同。
中的五种离子,浓度均为0.01mol·L-1,溶液体积为1L。对溶液A进行以下实验,整个过程如图所示(部分产物省略),溶液B与溶液A中所含阴离子种类相同。

已知:下表为相应阳离子形成氢氧化物沉淀时所对应的pH范围
请回答下列问题:
(1)溶液A中含有的离子为___________ 。
(2)反应①的离子方程式为___________ 。
(3)沉淀甲是___________ ,沉淀乙是___________ (填化学式)。
(4)固体C可能是___________ (填字母)。
a.CuO b.Cu(OH)2 c.CuSO4 d.CuCl2
(5)气体甲、气体乙都能造成环境问题,将等体积的气体甲和乙通入足量NaOH溶液中,被完全吸收,写出反应的离子方程式___________ 。
(6)若向原溶液A中加入足量的NaOH溶液,充分反应后将沉淀过滤、洗涤、干燥并灼烧至恒重,得到固体的质量为___________ g。
 、
、 、Cl-、
、Cl-、 、
、 中的五种离子,浓度均为0.01mol·L-1,溶液体积为1L。对溶液A进行以下实验,整个过程如图所示(部分产物省略),溶液B与溶液A中所含阴离子种类相同。
中的五种离子,浓度均为0.01mol·L-1,溶液体积为1L。对溶液A进行以下实验,整个过程如图所示(部分产物省略),溶液B与溶液A中所含阴离子种类相同。
已知:下表为相应阳离子形成氢氧化物沉淀时所对应的pH范围
| 阳离子 | 开始沉淀时pH | 沉淀完全时pH |
| Fe2+ | 5.9 | 8.4 |
| Fe3+ | 1.1 | 3.0 |
| Cu2+ | 4.2 | 6.7 |
| Al3+ | 3.0 | 4.7 |
(1)溶液A中含有的离子为
(2)反应①的离子方程式为
(3)沉淀甲是
(4)固体C可能是
a.CuO b.Cu(OH)2 c.CuSO4 d.CuCl2
(5)气体甲、气体乙都能造成环境问题,将等体积的气体甲和乙通入足量NaOH溶液中,被完全吸收,写出反应的离子方程式
(6)若向原溶液A中加入足量的NaOH溶液,充分反应后将沉淀过滤、洗涤、干燥并灼烧至恒重,得到固体的质量为
您最近一年使用:0次
名校
解题方法
4 . 铋酸钠(NaBiO3)常用作Mn2+鉴定的强氧化剂,某研究小组用浮选过的辉铋矿(主要成分是Bi2S3,还含少量Bi2O3、SiO2等杂质)制备铋酸钠,其流程如图:

已知:①NaBiO3是一种难溶于水的物质②BiCl3极易水解生成不溶性的BiOCl沉淀。请回答下列问题:
(1)为了提高溶浸工序中原料的浸出率,可以采取的措施有______ (填标号)。
a.粉碎矿石 b.搅拌 c.加入足量的蒸馏水 d.降低温度
(2)滤渣A的主要成分为______ (填化学式),溶浸时通常加入FeCl3溶液和浓盐酸,加入的浓盐酸需过量的目的是______ 。
(3)通过反应③实现FeCl3的循环利用,写出该反应的离子方程式______ 。
(4)反应④的化学方程式为______ 。
(5)NaBiO3可在酸性介质中将Mn2+氧化为MnO ,故可用于Mn2+的鉴定。已知NaBiO3被还原为Bi3+,该反应的离子方程式为
,故可用于Mn2+的鉴定。已知NaBiO3被还原为Bi3+,该反应的离子方程式为______ 。
(6)实验室为了测定NaBiO3样品的纯度,需要配制250mL0.500mol/LFeSO4溶液,所需要的玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管外,还需要______ 。
(7)取上述NaBiO3样品10.0g,加入稀硫酸和MnSO4溶液使其完全溶解,稀释至100mL,取出20.00mL溶液,然后用新配制的0.500mol/LFeSO4溶液进行滴定,滴定完成后消耗24.80mLFeSO4溶液。则该样品中NaBiO3纯度为______ %(结果保留小数点后一位)。

已知:①NaBiO3是一种难溶于水的物质②BiCl3极易水解生成不溶性的BiOCl沉淀。请回答下列问题:
(1)为了提高溶浸工序中原料的浸出率,可以采取的措施有
a.粉碎矿石 b.搅拌 c.加入足量的蒸馏水 d.降低温度
(2)滤渣A的主要成分为
(3)通过反应③实现FeCl3的循环利用,写出该反应的离子方程式
(4)反应④的化学方程式为
(5)NaBiO3可在酸性介质中将Mn2+氧化为MnO
 ,故可用于Mn2+的鉴定。已知NaBiO3被还原为Bi3+,该反应的离子方程式为
,故可用于Mn2+的鉴定。已知NaBiO3被还原为Bi3+,该反应的离子方程式为(6)实验室为了测定NaBiO3样品的纯度,需要配制250mL0.500mol/LFeSO4溶液,所需要的玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管外,还需要
(7)取上述NaBiO3样品10.0g,加入稀硫酸和MnSO4溶液使其完全溶解,稀释至100mL,取出20.00mL溶液,然后用新配制的0.500mol/LFeSO4溶液进行滴定,滴定完成后消耗24.80mLFeSO4溶液。则该样品中NaBiO3纯度为
您最近一年使用:0次
5 . 某化学小组用部分氧化的FeSO4为原料,以萃取剂X(甲基异丁基甲酮)萃取法制取高纯氧化铁(Fe2O3),并进行铁含量的测定。主要操作步骤如下:
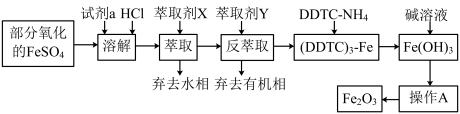
已知:①在较高的盐酸浓度下,Fe3+能溶解于甲基异丁基甲酮,当盐酸浓度降低时,该化合物解离。
②3DDTC-NH4+Fe3+=(DDTC)3-Fe↓+3NH 。
。
请回答下列问题:
(1)写出加入试剂a发生反应的离子方程式_________ 。
(2)溶液中加入萃取剂X,转移至分液漏斗中,塞上玻璃塞振摇,振摇几次后需打开分液漏斗的___ 放气;为提高萃取率和产品产量,实验时应进行的操作是__________ 。
(3)可作反萃取的萃取剂Y的最佳试剂是(填试剂名称)____ 。
(4)操作A为_____ 、_____ 、______ 。产品处理时,温度对产品的纯度有很大影响。已知温度对产物纯度的影响如图所示,则温度最好控制在______ ℃。

(5)现准确称取4.000g样品,经酸溶、还原为Fe2+,在容量瓶中配成100mL溶液,用______ (填仪器名称)移取25.00 mL溶液于锥形瓶中,用0.l000mol/L的K2Cr2O7溶液进行滴定,消耗K2Cr2O7溶液20.60mL。产品中铁的含量为______ (假设杂质不与K2Cr2O7反应)。

已知:①在较高的盐酸浓度下,Fe3+能溶解于甲基异丁基甲酮,当盐酸浓度降低时,该化合物解离。
②3DDTC-NH4+Fe3+=(DDTC)3-Fe↓+3NH
 。
。请回答下列问题:
(1)写出加入试剂a发生反应的离子方程式
(2)溶液中加入萃取剂X,转移至分液漏斗中,塞上玻璃塞振摇,振摇几次后需打开分液漏斗的
(3)可作反萃取的萃取剂Y的最佳试剂是(填试剂名称)
(4)操作A为

(5)现准确称取4.000g样品,经酸溶、还原为Fe2+,在容量瓶中配成100mL溶液,用
您最近一年使用:0次
2020-07-28更新
|
390次组卷
|
6卷引用:宁夏石嘴山市第三中学2023-2024学年高三上学期第二次月考 化学试题
名校
解题方法
6 . 向含有0.8 mol的稀硝酸中慢慢加入22.4 g的铁粉,假设反应分为两个阶段。
第一阶段为:Fe+HNO3(稀)→Fe(NO3)3+NO↑+H2O
(1)写出这两个阶段发生反应的离子方程式:
第一阶段:_______________________________________________ 。
第二阶段:_______________________________________________ 。
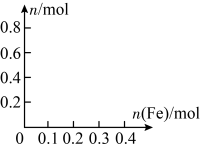
(2)在图中画出溶液中Fe2+、Fe3+、 的物质的量随加入铁粉的物质的量变化的关系图象(横坐标为加入铁粉的物质的量,纵坐标是溶液中离子的物质的量)
的物质的量随加入铁粉的物质的量变化的关系图象(横坐标为加入铁粉的物质的量,纵坐标是溶液中离子的物质的量) ________ 。
第一阶段为:Fe+HNO3(稀)→Fe(NO3)3+NO↑+H2O
(1)写出这两个阶段发生反应的离子方程式:
第一阶段:
第二阶段:
(2)在图中画出溶液中Fe2+、Fe3+、
 的物质的量随加入铁粉的物质的量变化的关系图象(横坐标为加入铁粉的物质的量,纵坐标是溶液中离子的物质的量)
的物质的量随加入铁粉的物质的量变化的关系图象(横坐标为加入铁粉的物质的量,纵坐标是溶液中离子的物质的量) 
您最近一年使用:0次
2016-12-09更新
|
424次组卷
|
2卷引用:宁夏石嘴山三中2016届高三(上)第四次质检化学试卷(解析版)



