名校
1 . 二茂铁[Fe(C5H5)2,Fe为 价]是最早被发现的夹心配合物,橙色晶体,100℃ 以上升华,熔点172℃,沸点249℃,难溶于水,空气中稳定,与酸、碱一般不作用。实验室中,先由二聚环戊二烯C10H12(沸点170℃)热解聚制备环戊二烯C5H6(密度0.88g·cm-3,熔点-85℃,沸点42.5℃)(图1),然后制备二茂铁(图2),最后纯化(图3),夹持装置已略。回答下列问题:
价]是最早被发现的夹心配合物,橙色晶体,100℃ 以上升华,熔点172℃,沸点249℃,难溶于水,空气中稳定,与酸、碱一般不作用。实验室中,先由二聚环戊二烯C10H12(沸点170℃)热解聚制备环戊二烯C5H6(密度0.88g·cm-3,熔点-85℃,沸点42.5℃)(图1),然后制备二茂铁(图2),最后纯化(图3),夹持装置已略。回答下列问题:

(1)检查装置气密性并在烧瓶中加入二聚环戊二烯。实验中需要一直慢慢地通入N2,其作用是_______ 。将电热棒调至360~400℃,同时170℃油浴加热烧瓶,油浴加热的优点是_______ 。反应完成后在接收瓶中得到环戊二烯纯品。
(2)将磁子和足量 粉末放在三颈烧瓶中,加入适量有机溶剂和
粉末放在三颈烧瓶中,加入适量有机溶剂和 环戊二烯,缓慢搅拌,烧瓶左侧口用A塞紧,中间瓶口装上仪器C(已打开旋塞B和玻璃塞),右侧口接带T形管的汞起泡器和氮气瓶,用氮气流吹洗烧瓶和C直至空气完全吹出,关上B,将溶解了11.94gFeCl2·4H2O的有机溶剂注入仪器C,……打开B,滴加完后快速搅拌30min,制备反应结束。……向烧瓶中加入稍过量的盐酸和适量碎冰。……将烧瓶内的沉淀收集到过滤器上,用水洗涤,干燥,得到二茂铁粗品。
环戊二烯,缓慢搅拌,烧瓶左侧口用A塞紧,中间瓶口装上仪器C(已打开旋塞B和玻璃塞),右侧口接带T形管的汞起泡器和氮气瓶,用氮气流吹洗烧瓶和C直至空气完全吹出,关上B,将溶解了11.94gFeCl2·4H2O的有机溶剂注入仪器C,……打开B,滴加完后快速搅拌30min,制备反应结束。……向烧瓶中加入稍过量的盐酸和适量碎冰。……将烧瓶内的沉淀收集到过滤器上,用水洗涤,干燥,得到二茂铁粗品。
①仪器C的名称为_______ 。
②将空气完全吹出的目的是_______ 。
③加入碎冰的作用是_______ 。
④证明盐酸已稍过量的试剂是_______ 。
⑤写出生成二茂铁的反应的化学方程式:_______ 。
(3)将盛有粗品的培养皿放在电热板上加热,最终得到纯品9.49g,二茂铁的产率为_______ %(保留到小数点后一位)。
 价]是最早被发现的夹心配合物,橙色晶体,100℃ 以上升华,熔点172℃,沸点249℃,难溶于水,空气中稳定,与酸、碱一般不作用。实验室中,先由二聚环戊二烯C10H12(沸点170℃)热解聚制备环戊二烯C5H6(密度0.88g·cm-3,熔点-85℃,沸点42.5℃)(图1),然后制备二茂铁(图2),最后纯化(图3),夹持装置已略。回答下列问题:
价]是最早被发现的夹心配合物,橙色晶体,100℃ 以上升华,熔点172℃,沸点249℃,难溶于水,空气中稳定,与酸、碱一般不作用。实验室中,先由二聚环戊二烯C10H12(沸点170℃)热解聚制备环戊二烯C5H6(密度0.88g·cm-3,熔点-85℃,沸点42.5℃)(图1),然后制备二茂铁(图2),最后纯化(图3),夹持装置已略。回答下列问题:
(1)检查装置气密性并在烧瓶中加入二聚环戊二烯。实验中需要一直慢慢地通入N2,其作用是
(2)将磁子和足量
 粉末放在三颈烧瓶中,加入适量有机溶剂和
粉末放在三颈烧瓶中,加入适量有机溶剂和 环戊二烯,缓慢搅拌,烧瓶左侧口用A塞紧,中间瓶口装上仪器C(已打开旋塞B和玻璃塞),右侧口接带T形管的汞起泡器和氮气瓶,用氮气流吹洗烧瓶和C直至空气完全吹出,关上B,将溶解了11.94gFeCl2·4H2O的有机溶剂注入仪器C,……打开B,滴加完后快速搅拌30min,制备反应结束。……向烧瓶中加入稍过量的盐酸和适量碎冰。……将烧瓶内的沉淀收集到过滤器上,用水洗涤,干燥,得到二茂铁粗品。
环戊二烯,缓慢搅拌,烧瓶左侧口用A塞紧,中间瓶口装上仪器C(已打开旋塞B和玻璃塞),右侧口接带T形管的汞起泡器和氮气瓶,用氮气流吹洗烧瓶和C直至空气完全吹出,关上B,将溶解了11.94gFeCl2·4H2O的有机溶剂注入仪器C,……打开B,滴加完后快速搅拌30min,制备反应结束。……向烧瓶中加入稍过量的盐酸和适量碎冰。……将烧瓶内的沉淀收集到过滤器上,用水洗涤,干燥,得到二茂铁粗品。①仪器C的名称为
②将空气完全吹出的目的是
③加入碎冰的作用是
④证明盐酸已稍过量的试剂是
⑤写出生成二茂铁的反应的化学方程式:
(3)将盛有粗品的培养皿放在电热板上加热,最终得到纯品9.49g,二茂铁的产率为
您最近一年使用:0次
2022-05-29更新
|
405次组卷
|
2卷引用:安徽师范大学附属中学2022届高三适应性考试理综化学试题
2 . 化合物X在一定条件下可发生如图转化,有关叙述错误的是


A.溶液C到溶液D中发生的离子方程式为:Fe3++3SCN— Fe(SCN)3 Fe(SCN)3 |
| B.E为CO,物质的量为0.05mol |
| C.X为Fe(CO)4 |
| D.过量的稀硫酸若换成盐酸,会造成环境污染 |
您最近一年使用:0次
2021-06-30更新
|
2098次组卷
|
7卷引用:安徽省淮北市2021届高三第一次模拟考试化学试题
安徽省淮北市2021届高三第一次模拟考试化学试题(已下线)专题三 能力提升检测卷 (测) — 2022年高考化学一轮复习讲练测(新教材新高考)辽宁省实验中学2022届高三第一次阶段性考试化学试题(已下线)专题06 常见金属及其化合物-备战2022年高考化学学霸纠错(全国通用)(已下线)专题14物质的反应和转化-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题13物质的反应和转化-2022年高考真题+模拟题汇编(全国卷)(已下线)专题14物质的反应和转化-五年(2018~2022)高考真题汇编(全国卷)
3 . 某化学兴趣小组对硫酸亚铁的性质进行探究并做如下实验,将称量好的硫酸亚铁溶解于一定浓度的稀硫酸中配制成 的溶液:
的溶液:
回答下列问题:
(1)进一步研究证实,黑色沉淀的主要成分是 。
。 溶液呈碱性,
溶液呈碱性, 溶液与其反应不生成
溶液与其反应不生成 而生成
而生成 的可能原因是
的可能原因是_______ 。
(2用离子方程式表示步骤ⅱ中溶液变红的原因:_______ 、_______ 。
(3)甲同学探究步骤ⅲ中溶液褪色的原因,提出如下假设:
a. 被
被 还原 b.
还原 b. 被
被 氧化 c.
氧化 c. 被
被 氧化
氧化
乙同学根据上述实验认为假设b不成立,他依据的现象是_____ 。
(4)甲同学利用上述部分试剂,通过以下实验验证了(3)中假设c成立。请将以下实验操作及现象补充完整。
 的溶液:
的溶液:| 实验序号 | 操作及现象 |
| ⅰ | 取 上述 上述 溶液于试管中,逐滴加入少量 溶液于试管中,逐滴加入少量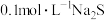 溶液,产生大量黑色沉淀 溶液,产生大量黑色沉淀 |
| ⅱ | 取 上述 上述 溶液于试管中,加入2滴 溶液于试管中,加入2滴 溶液无现象,通入一段时间 溶液无现象,通入一段时间 ,溶液变为浅红色 ,溶液变为浅红色 |
| ⅲ | 重复实验ⅱ,向浅红色溶液中加入5% 溶液至过量,产生无色气体(经检验为 溶液至过量,产生无色气体(经检验为 ),溶液变为深红色中,且红色很快褪去 ),溶液变为深红色中,且红色很快褪去 |
(1)进一步研究证实,黑色沉淀的主要成分是
 。
。 溶液呈碱性,
溶液呈碱性, 溶液与其反应不生成
溶液与其反应不生成 而生成
而生成 的可能原因是
的可能原因是(2用离子方程式表示步骤ⅱ中溶液变红的原因:
(3)甲同学探究步骤ⅲ中溶液褪色的原因,提出如下假设:
a.
 被
被 还原 b.
还原 b. 被
被 氧化 c.
氧化 c. 被
被 氧化
氧化乙同学根据上述实验认为假设b不成立,他依据的现象是
(4)甲同学利用上述部分试剂,通过以下实验验证了(3)中假设c成立。请将以下实验操作及现象补充完整。
| 步骤 | 试剂及操作 | 现象 |
| 1 | 取实验ⅲ中褪色后溶液少量于试管,滴加 溶液 溶液 | ① |
| 2 | ② | 溶液变为红色 |
您最近一年使用:0次
2021-06-25更新
|
266次组卷
|
2卷引用:安徽省安庆市第一中学龙山校区2021-2022学年高一下学期3月阶段性考试化学试题
名校
解题方法
4 . 某溶液X中可能含有 、
、 、
、 、
、 、
、 、
、 和
和 中的几种,且所含阴离子的物质的量相等。为确定该溶液X的成分,某学习小组做了如下实验,下列说法错误的是
中的几种,且所含阴离子的物质的量相等。为确定该溶液X的成分,某学习小组做了如下实验,下列说法错误的是

 、
、 、
、 、
、 、
、 、
、 和
和 中的几种,且所含阴离子的物质的量相等。为确定该溶液X的成分,某学习小组做了如下实验,下列说法错误的是
中的几种,且所含阴离子的物质的量相等。为确定该溶液X的成分,某学习小组做了如下实验,下列说法错误的是
A.产生气体乙的方程式为: |
| B.气体甲能使湿润的红色石蕊试纸变蓝 |
C. 、 、 一定存在, 一定存在, 和 和 可能都存在 可能都存在 |
D.该溶液中只存在上述离子中的 、 、 、 、 、 、 四种离子 四种离子 |
您最近一年使用:0次
2020-10-26更新
|
685次组卷
|
3卷引用:安徽省池州市第一中学2021届高三上学期9月月考化学试题
名校
5 . 经多年勘测,2018年11月23日省自然资源厅发布消息称在皖江地区发现特大铜矿床,具有重大实际意义。以黄铜矿(主要成分为CuFeS2,含有少量PbS、Al2O3、SiO2)为原料制取胆矾的流程如图:


已知:常温下Ksp[Fe(OH)3]=8.0×10-38,Ksp[Al(OH)3]=3.0×10-33,Ksp[Cu(OH)2]=3.0×10-20。
(1)CuFeS2中硫元素的化合价为___________ ,硫元素在周期表中的位置是___________ 。写出上述流程中生成亚硫酸铵的离子方程式:___________ 。
(2)最适合的试剂A是___________ (写化学式)溶液,固体2的成分为PbSO4和___________ 。当试剂A的浓度为6mol·L-1时,“浸出”实验中,铜的浸出率结果如图所示。所采用的最佳实验条件(温度、时间)为___________ 。
(3)最适合的试剂B是___________ (填序号),最适合的试剂C是___________ (填序号),固体3的成分为___________ 。
a.Cl2 b.CuO c.酸性高锰酸钾溶液 d.NaOH e.H2O2溶液 f.K2CO3
(4)操作1如在实验室中进行,用到的玻璃仪器有烧杯、玻璃棒和___________ ,操作2的步骤为___________ ,___________ ,过滤、洗涤。
(5)根据已知图象信息,请计算:当Fe3+完全沉淀时,溶液中Al3+理论最大浓度为___________ 。
(提示:当离子浓度≤1×10-5mol·L时,认为该离子沉淀完全)


已知:常温下Ksp[Fe(OH)3]=8.0×10-38,Ksp[Al(OH)3]=3.0×10-33,Ksp[Cu(OH)2]=3.0×10-20。
(1)CuFeS2中硫元素的化合价为
(2)最适合的试剂A是
(3)最适合的试剂B是
a.Cl2 b.CuO c.酸性高锰酸钾溶液 d.NaOH e.H2O2溶液 f.K2CO3
(4)操作1如在实验室中进行,用到的玻璃仪器有烧杯、玻璃棒和
(5)根据已知图象信息,请计算:当Fe3+完全沉淀时,溶液中Al3+理论最大浓度为
(提示:当离子浓度≤1×10-5mol·L时,认为该离子沉淀完全)
您最近一年使用:0次
2019-03-20更新
|
522次组卷
|
4卷引用:【市级联考】安徽省黄山市2019届高三上学期一模检测理科综合化学试题



