1 . I.酸碱中和滴定是一种重要的实验方法,用 标准溶液溶液滴定未知浓度的醋酸
标准溶液溶液滴定未知浓度的醋酸
(1) 标准溶液盛放在
标准溶液盛放在_______ (填“酸或碱”)式滴定管中。
(2)该实验中选择的指示剂是_______ 。
(3)根据下列数据,请计算待测醋酸的浓度:_______  。
。
(4)量取标准液的碱式滴定管未润洗,会造成测定结果_______ (填“偏高或偏低或不变”) 。
Ⅱ.按要求填空
(5)FeCl3溶液蒸发灼烧最终得到的物质_______ (写化学式 )。
(6)泡沫灭火器原理_______ (写离子反应方程式)。
 标准溶液溶液滴定未知浓度的醋酸
标准溶液溶液滴定未知浓度的醋酸(1)
 标准溶液盛放在
标准溶液盛放在(2)该实验中选择的指示剂是
(3)根据下列数据,请计算待测醋酸的浓度:
 。
。| 滴定次数 | 待测液体积(mL) | 标准液体积(mL | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 20.00 | 0.60 | 20.60 |
| 第二次 | 20.00 | 2.00 | 24.10 |
| 第三次 | 20.00 | 4.00 | 24.00 |
(4)量取标准液的碱式滴定管未润洗,会造成测定结果
Ⅱ.按要求填空
(5)FeCl3溶液蒸发灼烧最终得到的物质
(6)泡沫灭火器原理
您最近一年使用:0次
解题方法
2 . 2020年第七十五届联合国大会上,中国向世界郑重承诺在2030年前实现碳达峰,在2060年前实现碳中和。大力发展绿色能源、清洁能源是实现碳中和的最有效方法。
(1)下图是_______ 装置,能量转化是,_____ 能转化为_____ 能。______ 极,发生_____ (填“氧化”或“还原”)反应。
(3)Cu棒,上发生的电极反应是______ 。
(4)溶液中H⁺向______ (填“Zn”或“Cu”)电极定向移动。
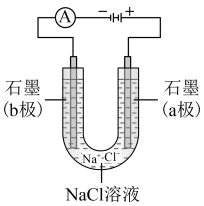
(5)下图是_____ 装置,a极是该电池的_______ 极,b极是该电池的_____ 极。
(1)下图是
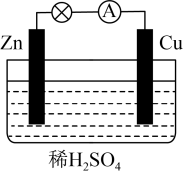
(3)Cu棒,上发生的电极反应是
(4)溶液中H⁺向
(5)下图是
您最近一年使用:0次
3 . 反应;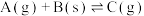
 ,在其他条件不变时,改变其中一个条件,则生成
,在其他条件不变时,改变其中一个条件,则生成 的速率(填“增大”、“不变”、“减小”):
的速率(填“增大”、“不变”、“减小”):
(1)升温_______ 。
(2)使用催化剂_______ 。
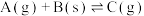
 ,在其他条件不变时,改变其中一个条件,则生成
,在其他条件不变时,改变其中一个条件,则生成 的速率(填“增大”、“不变”、“减小”):
的速率(填“增大”、“不变”、“减小”):(1)升温
(2)使用催化剂
您最近一年使用:0次
解题方法
4 . 电解原理在化学工业中有广泛应用。下图表示一个电解池,其中a为电解质溶液,X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:___________ (填写“阳极”或“阴极”)。
(2)若X、Y都是惰性电极,a是饱和食盐水,Y极上的电极反应式为___________ 。
(3)若X、Y都是惰性电极,a是CuCl2溶液,X极的电极反应式为___________ 。
(4)若要用该装置电解精炼粗铜,电解液a选用CuSO4溶液,则Y电极的材料是___________ 。
(5)若要用电镀方法在铁表面镀一层金属银,应该选择的的方案是___________。 填字母编号
填字母编号

(2)若X、Y都是惰性电极,a是饱和食盐水,Y极上的电极反应式为
(3)若X、Y都是惰性电极,a是CuCl2溶液,X极的电极反应式为
(4)若要用该装置电解精炼粗铜,电解液a选用CuSO4溶液,则Y电极的材料是
(5)若要用电镀方法在铁表面镀一层金属银,应该选择的的方案是___________。
 填字母编号
填字母编号
| 方案 | X | Y |  溶液 溶液 |
| A | 银 | 石墨 | AgNO3 |
| B | 银 | 铁 |  |
| C | 铁 | 银 | 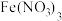 |
| D | 铁 | 银 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
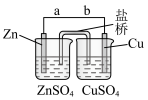
5 . 某学生利用下面实验装置探究盐桥式原电池的工作原理。
(1)锌电极为电池的___________ 极,电极上发生的是___________ 反应(“氧化”或“还原”),电极反应式为___________ ;铜电极为电池的___________ 极,电极上发生的是___________ 反应(“氧化”或“还原”),电极反应式为___________ 。
(2)导线中电子流向由___________ 流向___________ (用a、b表示)。
(3)若装置中铜电极的质量增加0.64g,则导线中转移的电子的物质的量为___________ ;
(4)若ZnSO4溶液中含有杂质Cu2+,会加速Zn电极的腐蚀、还可能导致电流在较短时间内衰减。欲除去Cu2+,最好选用下列试剂中的___________(填代号)。
(5)反应一段时间后右侧烧杯中Cu2+浓度是___________ (填增大,减小或不变)。
(1)锌电极为电池的
(2)导线中电子流向由
(3)若装置中铜电极的质量增加0.64g,则导线中转移的电子的物质的量为
(4)若ZnSO4溶液中含有杂质Cu2+,会加速Zn电极的腐蚀、还可能导致电流在较短时间内衰减。欲除去Cu2+,最好选用下列试剂中的___________(填代号)。
| A.NaOH | B.Zn | C.Fe | D.H2SO4 |
(5)反应一段时间后右侧烧杯中Cu2+浓度是
您最近一年使用:0次
6 . 现有含AgBr的饱和溶液:
(1)AgBr的沉淀溶解平衡方程式:___________ ,Ksp的表达式是___________ ;
(2)加入固体AgNO3,则c(Ag+)___________ (填“变大”、“变小”或“不变”,下同);
(3)加入更多的AgBr固体,则c(Ag+)___________ ;
(1)AgBr的沉淀溶解平衡方程式:
(2)加入固体AgNO3,则c(Ag+)
(3)加入更多的AgBr固体,则c(Ag+)
您最近一年使用:0次
7 . 回答下列问题:
(1)FeCl3的水溶液呈___________ (填“酸”“中”或“碱”)性,原因是___________ (用离子方程式表示);实验室在配制FeCl3溶液时,常将FeCl3固体先溶于较浓的盐酸中,然后再用蒸馏水将其稀释到所需的浓度,以___________ (填“促进”或“抑制”)其水解。
(2)将FeCl3溶液蒸干、灼烧,最后得到的主要固体产物是___________ 。
(1)FeCl3的水溶液呈
(2)将FeCl3溶液蒸干、灼烧,最后得到的主要固体产物是
您最近一年使用:0次
解题方法
8 . 常温下:
(1)在0.001 mol/L HCl溶液中,c(H+)=___________ ,c(OH-)=___________ 。
(2)在0.001 mol/L NaOH溶液中,c(H+)=___________ ,由水电离出的c(H+)=___________ 。
(3)在pH=3的NH4Cl溶液中,水电离出的c(H+)=___________ 。
(1)在0.001 mol/L HCl溶液中,c(H+)=
(2)在0.001 mol/L NaOH溶液中,c(H+)=
(3)在pH=3的NH4Cl溶液中,水电离出的c(H+)=
您最近一年使用:0次
9 . 完成下列问题。
(1)4g硫粉在 中完全燃烧生成
中完全燃烧生成 气体,放出37kJ的热量,写出S燃烧的热化学方程式
气体,放出37kJ的热量,写出S燃烧的热化学方程式____ 。
(2)某反应的反应物A浓度在5min内由6mol·L-1变成了2mol·L-1,则v(A)=_______ 。
(3)反应A(g)+B(s)⇌C(g) ΔH<0,在其他条件不变时,改变其中一个条件,则生成C的速率(填“增大”、“不变”、“减小”):
①升温_______ ;
②增大压强_______ ;
③加正催化剂_______ 。
(4)氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+6C(s)+2N2(g) Si3N4(s)+6CO(g)。
Si3N4(s)+6CO(g)。
①该反应的平衡常数表达式为K=_______ ;
②若知上述反应为吸热反应,升高温度,其平衡常数值_______ (填“增大”、“减小”或“不变”)。
(5)在密闭容器中的可逆反应CO(g)+NO2(g)⇌CO2(g)+NO(g) ΔH<0。达到平衡后:
①扩大容器体积,平衡_______ 移动(填“正向”、“逆向”、“不”),c(NO2)将_______ (填“增大”、“减小”、“不变”),反应混合物的颜色将变_______ (填“深”、“浅”、“不变”)。
②升高温度平衡_______ 移动(填“正向”、“逆向”、“不”),
(6)①水的离子积常数Kw表达式:_______ 常温下,水的离子积常数Kw=_______ mol2·L-2。
②影响因素:i.水的离子积常数只受_______ 的影响,ii.升高温度,Kw_______ 。
(7)常温下,溶液的酸碱性与pH的关系是:pH=7,溶液呈_______ ,pH越小,溶液的酸性越_______ ,溶液的碱性越_______ ,pH的适用范围是_______ 。
(8) 水解的离子方程式为
水解的离子方程式为_______ 。
(1)4g硫粉在
 中完全燃烧生成
中完全燃烧生成 气体,放出37kJ的热量,写出S燃烧的热化学方程式
气体,放出37kJ的热量,写出S燃烧的热化学方程式(2)某反应的反应物A浓度在5min内由6mol·L-1变成了2mol·L-1,则v(A)=
(3)反应A(g)+B(s)⇌C(g) ΔH<0,在其他条件不变时,改变其中一个条件,则生成C的速率(填“增大”、“不变”、“减小”):
①升温
②增大压强
③加正催化剂
(4)氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+6C(s)+2N2(g)
 Si3N4(s)+6CO(g)。
Si3N4(s)+6CO(g)。①该反应的平衡常数表达式为K=
②若知上述反应为吸热反应,升高温度,其平衡常数值
(5)在密闭容器中的可逆反应CO(g)+NO2(g)⇌CO2(g)+NO(g) ΔH<0。达到平衡后:
①扩大容器体积,平衡
②升高温度平衡
(6)①水的离子积常数Kw表达式:
②影响因素:i.水的离子积常数只受
(7)常温下,溶液的酸碱性与pH的关系是:pH=7,溶液呈
(8)
 水解的离子方程式为
水解的离子方程式为
您最近一年使用:0次
解题方法
10 . 如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。请按要求回答相关问题:
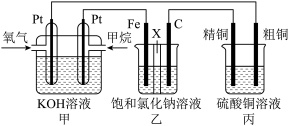
(1)甲是燃料电池,通入甲烷的电极作_______ 极(填“正”或“负”),电极反应式为_______ 。
(2)乙是_______ 池,石墨(C)作_______ 极(填“阴”或“阳”),发生_______ 反应(填“氧化”或“还原”),电极反应式为_______ 。
(3)①丙中粗铜作_______ 极(填“阴”或“阳”);
②电解一段时间后硫酸铜溶液中的Cu2+会_______ (填“增大”或“减小”或“不变”);
③若在标准状况下,有2.24L氧气参加反应,丙装置中析出精铜的质量为_______ g。

(1)甲是燃料电池,通入甲烷的电极作
(2)乙是
(3)①丙中粗铜作
②电解一段时间后硫酸铜溶液中的Cu2+会
③若在标准状况下,有2.24L氧气参加反应,丙装置中析出精铜的质量为
您最近一年使用:0次



