1 . 已知: ,
, 。25℃时,向
。25℃时,向 溶液中滴加
溶液中滴加 的NaOH溶液。溶液中
的NaOH溶液。溶液中 与加入NaOH溶液体积的关系如图所示。下列说法
与加入NaOH溶液体积的关系如图所示。下列说法错误 的是
 ,
, 。25℃时,向
。25℃时,向 溶液中滴加
溶液中滴加 的NaOH溶液。溶液中
的NaOH溶液。溶液中 与加入NaOH溶液体积的关系如图所示。下列说法
与加入NaOH溶液体积的关系如图所示。下列说法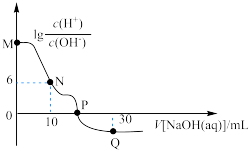
A.M点溶液中存在: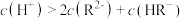 |
B.25℃时. 的水解常数 的水解常数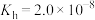 |
| C.P点加入NaOH溶液的体积小于20mL |
D.Q点溶液中存在: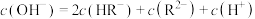 |
您最近一年使用:0次
2 . 回答下列问题:
(1)实验室在配制 的溶液时,常将
的溶液时,常将 固体先溶于较浓的硝酸中,再用蒸馏水稀释到所需的浓度,其目是
固体先溶于较浓的硝酸中,再用蒸馏水稀释到所需的浓度,其目是________________ 。
(2)将 溶液蒸干再灼烧,最后得到的主要固体物质是
溶液蒸干再灼烧,最后得到的主要固体物质是______ (写化学式,下同);将 溶液蒸干再灼烧,最后得到的主要固体物质是
溶液蒸干再灼烧,最后得到的主要固体物质是______ 。
(3)已知 晶体在空气中加热时,释放部分结晶水,同时生成
晶体在空气中加热时,释放部分结晶水,同时生成 (碱式氯化镁)或
(碱式氯化镁)或 ,下列是关于
,下列是关于 的综合应用:
的综合应用:______ 环境中加热。
(4)某小组同学探究饱和 和
和 溶液混合反应的实验,打开活塞向烧瓶中的
溶液混合反应的实验,打开活塞向烧瓶中的 加入饱和
加入饱和 溶液,产生大量的白色胶状沉淀,出现上述现象的原因是
溶液,产生大量的白色胶状沉淀,出现上述现象的原因是__________ (请用反应的离子方程式表示)。
(1)实验室在配制
 的溶液时,常将
的溶液时,常将 固体先溶于较浓的硝酸中,再用蒸馏水稀释到所需的浓度,其目是
固体先溶于较浓的硝酸中,再用蒸馏水稀释到所需的浓度,其目是(2)将
 溶液蒸干再灼烧,最后得到的主要固体物质是
溶液蒸干再灼烧,最后得到的主要固体物质是 溶液蒸干再灼烧,最后得到的主要固体物质是
溶液蒸干再灼烧,最后得到的主要固体物质是(3)已知
 晶体在空气中加热时,释放部分结晶水,同时生成
晶体在空气中加热时,释放部分结晶水,同时生成 (碱式氯化镁)或
(碱式氯化镁)或 ,下列是关于
,下列是关于 的综合应用:
的综合应用: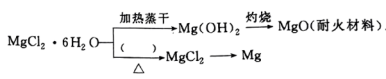
(4)某小组同学探究饱和
 和
和 溶液混合反应的实验,打开活塞向烧瓶中的
溶液混合反应的实验,打开活塞向烧瓶中的 加入饱和
加入饱和 溶液,产生大量的白色胶状沉淀,出现上述现象的原因是
溶液,产生大量的白色胶状沉淀,出现上述现象的原因是
您最近一年使用:0次
名校
3 . 回答下列问题
(1)制玻璃的原材料是石英、纯碱和大理石,写出碳酸钠在玻璃熔炉中反应的化学方程式为___________ 。建筑装饰中常在玻璃上雕刻图案或花纹,用于刻蚀玻璃的化学试剂是___________ (填化学式)。往Na2SiO3溶液中通入足量CO2气体发生的化学方程式为:___________ 。用Na2SiO3水溶液浸泡过的棉花不易燃烧,说明Na2SiO3可用作___________ 。
(2)① 是一种无色气体,在空气中能发生爆炸性自燃生成固态
是一种无色气体,在空气中能发生爆炸性自燃生成固态 和液态
和液态 。已知室温下
。已知室温下 自燃放出热量713.5kJ。写出室温下
自燃放出热量713.5kJ。写出室温下 自燃的热化学方程式
自燃的热化学方程式___________ 。
②在25℃、101kPa下,一定质量的无水乙醇(C2H6O)完全燃烧时放出热量 ,燃烧生成的
,燃烧生成的 用过量饱和石灰水吸收可得
用过量饱和石灰水吸收可得 沉淀,则在此条件下,1mol乙醇的燃烧热方程式为:
沉淀,则在此条件下,1mol乙醇的燃烧热方程式为:___________ 。
(3)某温度时,在2L的密闭容器中,X、Y、Z(均为气体)的物质的量随时间的变化曲线如图所示。
①由图中所给数据进行分析,该反应的化学方程式为___________ 。
②反应从开始至2min,用Z的浓度变化表示的平均反应速率v(Z)=___________ 。
(1)制玻璃的原材料是石英、纯碱和大理石,写出碳酸钠在玻璃熔炉中反应的化学方程式为
(2)①
 是一种无色气体,在空气中能发生爆炸性自燃生成固态
是一种无色气体,在空气中能发生爆炸性自燃生成固态 和液态
和液态 。已知室温下
。已知室温下 自燃放出热量713.5kJ。写出室温下
自燃放出热量713.5kJ。写出室温下 自燃的热化学方程式
自燃的热化学方程式②在25℃、101kPa下,一定质量的无水乙醇(C2H6O)完全燃烧时放出热量
 ,燃烧生成的
,燃烧生成的 用过量饱和石灰水吸收可得
用过量饱和石灰水吸收可得 沉淀,则在此条件下,1mol乙醇的燃烧热方程式为:
沉淀,则在此条件下,1mol乙醇的燃烧热方程式为:(3)某温度时,在2L的密闭容器中,X、Y、Z(均为气体)的物质的量随时间的变化曲线如图所示。

①由图中所给数据进行分析,该反应的化学方程式为
②反应从开始至2min,用Z的浓度变化表示的平均反应速率v(Z)=
您最近一年使用:0次
解题方法
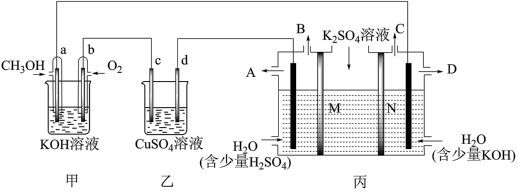
4 . 当今社会的主题之一:发展经济,节能减排。而燃料电池因其无污染,且原料来源广可再生被人们青睐,广泛应用于生产、生活、科学研究中,现有如下图所示装置,所有电极均为Pt,请按要求回答下列问题:______ (填“原电池”或“电解池”)。
(2)乙池中c极的电极反应______ 。
(3)若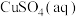 足够,电解一段时间后,要恢复到原来的状态,则可加入____。
足够,电解一段时间后,要恢复到原来的状态,则可加入____。
(4)现用丙装置电解硫酸钾溶液制取氢气、氧气、硫酸和氢氧化钾,其中M、N为离子交换膜,只允许某些离子通过,则A出口导出的溶液溶质为_______ (写化学式),M为____ 离子交换膜(填“阴”或“阳”)。
(2)乙池中c极的电极反应
(3)若
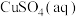 足够,电解一段时间后,要恢复到原来的状态,则可加入____。
足够,电解一段时间后,要恢复到原来的状态,则可加入____。| A.CuO | B. | C. | D. |
(4)现用丙装置电解硫酸钾溶液制取氢气、氧气、硫酸和氢氧化钾,其中M、N为离子交换膜,只允许某些离子通过,则A出口导出的溶液溶质为
您最近一年使用:0次
解题方法
5 . 常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
请回答:
(1)从①组情况分析,HA是___________ (填“强酸”或“弱酸”)。
(2)②组情况表明,c___________ (填“大于”、“小于”或“等于”)0.2mol/L。混合液中离子浓度c(A-)与c(Na+)的大小关系是:c(A-)___________ c(Na+) (“大于”、“小于”或“等于”)。
(3)从③组实验结果分析,说明HA的电离程度___________ (填“大于”、“小于”或“等于”)NaA的水解程度。
(4)①组实验所得混合溶液中由水电离出的c(OH-)=___________ mol∙L-1。
| 实验编号 | HA物质的量浓度(mol/L) | NaOH物质的量浓度(mol/L) | 混合溶液的 pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH<7 |
(1)从①组情况分析,HA是
(2)②组情况表明,c
(3)从③组实验结果分析,说明HA的电离程度
(4)①组实验所得混合溶液中由水电离出的c(OH-)=
您最近一年使用:0次
6 . 水中存在电离平衡:H2O H++OH-。若在水中分别加入下列各物质:
H++OH-。若在水中分别加入下列各物质:
①NaOH(s) ②NH4Cl(s) ③Na2CO3(s) ④CH3COOH(l) ⑤K2SO4(s),试回答下列问题:
(1)能使水的电离平衡向左移动的是___________ ,不发生移动的是___________ 。(用序号填空)
(2)溶液呈酸性的是___________ ,溶液呈碱性的是___________ 。(用序号填空)
(3)能促进水的电离,且溶液pH>7的是___________ 。(用序号填空)
(4)将0.1mol CH3COOH溶于水制成1L溶液,此溶液的物质的量浓度为0.1mol/L,经测定溶液中c(CH3COO-)为1.4×10-3mol∙L-1,此温度下醋酸的电离常数Ka=___________ ,温度升高,Ka将___________ (填“变大”、“不变”或“变小”)。
(5)向 溶液中滴入酚酞试液,观察到的现象是
溶液中滴入酚酞试液,观察到的现象是___________ ,若微热溶液,观察到的现象是___________ ,由此证明碳酸钠的水解是___________ (填“吸热”或“放热”)反应。 溶液中
溶液中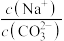
___________ 2(填“大于”或“小于”),能使其比值接近2的措施是___________ (填序号)。
①加入适量盐酸 ②加入适量NaOH固体 ③加入适量KOH固体 ④加热
 H++OH-。若在水中分别加入下列各物质:
H++OH-。若在水中分别加入下列各物质:①NaOH(s) ②NH4Cl(s) ③Na2CO3(s) ④CH3COOH(l) ⑤K2SO4(s),试回答下列问题:
(1)能使水的电离平衡向左移动的是
(2)溶液呈酸性的是
(3)能促进水的电离,且溶液pH>7的是
(4)将0.1mol CH3COOH溶于水制成1L溶液,此溶液的物质的量浓度为0.1mol/L,经测定溶液中c(CH3COO-)为1.4×10-3mol∙L-1,此温度下醋酸的电离常数Ka=
(5)向
 溶液中滴入酚酞试液,观察到的现象是
溶液中滴入酚酞试液,观察到的现象是 溶液中
溶液中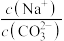
①加入适量盐酸 ②加入适量NaOH固体 ③加入适量KOH固体 ④加热
您最近一年使用:0次
7 . Ⅰ.
(1) 的水溶液呈
的水溶液呈_____ (填“酸”、“中”、“碱”)性,常温时的
_____ 7(填“>”“=”、“<”),实验室在配制 的溶液时,常将
的溶液时,常将 固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以
固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以_____ (填“促进”、“抑制”)其水解。
Ⅱ.常温下有浓度均为 的四种溶液:①
的四种溶液:① 、②
、② 、③HCl、④
、③HCl、④ 。
。
(2)有人称溶液①是油污的“清道夫”,原因是_____ (用离子方程式解释)。
(3)溶液②中,
_____  。
。
(4)将10mL溶液③加水稀释至100mL,则此时溶液中由水电离出的
_____ 。
(5)取④的溶液 ,向其中加入含
,向其中加入含 的溶液后呈中性,则
的溶液后呈中性,则 电离平衡常数
电离平衡常数
_____ 。
(1)
 的水溶液呈
的水溶液呈
 的溶液时,常将
的溶液时,常将 固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以
固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以Ⅱ.常温下有浓度均为
 的四种溶液:①
的四种溶液:① 、②
、② 、③HCl、④
、③HCl、④ 。
。(2)有人称溶液①是油污的“清道夫”,原因是
(3)溶液②中,

 。
。(4)将10mL溶液③加水稀释至100mL,则此时溶液中由水电离出的

(5)取④的溶液
 ,向其中加入含
,向其中加入含 的溶液后呈中性,则
的溶液后呈中性,则 电离平衡常数
电离平衡常数
您最近一年使用:0次
解题方法
8 . 回答下列问题。
(1)已知草酸是二元弱酸,常温下测得 的
的 的
的 为4.8,则此
为4.8,则此 溶液中
溶液中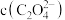
___________ (填“大于”“小于”或“等于”) 。
。
(2)泡沫灭火器内装有 饱和溶液,该溶液呈碱性的原因是
饱和溶液,该溶液呈碱性的原因是___________ (用离子方程式表示);灭火器内另一容器中装有 溶液,该溶液呈酸性的原因是
溶液,该溶液呈酸性的原因是___________ (用离子方程式表示)。当意外失火时,将泡沫灭火器倒过来摇动即可使药液混合,喷出大量的白色泡沫,阻止火势蔓延,其相关的离子方程式为___________ 。
(3)常温时的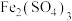 的水溶液
的水溶液
___________ 7(填“>”、“=”、“<”)。原因是___________ (用离子方程式表示)。配制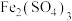 的溶液时,常在溶液中加入一些
的溶液时,常在溶液中加入一些___________ 以抑制其水解。
(4)氯化铝溶液蒸干、灼烧后得到的固体物质是___________ 。
(1)已知草酸是二元弱酸,常温下测得
 的
的 的
的 为4.8,则此
为4.8,则此 溶液中
溶液中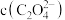
 。
。(2)泡沫灭火器内装有
 饱和溶液,该溶液呈碱性的原因是
饱和溶液,该溶液呈碱性的原因是 溶液,该溶液呈酸性的原因是
溶液,该溶液呈酸性的原因是(3)常温时的
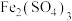 的水溶液
的水溶液
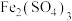 的溶液时,常在溶液中加入一些
的溶液时,常在溶液中加入一些(4)氯化铝溶液蒸干、灼烧后得到的固体物质是
您最近一年使用:0次
9 . 按要求填空
(1) 是一种无色气体,在空气中能发生爆炸性自燃生成固态
是一种无色气体,在空气中能发生爆炸性自燃生成固态 和液态
和液态 。已知室温下
。已知室温下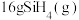 自燃放出热量713.5kJ。写出室温下
自燃放出热量713.5kJ。写出室温下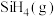 自燃的热化学方程式
自燃的热化学方程式__________ 。
(2)在101kPa时, 在
在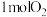 中完全燃烧生成2mol液态水,放出571.6kJ的热量,
中完全燃烧生成2mol液态水,放出571.6kJ的热量, 的燃烧热为
的燃烧热为__________ ,表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为__________ 。
(3)在25℃、101kPa下,一定质量的无水乙醇完全燃烧时放出热量 ,燃烧生成的
,燃烧生成的 用过量饱和石灰水吸收可得
用过量饱和石灰水吸收可得 沉淀,则在此条件下,1mol乙醇完全燃烧的
沉淀,则在此条件下,1mol乙醇完全燃烧的
__________ kJ/mol。
(4)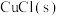 与
与 反应生成
反应生成 和一种黑色固体。在25℃、101kPa下,已知该反应每转移
和一种黑色固体。在25℃、101kPa下,已知该反应每转移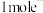 ,放热44.5kJ,该反应的热化学方程式
,放热44.5kJ,该反应的热化学方程式__________ 。
(5)已知反应:

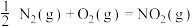



则反应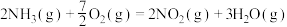 的
的 为
为__________ kJ/mol(用 ,
, ,
, 表示)
表示)
(1)
 是一种无色气体,在空气中能发生爆炸性自燃生成固态
是一种无色气体,在空气中能发生爆炸性自燃生成固态 和液态
和液态 。已知室温下
。已知室温下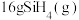 自燃放出热量713.5kJ。写出室温下
自燃放出热量713.5kJ。写出室温下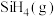 自燃的热化学方程式
自燃的热化学方程式(2)在101kPa时,
 在
在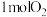 中完全燃烧生成2mol液态水,放出571.6kJ的热量,
中完全燃烧生成2mol液态水,放出571.6kJ的热量, 的燃烧热为
的燃烧热为 燃烧热的热化学方程式为
燃烧热的热化学方程式为(3)在25℃、101kPa下,一定质量的无水乙醇完全燃烧时放出热量
 ,燃烧生成的
,燃烧生成的 用过量饱和石灰水吸收可得
用过量饱和石灰水吸收可得 沉淀,则在此条件下,1mol乙醇完全燃烧的
沉淀,则在此条件下,1mol乙醇完全燃烧的
(4)
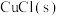 与
与 反应生成
反应生成 和一种黑色固体。在25℃、101kPa下,已知该反应每转移
和一种黑色固体。在25℃、101kPa下,已知该反应每转移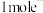 ,放热44.5kJ,该反应的热化学方程式
,放热44.5kJ,该反应的热化学方程式(5)已知反应:


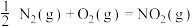



则反应
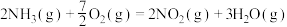 的
的 为
为 ,
, ,
, 表示)
表示)
您最近一年使用:0次
名校
解题方法
10 . 磷的含氧酸具有重要的性质和应用。
(1) 是二元弱酸,某温度下,
是二元弱酸,某温度下, 的
的 溶液
溶液 ,即溶液中
,即溶液中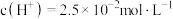 。求该温度下
。求该温度下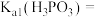
_______ 。( 的第二步电离忽略不计,结果用科学记数法表示,保留两位有效数字)
的第二步电离忽略不计,结果用科学记数法表示,保留两位有效数字)
(2) 是三元中强酸,
是三元中强酸, 时,
时, 与
与 溶液反应,反应混合物中含磷各微粒的分布分数(平衡时某微粒的浓度占微粒浓度之和的分数)与
溶液反应,反应混合物中含磷各微粒的分布分数(平衡时某微粒的浓度占微粒浓度之和的分数)与 的关系如图所示:
的关系如图所示:
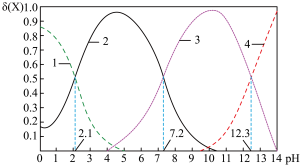
① 溶液显碱性,原因是
溶液显碱性,原因是________ ,若向溶液中加入足量的 溶液,溶液则显酸性,其原因是
溶液,溶液则显酸性,其原因是________ (用离子方程式表示)。
② 时,溶液中的
时,溶液中的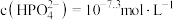 ,则
,则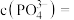
______  。
。
③ 时,溶液中由水电离出的
时,溶液中由水电离出的
______  。
。
④已知: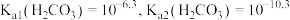 ,写出足量碳酸钠与
,写出足量碳酸钠与 反应的化学方程式:
反应的化学方程式:_______ 。
⑤以酚䣭为指示剂,当溶液由无色变为浅红色时,写出发生主要反应的离子方程:______ 。
⑥ 时,溶液中的电荷守恒关系为
时,溶液中的电荷守恒关系为_________ 。
(1)
 是二元弱酸,某温度下,
是二元弱酸,某温度下, 的
的 溶液
溶液 ,即溶液中
,即溶液中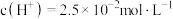 。求该温度下
。求该温度下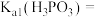
 的第二步电离忽略不计,结果用科学记数法表示,保留两位有效数字)
的第二步电离忽略不计,结果用科学记数法表示,保留两位有效数字)(2)
 是三元中强酸,
是三元中强酸, 时,
时, 与
与 溶液反应,反应混合物中含磷各微粒的分布分数(平衡时某微粒的浓度占微粒浓度之和的分数)与
溶液反应,反应混合物中含磷各微粒的分布分数(平衡时某微粒的浓度占微粒浓度之和的分数)与 的关系如图所示:
的关系如图所示:
①
 溶液显碱性,原因是
溶液显碱性,原因是 溶液,溶液则显酸性,其原因是
溶液,溶液则显酸性,其原因是②
 时,溶液中的
时,溶液中的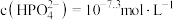 ,则
,则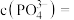
 。
。③
 时,溶液中由水电离出的
时,溶液中由水电离出的
 。
。④已知:
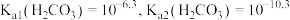 ,写出足量碳酸钠与
,写出足量碳酸钠与 反应的化学方程式:
反应的化学方程式:⑤以酚䣭为指示剂,当溶液由无色变为浅红色时,写出发生主要反应的离子方程:
⑥
 时,溶液中的电荷守恒关系为
时,溶液中的电荷守恒关系为
您最近一年使用:0次



