名校
1 . 氧化还原反应在生活、生产与科学实验中有重要作用。
回答下列问题:
(1)亚硝酸钠( )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。
①误食 会导致入体血红蛋白中的
会导致入体血红蛋白中的 转化为
转化为 而中毒,该过程中
而中毒,该过程中 发生反应
发生反应_____ (填“氧化”或“还原”,下同),服用维生素 可将
可将 转化为
转化为 从而解毒,这说明维生素
从而解毒,这说明维生素 具有
具有________ 性。
②实验室可利用反应 制备少量
制备少量 ,若反应中有
,若反应中有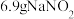 固体生成,则转移电子的物质的量为
固体生成,则转移电子的物质的量为________  。
。
(2) 、
、 是常用的氧化剂。
是常用的氧化剂。
①已知: 、
、 、
、 、
、 和一些未知物组成一个氧化还原反应,其中
和一些未知物组成一个氧化还原反应,其中 是氧化产物,则还原性:
是氧化产物,则还原性:
_________  (填“
(填“ ”或“
”或“ ”)。
”)。
②请结合①中反应,写出一个能证明氧化性 的离子方程式:
的离子方程式:___________________ 。
(3)高铁酸钾( )是一种高效多功能的新型非氯绿色消毒剂。
)是一种高效多功能的新型非氯绿色消毒剂。
①工业上可通过次氯酸盐氧化法制备 :
: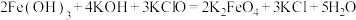 。请写出该反应的离子方程式并用双线桥法标出电子转移的方向与数目:
。请写出该反应的离子方程式并用双线桥法标出电子转移的方向与数目:___________________ 。
② 净水原理如图所示:
净水原理如图所示:

若过程 中转移
中转移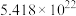 个电子,需
个电子,需____________ 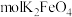 。
。
③向 溶液中加入适量的饱和
溶液中加入适量的饱和 溶液,有
溶液,有 析出,写出该反应的离子方程式:
析出,写出该反应的离子方程式:____________ 。
回答下列问题:
(1)亚硝酸钠(
 )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。①误食
 会导致入体血红蛋白中的
会导致入体血红蛋白中的 转化为
转化为 而中毒,该过程中
而中毒,该过程中 发生反应
发生反应 可将
可将 转化为
转化为 从而解毒,这说明维生素
从而解毒,这说明维生素 具有
具有②实验室可利用反应
 制备少量
制备少量 ,若反应中有
,若反应中有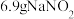 固体生成,则转移电子的物质的量为
固体生成,则转移电子的物质的量为 。
。(2)
 、
、 是常用的氧化剂。
是常用的氧化剂。①已知:
 、
、 、
、 、
、 和一些未知物组成一个氧化还原反应,其中
和一些未知物组成一个氧化还原反应,其中 是氧化产物,则还原性:
是氧化产物,则还原性:
 (填“
(填“ ”或“
”或“ ”)。
”)。②请结合①中反应,写出一个能证明氧化性
 的离子方程式:
的离子方程式:(3)高铁酸钾(
 )是一种高效多功能的新型非氯绿色消毒剂。
)是一种高效多功能的新型非氯绿色消毒剂。①工业上可通过次氯酸盐氧化法制备
 :
: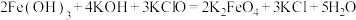 。请写出该反应的离子方程式并用双线桥法标出电子转移的方向与数目:
。请写出该反应的离子方程式并用双线桥法标出电子转移的方向与数目:②
 净水原理如图所示:
净水原理如图所示:
若过程
 中转移
中转移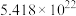 个电子,需
个电子,需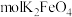 。
。③向
 溶液中加入适量的饱和
溶液中加入适量的饱和 溶液,有
溶液,有 析出,写出该反应的离子方程式:
析出,写出该反应的离子方程式:
您最近一年使用:0次
名校
解题方法
2 .  广泛用于纸浆漂白、杀菌消毒等领域,因
广泛用于纸浆漂白、杀菌消毒等领域,因 消毒效果好、不产生致癌物或诱变剂,已被广泛应用于污水处理工程。一种制备
消毒效果好、不产生致癌物或诱变剂,已被广泛应用于污水处理工程。一种制备 的方法为
的方法为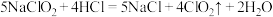 。下列说法错误的是
。下列说法错误的是
A.该反应能说明 是酸性氧化物 是酸性氧化物 |
B.该反应的离子方程式为 |
C.该反应还原产物与氧化产物的物质的量之比为 |
D.当还原产物均为 时,等质量的 时,等质量的 的氧化能力是 的氧化能力是 的2.63倍 的2.63倍 |
您最近一年使用:0次
名校
3 . 氯气可用于工业制盐酸。氢气在氯气中燃烧生成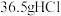 时,下列说法正确的是
时,下列说法正确的是
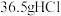 时,下列说法正确的是
时,下列说法正确的是A.有 氧化剂被还原 氧化剂被还原 |
B.有 氯元素被氧化 氯元素被氧化 |
C.反应过程中有 电子转移 电子转移 |
D.有 氢元素发生还原反应 氢元素发生还原反应 |
您最近一年使用:0次
4 . Ⅰ.钠是典型的金属元素,钠的化合物具有广泛的用途。请回答以下问题:
(1)15.6g 溶于水中配制成2L的溶液,其中
溶于水中配制成2L的溶液,其中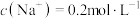 ,则X的摩尔质量为
,则X的摩尔质量为______ 。
(2) 易溶于水且溶解时吸热,有咸味,遇酸易放出气体,人误食会中毒.已知
易溶于水且溶解时吸热,有咸味,遇酸易放出气体,人误食会中毒.已知 能发生如下反应:
能发生如下反应: 。上述反应中HI在反应中体现的性质为
。上述反应中HI在反应中体现的性质为______ 。标况下,每生成11.2L的NO气体,转移的电子数约为______ 个。
(3)某届奥运会期间,由于工作人员将84消毒液(有效成分NaClO)与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与 反应产生
反应产生 促进藻类快速生长。该反应说明氧化性:NaClO
促进藻类快速生长。该反应说明氧化性:NaClO______  (填“>”或“<”);当参加反应的NaClO和
(填“>”或“<”);当参加反应的NaClO和 的个数比为1∶1时,该反应的还原产物为
的个数比为1∶1时,该反应的还原产物为______ (填字母序号)。
A. B.
B. C.
C. D.NaCl E.NaClO
D.NaCl E.NaClO
Ⅱ.化工专家侯德榜发明的侯氏制碱法为我国经济发展做出了重要贡献。侯氏制碱法的工艺流程图如下:

(4)工艺流程中“碳酸化”时发生主要反应的化学方程式为______ 。
(5)流程中可循环利用的物质为______ (填化学式)。
(6)产品分析:把5.8g含有少量NaCl杂质的 样品与足量稀硫酸反应后,产生的气体先通过足量浓硫酸,再通过足量
样品与足量稀硫酸反应后,产生的气体先通过足量浓硫酸,再通过足量 ,
, 增重1.4g,则产品纯度为
增重1.4g,则产品纯度为______ (用百分数表示,保留到小数点后1位)。
(1)15.6g
 溶于水中配制成2L的溶液,其中
溶于水中配制成2L的溶液,其中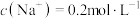 ,则X的摩尔质量为
,则X的摩尔质量为(2)
 易溶于水且溶解时吸热,有咸味,遇酸易放出气体,人误食会中毒.已知
易溶于水且溶解时吸热,有咸味,遇酸易放出气体,人误食会中毒.已知 能发生如下反应:
能发生如下反应: 。上述反应中HI在反应中体现的性质为
。上述反应中HI在反应中体现的性质为(3)某届奥运会期间,由于工作人员将84消毒液(有效成分NaClO)与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与
 反应产生
反应产生 促进藻类快速生长。该反应说明氧化性:NaClO
促进藻类快速生长。该反应说明氧化性:NaClO (填“>”或“<”);当参加反应的NaClO和
(填“>”或“<”);当参加反应的NaClO和 的个数比为1∶1时,该反应的还原产物为
的个数比为1∶1时,该反应的还原产物为A.
 B.
B. C.
C. D.NaCl E.NaClO
D.NaCl E.NaClOⅡ.化工专家侯德榜发明的侯氏制碱法为我国经济发展做出了重要贡献。侯氏制碱法的工艺流程图如下:

(4)工艺流程中“碳酸化”时发生主要反应的化学方程式为
(5)流程中可循环利用的物质为
(6)产品分析:把5.8g含有少量NaCl杂质的
 样品与足量稀硫酸反应后,产生的气体先通过足量浓硫酸,再通过足量
样品与足量稀硫酸反应后,产生的气体先通过足量浓硫酸,再通过足量 ,
, 增重1.4g,则产品纯度为
增重1.4g,则产品纯度为
您最近一年使用:0次
5 .  常用作食盐中的补碘剂,可用“氯酸钾四化法”制备,该方法的第一步反应为:
常用作食盐中的补碘剂,可用“氯酸钾四化法”制备,该方法的第一步反应为: 。下列说法正确的是
。下列说法正确的是
 常用作食盐中的补碘剂,可用“氯酸钾四化法”制备,该方法的第一步反应为:
常用作食盐中的补碘剂,可用“氯酸钾四化法”制备,该方法的第一步反应为: 。下列说法正确的是
。下列说法正确的是A.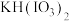 为还原产物 为还原产物 |
B.产生5.6L(标准状况) 时,转移5mol电子 时,转移5mol电子 |
C.可用澄清石灰水吸收反应产生的 制备漂白粉 制备漂白粉 |
| D.反应中氧化剂和还原剂的物质的量之比为6∶11 |
您最近一年使用:0次
6 . 用NA表示阿伏加德罗常数的值,下列叙述正确的是
A.标准状况下,22.4L 与 与 的混合气体,总电子数为10NA 的混合气体,总电子数为10NA |
B.78g 中含有的离子总数为4 NA 中含有的离子总数为4 NA |
C.11.2L的 和CO混合气体,原子总数为NA 和CO混合气体,原子总数为NA |
D.1mol 与足量的Fe充分反应,转移电子数为3 NA 与足量的Fe充分反应,转移电子数为3 NA |
您最近一年使用:0次
解题方法
7 . 利用 和溴酸盐溶液制备高溴酸盐的反应为
和溴酸盐溶液制备高溴酸盐的反应为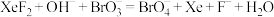 (未配平).下列说法正确的是
(未配平).下列说法正确的是
 和溴酸盐溶液制备高溴酸盐的反应为
和溴酸盐溶液制备高溴酸盐的反应为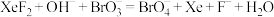 (未配平).下列说法正确的是
(未配平).下列说法正确的是A.氧化剂为 ,还原产物为 ,还原产物为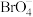 | B.若生成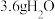 ,则该反应中转移 ,则该反应中转移 电子 电子 |
C. 中各原子均满足8电子稳定结构 中各原子均满足8电子稳定结构 | D. 中心原子的价层电子对数为2,杂化方式为 中心原子的价层电子对数为2,杂化方式为 |
您最近一年使用:0次
8 . 已知反应(1)、(2)分别是从海藻灰和智利硝石中提取碘的主要反应:
(1)2NaI+MnO2+3H2SO4=2NaHSO4+MnSO4+2H2O+I2
(2)2NaIO3+5NaHSO3=2Na2SO4+3NaHSO4+H2O+I2
下列说法正确的是
(1)2NaI+MnO2+3H2SO4=2NaHSO4+MnSO4+2H2O+I2
(2)2NaIO3+5NaHSO3=2Na2SO4+3NaHSO4+H2O+I2
下列说法正确的是
| A.两个反应中NaHSO4均为氧化产物 |
| B.I2在反应(1)中是还原产物,在反应(2)中是氧化产物 |
C.氧化性:MnO2>IO >I2 >I2 |
| D.反应(1)、(2)中生成等量的I2时转移电子数之比为1:5 |
您最近一年使用:0次
9 . 氧化还原反应是一类重要的反应,请按要求完成下列题目。
(1)对反应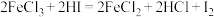 作分析,并用单线桥法标出电子转移的方向和数目:
作分析,并用单线桥法标出电子转移的方向和数目:___________ 。该反应中,___________ 是氧化产物。
(2)在一定条件下,反应 能顺利进行,对此反应的分析合理的是___________(填序号)。
能顺利进行,对此反应的分析合理的是___________(填序号)。
(3)在反应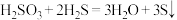 中,氧化产物与还原产物的质量比为
中,氧化产物与还原产物的质量比为___________ 。
(1)对反应
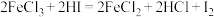 作分析,并用单线桥法标出电子转移的方向和数目:
作分析,并用单线桥法标出电子转移的方向和数目:(2)在一定条件下,反应
 能顺利进行,对此反应的分析合理的是___________(填序号)。
能顺利进行,对此反应的分析合理的是___________(填序号)。| A.该反应是置换反应 |
B.反应中 被氧化为 被氧化为 |
| C.在反应中体现了金属铜的还原性 |
D.在反应中每生成 转移 转移 电子 电子 |
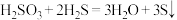 中,氧化产物与还原产物的质量比为
中,氧化产物与还原产物的质量比为
您最近一年使用:0次
名校
10 . 二级化氧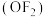 可用作极强的氧化剂和氟化剂。已知:①
可用作极强的氧化剂和氟化剂。已知:① (
( 溶液的浓度为2%),②
溶液的浓度为2%),②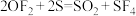 。下列说法错误的是
。下列说法错误的是
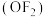 可用作极强的氧化剂和氟化剂。已知:①
可用作极强的氧化剂和氟化剂。已知:① (
( 溶液的浓度为2%),②
溶液的浓度为2%),②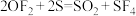 。下列说法错误的是
。下列说法错误的是A. 分子中O元素的化合价为 分子中O元素的化合价为 价 价 |
B.反应①中,每生成1个 ,转移2个电子 ,转移2个电子 |
C.反应②中, 既是氧化产物又是还原产物 既是氧化产物又是还原产物 |
D.氧化性的强弱比较: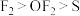 |
您最近一年使用:0次



