1 . 设 为阿伏加德罗常数的值,下列说法
为阿伏加德罗常数的值,下列说法不正确 的是
 为阿伏加德罗常数的值,下列说法
为阿伏加德罗常数的值,下列说法A.0.31g基态P原子中,含p能级电子的数目为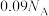 |
B.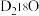 和 和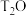 的混合物1.1g,含有的质子数为 的混合物1.1g,含有的质子数为 |
C.基态Fe原子的价层电子排布式: |
D.向FeI2的溶液中通入适量氯气,当有1molFe2+被氧化时,该反应转移的电子数至少为 |
您最近一年使用:0次
2 . 工业上,接触法制备硫酸的原理如下:
① ;②
;②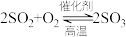 ;③
;③ 的浓硫酸吸收。
的浓硫酸吸收。
设 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是
①
 ;②
;②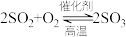 ;③
;③ 的浓硫酸吸收。
的浓硫酸吸收。设
 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是A.①中每生成 时转移电子数为 时转移电子数为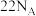 |
B.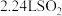 含原子数为 含原子数为 |
C.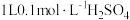 溶液含氧原子总数为 溶液含氧原子总数为 |
D.②中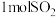 和 和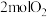 反应生成的 反应生成的 分子数为 分子数为 |
您最近一年使用:0次
3 . 分析以下A-D四个涉及H2O2的反应(未配平),填空:
A.
B.
C.
D.
(1)H2O2仅体现氧化性的是_______ ;H2O2仅体现还原性的是_______ ;H2O2既体现氧化性又体现还原性的是_______ ;H2O2既不能体现氧化性又不能体现还原性的是_______ (填代号)。
(2)D反应中1分子还原剂完全反应转移电子为_______ 个。
(3)ClO2是一种高效水处理剂,可用亚氯酸钠和稀盐酸为原料制备: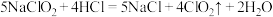 。该反应中氧化剂是
。该反应中氧化剂是_______ ,请用双线桥标明电子转移的方向和数目_______ 。
(4)海水制得的粗盐中常常含有泥沙、Ca2+、Mg2+、 等杂,粗盐提纯的步骤有:①加入过量的BaCl2溶液 ②加入过量的Na2CO3溶液 ③加入过量的NaOH溶液 ④用适量的盐酸调节溶液至中性 ⑤溶解 ⑥过滤 ⑦蒸发,正确的操作顺序是
等杂,粗盐提纯的步骤有:①加入过量的BaCl2溶液 ②加入过量的Na2CO3溶液 ③加入过量的NaOH溶液 ④用适量的盐酸调节溶液至中性 ⑤溶解 ⑥过滤 ⑦蒸发,正确的操作顺序是_______ (填选项字母)
A.⑤⑥①②③④⑥⑦ B.⑤⑥①③②⑥④⑦ C.⑤⑥②③①⑥④⑦ D.⑤⑥③①②⑥④⑦ E.⑤⑥③②①⑥④⑦
A.

B.

C.

D.

(1)H2O2仅体现氧化性的是
(2)D反应中1分子还原剂完全反应转移电子为
(3)ClO2是一种高效水处理剂,可用亚氯酸钠和稀盐酸为原料制备:
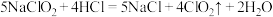 。该反应中氧化剂是
。该反应中氧化剂是(4)海水制得的粗盐中常常含有泥沙、Ca2+、Mg2+、
 等杂,粗盐提纯的步骤有:①加入过量的BaCl2溶液 ②加入过量的Na2CO3溶液 ③加入过量的NaOH溶液 ④用适量的盐酸调节溶液至中性 ⑤溶解 ⑥过滤 ⑦蒸发,正确的操作顺序是
等杂,粗盐提纯的步骤有:①加入过量的BaCl2溶液 ②加入过量的Na2CO3溶液 ③加入过量的NaOH溶液 ④用适量的盐酸调节溶液至中性 ⑤溶解 ⑥过滤 ⑦蒸发,正确的操作顺序是A.⑤⑥①②③④⑥⑦ B.⑤⑥①③②⑥④⑦ C.⑤⑥②③①⑥④⑦ D.⑤⑥③①②⑥④⑦ E.⑤⑥③②①⑥④⑦
您最近一年使用:0次
4 . 下列化学反应中电子转移的表示方法正确的是
A.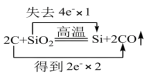 | B.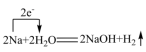 |
C.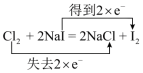 | D.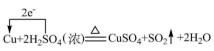 |
您最近一年使用:0次
2024-01-06更新
|
100次组卷
|
25卷引用:江西省抚州市乐安县第二中学2023-2024学年高一上学期11月期中化学试题
江西省抚州市乐安县第二中学2023-2024学年高一上学期11月期中化学试题江西省清江中学2023-2024学年高一上学期11月期中化学试题(已下线)专题03 氧化还原反应【考题猜想】(10大题型)-2023-2024学年高一化学上学期期中考点大串讲(人教版2019必修第一册)河北省衡水市武强中学2023-2024学年高一上学期期中考试化学试题江西师范大学附属中学2023-2024学年高一上学期素养测试化学试题湖北省武汉市黄陂区部分学校 2022-2023学年高一上学期期中考试化学试题湖南省常德市第一中学2023-2024学年高一上学期期中考试化学试题河北省石家庄精英中学2023-2024学年高一上学期期中考试化学试题河北省保定市唐县第一中学2023-2024学年高一上学期12月期中考试化学试题江西省宜春市上高二中2023-2024学年高一上学期第三次月考化学试题 湖北省武汉市武昌实验中学2021-2022学年高一上学期10月月考化学试题四川省广元中学2022-2023学年高一上学期第一次段考化学试题(已下线)第03讲 氧化还原反应的基本概念-【暑假自学课】2023年新高一化学暑假精品课(人教版2019必修第一册)(已下线)第10讲 氧化还原反应的基本概念-【暑假自学课】2023年新高一化学暑假精品课(鲁科版2019必修第一册)宁夏石嘴山市第三中学2023-2024学年高三上学期开学检测化学试题湖南省株洲市第二中学2023-2024学年高一上学期第二次适应性检测化学试题 辽宁省鞍山市普通高中2023-2024学年高一上学期10月月考化学(A卷)试题河北省石家庄市2023-2024学年高一上学期第二次月考化学试题天津市第五中学2023-2024学年高一上学期10月月考化学试题辽宁省大连保税区第一高级中学2023-2024学年高一上学期10月月考化学(A)试题安徽省合肥市第三中学2023-2024学年高一上学期10月份学情调研化学试题贵州省毕节市民族中学2023-2024学年上学期高一12月化学试卷黑龙江省佳木斯高中教学联合体佳木斯八中等学校联考2023-2024学年高三上学期10月月考化学试题黑龙江省大庆市大庆中学2023-2024学年高一下学期开学化学试题(已下线)第04讲 氧化还原反应的基本概念和规律(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
5 . 钠及其化合物的生产、应用,是化工生产与研究的重要组成部分。
(1) 用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备
用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备 并检验其纯度的实验流程如图所示。回答下列问题:
并检验其纯度的实验流程如图所示。回答下列问题:

① 样品加水溶解生成1.5mol气体,转移电子数为
样品加水溶解生成1.5mol气体,转移电子数为___________ 。
②样液中加入 后产生能使带火星木条复燃的气体,说明
后产生能使带火星木条复燃的气体,说明 与水反应的过程中还生成了
与水反应的过程中还生成了___________ (化学式)。
③滤液中加入 溶液产生白色沉淀,说明
溶液产生白色沉淀,说明 样品中含有
样品中含有___________ 杂质
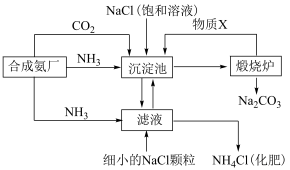
(2)我国化学家侯德榜发明的“联合制碱法”为世界制碱工业做出了巨大贡献。下图为联合制碱法的主要过程(部分物质已略去)。
已知:i. 溶于水生成碱,与酸反应生成盐,如
溶于水生成碱,与酸反应生成盐,如 。
。
ⅱ.有关物质的溶解度(20℃)
①煅烧炉中反应的化学方程式为___________ ,物质X是___________ 。沉淀池中发生反应的化学方程式为___________ 。
②下列说法正确的是___________ (填字母)。
A.沉淀池中有 析出,因为一定条件下
析出,因为一定条件下 的溶解度最小
的溶解度最小
B.滤液中主要含有NaCl、 和
和
C.设计循环的目的是提高原料的利用率
(1)
 用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备
用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备 并检验其纯度的实验流程如图所示。回答下列问题:
并检验其纯度的实验流程如图所示。回答下列问题:
①
 样品加水溶解生成1.5mol气体,转移电子数为
样品加水溶解生成1.5mol气体,转移电子数为②样液中加入
 后产生能使带火星木条复燃的气体,说明
后产生能使带火星木条复燃的气体,说明 与水反应的过程中还生成了
与水反应的过程中还生成了③滤液中加入
 溶液产生白色沉淀,说明
溶液产生白色沉淀,说明 样品中含有
样品中含有(2)我国化学家侯德榜发明的“联合制碱法”为世界制碱工业做出了巨大贡献。下图为联合制碱法的主要过程(部分物质已略去)。

已知:i.
 溶于水生成碱,与酸反应生成盐,如
溶于水生成碱,与酸反应生成盐,如 。
。ⅱ.有关物质的溶解度(20℃)
| 物质 | NaCl |  |  |  |
| 溶解度/g | 36.0 | 21.7 | 9.6 | 37.2 |
②下列说法正确的是
A.沉淀池中有
 析出,因为一定条件下
析出,因为一定条件下 的溶解度最小
的溶解度最小B.滤液中主要含有NaCl、
 和
和
C.设计循环的目的是提高原料的利用率
您最近一年使用:0次
名校
解题方法
6 . 化合物 (结构简式为
(结构简式为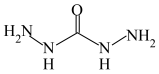 )是一种锅炉水添加剂,能除去锅炉水中的溶解氧,并可使锅炉壁钝化。钝化反应为
)是一种锅炉水添加剂,能除去锅炉水中的溶解氧,并可使锅炉壁钝化。钝化反应为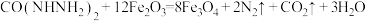 。下列说法正确的是
。下列说法正确的是
 (结构简式为
(结构简式为 )是一种锅炉水添加剂,能除去锅炉水中的溶解氧,并可使锅炉壁钝化。钝化反应为
)是一种锅炉水添加剂,能除去锅炉水中的溶解氧,并可使锅炉壁钝化。钝化反应为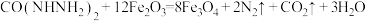 。下列说法正确的是
。下列说法正确的是| A.该反应是熵减过程 |
B. 可写成 可写成 ,属于混合物 ,属于混合物 |
| C.反应中C、N元素均被氧化 |
D.每生成 ,反应中转移 ,反应中转移 电子 电子 |
您最近一年使用:0次
2023-12-02更新
|
259次组卷
|
5卷引用:江西省部分地区2023-2024学年高三上学期11月期中化学试题
江西省部分地区2023-2024学年高三上学期11月期中化学试题河南省部分名校2023-2024学年高三上学期11月期中化学试题贵州省贵阳市2023-2024学年高三上学期11月质量检测化学试题湖北省九师联盟2024届高三11月质检化学试题(已下线)专题06 化学反应速率与平衡-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)
名校
7 . 关于反应 ,下列说法不正确的是
,下列说法不正确的是
 ,下列说法不正确的是
,下列说法不正确的是A.该反应中 中N元素被氧化 中N元素被氧化 |
| B.氧化产物与还原产物的物质的量之比为3∶4 |
C.反应中每生成1.4mol  时转移的电子数为4.8 时转移的电子数为4.8 |
D. 发生还原反应 发生还原反应 |
您最近一年使用:0次
2023-12-01更新
|
162次组卷
|
3卷引用:江西省抚州市资溪县第一中学2023-2024学年高一上学期11月期中考试化学试题
名校
8 . NA代表阿伏加德罗常数的值。下列说法正确的是
| A.标准状况下,2.24 L N2和O2的混合气体中气体分子总数为0.2NA |
| B.39 g Na2O2中含有的离子总数为1.5NA |
| C.1 mol Cl2与足量的Fe反应,转移电子数为3NA |
| D.1 mol OH-所含电子数为9NA |
您最近一年使用:0次
2023-11-26更新
|
372次组卷
|
3卷引用:江西省宜春市高安市灰埠中学2023-2024学年高一上学期11月期中化学试题
9 .  在电池、玻璃、有机合成等工业生产中应用广泛。利用粗
在电池、玻璃、有机合成等工业生产中应用广泛。利用粗 (含有MnO和
(含有MnO和 杂质)制取纯
杂质)制取纯 的流程如图。
的流程如图。

下列说法错误的是
 在电池、玻璃、有机合成等工业生产中应用广泛。利用粗
在电池、玻璃、有机合成等工业生产中应用广泛。利用粗 (含有MnO和
(含有MnO和 杂质)制取纯
杂质)制取纯 的流程如图。
的流程如图。
下列说法错误的是
| A.酸浸过程中有复分解反应发生 |
| B.操作X用到的玻璃仪器为玻璃棒、漏斗、烧杯 |
C.氧化过程中每生成1mol ,转移的电子数为 ,转移的电子数为 |
D. 与热的NaOH溶液反应的离子方程式为 与热的NaOH溶液反应的离子方程式为 |
您最近一年使用:0次
2023-11-10更新
|
77次组卷
|
2卷引用:江西省赣州市部分市县学校2023-2024学年高三上学期期中考试化学试题
名校
解题方法
10 . 工业上用生物法处理 的原理如下:
的原理如下:
反应1:
反应2: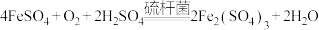
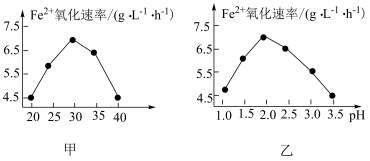
以硫杆菌作催化剂时,反应温度及溶液 对
对 氧化速率的影响分别如图甲、图乙所示。下列有关说法错误的是
氧化速率的影响分别如图甲、图乙所示。下列有关说法错误的是
 的原理如下:
的原理如下:反应1:

反应2:
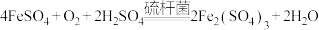
以硫杆菌作催化剂时,反应温度及溶液
 对
对 氧化速率的影响分别如图甲、图乙所示。下列有关说法错误的是
氧化速率的影响分别如图甲、图乙所示。下列有关说法错误的是
A.反应1的条件下,还原性: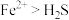 |
B.当反应温度过高时, 氧化速率下降的原因可能是硫杆菌失去活性 氧化速率下降的原因可能是硫杆菌失去活性 |
C.由图甲和图乙可得出结论:使用硫杆菌作催化剂的最佳条件为 、 、 |
D.当反应1中转移 电子时,反应1中消耗的 电子时,反应1中消耗的 在标准状况下的体积为 在标准状况下的体积为 |
您最近一年使用:0次
2023-11-09更新
|
118次组卷
|
2卷引用:江西省赣州市十八县23校2023-2024学年高二上学期期中联考化学试题



