1 . 下列有关硫及其化合物的性质与用途具有对应关系的是
| A.硫单质呈黄色,可用作橡胶硫化剂 |
B. 具有还原性,可用于漂白草编织物 具有还原性,可用于漂白草编织物 |
C. 具有还原性,可用于处理自来水中残留的 具有还原性,可用于处理自来水中残留的 |
| D.浓硫酸具有强氧化性,可用作酯化反应的催化剂 |
您最近一年使用:0次
名校
解题方法
2 . 在含有大量的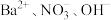 的溶液中,还可能大量共存的离子是
的溶液中,还可能大量共存的离子是
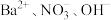 的溶液中,还可能大量共存的离子是
的溶液中,还可能大量共存的离子是A. | B. | C. | D. |
您最近一年使用:0次
2024-01-28更新
|
187次组卷
|
2卷引用:2024年江苏省靖江高级中学学业水平合格性考试化学试题
3 . 下列实验方案不能达到实验目的的是
| A.用过滤法除去NaCl溶液中的泥沙 |
| B.用蒸馏法分离乙酸(沸点118℃)与乙醚(沸点34℃) |
| C.用石灰水鉴别NaHCO3与Na2CO3 |
| D.用盐酸酸化的BaCl2溶液检验Na2SO3是否变质 |
您最近一年使用:0次
名校
解题方法
4 . 硫及其化合物有着广泛的作用。硫元素具有多种化合价,在一定条件下能发生相互转化。不同温度下硫单质的状态和分子结构不同,S8环状分子的结构为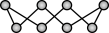 。合理应用和处理含硫的化合物,在生产生活中有重要意义。下列有关硫及其化合物的性质与用途具有对应关系的是
。合理应用和处理含硫的化合物,在生产生活中有重要意义。下列有关硫及其化合物的性质与用途具有对应关系的是
 。合理应用和处理含硫的化合物,在生产生活中有重要意义。下列有关硫及其化合物的性质与用途具有对应关系的是
。合理应用和处理含硫的化合物,在生产生活中有重要意义。下列有关硫及其化合物的性质与用途具有对应关系的是| A.硫单质呈黄色,可用作橡胶硫化剂 |
| B.SO2具有氧化性,可用于漂白草编织物 |
| C.Na2SO3具有还原性,可用于处理自来水中残留的Cl2 |
| D.浓硫酸具有强氧化性,可用作酯化反应的催化剂 |
您最近一年使用:0次
2023-03-23更新
|
686次组卷
|
4卷引用:江苏省连云港高级中学2022-2023学年高二下学期第二次学情检测化学试题
江苏省连云港高级中学2022-2023学年高二下学期第二次学情检测化学试题江苏省苏锡常镇四市2022-2023学年高三下学期教学情况调研(一)(3月)化学试题(已下线)江苏省南京市盐城市2023届高三3月第二次模拟考试化学试题变式题(选择题6-10)(已下线)专题05 元素化合物性质
名校
解题方法
5 . 在指定条件下,下列选项所示的物质间转化能实现的是
A.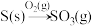 | B.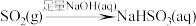 |
C.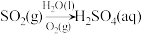 | D. |
您最近一年使用:0次
名校
6 . 钠的化合物在生活、生产中有广泛应用,下列有关物质的性质与用途具有对应关系的是
A. 固体能溶于水,可用作调味品 固体能溶于水,可用作调味品 | B. 具有强氧化性,可用作消毒剂 具有强氧化性,可用作消毒剂 |
C. 受热易分解,可用于中和胃酸 受热易分解,可用于中和胃酸 | D. 具有还原性,可用于漂白纸浆 具有还原性,可用于漂白纸浆 |
您最近一年使用:0次
解题方法
7 . 室温下,通过实验研究亚硫酸盐的性质,已知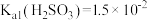 ,
,
下列说法正确的是
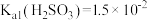 ,
,
| 实验 | 实验操作和现象 |
| 1 | 把一定量的 通入氨水,测所得溶液pH=7 通入氨水,测所得溶液pH=7 |
| 2 | 向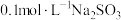 溶液中加入一定量的 溶液中加入一定量的 溶液,使亚硫酸根离子完全沉淀 溶液,使亚硫酸根离子完全沉淀 |
| 3 | 向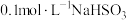 溶液中滴入等浓度等体积的NaOH溶液 溶液中滴入等浓度等体积的NaOH溶液 |
| 4 | 把少量氯气通入 溶液中,测得溶液pH变小 溶液中,测得溶液pH变小 |
A.实验1中,可计算出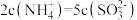 |
B.实验2反应静置后的上层清液中有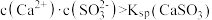 |
C.实验3中: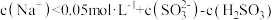 |
| D.实验4中说明氯气溶于水显酸性 |
您最近一年使用:0次
解题方法
8 . 图1是自然界中硫元素的存在示意图,图2表示硫元素的常见化合价与部分物质类别的对应关系。请回答下列问题:
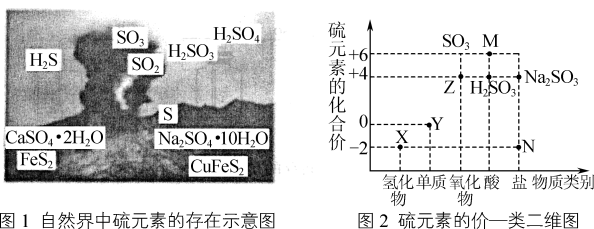
(1)图1中能与水反应生成强酸的物质的化学式为___________ 。
(2)煤的燃烧会产生大量SO2造成环境污染,下列关于SO2治理措施不可行的是___________(填字母)。
(3)Cu和M的浓溶液反应生成Z的化学方程式为___________ 。
(4)Na2SO3溶液易变质,实验室验证Na2SO3溶液已变质的操作和现象是___________ 。

(1)图1中能与水反应生成强酸的物质的化学式为
(2)煤的燃烧会产生大量SO2造成环境污染,下列关于SO2治理措施不可行的是___________(填字母)。
| A.在燃煤中添加生石灰固硫 | B. SO2 |
| C.将煤燃烧产生的尾气排放到高空 | D.用氨水吸收烟气中的SO2 |
(4)Na2SO3溶液易变质,实验室验证Na2SO3溶液已变质的操作和现象是
您最近一年使用:0次
9 . 硫和硒(34Se)在元素周期表中位于同一主族,均是生产生活中重要的非金属元素。
(1)含+4价硫元素的化合物有SO2、H2SO3和X等。
①SO2能使品红溶液褪色,说明SO2具有的化学性质是___________ 。
②已知X属于钠盐。写出X与稀硫酸反应生成SO2的化学方程式:___________ 。
(2)以工业硒为原料制备高纯硒时的主要物质转化关系如图所示。
工业硒(Se)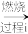 SeO2
SeO2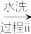 H2SeO3
H2SeO3 Se
Se 高纯硒
高纯硒
①下列说法正确的是___________ (填字母序号)。
A.硒原子的最外层有6个电子
B.硒元素的非金属性强于硫元素的非金属性
C.SeO2属于酸性氧化物
D.过程ⅰ中硒被氧化
②过程ⅲ中使用的还原剂为N2H4·nH2O,对应产物是N2.理论上,过程ⅰ消耗的O2与过程ⅲ消耗的N2H4·nH2O的物质的量之比为___________ (工业硒中杂质与O2的反应可忽略)。
(1)含+4价硫元素的化合物有SO2、H2SO3和X等。
①SO2能使品红溶液褪色,说明SO2具有的化学性质是
②已知X属于钠盐。写出X与稀硫酸反应生成SO2的化学方程式:
(2)以工业硒为原料制备高纯硒时的主要物质转化关系如图所示。
工业硒(Se)
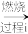 SeO2
SeO2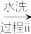 H2SeO3
H2SeO3 Se
Se 高纯硒
高纯硒①下列说法正确的是
A.硒原子的最外层有6个电子
B.硒元素的非金属性强于硫元素的非金属性
C.SeO2属于酸性氧化物
D.过程ⅰ中硒被氧化
②过程ⅲ中使用的还原剂为N2H4·nH2O,对应产物是N2.理论上,过程ⅰ消耗的O2与过程ⅲ消耗的N2H4·nH2O的物质的量之比为
您最近一年使用:0次
名校
解题方法
10 . 下列离子方程式表达不正确 的是
A.用氨水吸收废气中的氮氧化物:NO + NO2 + 2OH-=2NO + H2O + H2O |
B.用烧碱溶液除去铝片表面的氧化膜:Al2O3 + 2OH-=2AlO + H2O + H2O |
C.用亚硫酸钠溶液处理纸浆中残氯:SO + 2OH-+ Cl2=2Cl-+ SO + 2OH-+ Cl2=2Cl-+ SO + H2O + H2O |
D.用食醋消除松花蛋中的氨味:CH3COOH + NH3=CH3COO-+ NH |
您最近一年使用:0次



