名校
解题方法
1 . 下列“解释或结论”与“实验操作及现象”不相符 的一组是
| 序号 | 实验操作及现象 | 解释或结论 |
| A | 将氯水滴入KI-淀粉溶液中,溶液变成蓝色 | Cl2的氧化性强于I2 |
| B | 将打磨后的镁条放入盛有稀盐酸的试管中,用手触摸试管外壁感觉变热 | 镁条与稀盐酸反应是放热反应 |
| C | 某钠盐溶于盐酸,产生能使澄清石灰水变浑浊的无色无味气体 | 该盐一定是Na2CO3 |
| D | 滴加稀NaOH溶液,将湿润的红色石蕊试纸置于试管口,试纸不变蓝 | 不能确定原溶液中含 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . 依据下列实验现象,分析所得结论不正确 的是
| ① | ② | ③ | ④ | |
| 实验方案 |  | 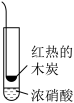 | 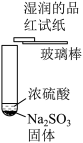 | 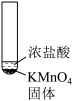 |
| 实验现象 | 试管中有红棕色气体出现 | 试管中有红棕色气体出现 | 试管中有刺激性气味的气体出现,且品红试纸褪色 | 试管中有黄绿色气体出现 |
| A.①中产生的气体一定是混合气体 |
| B.②的气体中经检测还含有CO2,说明木炭与浓硝酸一定发生了反应 |
| C.③发生的反应不属于氧化还原反应 |
| D.氧化性:KMnO4>Cl2 |
您最近一年使用:0次
名校
解题方法
3 . 为测定Na2CO3与Na2SO3混合物中各组分的含量,设计如下实验方案:
(1)方案一:称取一定质量的样品(30g),置于坩埚中加热至恒重,冷却,称取剩余固体质量为31.6g,计算。①实验中加热至恒重的目的是_______ 。②样品中Na2CO3的质量分数为_______ 。
(2)方案二:以下图所示装置进行实验:(铁架台、铁夹等仪器未在图中画出)
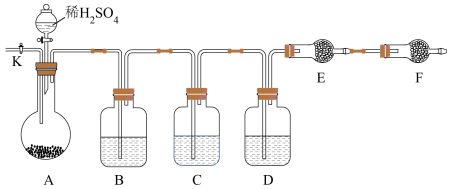
①已知仪器C中装有品红溶液,其作用是_______ ,
②实验室中备有以下常用试剂:a.浓硫酸 b.品红溶液 c.酸性高锰酸钾溶液 d.氢氧化钠溶液e.无水硫酸铜 f.碱石灰 g.五氧化二磷 h.无水氯化钙 请将下列容器中应盛放的试剂序号填入相应空格:B中_______ ,D中_______ ,E中_______ 。
③实验过程中,当仪器A内的固体反应完全后,需打开活塞K,向A中通入大量的氮气。这样做的目的是_______ 。
(3)方案三:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量BaCl2溶液。过滤、洗涤、干燥沉淀,称量固体质量。实验中判断沉淀洗干净的方法是_______ 。
(1)方案一:称取一定质量的样品(30g),置于坩埚中加热至恒重,冷却,称取剩余固体质量为31.6g,计算。①实验中加热至恒重的目的是
(2)方案二:以下图所示装置进行实验:(铁架台、铁夹等仪器未在图中画出)

①已知仪器C中装有品红溶液,其作用是
②实验室中备有以下常用试剂:a.浓硫酸 b.品红溶液 c.酸性高锰酸钾溶液 d.氢氧化钠溶液e.无水硫酸铜 f.碱石灰 g.五氧化二磷 h.无水氯化钙 请将下列容器中应盛放的试剂序号填入相应空格:B中
③实验过程中,当仪器A内的固体反应完全后,需打开活塞K,向A中通入大量的氮气。这样做的目的是
(3)方案三:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量BaCl2溶液。过滤、洗涤、干燥沉淀,称量固体质量。实验中判断沉淀洗干净的方法是
您最近一年使用:0次
2023-08-22更新
|
75次组卷
|
2卷引用:山西省运城市康杰中学2022-2023学年高一下学期3月月考化学试题
名校
4 . 某研究小组同学为探究锌与硫酸反应生成 SO2、H2的临界浓度(浓硫酸能与锌反应生成 SO2的最低浓度)设计了如图实验 (加热和夹持装置已省略)。
已知:锌与浓硫酸开始时反应缓慢,可以适当加热以加速其反应,当有大量气泡生成时,该反应速率会明显加快并伴有大量的热放出。
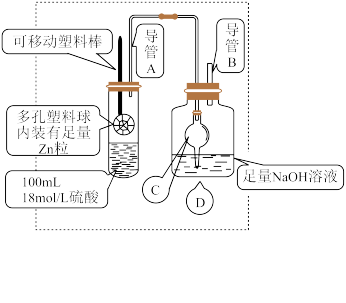
(1)请写出锌与硫酸反应产生 SO2的化学方程式_______ 。
(2)在组装仪器之后,加入试剂之前必须进行的操作是_______ 。
(3)装置中干燥管C的作用是_______ 。
(4)移动塑料棒,使锌浸没到硫酸中充分反应,反应结束后向D 装置中加入足量的 H2O2溶液,再加入足量的BaCl2溶液,充分反应后将所得沉淀过滤、洗涤、干燥、称量得到固体质量为a克。
①加入 H2O2溶液发生反应的离子方程式是_______ 。
②浓硫酸与锌反应的临界浓度为:_______ mol/L。(用含a的计算式表示,忽略溶液体积变化)
(5)导管A竖直部分较长,其作用是_______ 。
(6)另甲同学提出测定方案:将D中的溶液酸化后,利用标准酸性KMnO4溶液测定原溶液中的SO ,从而计算临界浓度。乙同学认为相对于(4)中的测定方法,此方案会使测定结果偏高,你认为乙同学的理由是
,从而计算临界浓度。乙同学认为相对于(4)中的测定方法,此方案会使测定结果偏高,你认为乙同学的理由是_______ 。
已知:锌与浓硫酸开始时反应缓慢,可以适当加热以加速其反应,当有大量气泡生成时,该反应速率会明显加快并伴有大量的热放出。

(1)请写出锌与硫酸反应产生 SO2的化学方程式
(2)在组装仪器之后,加入试剂之前必须进行的操作是
(3)装置中干燥管C的作用是
(4)移动塑料棒,使锌浸没到硫酸中充分反应,反应结束后向D 装置中加入足量的 H2O2溶液,再加入足量的BaCl2溶液,充分反应后将所得沉淀过滤、洗涤、干燥、称量得到固体质量为a克。
①加入 H2O2溶液发生反应的离子方程式是
②浓硫酸与锌反应的临界浓度为:
(5)导管A竖直部分较长,其作用是
(6)另甲同学提出测定方案:将D中的溶液酸化后,利用标准酸性KMnO4溶液测定原溶液中的SO
 ,从而计算临界浓度。乙同学认为相对于(4)中的测定方法,此方案会使测定结果偏高,你认为乙同学的理由是
,从而计算临界浓度。乙同学认为相对于(4)中的测定方法,此方案会使测定结果偏高,你认为乙同学的理由是
您最近一年使用:0次
5 . 以Na2SO3溶液和不同金属的硫酸盐溶液作为实验对象,探究盐的性质和盐溶液间反应的多样性。
(1)经检验,现象Ⅰ中的白色沉淀是Ag2SO3。用离子方程式解释现象Ⅰ:____________ 。
(2)经检验,现象Ⅱ的棕黄色沉淀中不含 ,含有Cu+、Cu2+和
,含有Cu+、Cu2+和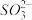 。
。
已知:Cu+ Cu +Cu2+,Cu2+
Cu +Cu2+,Cu2+ CuI↓(白色)+I2。
CuI↓(白色)+I2。
①用稀硫酸证实沉淀中含有Cu+的实验现象是_____________ 。
②通过下列实验证实,沉淀中含有Cu2+和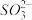 。
。
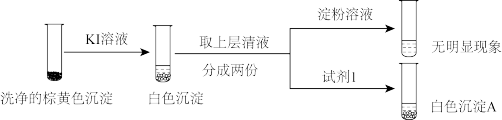
a.白色沉淀A是BaSO4,试剂1是____________ 。
b.证实沉淀中含有Cu+和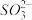 的理由是
的理由是___________ 。
(3)已知:Al2(SO3)3在水溶液中不存在。经检验,现象Ⅲ的白色沉淀中无 ,该白色沉淀既能溶于强酸,又能溶于强碱,还可使酸性KMnO4溶液褪色。
,该白色沉淀既能溶于强酸,又能溶于强碱,还可使酸性KMnO4溶液褪色。
①推测沉淀中含有亚硫酸根和________ 。
②对于沉淀中亚硫酸根的存在形式提出两种假设:i.被Al(OH)3所吸附;ii.存在于铝的碱式盐中。对假设ii设计了对比实验,证实了假设ii成立。
a.将对比实验方案补充完整。
步骤一: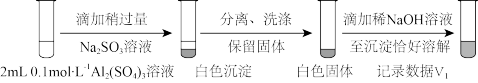
步骤二:_____________ (按上图形式呈现)。
(4)根据实验,亚硫酸盐的性质有___________ 。盐溶液间反应的多样性与__________ 有关。
| 实验 | 试剂 | 现象 | |
| 滴管 | 试管 | ||
 2 mL | 0.2 mol·L−1 Na2SO3溶液 | 饱和Ag2SO4溶液 | Ⅰ.产生白色沉淀 |
| 0.2 mol·L−1 CuSO4 | Ⅱ.溶液变绿,继续滴加产生棕黄色沉淀 | ||
| 0.1 mol·L−1 Al2(SO4)3溶液 | Ⅲ.开始无明显变化,继续滴加产生白色沉淀 | ||
(2)经检验,现象Ⅱ的棕黄色沉淀中不含
 ,含有Cu+、Cu2+和
,含有Cu+、Cu2+和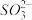 。
。已知:Cu+
 Cu +Cu2+,Cu2+
Cu +Cu2+,Cu2+ CuI↓(白色)+I2。
CuI↓(白色)+I2。①用稀硫酸证实沉淀中含有Cu+的实验现象是
②通过下列实验证实,沉淀中含有Cu2+和
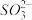 。
。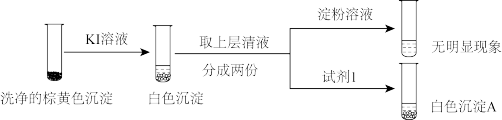
a.白色沉淀A是BaSO4,试剂1是
b.证实沉淀中含有Cu+和
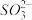 的理由是
的理由是(3)已知:Al2(SO3)3在水溶液中不存在。经检验,现象Ⅲ的白色沉淀中无
 ,该白色沉淀既能溶于强酸,又能溶于强碱,还可使酸性KMnO4溶液褪色。
,该白色沉淀既能溶于强酸,又能溶于强碱,还可使酸性KMnO4溶液褪色。①推测沉淀中含有亚硫酸根和
②对于沉淀中亚硫酸根的存在形式提出两种假设:i.被Al(OH)3所吸附;ii.存在于铝的碱式盐中。对假设ii设计了对比实验,证实了假设ii成立。
a.将对比实验方案补充完整。
步骤一:
步骤二:
(4)根据实验,亚硫酸盐的性质有
您最近一年使用:0次
2019-01-30更新
|
2282次组卷
|
3卷引用:2020届四川省成都市第七中学高三二月份网络教学质量监测卷化学试题
名校
解题方法
6 . 下列实验中,对应的现象以及结论都正确且两者具有因果关系的是
| 选项 | 实验 | 现象 | 结论 |
| A | 将过量铁粉加入稀硝酸中,充分反应后滴加KSCN溶液 | 有气体生成,溶液呈血红色 | 稀硝酸将Fe氧化为Fe3+ |
| B | 将铜粉加入1.0mol/LFe2(SO4)3溶液中 | 溶液由黄色变为蓝绿(青)色 | 金属铁比铜活泼 |
| C | 向久置的FeCl2溶液中加入酸性KMnO4溶液 | KMnO4溶液紫色褪去 | FeCl2溶液没有完全被氧化 |
| D | 将少量Na2SO3样品溶于足量稀盐酸中,静置,取上层溶液于试管中,滴加BaCl2溶液 | 产生白色沉淀 | 该Na2SO3样品已经变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-06-19更新
|
361次组卷
|
4卷引用:黑龙江省哈尔滨市第九中学2020-2021学年高二下学期6月月考化学试题
黑龙江省哈尔滨市第九中学2020-2021学年高二下学期6月月考化学试题湖南省衡阳师范学院祁东附属中学2021-2022学年高三上学期12月月考化学试题(已下线)考点15 铁及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点15 铁及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)
解题方法
7 . 室温下,探究0.1mol∙L-1NaHSO3溶液的性质,下列实验方案能达到探究目的的是
| 选项 | 探究目的 | 实验方案 |
| A | 是否含有 | 向2mL NaHSO3溶液中滴加几滴Ba(NO3)2溶液,观察溶液中是否有白色沉淀产生 |
| B |  是否水解 是否水解 | 向2mL NaHSO3溶液中滴加几滴酚酞试液,观察溶液颜色变化 |
| C |  是否有还原性 是否有还原性 | 向2mL NaHSO3溶液中滴加几滴KMnO4溶液,观察溶液颜色变化 |
| D |  是否有氧化性 是否有氧化性 | 向2mL NaHSO3溶液中滴加几滴KIO3溶液,充分反应后滴加几滴淀粉溶液,观察溶液颜色变化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
8 . 常用的自来水消毒剂有二氧化氯( )和高铁酸钾(
)和高铁酸钾( )等。
)等。
Ⅰ.某研究性学习小组利用如图装置由二氧化氯制备 。
。
已知:①温度较高, 易分解为
易分解为 和
和 。
。
② 与碱溶液发生歧化反应生成等物质的量的氯酸盐和另一种盐。
与碱溶液发生歧化反应生成等物质的量的氯酸盐和另一种盐。
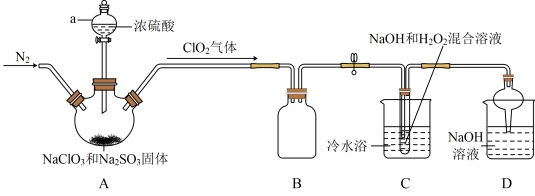
(1)盛放 和
和 固体的仪器名称是
固体的仪器名称是___________ ;B装置的作用是___________ 。
(2)C中反应为___________ 反应(选填“放热”或“吸热”);若撤去装置C中的冷水浴,导致产品中可能混有的杂质是___________ 。
(3)装置D是处理尾气,反应的离子方程式___________ 。
(4)实验结束后,继续通入一段时间 的目的是
的目的是___________ 。
(5)将 气体通入到足量
气体通入到足量 溶液中,溶液变棕黄色;再向其中加入适量苯,振荡、静置,观察到
溶液中,溶液变棕黄色;再向其中加入适量苯,振荡、静置,观察到___________ ,证明 具有氧化性。
具有氧化性。
Ⅱ.可用于生活垃圾渗透液的脱氮(将含氮物质转化为 )处理。
)处理。
(6) 溶于水时,与水反应生成氢氧化铁胶体,同时放出氧气,该反应的化学方程式为
溶于水时,与水反应生成氢氧化铁胶体,同时放出氧气,该反应的化学方程式为___________ 。
 )和高铁酸钾(
)和高铁酸钾( )等。
)等。Ⅰ.某研究性学习小组利用如图装置由二氧化氯制备
 。
。已知:①温度较高,
 易分解为
易分解为 和
和 。
。②
 与碱溶液发生歧化反应生成等物质的量的氯酸盐和另一种盐。
与碱溶液发生歧化反应生成等物质的量的氯酸盐和另一种盐。
(1)盛放
 和
和 固体的仪器名称是
固体的仪器名称是(2)C中反应为
(3)装置D是处理尾气,反应的离子方程式
(4)实验结束后,继续通入一段时间
 的目的是
的目的是(5)将
 气体通入到足量
气体通入到足量 溶液中,溶液变棕黄色;再向其中加入适量苯,振荡、静置,观察到
溶液中,溶液变棕黄色;再向其中加入适量苯,振荡、静置,观察到 具有氧化性。
具有氧化性。Ⅱ.可用于生活垃圾渗透液的脱氮(将含氮物质转化为
 )处理。
)处理。(6)
 溶于水时,与水反应生成氢氧化铁胶体,同时放出氧气,该反应的化学方程式为
溶于水时,与水反应生成氢氧化铁胶体,同时放出氧气,该反应的化学方程式为
您最近一年使用:0次
9 . 下列实验设计能达到预期实验目的的是
| 实验目的 | 实验设计 | |
| A | 制取Fe(NO3)2溶液 | 将FeO加入盛有稀硝酸的试管中,振荡使其反应 |
| B | 验证Na2O2与CO2反应放热 | 将撒有Na2O2的脱脂棉放在石棉网上,然后向其中通入CO2,观察现象 |
| C | 探究H2O2的氧化性 | 向盛有Na2SO3溶液的试管中滴入过氧化氢溶液,观察现象 |
| D | 除去CO2中少量SO2 | 将气体依次通过足量饱和Na2CO3溶液,浓硫酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



