12-13高三下·安徽安庆·阶段练习
1 . 硫及其化合物有广泛的应用,对SO2性质的研究是高中化学教学的一项重要内容。
(1)对比研究是一种重要的研究方法。若将硫的单质及部分化合物按如下表所示分成3 组,则第2组中物质M的化学式是_______ 。
Ⅱ.某校化学学习小组用下图所示的实验装置研究SO2气体还原Fe3+、Br2的反应。
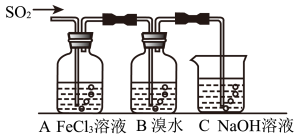
(2)下列实验方案可以用于在实验室制取所需SO2的是_______________________ 。
A.Na2SO3溶液与HNO3 B.Na2SO3固体浓硫酸
C.固体硫在纯氧中燃烧 D.铜与热的浓硫酸
(3)装置C的作用是除去多余的SO2,防止污染空气。已知在用氢氧化钠溶液吸收SO2的 过程中,往往得到Na2SO3和NaHSO3的混合溶液,常温下,溶液pH随n(SO ):n(HSO
):n(HSO )变化关系如下表
)变化关系如下表
当吸收液中n(SO ):n(HSO
):n(HSO )=10:1时,溶液中离子浓度关系正确的是
)=10:1时,溶液中离子浓度关系正确的是____________________ 。
A.c(Na+)+ c(H+)= 2c(SO )+ c(HSO
)+ c(HSO )+ c(OH—)
)+ c(OH—)
B.c(Na+)>c(HSO >c(SO
>c(SO )>c(OH—)>c(H+)
)>c(OH—)>c(H+)
C.c(Na+)>c(SO )>c(HSO
)>c(HSO )>c(OH—)>c(H+)
)>c(OH—)>c(H+)
(4)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中反应后的溶液分成三份,并设计了如下探究实验,请你评价并参与他们的探究过程(限选试剂:KMnO4溶液、KSCN溶液、BaCl2溶液、稀硫酸、稀盐酸、稀硝 酸、Ba(NO3)2溶液、新制的氯水)
上述方案①得出的结论是否合理____________________ ,原因_______________________________ 。如果他们设计的方案②与方案③均合理并且得到相应结论,请你将上面表格补充完整___________________ ,___________________ 。
(5)装置B中能表明Br—的还原性弱于SO2的现象是__________________________ 。
(1)对比研究是一种重要的研究方法。若将硫的单质及部分化合物按如下表所示分成3 组,则第2组中物质M的化学式是
| 第1组 | 第2组 | 第3组 |
| S (单质) | SO2、H2SO3、M、NaHSO3 | SO3、H2SO4、Na2SO4、NaHSO4 |

(2)下列实验方案可以用于在实验室制取所需SO2的是
A.Na2SO3溶液与HNO3 B.Na2SO3固体浓硫酸
C.固体硫在纯氧中燃烧 D.铜与热的浓硫酸
(3)装置C的作用是除去多余的SO2,防止污染空气。已知在用氢氧化钠溶液吸收SO2的 过程中,往往得到Na2SO3和NaHSO3的混合溶液,常温下,溶液pH随n(SO
 ):n(HSO
):n(HSO )变化关系如下表
)变化关系如下表| n(SO32—):n(HSO3—) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
 ):n(HSO
):n(HSO )=10:1时,溶液中离子浓度关系正确的是
)=10:1时,溶液中离子浓度关系正确的是A.c(Na+)+ c(H+)= 2c(SO
 )+ c(HSO
)+ c(HSO )+ c(OH—)
)+ c(OH—)B.c(Na+)>c(HSO
 >c(SO
>c(SO )>c(OH—)>c(H+)
)>c(OH—)>c(H+)C.c(Na+)>c(SO
 )>c(HSO
)>c(HSO )>c(OH—)>c(H+)
)>c(OH—)>c(H+)(4)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中反应后的溶液分成三份,并设计了如下探究实验,请你评价并参与他们的探究过程(限选试剂:KMnO4溶液、KSCN溶液、BaCl2溶液、稀硫酸、稀盐酸、稀硝 酸、Ba(NO3)2溶液、新制的氯水)
| 序号 | 实验方案 | 实验现象 | 结论 |
| 方案① | 往第一份试液中加入KMnO4溶液溶液 | 紫红色褪去 | SO2与Fe3+反应生成了Fe2+ |
| 方案② | 往第二份试液中加入 | SO2与Fe3+反应生成了Fe2+ | |
| 方案③ | 往第二份试液中加入 | SO2与Fe3+反应生成了SO |
(5)装置B中能表明Br—的还原性弱于SO2的现象是
您最近一年使用:0次
名校
解题方法
2 . 下列说法不正确旳是
| A.浓硫酸和浓硝酸都具有强氧化性,都能把HCl气体氧化 |
| B.浓硝酸在光照条件下颜色变黄,说明浓硝酸不稳定 |
| C.同温同压下,两份相同质量的锌粉,分别与足量的稀硫酸和浓硫酸反应,产生气体的体积相同 |
| D.将SO2气体通入BaCl2溶液中至饱和未见沉淀生成,继续通入NH3则有沉淀生成 |
您最近一年使用:0次
2023-03-27更新
|
717次组卷
|
2卷引用:宁夏银川市第二中学2022-2023学年高一下学期第一次月考化学试题
3 . 下列实验操作能达到实验目的的是
A.将NO和 的混合气体通过氢氧化钠溶液进行分离 的混合气体通过氢氧化钠溶液进行分离 |
| B.为检验某品牌食盐中是否含有碘元素,将样品溶解后滴加淀粉溶液 |
C.向 溶液中滴加氢硫酸,产生淡黄色沉淀,证明 溶液中滴加氢硫酸,产生淡黄色沉淀,证明 具有氧化性 具有氧化性 |
D.向浓 中插入红热的炭,产生红棕色气体,证明炭可与浓 中插入红热的炭,产生红棕色气体,证明炭可与浓 反应生成 反应生成 |
您最近一年使用:0次
名校
解题方法
4 . 下列反应中硫酸既表现氧化性,又表现酸性的有
| A.H2SO4+Na2SO3=Na2SO4+H2O+SO2↑ |
B.2H2SO4(浓)+C 2SO2↑+CO2↑+2H2O 2SO2↑+CO2↑+2H2O |
C.2H2SO4(浓)+Cu CuSO4+2H2O+SO2↑ CuSO4+2H2O+SO2↑ |
D.H2SO4(浓)+NaCl NaHSO4+HCl↑ NaHSO4+HCl↑ |
您最近一年使用:0次
5 . 下表为元素周期表的一部分,表中所列的字母分别代表一种化学元素,回答(1)(2)两小问
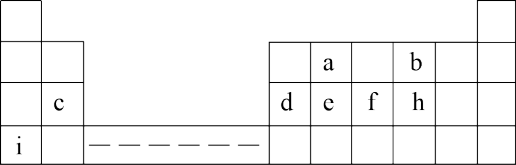
(1)a、b、c三种元素的原子半径由大到小的顺序是___________ (填元素符号);
(2)c、d、e三种元素最高价氧化物对应水化物中碱性最强的是_____ (填水化物的化学式)。
(3)配平下列离子方程式___ __MnO + ____Cl- + ____H+= ______Mn2+ + _____Cl2 + ___H2O
+ ____Cl- + ____H+= ______Mn2+ + _____Cl2 + ___H2O
(4)保持洁净安全的生存环境已成为全人类的共识。二氧化硫是引起酸雨的一种主要物质,必须严格控制排放。酸雨降落到地面后,其中的亚硫酸在空气中被氧气逐渐氧化生成硫酸,使酸性进一步增强,写出这一过程的化学方程式:___________ 。

(1)a、b、c三种元素的原子半径由大到小的顺序是
(2)c、d、e三种元素最高价氧化物对应水化物中碱性最强的是
(3)配平下列离子方程式
 + ____Cl- + ____H+= ______Mn2+ + _____Cl2 + ___H2O
+ ____Cl- + ____H+= ______Mn2+ + _____Cl2 + ___H2O(4)保持洁净安全的生存环境已成为全人类的共识。二氧化硫是引起酸雨的一种主要物质,必须严格控制排放。酸雨降落到地面后,其中的亚硫酸在空气中被氧气逐渐氧化生成硫酸,使酸性进一步增强,写出这一过程的化学方程式:
您最近一年使用:0次
名校
解题方法
6 . 某学生做如下实验:第一步,在淀粉-KI溶液中,滴入少量NaClO溶液,并加入少量稀硫酸,溶液立即变蓝;第二步,在上述蓝色溶液中,滴加足量的Na2SO3溶液,蓝色逐渐消失。下列有关该同学对实验原理的解释和所得结论的叙述不正确的是
A.氧化性:ClO->I2>SO |
| B.蓝色消失的原因是Na2SO3溶液具有漂白性 |
| C.淀粉-KI溶液变蓝是因为I-被ClO-氧化为I2,I2使淀粉变蓝 |
| D.若将Na2SO3溶液加入氯水中,氯水褪色 |
您最近一年使用:0次
2022-04-03更新
|
110次组卷
|
4卷引用:云南省曲靖市马龙区一中2021-2022学年高一下学期2月考试化学试题
名校
7 . X、Y、Z、R、T为短周期主族元素,其中R原子的最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Y与T同主族。五种元素原子半径与原子序数之间的关系如图所示。下列推断正确的是


| A.Z2Y和Z2Y2的阴阳离子个数比相同 |
| B.简单氢化物的稳定性:Y<T |
| C.最高价氧化物对应水化物的酸性:T<R |
| D.由X、T、Y、Z四种元素组成的常见化合物溶液显碱性 |
您最近一年使用:0次
2023-04-06更新
|
238次组卷
|
2卷引用:云南省玉溪第一中学2022-2023学年高二上学期第一次月考化学试题
名校
解题方法
8 . 在探究SO2的性质实验中,下列实验现象及得出的结论不正确的是
| A.向溴水中通入SO2,溶液褪色,说明SO2具有还原性 |
| B.向紫色石蕊溶液中通入SO2,溶液由先变红色后褪色,说明SO2具有漂白性 |
| C.向SO2水溶液中滴加Ba(NO3)2溶液,产生的白色沉淀是BaSO4 |
| D.向SO2水溶液中加入NaHCO3粉末,有气泡产生,说明H2SO3的酸性强于H2CO3 |
您最近一年使用:0次
名校
9 . 下列实验操作和现象与所得结论一定正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 向黄色的Fe(NO3)3溶液中滴加氢碘酸 | 溶液变为紫红色 | 氧化性: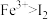 |
| B | 向某无色溶液中滴加稀盐酸,将产生的无色气体通入品红溶液 | 品红溶液褪色 | 原溶液中含有  |
| C | 一定温度下,向K2Cr2O7溶液中加入少量KOH | 溶液橙色变浅 | 减小H+浓度,  的平衡正向移动 的平衡正向移动 |
| D | 向Mg2+和Cu2+共存的溶液中滴加适量NaOH溶液,过滤、洗涤 | 得到白色沉淀 | 相同温度下,溶度积常数: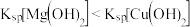 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
10 . 下列“解释或结论”与“实验操作及现象”不相符 的一组是
| 序号 | 实验操作及现象 | 解释或结论 |
| A | 将氯水滴入KI-淀粉溶液中,溶液变成蓝色 | Cl2的氧化性强于I2 |
| B | 将打磨后的镁条放入盛有稀盐酸的试管中,用手触摸试管外壁感觉变热 | 镁条与稀盐酸反应是放热反应 |
| C | 某钠盐溶于盐酸,产生能使澄清石灰水变浑浊的无色无味气体 | 该盐一定是Na2CO3 |
| D | 滴加稀NaOH溶液,将湿润的红色石蕊试纸置于试管口,试纸不变蓝 | 不能确定原溶液中含 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



