1 . 氮化硼、磷化硼均是受到高度关注的耐磨涂料。磷化硼的晶胞及某些原子的分数坐标如图所示,下列说法正确的是
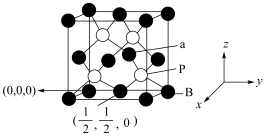
| A.磷化硼中P的价层电子对数为4 | B.熔点:BN<BP |
| C.磷化硼不溶于水,但可能溶于苯 | D.a原子的分数坐标为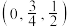 |
您最近一年使用:0次
名校
解题方法
2 . 硅微粒非常坚硬,比较晶体硅与碳化硅的熔点高低并解释说明___________ 。
您最近一年使用:0次
名校
解题方法
3 . 高二化学组组织同学们制作晶体模型。8班张宇涵同学提交了金刚石的晶体结构模型,17班路雪同学提交了氯化钠的晶胞模型,如下图所示。下列说法不正确的是


A.金刚石晶体中,碳原子采取 杂化轨道成键,形成共价键三维骨架网络 杂化轨道成键,形成共价键三维骨架网络 |
B. 金刚石晶体中含 金刚石晶体中含 键 键 |
C.氯化钠晶体中,1个 周围有12个距离最近且相等的 周围有12个距离最近且相等的 |
D.氯化钠晶胞为立方体,若棱长为 ,则晶体密度为 ,则晶体密度为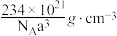 |
您最近一年使用:0次
4 . 氮化硼是一种重要的无机非金属材料,在工业生产中有着重要的作用。常见的三种氮化硼晶体结构如下图:
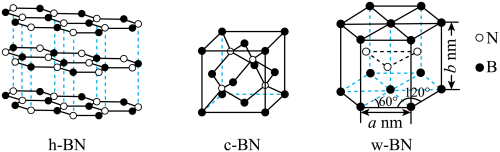
A.h-BN晶体中存在大 键 键 |
| B.c-BN晶体中由B、N构成最小的环为6元环 |
| C.w-BN晶体中B的配位数为12 |
D.w-BN晶体的密度可表示为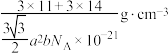 |
您最近一年使用:0次
2024-04-19更新
|
305次组卷
|
5卷引用:河北省张家口市尚义县第一中学等校2023-2024学年高三下学期4月模拟测试化学试题
解题方法
5 . 硼酸晶体有类似于石墨的片层状结构。下列说法不正确的是
| A.氧化铍熔点较高,可用作耐火材料 |
| B.电解熔融氯化铍制备铍单质 |
| C.用碳原子取代晶体硅中部分原子,硬度变大 |
D.不慎将碱液沾到皮肤上,立即用大量水冲洗,再涂上 的硼酸 的硼酸 |
您最近一年使用:0次
解题方法
6 . 近年来我国科技研究取得重大成就,科技创新离不开化学。下列相关叙述错误的是
| A.战斗机的隐形涂层含石墨烯,石墨烯、石墨互为同素异形体 |
| B.中国空间站太阳翼使用氮化镓(GaN)半导体材料,GaN属于新型无机非金属材料 |
| C.可再生生物降解餐具的成分为聚乳酸(PLA),PLA属于有机高分子材料 |
| D.天问一号探测器使用新型SiC增强铝基复合材料,SiC具有硬度大、熔点低的特点 |
您最近一年使用:0次
名校
解题方法
7 . 中医药学认为,雄黄(As4S4),外用可以治疗疥癣恶疮、蛇虫咬伤等;微量内服,可治惊痫、疮毒等症。雄黄遇热易氧化为As2O3(俗称砒霜),虽在古时常用做毒药,但科学家却发现它对治疗白血病有明显的作用。砷的其它化合物也在研究和生产中有着许多重要用途。____ ,核外电子占据的最高能级的电子云轮廓图形状为____ 。
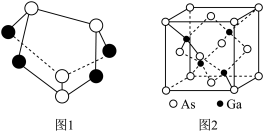
(2)雄黄(As4S4)的结构如上图1所示,As原子的杂化形式为_____ 。
(3)Na3AsO4常用作杀虫剂、防腐剂,它含有的化学键类型包括____ ;AsO43-的空间构型为_____ 。
(4)砷化镓是优良的半导体材料,其晶胞结构如图2所示。立方砷化镓晶体与立方氮化硼晶体结构类似,两种晶体中熔点较高的是____ ;砷化镓密度为 ,Ga和As原子半径分别为r1pm和r2pm,阿伏加德罗常数值为
,Ga和As原子半径分别为r1pm和r2pm,阿伏加德罗常数值为 ,则砷化镓晶体的空间利用率为
,则砷化镓晶体的空间利用率为_____ 。
(2)雄黄(As4S4)的结构如上图1所示,As原子的杂化形式为
(3)Na3AsO4常用作杀虫剂、防腐剂,它含有的化学键类型包括
(4)砷化镓是优良的半导体材料,其晶胞结构如图2所示。立方砷化镓晶体与立方氮化硼晶体结构类似,两种晶体中熔点较高的是
 ,Ga和As原子半径分别为r1pm和r2pm,阿伏加德罗常数值为
,Ga和As原子半径分别为r1pm和r2pm,阿伏加德罗常数值为 ,则砷化镓晶体的空间利用率为
,则砷化镓晶体的空间利用率为
您最近一年使用:0次
解题方法
8 . 工业上用焦炭还原石英砂制得粗硅,下列说法不正确的是( 为阿伏伽德罗常数)
为阿伏伽德罗常数)
 为阿伏伽德罗常数)
为阿伏伽德罗常数)A.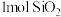 中含有 中含有 键数目为 键数目为 | B.消耗 焦炭转移 焦炭转移 电子 电子 |
C. (氧化产物): (氧化产物): 还原产物)=2:1 还原产物)=2:1 | D.可用氯化氢气体将硅与杂质分离 |
您最近一年使用:0次
2024-04-15更新
|
262次组卷
|
2卷引用:浙江省金华市十校2023-2024学年高三下学期4月模拟考试化学试题
9 .  是一种无机非金属材料,立方
是一种无机非金属材料,立方 的硬度仅次于金刚石,其晶胞如下图所示.下列说法
的硬度仅次于金刚石,其晶胞如下图所示.下列说法不正确 的是
 是一种无机非金属材料,立方
是一种无机非金属材料,立方 的硬度仅次于金刚石,其晶胞如下图所示.下列说法
的硬度仅次于金刚石,其晶胞如下图所示.下列说法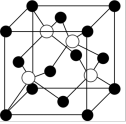
A.立方 属于共价晶体 属于共价晶体 | B.1个晶胞中含有4个B和4个N |
| C.距离每个B最近的N有4个 | D. 立方 立方 中含有 中含有 共价键 共价键 |
您最近一年使用:0次
解题方法
10 . 氮元素能与金属或者非金属元素形成种类繁多、应用广泛的化合物。
(1)基态N原子的价层电子轨道表示式是___________ 。
(2)与碳氢化合物类似,N、H两元素之间也可以形成氮烷、氮烯。
①在最简单的氮烯分子中,N的杂化方式是___________ 。
② 具有很强的还原性,是常用的火箭推进剂,它在常温常压下为无色液体。判断
具有很强的还原性,是常用的火箭推进剂,它在常温常压下为无色液体。判断 是否溶于水并说明理由
是否溶于水并说明理由___________ 。
(3)配合物 可用作广谱杀菌剂,其中Cu属于
可用作广谱杀菌剂,其中Cu属于___________ 区元素,该配合物中的配位原子是___________ ,配位数是___________ 。
(4) 的某种晶体结构中,原子间均以单键结合,其硬度比金刚石大,原因是
的某种晶体结构中,原子间均以单键结合,其硬度比金刚石大,原因是___________ 。
(5) 和
和 形成的化合物是一种重要的半导体材料。其某种晶胞形状为立方体,边长为
形成的化合物是一种重要的半导体材料。其某种晶胞形状为立方体,边长为 ,结构如图所示。
,结构如图所示。 最近的
最近的 有
有___________ 个。
②已知阿伏加德罗常数为 ,氮化镓(GaN)的摩尔质量为
,氮化镓(GaN)的摩尔质量为 ,该晶体的密度表达式为
,该晶体的密度表达式为___________  (
( )。
)。
(1)基态N原子的价层电子轨道表示式是
(2)与碳氢化合物类似,N、H两元素之间也可以形成氮烷、氮烯。
①在最简单的氮烯分子中,N的杂化方式是
②
 具有很强的还原性,是常用的火箭推进剂,它在常温常压下为无色液体。判断
具有很强的还原性,是常用的火箭推进剂,它在常温常压下为无色液体。判断 是否溶于水并说明理由
是否溶于水并说明理由(3)配合物
 可用作广谱杀菌剂,其中Cu属于
可用作广谱杀菌剂,其中Cu属于(4)
 的某种晶体结构中,原子间均以单键结合,其硬度比金刚石大,原因是
的某种晶体结构中,原子间均以单键结合,其硬度比金刚石大,原因是(5)
 和
和 形成的化合物是一种重要的半导体材料。其某种晶胞形状为立方体,边长为
形成的化合物是一种重要的半导体材料。其某种晶胞形状为立方体,边长为 ,结构如图所示。
,结构如图所示。
 最近的
最近的 有
有②已知阿伏加德罗常数为
 ,氮化镓(GaN)的摩尔质量为
,氮化镓(GaN)的摩尔质量为 ,该晶体的密度表达式为
,该晶体的密度表达式为 (
( )。
)。
您最近一年使用:0次



