1 . 下图所示的几种碳单质,关于它们的说法错误的是
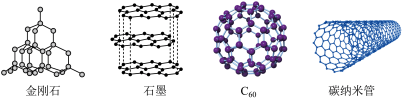

| A.四种碳单质互为同素异形体,其中石墨和碳纳米管均可导电 |
B.金刚石晶体中每个 原子被6个六元环所共用 原子被6个六元环所共用 |
C. 石墨晶体中含有的六元环的数目为 石墨晶体中含有的六元环的数目为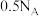 |
D. 晶体中每个 晶体中每个 分子周围与它最近且等距的 分子周围与它最近且等距的 分子有12个 分子有12个 |
您最近一年使用:0次
解题方法
2 . 下列叙述正确的是
A. 空间结构呈三角锥形,存在手性异构体 空间结构呈三角锥形,存在手性异构体 |
| B.NaCl晶体中只存在静电引力作用 |
C. 是直线形分子 是直线形分子 |
| D.金刚石是典型的分子晶体,熔点高,硬度大 |
您最近一年使用:0次
解题方法
3 . 磷的单质及其化合物用途非常广泛。回答下列问题:
(1)白磷晶胞属于面心立方最密堆积,每个 周围距离最近的
周围距离最近的 个数为
个数为___________ ;白磷隔绝空气加热转化为红磷,红磷是巨型分子,无定型结构,能证明白磷是晶体的实验验证方法是___________ 。
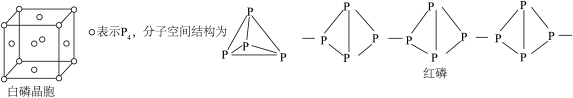
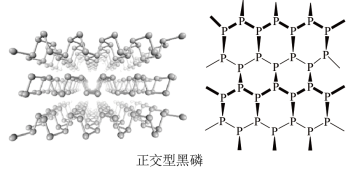
(2)黑磷晶体是一种新型材料,其中正交型黑磷具有类似石墨的片层结构。每一层内P原子形成六元环彼此相接,每个空间六元环中平均含有的P原子个数为___________ 。白磷和正交型黑磷相比,熔点较高的是___________ ,原因是___________ 。
(3)BP是一种超硬耐磨涂层材料,晶胞结构与金刚石晶胞相似,其晶胞可看作金刚石晶胞内部的C原子被B原子替代,顶点和面心的C原子被P原子替代,晶胞参数为apm。沿z轴从上往下俯视的晶胞投影图如下所示。
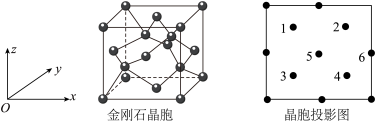
①投影图中原子5代表___________ 原子(填“P”或“B”)。
②若投影图中原子1的分数坐标是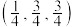 ,则原子6的分数坐标是
,则原子6的分数坐标是___________ ,原子1、6之间的距离为___________ pm。
(1)白磷晶胞属于面心立方最密堆积,每个
 周围距离最近的
周围距离最近的 个数为
个数为
(2)黑磷晶体是一种新型材料,其中正交型黑磷具有类似石墨的片层结构。每一层内P原子形成六元环彼此相接,每个空间六元环中平均含有的P原子个数为

(3)BP是一种超硬耐磨涂层材料,晶胞结构与金刚石晶胞相似,其晶胞可看作金刚石晶胞内部的C原子被B原子替代,顶点和面心的C原子被P原子替代,晶胞参数为apm。沿z轴从上往下俯视的晶胞投影图如下所示。

①投影图中原子5代表
②若投影图中原子1的分数坐标是
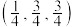 ,则原子6的分数坐标是
,则原子6的分数坐标是
您最近一年使用:0次
4 . 化学与科学、社会、历史密切相关,下列叙述错误的是
| A.敦煌壁画的颜料之一云母为聚硅酸盐,其阴离子以硅氧四面体为结构单元构成 |
B.用纳米技术催化 合成可降解塑料聚碳酸酯,可实现“碳”的循环利用 合成可降解塑料聚碳酸酯,可实现“碳”的循环利用 |
C.纳米铁粉可以高效地吸咐去除污水中的 、 、 、 、 等重金属离子 等重金属离子 |
| D.“垃圾分类”将易腐垃圾转化成热值较高的可燃性气体,属于生物质能热化学转换 |
您最近一年使用:0次
2023-07-11更新
|
62次组卷
|
2卷引用:安徽省安庆、池州、铜陵三市2022-2023学年高二下学期期末检测化学试题
5 . 氮的化合物丰富多彩,请回答:
(1)HSCN的结构有两种,这两种分子结构中除氢外各原子均满足八电子稳定结构(无配位键),请画出沸点高的分子的结构式_______ , 解释沸点高的原因_______ 。
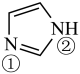
(2)杂环化合物咪唑结构如图,已知分子中的大π键可用符号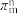 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为 ),眯唑分子中的大π键可表示为
),眯唑分子中的大π键可表示为 ,则咪唑分子中②号氮的杂化方式为
,则咪唑分子中②号氮的杂化方式为_______ , 结合质子能力更强的氮原子是_______ (填“①”或“②”)。
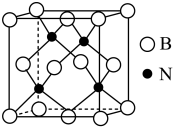
(3)立方氮化硼硬度仅次于金刚石,但热稳定性远高于金刚石,其晶胞结构如图所示,立方氮化硼属于_______ 晶体, 其中硼原子的配位数为_______ 。
(4)SiCl4、NCl3均可发生水解反应,SiCl4水解机理如图:
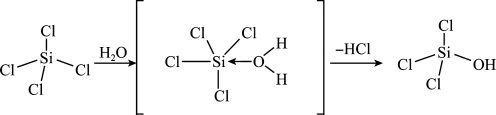
已知中间体SiCl4(H2O)的中心原子Si采取的杂化类型为sp3d,下列关于该中间体VSEPR模型的空间结构推断合理的是_______ (填标号)。
a.正四面体 b.三角双锥 c.正八面体
请画出NCl3水解时生成的中间体_______ 。
(1)HSCN的结构有两种,这两种分子结构中除氢外各原子均满足八电子稳定结构(无配位键),请画出沸点高的分子的结构式
(2)杂环化合物咪唑结构如图,已知分子中的大π键可用符号
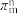 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为 ),眯唑分子中的大π键可表示为
),眯唑分子中的大π键可表示为 ,则咪唑分子中②号氮的杂化方式为
,则咪唑分子中②号氮的杂化方式为
(3)立方氮化硼硬度仅次于金刚石,但热稳定性远高于金刚石,其晶胞结构如图所示,立方氮化硼属于

(4)SiCl4、NCl3均可发生水解反应,SiCl4水解机理如图:

已知中间体SiCl4(H2O)的中心原子Si采取的杂化类型为sp3d,下列关于该中间体VSEPR模型的空间结构推断合理的是
a.正四面体 b.三角双锥 c.正八面体
请画出NCl3水解时生成的中间体
您最近一年使用:0次
6 . 近年来,我国航空工业发展迅速。下列说法错误的是
| A.“天问一号”探测器用到聚酰亚胺薄膜,聚酰亚胺属于高分子材料 |
| B.C919飞机发动机用到大量碳纤维材料,碳纤维属于有机高分子材料 |
| C.“嫦娥五号”月壤样品中发现天然玻璃,玻璃属于无机非金属材料 |
| D.“祝融号”火星车选用新型铝基碳化硅复合材料,碳化硅(SiC)属于共价晶体 |
您最近一年使用:0次
名校
解题方法
7 . 下列说法正确的是
A. 和 和 中C、O、N杂化方式均相同 中C、O、N杂化方式均相同 |
B. 和 和 分子都是含极性键的极性分子 分子都是含极性键的极性分子 |
| C.最外层电子数为2的元素都分布在s区 |
| D.石墨晶体层内是共价键,层与层间是范德华力,所以石墨是一种过渡晶体 |
您最近一年使用:0次
名校
解题方法
8 . 完成下列问题
Ⅰ.氨是重要的化工原料,已知NH3(g)在纯氧中燃烧的能量变化如图。

(1)已知: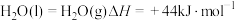 ,则NH3(g)的燃烧热的热化学方程式为
,则NH3(g)的燃烧热的热化学方程式为_______ 。
Ⅱ.火箭推进器中装有肼(N2H4)和过氧化氢。已知下列各物质反应的热化学方程式:
①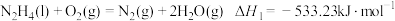
②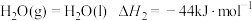
③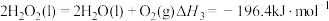
(2)以下选项中,是氮原子激发态的电子排布式,且其中能量较高的是_______ 。(填标号)
a.1s22s22p23s1 b.ls22s22p43d2 c.1s22s12p5 d.1s22s22p13p2
(3)N2H4晶体的晶胞结构_______ (填“是”或者“不”)符合分子密堆积,原因是_______ 。
(4)16g液态联氨与足量过氧化氢反应生成氮气和水蒸气,放出热量为:_______ (保留小数点后一位有效数字)。
(5)在高温下,N2H4可完全分解为NH3、N2及H2,实验测得分解产物中N2与H2的物质的量之比为3∶2,则该分解反应的化学方程式为_______ 。
(6)有以下物质:①碘、②金刚砂、③氨气、④氯化钠、⑤水晶、⑥肼,它们的熔点由高到低的顺序为_______ (用序号表示)。
Ⅰ.氨是重要的化工原料,已知NH3(g)在纯氧中燃烧的能量变化如图。

(1)已知:
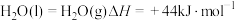 ,则NH3(g)的燃烧热的热化学方程式为
,则NH3(g)的燃烧热的热化学方程式为Ⅱ.火箭推进器中装有肼(N2H4)和过氧化氢。已知下列各物质反应的热化学方程式:
①
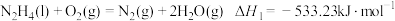
②
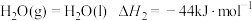
③
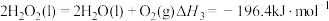
(2)以下选项中,是氮原子激发态的电子排布式,且其中能量较高的是
a.1s22s22p23s1 b.ls22s22p43d2 c.1s22s12p5 d.1s22s22p13p2
(3)N2H4晶体的晶胞结构
(4)16g液态联氨与足量过氧化氢反应生成氮气和水蒸气,放出热量为:
(5)在高温下,N2H4可完全分解为NH3、N2及H2,实验测得分解产物中N2与H2的物质的量之比为3∶2,则该分解反应的化学方程式为
(6)有以下物质:①碘、②金刚砂、③氨气、④氯化钠、⑤水晶、⑥肼,它们的熔点由高到低的顺序为
您最近一年使用:0次
9 . 下列关于物质的说法正确的是
| A.在金刚石晶体中,最小的环上有6个碳原子 |
| B.杯酚是一种常见的超分子,能与C60结合,不能与C70结合,因此可实现C60和C70的分离 |
| C.B3N3H6(无机苯)的结构与苯类似,其熔点主要取决于所含化学键的键能 |
| D.某些金属盐灼烧呈现不同焰色是因为电子从低能级跃迁至较高能级时吸收光的波长不同 |
您最近一年使用:0次
2023-06-25更新
|
156次组卷
|
2卷引用:浙江省温州市十校联合体2022-2023学年高二下学期期末联考化学试题
10 . 2023年3月16日发布的最新款华为MateX3将石墨烯正式应用到手机里,利用石墨烯薄片液冷散热系统成为全球最强散热手机系统。石墨烯是由碳原子组成的最薄、最轻、最强材料,被誉为“材料之王”。回答下列问题:
(1)写出基态C原子的电子排布式_______ 。
(2)氧硫化碳(COS)是一种无机化合物,结构上与CO2类似。
①氧硫化碳(COS)含有的化学键类型_______ 。
A.σ键 B.π键 C.金属键 D.离子键
②C、O、S的电负性大小顺序是_______ (用元素符号表示)。
(3)石墨烯是只由一层碳原子所构成的平面薄膜,结构如图所示。

石墨烯中C原子的轨道杂化方式为_______ ,从石墨中剥离得到石墨烯需克服的作用是_______ ;在石墨烯中,每个六元环占有个_______ C原子。
(4)比较碳化硅(化学式:SiC)与晶体硅、金刚石三者的熔点高低_______ (用化学式表示);从物质结构角度解释原因_______ 。
(5)石墨烯可转化为富勒烯(C60),某金属M与C60可制备一种低温超导材料,晶胞如图所示,M原子位于晶胞的棱上与内部,该晶胞中M原子的个数为_______ ,该材料的化学式为_______ 。

(1)写出基态C原子的电子排布式
(2)氧硫化碳(COS)是一种无机化合物,结构上与CO2类似。
①氧硫化碳(COS)含有的化学键类型
A.σ键 B.π键 C.金属键 D.离子键
②C、O、S的电负性大小顺序是
(3)石墨烯是只由一层碳原子所构成的平面薄膜,结构如图所示。

石墨烯中C原子的轨道杂化方式为
(4)比较碳化硅(化学式:SiC)与晶体硅、金刚石三者的熔点高低
(5)石墨烯可转化为富勒烯(C60),某金属M与C60可制备一种低温超导材料,晶胞如图所示,M原子位于晶胞的棱上与内部,该晶胞中M原子的个数为

您最近一年使用:0次



