10-11高二下·山东烟台·期末
1 . “人文奥运”的一个重要体现是:坚决反对运动员服用兴奋剂。某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是
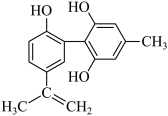
A.遇 溶液显紫色,因为该物质与苯酚属于同系物 溶液显紫色,因为该物质与苯酚属于同系物 |
B.滴入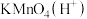 溶液,观察紫色褪去,能证明结构中存在碳碳双键 溶液,观察紫色褪去,能证明结构中存在碳碳双键 |
C. 该物质与浓溴水和 该物质与浓溴水和 反应最多消耗 反应最多消耗 和 和 分别为 分别为 、 、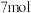 |
| D.该分子中的所有碳原子不可能共平面 |
您最近一年使用:0次
2023-03-26更新
|
258次组卷
|
11卷引用:山西省怀仁县第八中学2016-2017学年高二(普通班)下学期期末考试化学试题
山西省怀仁县第八中学2016-2017学年高二(普通班)下学期期末考试化学试题(已下线)2010—2011学年山东省烟台市高二下学期期末模块检测化学试卷(已下线)2011-2012学年浙江省温州八校高二上学期期末联考化学试卷(已下线)2012-2013学年浙江省杭州地区七校高二期中联考化学试卷(已下线)2012-2013学年山东省聊城市某重点中学高二第四次模块检测化学试卷(已下线)2013-2014学年湖南省衡阳市八中高二上学期期中考试化学试卷(已下线)2013-2014湖南省衡阳市八中上学期期中考试高二化学试卷2014-2015学年辽宁省沈阳市沈阳二中高二下期中化学试卷陕西省渭南市尚德中学2018-2019学年高二下学期期中考试化学试题北京市海淀区教师进修学校2022-2023学年高二下学期3月月考化学试题河南省商丘市十校联考2023-2024学年高二下学期期末考试化学试题
名校
解题方法
2 . 室温下,通过下列实验探究NaHS溶液的性质。
实验1:向0.1 mol/L NaHS溶液中滴加几滴酚酞试剂,溶液变红
实验2:向0.1 mol/L NaHS溶液中通入过量氯气,无淡黄色沉淀产生
实验3:向0.1 mol/L NaHS溶液中加入等体积0.1 mol/L NaOH溶液充分混合
实验4:向0.1 mol/L NaHS溶液中滴加过量 溶液,产生黑色沉淀
溶液,产生黑色沉淀
下列有关说法正确的是
实验1:向0.1 mol/L NaHS溶液中滴加几滴酚酞试剂,溶液变红
实验2:向0.1 mol/L NaHS溶液中通入过量氯气,无淡黄色沉淀产生
实验3:向0.1 mol/L NaHS溶液中加入等体积0.1 mol/L NaOH溶液充分混合
实验4:向0.1 mol/L NaHS溶液中滴加过量
 溶液,产生黑色沉淀
溶液,产生黑色沉淀下列有关说法正确的是
A.实验1证明: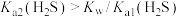 |
B.实验2证明: 不能被 不能被 氧化 氧化 |
C.实验3中所得溶液中: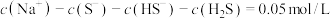 |
D.实验4反应静置后的上层清液中有 |
您最近一年使用:0次
2023-01-08更新
|
571次组卷
|
3卷引用:山西省大同市第一中学校2022-2023学年高二上学期期末考试化学试卷
名校
解题方法
3 . 铁是日常生活中最常见的金属,某班同学在学习铁的知识时,有下列问题:
问题1:铁为何称为黑色金属?
问题2:CuO在高温下可分解为Cu2O和O2,Fe2O3在高温下可分解为FeO和O2吗?
(1)对于问题1,同学们上网查找,有两种解释:
A.因为在铁表面上有黑色的铁的氧化物,所以叫黑色金属
B.因为铁的粉末为黑色,铁的氧化物也均为黑色,所以叫黑色金属
①你认为正确的说法是__________ 。
②若有一黑色粉末,如何鉴别是铁粉,还是Fe3O4?______________________________________ 。
③若有一黑色粉末,为铁和四氧化三铁的混合物,如何证明其中有Fe3O4(只要求简述实验方法)?____________________________________ 。
(2)对于问题2,同学们准备实验探究,他们设想了两种方法:
A.将三氧化二铁高温灼烧,看灼烧前后颜色是否变化。
B.将三氧化二铁高温灼烧,看灼烧前后质量是否变化。
①实验中应将Fe2O3放在__________ (填仪器名称)中灼烧。
②方法A中,如果高温灼烧后颜色由__________ 变为__________ ,说明Fe2O3确实发生了变化。能说明生成的一定为FeO吗?__________ ,理由是________________________ 。
③方法B中,如果发生了预期的反应,固体高温灼烧前后质量比应为________ ,但是,实验结果固体灼烧前后质量比为30∶29,则高温灼烧后生成物是____________________ 。
④比较两种方法,你认为较好的方法是__________ 。
问题1:铁为何称为黑色金属?
问题2:CuO在高温下可分解为Cu2O和O2,Fe2O3在高温下可分解为FeO和O2吗?
(1)对于问题1,同学们上网查找,有两种解释:
A.因为在铁表面上有黑色的铁的氧化物,所以叫黑色金属
B.因为铁的粉末为黑色,铁的氧化物也均为黑色,所以叫黑色金属
①你认为正确的说法是
②若有一黑色粉末,如何鉴别是铁粉,还是Fe3O4?
③若有一黑色粉末,为铁和四氧化三铁的混合物,如何证明其中有Fe3O4(只要求简述实验方法)?
(2)对于问题2,同学们准备实验探究,他们设想了两种方法:
A.将三氧化二铁高温灼烧,看灼烧前后颜色是否变化。
B.将三氧化二铁高温灼烧,看灼烧前后质量是否变化。
①实验中应将Fe2O3放在
②方法A中,如果高温灼烧后颜色由
③方法B中,如果发生了预期的反应,固体高温灼烧前后质量比应为
④比较两种方法,你认为较好的方法是
您最近一年使用:0次
名校
解题方法
4 . 某小组设计实验探究 和浓盐酸反应的最低浓度以及氯气的性质,实验装置如图所示。
和浓盐酸反应的最低浓度以及氯气的性质,实验装置如图所示。
回答下列问题:
(1)装置B中试剂是________ (填名称),装置E的作用是____________ 。
(2)装置A中反应的离子方程式为______________ 。
(3)能证明氯的非金属性比硫强的实验现象是___________ 。经检验装置C中最终生成了 ,写出C中浑浊变澄清时反应的化学方程式:
,写出C中浑浊变澄清时反应的化学方程式:____________ 。
(4)根据装置D中现象,有人认为 被氧化了。请你设计实验证明他的观点是否正确:
被氧化了。请你设计实验证明他的观点是否正确:____________ 。
(5)实验完毕后,利用下列装置测定装置A中剩余盐酸的浓度:
将装置A中剩余溶液过滤,取 滤液进行实验,最终收集
滤液进行实验,最终收集 的体积为
的体积为 (已折合成标准状况)。
(已折合成标准状况)。
a.读数 b.冷却至室温 c.调平量气管和烧杯的液面
正确操作步骤的顺序为________ (填字母)。
②能与 反应的最低盐酸浓度为
反应的最低盐酸浓度为________  (用含
(用含 、
、 的代数式表示)。
的代数式表示)。
 和浓盐酸反应的最低浓度以及氯气的性质,实验装置如图所示。
和浓盐酸反应的最低浓度以及氯气的性质,实验装置如图所示。
回答下列问题:
(1)装置B中试剂是
(2)装置A中反应的离子方程式为
(3)能证明氯的非金属性比硫强的实验现象是
 ,写出C中浑浊变澄清时反应的化学方程式:
,写出C中浑浊变澄清时反应的化学方程式:(4)根据装置D中现象,有人认为
 被氧化了。请你设计实验证明他的观点是否正确:
被氧化了。请你设计实验证明他的观点是否正确:(5)实验完毕后,利用下列装置测定装置A中剩余盐酸的浓度:
将装置A中剩余溶液过滤,取
 滤液进行实验,最终收集
滤液进行实验,最终收集 的体积为
的体积为 (已折合成标准状况)。
(已折合成标准状况)。
a.读数 b.冷却至室温 c.调平量气管和烧杯的液面
正确操作步骤的顺序为
②能与
 反应的最低盐酸浓度为
反应的最低盐酸浓度为 (用含
(用含 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2024-04-04更新
|
656次组卷
|
5卷引用:山西省晋中市2024届高三第二次优生测试理综合化学试题-
山西省晋中市2024届高三第二次优生测试理综合化学试题-河南省濮阳市2024届高三下学期第二次模拟考试理科综合化学试题河南省濮阳市2024届高三第一次模拟考试理综-化学试题(已下线)题型9 实验综合题(25题)-2024年高考化学常考点必杀300题(新高考通用)2024届河南省鹤壁市高中高三下学期模拟预测化学试题
解题方法
5 . 铁及其化合物在生产、生活中有重要作用。回答下列问题:
I.硫酸亚铁晶体 在医药上常用作补血剂。某课外小组的同学通过实验测定补血剂中硫酸亚铁晶体的质量分数,实验步骤如图所示:
在医药上常用作补血剂。某课外小组的同学通过实验测定补血剂中硫酸亚铁晶体的质量分数,实验步骤如图所示:

(1)证明经步骤①得到的滤液中含有 的方法如下:取样,先滴加
的方法如下:取样,先滴加___________ ,再滴加少量氯水,该过程的现象为___________ 。
(2)步骤②加入氯水发生反应的离子方程式是___________ 。
(3)步骤③产生的红褐色物质成分是___________ (写化学式)。
(4)步骤④中一系列操作为___________ 、洗涤、干燥、灼烧。
(5)若所取补血剂质量为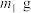 ,最终得到红棕色固体C的质量为
,最终得到红棕色固体C的质量为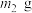 ,则补血剂中硫酸亚铁晶体的质量分数为
,则补血剂中硫酸亚铁晶体的质量分数为___________ (用含 、
、 的代数式表示,不考虑实验中铁元素的损失)。
的代数式表示,不考虑实验中铁元素的损失)。
II.高铁酸钾 是一种新型、高效、多功能绿色水处理剂。工业上制备高铁酸钾以及高铁酸钾处理污水的部分流程如下:
是一种新型、高效、多功能绿色水处理剂。工业上制备高铁酸钾以及高铁酸钾处理污水的部分流程如下:

(6)过程①制取1mol ,理论上需要
,理论上需要 物质的量为
物质的量为___________ ,步骤②中反应能够发生的原因是___________ ,分离出 固体的操作中使用的玻璃仪器有
固体的操作中使用的玻璃仪器有___________ 。
I.硫酸亚铁晶体
 在医药上常用作补血剂。某课外小组的同学通过实验测定补血剂中硫酸亚铁晶体的质量分数,实验步骤如图所示:
在医药上常用作补血剂。某课外小组的同学通过实验测定补血剂中硫酸亚铁晶体的质量分数,实验步骤如图所示:
(1)证明经步骤①得到的滤液中含有
 的方法如下:取样,先滴加
的方法如下:取样,先滴加(2)步骤②加入氯水发生反应的离子方程式是
(3)步骤③产生的红褐色物质成分是
(4)步骤④中一系列操作为
(5)若所取补血剂质量为
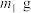 ,最终得到红棕色固体C的质量为
,最终得到红棕色固体C的质量为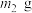 ,则补血剂中硫酸亚铁晶体的质量分数为
,则补血剂中硫酸亚铁晶体的质量分数为 、
、 的代数式表示,不考虑实验中铁元素的损失)。
的代数式表示,不考虑实验中铁元素的损失)。II.高铁酸钾
 是一种新型、高效、多功能绿色水处理剂。工业上制备高铁酸钾以及高铁酸钾处理污水的部分流程如下:
是一种新型、高效、多功能绿色水处理剂。工业上制备高铁酸钾以及高铁酸钾处理污水的部分流程如下:
(6)过程①制取1mol
 ,理论上需要
,理论上需要 物质的量为
物质的量为 固体的操作中使用的玻璃仪器有
固体的操作中使用的玻璃仪器有
您最近一年使用:0次
解题方法
6 . 研究+6价铬盐在不同条件下微粒的存在形式及氧化性强弱,某小组同学进行如下实验:
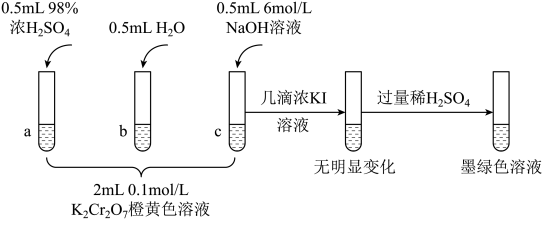
已知: (橙色)
(橙色)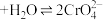 (黄色)
(黄色)
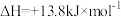 ,+6价铬盐在一定条件下可被还原为
,+6价铬盐在一定条件下可被还原为 ,
, 在水溶液中为绿色。
在水溶液中为绿色。
(1)试管c和b对比,推测试管c中的现象是_______ 。
(2)试管a和b对比,a中溶液橙色加深。甲认为温度也会影响平衡的移动,橙色加深不一定是c(H+)增大影响的结果;乙认为橙色加深一定是c(H+)增大对平衡的影响。你认为是否需要再设计实验证明?_______ (“是”或“否”),理由是_______ 。
(3)对比试管a、b、c中的实验现象,可以得到的结论是_______ 。
(4)试管c中继续滴加浓KI溶液、过量稀 ,分析上图的实验现象,得出的结论是
,分析上图的实验现象,得出的结论是_______ ,写出此过程中氧化还原反应的离子方程式:_______ 。
(5) 的
的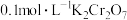 ,溶液中
,溶液中 离子数目
离子数目_______  (填“大于”、“小于”或“等于”,
(填“大于”、“小于”或“等于”, 为阿伏加德罗常数的值),溶液中
为阿伏加德罗常数的值),溶液中 的数目为
的数目为_______ 。

已知:
 (橙色)
(橙色)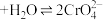 (黄色)
(黄色)
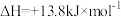 ,+6价铬盐在一定条件下可被还原为
,+6价铬盐在一定条件下可被还原为 ,
, 在水溶液中为绿色。
在水溶液中为绿色。(1)试管c和b对比,推测试管c中的现象是
(2)试管a和b对比,a中溶液橙色加深。甲认为温度也会影响平衡的移动,橙色加深不一定是c(H+)增大影响的结果;乙认为橙色加深一定是c(H+)增大对平衡的影响。你认为是否需要再设计实验证明?
(3)对比试管a、b、c中的实验现象,可以得到的结论是
(4)试管c中继续滴加浓KI溶液、过量稀
 ,分析上图的实验现象,得出的结论是
,分析上图的实验现象,得出的结论是(5)
 的
的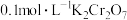 ,溶液中
,溶液中 离子数目
离子数目 (填“大于”、“小于”或“等于”,
(填“大于”、“小于”或“等于”, 为阿伏加德罗常数的值),溶液中
为阿伏加德罗常数的值),溶液中 的数目为
的数目为
您最近一年使用:0次
名校
7 . 某学习小组为了探究影响高锰酸钾酸性溶液与NaHSO3溶液反应速率的因素,该小组设计如表实验方案。
下列说法正确的是
| 实验 | V(NaHSO3)/mL c=0.1 mol/L | V(KMnO4)/mL c=0.6 mol/L | V(H2SO4)/mL c=0.1 mol/L | V(MnSO4)/mL c=0.1 mol/L | V(H2O)/mL | 褪色时间t/min |
| 1 | 3.0 | 2.0 | 1.0 | 0.0 | 2.0 | 8 |
| 2 | 3.0 | 2.0 | 2.0 | 0.0 | a | 6 |
| 3 | 4.0 | 2.0 | 2.0 | 0.0 | 0.0 | 4 |
| 4 | 4.0 | 2.0 | 1.0 | 0.5 | b | 3 |
A.该反应的离子方程式为:5 +2 +2 +6H+=2Mn2++5 +6H+=2Mn2++5 +3H2O +3H2O |
| B.a=1.0,b=0.5 |
C.实验3从反应开始到反应结束这段时间内反应速率v( )=0.025 mol/(L∙min) )=0.025 mol/(L∙min) |
D.实验证明 可能是该反应的催化剂 可能是该反应的催化剂 |
您最近一年使用:0次
2023-04-25更新
|
396次组卷
|
14卷引用:山西省吕梁市临县第一中学2021-2022学年高一下学期5月月考化学试题
山西省吕梁市临县第一中学2021-2022学年高一下学期5月月考化学试题广西玉林市普通高中2021-2022学年高一下学期期末考试化学试题河南省开封市五县2021-2022学年高二下学期期末考试化学试题(已下线)2.1.2 影响化学反应速率的因素 活化能 -2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)重庆市西南大学附属中学校2021-2022学年高一下学期期末考试化学试题(已下线)化学反应速率与化学平衡——课时2化学反应速率的影响因素(已下线)【2023】【高一下】【其他】【余高2】【高中化学】【刘尼尼收集】新疆生产建设兵团第一师高级中学2022-2023学年高一下学期4月月考化学试题贵州省遵义市仁怀市高中教育联盟2022-2023学年高一下学期5月期中考试化学试题(已下线)第05练 化学反应的速率与限度-2023年【暑假分层作业】高一化学(人教版2019必修第二册)山东省东营市利津县高级中学2022-2023学年高一下学期5月月考化学试题 四川省射洪中学2022—2023学年高一下学期(强基班)第三次月考化学试题四川省射洪中学校强基班2023-2024学年高一下学期4月第一次月考化学试题(已下线)清单04 化学反应的速率和限度(考点清单)(讲+练)-2023-2024学年高一化学下学期期末考点大串讲(人教版2019必修第二册)
解题方法
8 . 铋(Bi)的化合物广泛应用于电子、医药等领域。由辉铋矿(主要成分为Bi2S3含FeS2、CuO、SiO2等杂质)制备NaBiO3的工艺流程如下:
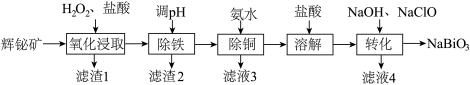
已知:
i. Bi3+易水解,NaBiO3难溶于冷水。
ii.“氧化浸取”时,铋元素转化为Bi3+,硫元素转化为硫单质。
iii. Cu(OH)2(s) +4NH3(g) Cu[(NH3)4]2+ (aq)+2OH—(aq)K=4.4×10-7。
Cu[(NH3)4]2+ (aq)+2OH—(aq)K=4.4×10-7。
回答下列问题:
(1)为提高“浸取”速率,采取的措施有:升高温度、___________ (写出一条);辉铋矿浸取率随温度的变化曲线如图,高于40℃时浸取率快速下降,其可能的原因是____________ 。

(2)“氧化浸取”时,H2O2和FeS2发生反应的物质的量之比为___________ 。
(3)“除铜”时发生反应:Cu2+ (aq) + 4NH3(g) Cu[(NH3)4]2+ (aq) K=2×1013,则Ksp[Cu(OH)2]=
Cu[(NH3)4]2+ (aq) K=2×1013,则Ksp[Cu(OH)2]=___________ ;NH3分子的空间结构为___________ 。
(4)“转化”时,生成NaBiO3的离子方程式为___________ 。
(5)已知酸性环境下,NaBiO3可以将Mn2+氧化成 、(
、(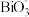 被还原成Bi3+),请设计一个原电池装置来证明这一点,在图中的方框内标出两烧杯溶液中溶质的化学式,并写出负极的电极反应式:
被还原成Bi3+),请设计一个原电池装置来证明这一点,在图中的方框内标出两烧杯溶液中溶质的化学式,并写出负极的电极反应式:___________ 。
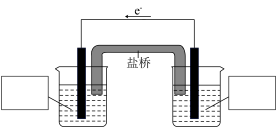
(6)取NaBiO3产品w g,加入足量稀硫酸和MnSO4稀溶液使其完全反应,再用a mol· L-1H2C2O4标准溶液滴定生成的 ,当溶液紫红色恰好褪去时,消耗bmL标准溶液,该产品的纯度为
,当溶液紫红色恰好褪去时,消耗bmL标准溶液,该产品的纯度为___________ (用含w、a、b的代数式表示)。

已知:
i. Bi3+易水解,NaBiO3难溶于冷水。
ii.“氧化浸取”时,铋元素转化为Bi3+,硫元素转化为硫单质。
iii. Cu(OH)2(s) +4NH3(g)
 Cu[(NH3)4]2+ (aq)+2OH—(aq)K=4.4×10-7。
Cu[(NH3)4]2+ (aq)+2OH—(aq)K=4.4×10-7。回答下列问题:
(1)为提高“浸取”速率,采取的措施有:升高温度、

(2)“氧化浸取”时,H2O2和FeS2发生反应的物质的量之比为
(3)“除铜”时发生反应:Cu2+ (aq) + 4NH3(g)
 Cu[(NH3)4]2+ (aq) K=2×1013,则Ksp[Cu(OH)2]=
Cu[(NH3)4]2+ (aq) K=2×1013,则Ksp[Cu(OH)2]=(4)“转化”时,生成NaBiO3的离子方程式为
(5)已知酸性环境下,NaBiO3可以将Mn2+氧化成
 、(
、(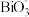 被还原成Bi3+),请设计一个原电池装置来证明这一点,在图中的方框内标出两烧杯溶液中溶质的化学式,并写出负极的电极反应式:
被还原成Bi3+),请设计一个原电池装置来证明这一点,在图中的方框内标出两烧杯溶液中溶质的化学式,并写出负极的电极反应式:
(6)取NaBiO3产品w g,加入足量稀硫酸和MnSO4稀溶液使其完全反应,再用a mol· L-1H2C2O4标准溶液滴定生成的
 ,当溶液紫红色恰好褪去时,消耗bmL标准溶液,该产品的纯度为
,当溶液紫红色恰好褪去时,消耗bmL标准溶液,该产品的纯度为
您最近一年使用:0次
名校
解题方法
9 . 铝是一种重要的金属,在生产、生活中具有许多重要的用途,下图是用铝土矿(主要成分是 ,此外还含有少量
,此外还含有少量 、
、 等杂质)制备铝的工艺流程:
等杂质)制备铝的工艺流程:
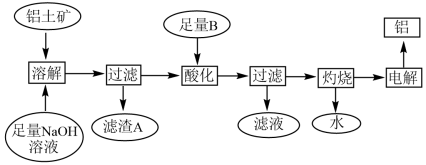
已知:溶液中的硅酸钠能与偏铝酸钠反应,生成硅铝酸盐沉淀,反应的化学方程式为 。
。
(1)铝土矿中的 与氢氧化钠溶液反应的离子方程式为
与氢氧化钠溶液反应的离子方程式为___________ 。
(2)在工艺流程中“酸化”时,加入的最佳物质B是___________ ,理由是___________ 。
(3)工业上用 与C、
与C、 在高温条件下反应制取
在高温条件下反应制取 ,理论上每消耗6.0g碳单质,转移1mol电子,该反应的化学方程式为
,理论上每消耗6.0g碳单质,转移1mol电子,该反应的化学方程式为___________ 。
(4)某同学为验证铝与氧化铁发生铝热反应得到的熔融物中还含有 ,设计了如下方案:取一块熔融物投入少量稀硫酸中,反应一段时间后,向混合液中滴加物质甲的溶液,观察溶液颜色的变化,即可证明熔融物中是否含有
,设计了如下方案:取一块熔融物投入少量稀硫酸中,反应一段时间后,向混合液中滴加物质甲的溶液,观察溶液颜色的变化,即可证明熔融物中是否含有 。则物质甲是
。则物质甲是___________ (填化学式),该同学设计的实验方案___________ (填“合理”或“不合理”),原因是___________ (若合理,则不用填写)。
 ,此外还含有少量
,此外还含有少量 、
、 等杂质)制备铝的工艺流程:
等杂质)制备铝的工艺流程:
已知:溶液中的硅酸钠能与偏铝酸钠反应,生成硅铝酸盐沉淀,反应的化学方程式为
 。
。(1)铝土矿中的
 与氢氧化钠溶液反应的离子方程式为
与氢氧化钠溶液反应的离子方程式为(2)在工艺流程中“酸化”时,加入的最佳物质B是
(3)工业上用
 与C、
与C、 在高温条件下反应制取
在高温条件下反应制取 ,理论上每消耗6.0g碳单质,转移1mol电子,该反应的化学方程式为
,理论上每消耗6.0g碳单质,转移1mol电子,该反应的化学方程式为(4)某同学为验证铝与氧化铁发生铝热反应得到的熔融物中还含有
 ,设计了如下方案:取一块熔融物投入少量稀硫酸中,反应一段时间后,向混合液中滴加物质甲的溶液,观察溶液颜色的变化,即可证明熔融物中是否含有
,设计了如下方案:取一块熔融物投入少量稀硫酸中,反应一段时间后,向混合液中滴加物质甲的溶液,观察溶液颜色的变化,即可证明熔融物中是否含有 。则物质甲是
。则物质甲是
您最近一年使用:0次
2021-12-17更新
|
268次组卷
|
2卷引用:山西省名校2021-2022学年高一上学期12月阶段性测试化学试题
10 . 氨气是一种重要化合物,在工农业生产、生活中有着重要应用。
(1)氨的催化氧化是工业生产硝酸的重要步骤。某化学课外活动小组设计了如图装置模拟该实验过程,并用水吸收制取硝酸(部分固定装置略去):
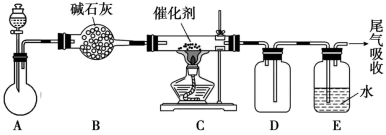
①装置A的分液漏斗中盛放浓氨水,则烧瓶中盛放的药品应该是___________ (填化学式)。
②装置C中反应的方程式为___________ ;反应后,装置E中除存在较多的H+外,还可能存在的一种阳离子是___________ ,试设计实验证明这种离子的存在:___________ 。
(2)下列哪个装置可以同时起到装置D和E的作用___________ (填标号)。
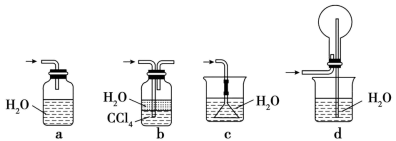
(3)若将氯气和氨气在集气瓶中混合,会出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一,请写出该反应的化学方程式:___________ ,该反应生成的还原产物的化学键类型是___________ 。
(1)氨的催化氧化是工业生产硝酸的重要步骤。某化学课外活动小组设计了如图装置模拟该实验过程,并用水吸收制取硝酸(部分固定装置略去):


①装置A的分液漏斗中盛放浓氨水,则烧瓶中盛放的药品应该是
②装置C中反应的方程式为
(2)下列哪个装置可以同时起到装置D和E的作用

(3)若将氯气和氨气在集气瓶中混合,会出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一,请写出该反应的化学方程式:
您最近一年使用:0次



