名校
1 . 维生素C是一种水溶性维生素,有强还原性、水溶液显酸性。化学式为 。某小组同学测定了某新鲜水果中维生素C的含量,实验报告如下:
。某小组同学测定了某新鲜水果中维生素C的含量,实验报告如下:
【实验目的】测定某新鲜水果中维生素C的含量。
【实验原理】 ,
,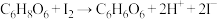 。
。
【实验用品】 标准溶液、指示剂、
标准溶液、指示剂、 溶液、
溶液、 溶液、蒸馏水等。
溶液、蒸馏水等。
【实验步骤】
(1)配制待测溶液:称取新鲜水果样品 ,加入适量蒸馏水进行粉碎、过滤,并将滤液转移至
,加入适量蒸馏水进行粉碎、过滤,并将滤液转移至 容量瓶中,定容,随后将待测溶液加到滴定管中。根据维生素C的性质,待测溶液应用
容量瓶中,定容,随后将待测溶液加到滴定管中。根据维生素C的性质,待测溶液应用___________ (填“酸式”或“碱式”)滴定管盛装。
(2)氧化还原滴定法:取(1)中配制好的待测溶液 于锥形瓶中,调节
于锥形瓶中,调节 至3,加入适量指示剂后,小心地滴入
至3,加入适量指示剂后,小心地滴入 标准溶液,直至滴定终点,记录相关数据。平行测定三次,计算新鲜水果中维生素
标准溶液,直至滴定终点,记录相关数据。平行测定三次,计算新鲜水果中维生素 的质量分数。
的质量分数。
①上述氧化还原滴定法应用___________ 作指示剂,滴定终点的现象为___________ 。
②除了样品的质量、待测溶液的体积外,计算新鲜水果中维生素C的质量分数还需要的数据有___________ 。
(3)库仑滴定法:取(1)中配制好的待测溶液 ,用库仑仪测定其中维生素C的含量。平行测定三次,计算新鲜水果中维生素C的质量分数。
,用库仑仪测定其中维生素C的含量。平行测定三次,计算新鲜水果中维生素C的质量分数。
已知:库仑仪中电解原理示意图如下。检测前,电解质溶液中 保持定值时,电解池不工作。将待测溶液加入电解池后,维生素C将
保持定值时,电解池不工作。将待测溶液加入电解池后,维生素C将 还原,库仑仪便立即自动进行电解到
还原,库仑仪便立即自动进行电解到 又回到原定值,测定结束,通过测定电解消托的电量可以求得维生素C的含量。
又回到原定值,测定结束,通过测定电解消托的电量可以求得维生素C的含量。

①库仑仪工作时电解池的阳极反应式为___________ 。
②若电解消耗的电量为Q库仑,维生素C的摩尔质量为 ,则新鲜水果中维生素C的质量分数为
,则新鲜水果中维生素C的质量分数为___________ 。(用含 的代数式表示)已知:电解中转移
的代数式表示)已知:电解中转移 电子所消耗的电量为96500库仑。
电子所消耗的电量为96500库仑。
③测定过程中,需控制电解质溶液 ,当
,当 时,部分
时,部分 易被空气中的
易被空气中的 直接氧化为
直接氧化为 ,该过程的离子方程式为
,该过程的离子方程式为___________ 。这部分非电解生成的 ;将导致测得的维生素C的含量
;将导致测得的维生素C的含量___________ 。(填“偏大”或“偏小”)。
 。某小组同学测定了某新鲜水果中维生素C的含量,实验报告如下:
。某小组同学测定了某新鲜水果中维生素C的含量,实验报告如下:【实验目的】测定某新鲜水果中维生素C的含量。
【实验原理】
 ,
,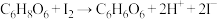 。
。【实验用品】
 标准溶液、指示剂、
标准溶液、指示剂、 溶液、
溶液、 溶液、蒸馏水等。
溶液、蒸馏水等。【实验步骤】
(1)配制待测溶液:称取新鲜水果样品
 ,加入适量蒸馏水进行粉碎、过滤,并将滤液转移至
,加入适量蒸馏水进行粉碎、过滤,并将滤液转移至 容量瓶中,定容,随后将待测溶液加到滴定管中。根据维生素C的性质,待测溶液应用
容量瓶中,定容,随后将待测溶液加到滴定管中。根据维生素C的性质,待测溶液应用(2)氧化还原滴定法:取(1)中配制好的待测溶液
 于锥形瓶中,调节
于锥形瓶中,调节 至3,加入适量指示剂后,小心地滴入
至3,加入适量指示剂后,小心地滴入 标准溶液,直至滴定终点,记录相关数据。平行测定三次,计算新鲜水果中维生素
标准溶液,直至滴定终点,记录相关数据。平行测定三次,计算新鲜水果中维生素 的质量分数。
的质量分数。①上述氧化还原滴定法应用
②除了样品的质量、待测溶液的体积外,计算新鲜水果中维生素C的质量分数还需要的数据有
(3)库仑滴定法:取(1)中配制好的待测溶液
 ,用库仑仪测定其中维生素C的含量。平行测定三次,计算新鲜水果中维生素C的质量分数。
,用库仑仪测定其中维生素C的含量。平行测定三次,计算新鲜水果中维生素C的质量分数。已知:库仑仪中电解原理示意图如下。检测前,电解质溶液中
 保持定值时,电解池不工作。将待测溶液加入电解池后,维生素C将
保持定值时,电解池不工作。将待测溶液加入电解池后,维生素C将 还原,库仑仪便立即自动进行电解到
还原,库仑仪便立即自动进行电解到 又回到原定值,测定结束,通过测定电解消托的电量可以求得维生素C的含量。
又回到原定值,测定结束,通过测定电解消托的电量可以求得维生素C的含量。
①库仑仪工作时电解池的阳极反应式为
②若电解消耗的电量为Q库仑,维生素C的摩尔质量为
 ,则新鲜水果中维生素C的质量分数为
,则新鲜水果中维生素C的质量分数为 的代数式表示)已知:电解中转移
的代数式表示)已知:电解中转移 电子所消耗的电量为96500库仑。
电子所消耗的电量为96500库仑。③测定过程中,需控制电解质溶液
 ,当
,当 时,部分
时,部分 易被空气中的
易被空气中的 直接氧化为
直接氧化为 ,该过程的离子方程式为
,该过程的离子方程式为 ;将导致测得的维生素C的含量
;将导致测得的维生素C的含量
您最近一年使用:0次
2023-12-11更新
|
105次组卷
|
3卷引用:山西省朔州市怀仁市2023-2024学年高二上学期1月期末化学试题
解题方法
2 . 8月1日起,为了国家信息安全,我国禁止镓和锗的出口,锗是一种重要的半导体材料,工业上用精硫锗矿(主要成分为 )制取高纯度锗的工艺流程如图所示:
)制取高纯度锗的工艺流程如图所示:
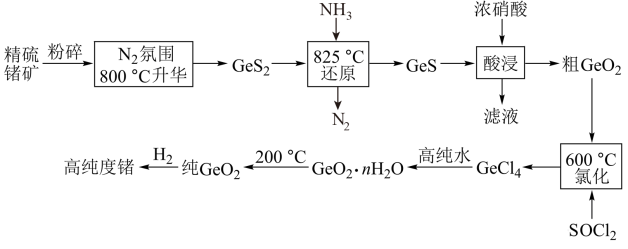
(1) 分子中各原子均达到8电子稳定结构,其结构式为
分子中各原子均达到8电子稳定结构,其结构式为___________ 。
(2)800℃升华时通入 的目的是:
的目的是:___________ 、___________ 。
(3)酸浸时Ge、S元素均被氧化到最高价态,写出该反应的离子方程式:___________ ,酸浸时温度不能过高的原因是___________ 。
(4) 易水解生成
易水解生成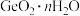 ,证明
,证明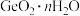 沉淀洗涤干净的方法是
沉淀洗涤干净的方法是___________ 。
(5)测定错的含量:称取0.5500g锗样品,加入双氧水溶解,再加入盐酸生成 ,以淀粉为指示剂,用
,以淀粉为指示剂,用 的碘酸钾标准溶液滴定,消耗碘酸钾的体积为24.80mL。已知:酸性条件下
的碘酸钾标准溶液滴定,消耗碘酸钾的体积为24.80mL。已知:酸性条件下 ,能将
,能将 氧化为
氧化为 ,①在滴定过程中依次发生的离子方程式为:
,①在滴定过程中依次发生的离子方程式为:___________ 、___________ ,②该样品中储的质量分数是___________ %(精确到0.01%)。
 )制取高纯度锗的工艺流程如图所示:
)制取高纯度锗的工艺流程如图所示:
(1)
 分子中各原子均达到8电子稳定结构,其结构式为
分子中各原子均达到8电子稳定结构,其结构式为(2)800℃升华时通入
 的目的是:
的目的是:(3)酸浸时Ge、S元素均被氧化到最高价态,写出该反应的离子方程式:
(4)
 易水解生成
易水解生成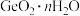 ,证明
,证明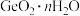 沉淀洗涤干净的方法是
沉淀洗涤干净的方法是(5)测定错的含量:称取0.5500g锗样品,加入双氧水溶解,再加入盐酸生成
 ,以淀粉为指示剂,用
,以淀粉为指示剂,用 的碘酸钾标准溶液滴定,消耗碘酸钾的体积为24.80mL。已知:酸性条件下
的碘酸钾标准溶液滴定,消耗碘酸钾的体积为24.80mL。已知:酸性条件下 ,能将
,能将 氧化为
氧化为 ,①在滴定过程中依次发生的离子方程式为:
,①在滴定过程中依次发生的离子方程式为:
您最近一年使用:0次
名校
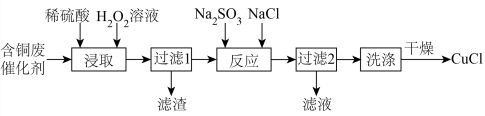
3 . 一种由含铜废催化剂(主要成分为Cu和少量Fe、 、CuO,
、CuO, 等)为原料制备CuCl的工艺流程如下:
等)为原料制备CuCl的工艺流程如下:
已知:CuCl为白色粉末,微溶于水,易溶于 浓度较大的体系
浓度较大的体系 不溶于乙醇,有水存在时易被
不溶于乙醇,有水存在时易被 氧化。
氧化。
回答下列问题:
(1)实验室需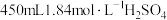 溶液,配制时需量取
溶液,配制时需量取_____ mL98%的硫酸溶液(密度为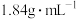 )。
)。
(2)“浸取”时, 的实际用量远远超过理论用量,可能原因是
的实际用量远远超过理论用量,可能原因是__ 。
(3)“反应”时, 与
与 、NaCl在溶液中反应生成CuCl沉淀的离子方程式为
、NaCl在溶液中反应生成CuCl沉淀的离子方程式为___ 。当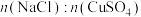 比值逐渐增大时,CuCl产率先增大后减小,原因是
比值逐渐增大时,CuCl产率先增大后减小,原因是_____ 。
(4)为测定某氯化亚铜样品中CuCl的含量,某同学设计如下实验:准确称取氯化亚铜样品mg,将其置于过量的 溶液中完全溶解,加入适量稀硫酸,用
溶液中完全溶解,加入适量稀硫酸,用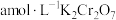 溶液滴定到终点,消耗
溶液滴定到终点,消耗 溶液bmL,
溶液bmL, 被还原为
被还原为 。样品中CuCl的质量分数为
。样品中CuCl的质量分数为_____ %(已知滴定过程发生的反应为 ,不考虑
,不考虑 氧化
氧化 )。
)。
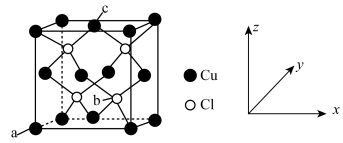
(5)①已知:CuCl的熔点为326℃,能升华,熔化呈液态时不导电。则CuCl晶体属于____ (填晶体类型)。
②若晶胞中a、c原子的分数坐标分别为(0,0,,0)、(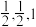 ),则b原子的分数坐标为
),则b原子的分数坐标为_____ 。
 、CuO,
、CuO, 等)为原料制备CuCl的工艺流程如下:
等)为原料制备CuCl的工艺流程如下:
已知:CuCl为白色粉末,微溶于水,易溶于
 浓度较大的体系
浓度较大的体系 不溶于乙醇,有水存在时易被
不溶于乙醇,有水存在时易被 氧化。
氧化。回答下列问题:
(1)实验室需
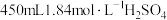 溶液,配制时需量取
溶液,配制时需量取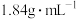 )。
)。(2)“浸取”时,
 的实际用量远远超过理论用量,可能原因是
的实际用量远远超过理论用量,可能原因是(3)“反应”时,
 与
与 、NaCl在溶液中反应生成CuCl沉淀的离子方程式为
、NaCl在溶液中反应生成CuCl沉淀的离子方程式为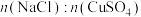 比值逐渐增大时,CuCl产率先增大后减小,原因是
比值逐渐增大时,CuCl产率先增大后减小,原因是(4)为测定某氯化亚铜样品中CuCl的含量,某同学设计如下实验:准确称取氯化亚铜样品mg,将其置于过量的
 溶液中完全溶解,加入适量稀硫酸,用
溶液中完全溶解,加入适量稀硫酸,用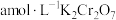 溶液滴定到终点,消耗
溶液滴定到终点,消耗 溶液bmL,
溶液bmL, 被还原为
被还原为 。样品中CuCl的质量分数为
。样品中CuCl的质量分数为 ,不考虑
,不考虑 氧化
氧化 )。
)。(5)①已知:CuCl的熔点为326℃,能升华,熔化呈液态时不导电。则CuCl晶体属于
②若晶胞中a、c原子的分数坐标分别为(0,0,,0)、(
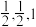 ),则b原子的分数坐标为
),则b原子的分数坐标为
您最近一年使用:0次
解题方法
4 . 氧钒碱式碳酸铵晶体 [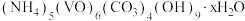 ]是制备多种光、电、磁材料的中间体,难溶于水,昜被氧化、可用
]是制备多种光、电、磁材料的中间体,难溶于水,昜被氧化、可用 与
与 反应制备。科研小组在实验室中对氧钒碱式碳酸铵晶体的制备和组成进行探究。回答下列问题:
反应制备。科研小组在实验室中对氧钒碱式碳酸铵晶体的制备和组成进行探究。回答下列问题:
Ⅰ.制备氧钒碱式碳酸铵晶体的装置和步骤如下。
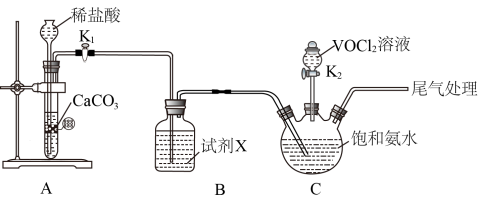
步骤一:按图安装好仪器,添加药品;
步骤二:打开 ,通入足量
,通入足量 ,充分反应后,关闭
,充分反应后,关闭 、打开
、打开 ,向三颈烧瓶中滴加适量
,向三颈烧瓶中滴加适量 溶液;
溶液;
步骤三:C中反应充分进行后,经一系列操作得到产品。
(1)图中盛放 溶液的仪器名称为
溶液的仪器名称为___________ ;试剂X的作用为___________ ; 中V元素的化合价为
中V元素的化合价为___________ 。
(2)步骤二中,通入足量 的作用为
的作用为___________ ;滴加 溶液时,参与反应的
溶液时,参与反应的 与
与 的物质的量之比为
的物质的量之比为___________ 。
Ⅱ.组成测定
(3)测定含钒量(杂质不参加反应):准确称量mg产品,用适量稀硫酸溶解后,依次加入稍过量的酸性 溶液、
溶液、 溶液、尿素,充分反应后,用
溶液、尿素,充分反应后,用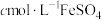 标准溶液滴定(
标准溶液滴定( ),达到滴定终点时消耗标准液的体积为VmL。则加入
),达到滴定终点时消耗标准液的体积为VmL。则加入 溶液的作用为
溶液的作用为___________ ;产品中钒元素的质量分数为___________ (用代数式表示)。
(4)测定结晶水含量:称取纯化后的产品4.26g,充分煅烧后,称得生成 的质量为2.184g,则x=
的质量为2.184g,则x=___________ 。
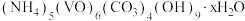 ]是制备多种光、电、磁材料的中间体,难溶于水,昜被氧化、可用
]是制备多种光、电、磁材料的中间体,难溶于水,昜被氧化、可用 与
与 反应制备。科研小组在实验室中对氧钒碱式碳酸铵晶体的制备和组成进行探究。回答下列问题:
反应制备。科研小组在实验室中对氧钒碱式碳酸铵晶体的制备和组成进行探究。回答下列问题:Ⅰ.制备氧钒碱式碳酸铵晶体的装置和步骤如下。

步骤一:按图安装好仪器,添加药品;
步骤二:打开
 ,通入足量
,通入足量 ,充分反应后,关闭
,充分反应后,关闭 、打开
、打开 ,向三颈烧瓶中滴加适量
,向三颈烧瓶中滴加适量 溶液;
溶液;步骤三:C中反应充分进行后,经一系列操作得到产品。
(1)图中盛放
 溶液的仪器名称为
溶液的仪器名称为 中V元素的化合价为
中V元素的化合价为(2)步骤二中,通入足量
 的作用为
的作用为 溶液时,参与反应的
溶液时,参与反应的 与
与 的物质的量之比为
的物质的量之比为Ⅱ.组成测定
(3)测定含钒量(杂质不参加反应):准确称量mg产品,用适量稀硫酸溶解后,依次加入稍过量的酸性
 溶液、
溶液、 溶液、尿素,充分反应后,用
溶液、尿素,充分反应后,用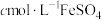 标准溶液滴定(
标准溶液滴定( ),达到滴定终点时消耗标准液的体积为VmL。则加入
),达到滴定终点时消耗标准液的体积为VmL。则加入 溶液的作用为
溶液的作用为(4)测定结晶水含量:称取纯化后的产品4.26g,充分煅烧后,称得生成
 的质量为2.184g,则x=
的质量为2.184g,则x=
您最近一年使用:0次
2023-05-20更新
|
249次组卷
|
3卷引用:山西省吕梁市2023届高三下学期三模理科综合化学试题
5 . 水合草酸铝酸钾晶体是一种化工原料,其晶体组成可表示为 (相对分子质量为462)。某化学兴趣小组设计实验制备水合草酸铝酸钾晶体并探究其性质。
(相对分子质量为462)。某化学兴趣小组设计实验制备水合草酸铝酸钾晶体并探究其性质。
I.制备水合草酸铝酸钾晶体:
步骤1:将 溶液和
溶液和 溶液混合,完全反应后过滤,分离出生成的
溶液混合,完全反应后过滤,分离出生成的 沉淀,并用水洗涤2~3次。
沉淀,并用水洗涤2~3次。
步骤2:称取 和
和 ,并用100mL水溶解得到溶液,再向所得溶液中加入步骤1得到的
,并用100mL水溶解得到溶液,再向所得溶液中加入步骤1得到的 沉淀,煮沸、浓缩,趁热过滤得到固体,将固体加入乙醇和水的体积比为1∶1的混合溶液中,过滤,用无水乙醇洗涤2~3次,得水合草酸铝酸钾晶体。
沉淀,煮沸、浓缩,趁热过滤得到固体,将固体加入乙醇和水的体积比为1∶1的混合溶液中,过滤,用无水乙醇洗涤2~3次,得水合草酸铝酸钾晶体。
(1)若步骤1中的NaOH溶液用氨水代替,则发生反应的离子方程式为_______ 。
(2)水合草酸铝酸钾在水中的溶解度_______ (填“大于”或“小于”)其在乙醇中的溶解度。
II.确定水合草酸铝酸钾晶体的组成:称取2.31g水合草酸铝酸钾晶体,进行热重分析,测得的固体失重率如表1所示。
表1
已知:固体失重率 %,其中
%,其中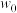 为原始固体的质量,
为原始固体的质量, 为某温度下剩余固体的质量。
为某温度下剩余固体的质量。
(3)c=_______ ;水合草酸铝酸钾晶体的化学式为_______ 。
(4)阶段2发生反应的化学方程式为_______ 。
III..测定某混合物中 的百分含量(设混合物中其他组分均不与酸性
的百分含量(设混合物中其他组分均不与酸性 溶液反应)。
溶液反应)。
已知:酸性 溶液可将
溶液可将 氧化并放出
氧化并放出 ,测定上述混合物中
,测定上述混合物中 的百分含量时,可用酸性
的百分含量时,可用酸性 标准溶液进行滴定。
标准溶液进行滴定。
(5)滴定时,酸性 溶液不能用碱式滴定管盛装的原因是
溶液不能用碱式滴定管盛装的原因是_______ ;滴定过程中发生反应的离子方程式为_______ 。
(6)取10.0g产物配成100mL溶液,从中取出20mL于锥形瓶中,用 的酸性
的酸性 溶液滴定至终点,重复滴定4次,消耗酸性
溶液滴定至终点,重复滴定4次,消耗酸性 溶液的体积如表2所示。
溶液的体积如表2所示。
表2
则该混合物中 的质量分数为
的质量分数为_______ 。
 (相对分子质量为462)。某化学兴趣小组设计实验制备水合草酸铝酸钾晶体并探究其性质。
(相对分子质量为462)。某化学兴趣小组设计实验制备水合草酸铝酸钾晶体并探究其性质。I.制备水合草酸铝酸钾晶体:
步骤1:将
 溶液和
溶液和 溶液混合,完全反应后过滤,分离出生成的
溶液混合,完全反应后过滤,分离出生成的 沉淀,并用水洗涤2~3次。
沉淀,并用水洗涤2~3次。步骤2:称取
 和
和 ,并用100mL水溶解得到溶液,再向所得溶液中加入步骤1得到的
,并用100mL水溶解得到溶液,再向所得溶液中加入步骤1得到的 沉淀,煮沸、浓缩,趁热过滤得到固体,将固体加入乙醇和水的体积比为1∶1的混合溶液中,过滤,用无水乙醇洗涤2~3次,得水合草酸铝酸钾晶体。
沉淀,煮沸、浓缩,趁热过滤得到固体,将固体加入乙醇和水的体积比为1∶1的混合溶液中,过滤,用无水乙醇洗涤2~3次,得水合草酸铝酸钾晶体。(1)若步骤1中的NaOH溶液用氨水代替,则发生反应的离子方程式为
(2)水合草酸铝酸钾在水中的溶解度
II.确定水合草酸铝酸钾晶体的组成:称取2.31g水合草酸铝酸钾晶体,进行热重分析,测得的固体失重率如表1所示。
表1
| 阶段 | 温度变化范围/℃ | 残留固体组成 | 固体失重率 |
| 1 | 47~340 |  | 11.69% |
| 2 | 340~533 |  | 32.47% |
 %,其中
%,其中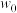 为原始固体的质量,
为原始固体的质量, 为某温度下剩余固体的质量。
为某温度下剩余固体的质量。(3)c=
(4)阶段2发生反应的化学方程式为
III..测定某混合物中
 的百分含量(设混合物中其他组分均不与酸性
的百分含量(设混合物中其他组分均不与酸性 溶液反应)。
溶液反应)。已知:酸性
 溶液可将
溶液可将 氧化并放出
氧化并放出 ,测定上述混合物中
,测定上述混合物中 的百分含量时,可用酸性
的百分含量时,可用酸性 标准溶液进行滴定。
标准溶液进行滴定。(5)滴定时,酸性
 溶液不能用碱式滴定管盛装的原因是
溶液不能用碱式滴定管盛装的原因是(6)取10.0g产物配成100mL溶液,从中取出20mL于锥形瓶中,用
 的酸性
的酸性 溶液滴定至终点,重复滴定4次,消耗酸性
溶液滴定至终点,重复滴定4次,消耗酸性 溶液的体积如表2所示。
溶液的体积如表2所示。表2
| 滴定次数 | 第一次 | 第二次 | 第三次 | 第四次 |
消耗酸性 溶液的体积/mL 溶液的体积/mL | 24.02 | 23.98 | 24.00 | 22.08 |
 的质量分数为
的质量分数为
您最近一年使用:0次
名校
6 . 某小组在实验室用NaClO溶液和NH3反应制备N2H4,并进行相关的性质探究实验。
Ⅰ.制备N2H4
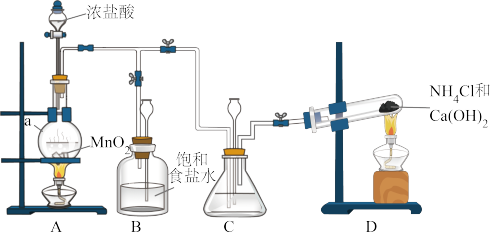
(1)仪器a的名称是___________ 。
(2)装置C中盛放的试剂是___________ 。装置B的作用是___________ 。
(3)制备N2H4的离子方程式为___________ 。
Ⅱ.测定产品中水合肼(N2H4 · H2O)的含量
(4)称取产品6.0 g,加入适量NaHCO3固体(滴定过程中,调节溶液的pH保持在6.5左右), 加水配成250 mL溶液,移取25.00 mL置于锥形瓶中,并滴加2 ~ 3滴淀粉溶液,用 0.3000 mol • L-1的碘标准溶液滴定(已知:N2H4·H2O+2I2 =N2↑ +4HI+H2O)。
①滴定到达终点的现象是___________ 。
②实验测得消耗碘标准溶液的平均值为20.00 mL,产品中水合腓的质量分数为___________ 。
Ⅲ.探究的还原性与碱性。将制得的耕分离提纯后,进行如图实验。

【查阅资料]AgOH在溶液中不稳定,易分解生成黑色的Ag2O,Ag2O可溶于氨水。
【提出假设】黑色固体可能是Ag、Ag2O中的一种或两种。
【实验验证】设计如下方案,进行实验。
(5)请完成表中的空白部分:①___________ ;②___________ 。
(6)实验表明,黑色固体主要成分是Ag,还有少量氧化银,请解释原因:___________ 。
Ⅰ.制备N2H4

(1)仪器a的名称是
(2)装置C中盛放的试剂是
(3)制备N2H4的离子方程式为
Ⅱ.测定产品中水合肼(N2H4 · H2O)的含量
(4)称取产品6.0 g,加入适量NaHCO3固体(滴定过程中,调节溶液的pH保持在6.5左右), 加水配成250 mL溶液,移取25.00 mL置于锥形瓶中,并滴加2 ~ 3滴淀粉溶液,用 0.3000 mol • L-1的碘标准溶液滴定(已知:N2H4·H2O+2I2 =N2↑ +4HI+H2O)。
①滴定到达终点的现象是
②实验测得消耗碘标准溶液的平均值为20.00 mL,产品中水合腓的质量分数为
Ⅲ.探究的还原性与碱性。将制得的耕分离提纯后,进行如图实验。

【查阅资料]AgOH在溶液中不稳定,易分解生成黑色的Ag2O,Ag2O可溶于氨水。
【提出假设】黑色固体可能是Ag、Ag2O中的一种或两种。
【实验验证】设计如下方案,进行实验。
| 操作 | 现象 | 实验结论 |
| i.取少量黑色固体于试管中,加入适量①_________ | 黑色固体部分溶解 | 黑色固体有Ag2O |
| ii.取少量黑色固体于试管中加入足量稀硝酸,振荡 | ②_________ | 黑色固体是Ag和Ag2O |
(6)实验表明,黑色固体主要成分是Ag,还有少量氧化银,请解释原因:
您最近一年使用:0次
2022-03-29更新
|
827次组卷
|
6卷引用:山西省太原市2022届高三下学期模拟考试(一模)理科综合化学试题
山西省太原市2022届高三下学期模拟考试(一模)理科综合化学试题(已下线)专题17化学实验综合题-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题16化学实验综合题-2022年高考真题+模拟题汇编(全国卷)(已下线)专题17化学实验综合题-五年(2018~2022)高考真题汇编(全国卷)四川省绵阳南山中学2022-2023学年高三上学期入学考试理综化学试题四川省绵阳市高中2022-2023学年高二下学期理科突击班6月月考化学试题
7 . 草酸(H2C2O4)及其化合物在医药、印染、塑料等方面扮演着重要角色,同时广泛应用于化学实验中。
(1)氧化还原滴定法是以溶液中氧化剂和还原剂之间的电子转移为基础的一种滴定分析方法,应用非常广泛。某草酸亚铁( )样品中含有草酸,某化学兴趣小组想用氧化还原滴定法测定该样品中
)样品中含有草酸,某化学兴趣小组想用氧化还原滴定法测定该样品中 的含量。实验方案如下:
的含量。实验方案如下:
Ⅰ.称量0.50g样品于锥形瓶中,加入适量稀硫酸溶解,水浴加热至70℃,加入足量 溶液,使其充分反应。
溶液,使其充分反应。
Ⅱ.向反应后的溶液中加入过量锌粉与稀硫酸,煮沸且完全反应后,用KSCN在点滴板上检验至溶液不变红,过滤至另一洁净的锥形瓶中,用0.0200mol/L的酸性高锰酸钾标准液滴定该溶液至终点,消耗高锰酸钾标准液16.00mL。
请回答下列问题:
①高锰酸钾标准液用___________ (填“酸式”或“碱式”)滴定管盛装,达到滴定终点的现象是___________ 。
②下列关于实验误差的说法正确的是___________ (填标号)。
A.步骤Ⅰ中,若加入的 溶液的量不足,则测得的
溶液的量不足,则测得的 含量偏高
含量偏高
B.步骤Ⅱ中,滴定前读数正确,滴定终点时仰视读数,测得的 含量偏低
含量偏低
C.步骤Ⅱ中,锥形瓶中有少量水未干燥,测得的 含量偏低
含量偏低
D.步骤Ⅱ中,过滤时间过长,可能导致测得的 含量偏低
含量偏低
③0.50g该样品中 的质量分数为
的质量分数为___________ (不考虑损耗)。
(2)常温下,改变0.1mol/L的 溶液的pH,溶液中
溶液的pH,溶液中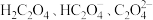 的物质的量分数(
的物质的量分数( )溶液pH的关系如图所示。回答下列问题:
)溶液pH的关系如图所示。回答下列问题:
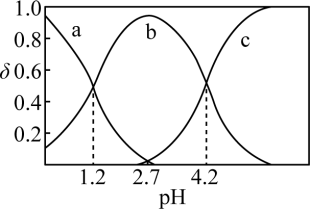
①曲线___________ (填“a”、“b”或“c”)代表 ,
, 时,溶液中
时,溶液中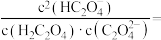
___________ 。
②pH从1.2增大至4.2的过程中,水的电离程度___________ (填“增大”、“减小”或“不变”)。
③ 溶液中存在的离子浓度大小关系为
溶液中存在的离子浓度大小关系为___________ 。
(1)氧化还原滴定法是以溶液中氧化剂和还原剂之间的电子转移为基础的一种滴定分析方法,应用非常广泛。某草酸亚铁(
 )样品中含有草酸,某化学兴趣小组想用氧化还原滴定法测定该样品中
)样品中含有草酸,某化学兴趣小组想用氧化还原滴定法测定该样品中 的含量。实验方案如下:
的含量。实验方案如下:Ⅰ.称量0.50g样品于锥形瓶中,加入适量稀硫酸溶解,水浴加热至70℃,加入足量
 溶液,使其充分反应。
溶液,使其充分反应。Ⅱ.向反应后的溶液中加入过量锌粉与稀硫酸,煮沸且完全反应后,用KSCN在点滴板上检验至溶液不变红,过滤至另一洁净的锥形瓶中,用0.0200mol/L的酸性高锰酸钾标准液滴定该溶液至终点,消耗高锰酸钾标准液16.00mL。
请回答下列问题:
①高锰酸钾标准液用
②下列关于实验误差的说法正确的是
A.步骤Ⅰ中,若加入的
 溶液的量不足,则测得的
溶液的量不足,则测得的 含量偏高
含量偏高B.步骤Ⅱ中,滴定前读数正确,滴定终点时仰视读数,测得的
 含量偏低
含量偏低C.步骤Ⅱ中,锥形瓶中有少量水未干燥,测得的
 含量偏低
含量偏低D.步骤Ⅱ中,过滤时间过长,可能导致测得的
 含量偏低
含量偏低③0.50g该样品中
 的质量分数为
的质量分数为(2)常温下,改变0.1mol/L的
 溶液的pH,溶液中
溶液的pH,溶液中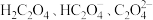 的物质的量分数(
的物质的量分数( )溶液pH的关系如图所示。回答下列问题:
)溶液pH的关系如图所示。回答下列问题:
①曲线
 ,
, 时,溶液中
时,溶液中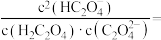
②pH从1.2增大至4.2的过程中,水的电离程度
③
 溶液中存在的离子浓度大小关系为
溶液中存在的离子浓度大小关系为
您最近一年使用:0次
2022-01-21更新
|
129次组卷
|
3卷引用:山西省吕梁市2021-2022学年高二上学期期末考试化学试题
名校
解题方法
8 . 钼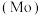 及其化合物广泛应用于医疗卫生、国防等领域。某镍钼矿中的镍和钼以NiS和
及其化合物广泛应用于医疗卫生、国防等领域。某镍钼矿中的镍和钼以NiS和 的形式存在,从镍钼矿中分离钼的一种工艺流程如图。
的形式存在,从镍钼矿中分离钼的一种工艺流程如图。 在“焙烧”过程中转化为
在“焙烧”过程中转化为 ;
;
②钼酸铵 为白色晶体,具有很高的水溶性,不溶于乙醇。
为白色晶体,具有很高的水溶性,不溶于乙醇。
(1)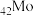 与
与 同族,基态
同族,基态 原子的价层电子排布式为
原子的价层电子排布式为__________ 。
(2)“焙烧”中 元素转化为
元素转化为 ,同时有
,同时有 生成,写出
生成,写出 在“焙烧”时发生反应的化学方程式:
在“焙烧”时发生反应的化学方程式:________________ 。
(3)下列说法正确的是__________(填标号)。
(4) 中存在的相互作用有__________(填标号)。
中存在的相互作用有__________(填标号)。
(5)经过结晶、过滤、洗涤、干燥等操作得到 ,洗涤时所选用的最佳试剂为
,洗涤时所选用的最佳试剂为__________ 。
(6)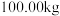 该镍钼矿(
该镍钼矿( 元素的质量分数为
元素的质量分数为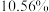 )通过该工艺最终得到
)通过该工艺最终得到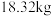 钼酸铵产品,则该工艺中钼酸铵的产率为
钼酸铵产品,则该工艺中钼酸铵的产率为__________  。(保留一位小数,产率=
。(保留一位小数,产率=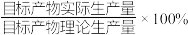 )
)
(7)氮化钼作为锂离子电池负极材料具有很好的发展前景。它属于填隙式氮化物,N原子部分填充在 原子立方晶格的八面体空隙中,晶胞结构如图所示。氮化钼的化学式为
原子立方晶格的八面体空隙中,晶胞结构如图所示。氮化钼的化学式为__________ , 原子周围与之等距离的
原子周围与之等距离的 原子个数为
原子个数为__________
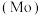 及其化合物广泛应用于医疗卫生、国防等领域。某镍钼矿中的镍和钼以NiS和
及其化合物广泛应用于医疗卫生、国防等领域。某镍钼矿中的镍和钼以NiS和 的形式存在,从镍钼矿中分离钼的一种工艺流程如图。
的形式存在,从镍钼矿中分离钼的一种工艺流程如图。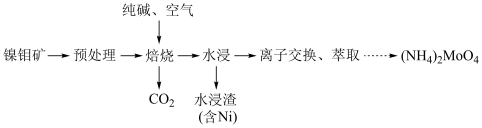
 在“焙烧”过程中转化为
在“焙烧”过程中转化为 ;
;②钼酸铵
 为白色晶体,具有很高的水溶性,不溶于乙醇。
为白色晶体,具有很高的水溶性,不溶于乙醇。(1)
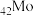 与
与 同族,基态
同族,基态 原子的价层电子排布式为
原子的价层电子排布式为(2)“焙烧”中
 元素转化为
元素转化为 ,同时有
,同时有 生成,写出
生成,写出 在“焙烧”时发生反应的化学方程式:
在“焙烧”时发生反应的化学方程式:(3)下列说法正确的是__________(填标号)。
A.电负性: |
B.离子半径: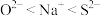 |
C.第一电离能: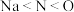 |
D.基态 中成对电子数与未成对电子数之比为 中成对电子数与未成对电子数之比为 |
(4)
 中存在的相互作用有__________(填标号)。
中存在的相互作用有__________(填标号)。| A.分子间作用力 | B.金属键 |
| C.共价键 | D.离子键 |
(5)经过结晶、过滤、洗涤、干燥等操作得到
 ,洗涤时所选用的最佳试剂为
,洗涤时所选用的最佳试剂为(6)
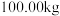 该镍钼矿(
该镍钼矿( 元素的质量分数为
元素的质量分数为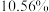 )通过该工艺最终得到
)通过该工艺最终得到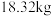 钼酸铵产品,则该工艺中钼酸铵的产率为
钼酸铵产品,则该工艺中钼酸铵的产率为 。(保留一位小数,产率=
。(保留一位小数,产率=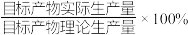 )
)(7)氮化钼作为锂离子电池负极材料具有很好的发展前景。它属于填隙式氮化物,N原子部分填充在
 原子立方晶格的八面体空隙中,晶胞结构如图所示。氮化钼的化学式为
原子立方晶格的八面体空隙中,晶胞结构如图所示。氮化钼的化学式为 原子周围与之等距离的
原子周围与之等距离的 原子个数为
原子个数为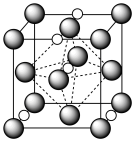
您最近一年使用:0次
2024-05-30更新
|
173次组卷
|
3卷引用:2024届山西省晋城市高三下学期第三次模拟考试理科综合试题-高中化学
名校
9 . 立方晶系Sb2O3对光稳定,是制备聚对苯二甲酸乙二醇酯的优良催化剂。制备的实验步骤如下:
①按下图装置安装仪器(加热仪器略),添加试剂,通入NH3,得到固液混合物。
②向容器a中加入一定量的蒸馏水,搅拌一段时间,过滤、洗涤、110℃烘干。
①SbCl3易水解成SbOCl,SbOCl难溶于乙醇、能溶于乙二醇,SbOCl也可水解为Sb2O3,但如果反应只发生在表面,则得不到单一晶型。
②无水乙醇和乙二醇都可能含少量水。
回答下列问题:
(1)步骤①生成Sb2(OCH2CH2O)3,写出化学方程式___________ 。
(2)仪器a的名称为___________ ,装置B的作用为___________ 。
(3)洗涤时Sb2O3晶体洗净的判断标准是___________ 。
(4)烘干时,晶体装在___________ (填仪器名称)。
(5)如果将乙二醇改为乙醇用上述同样方法制备,往往得到Sb2O3混晶,解释原因___________ 。
(6)用___________ 法可以测定Sb2O3是混晶还是单晶。
(7)取mg产品于锥形瓶中,用盐酸等试剂预处理后,用amol·L-1碘标准液滴定。接近终点时加入2滴淀粉溶液,继续滴定至终点,消耗碘标准液VmL。反应原理为 。
。
①滴定终点现象是___________ 。
②产品中Sb元素的质量分数是___________ 。
①按下图装置安装仪器(加热仪器略),添加试剂,通入NH3,得到固液混合物。
②向容器a中加入一定量的蒸馏水,搅拌一段时间,过滤、洗涤、110℃烘干。

①SbCl3易水解成SbOCl,SbOCl难溶于乙醇、能溶于乙二醇,SbOCl也可水解为Sb2O3,但如果反应只发生在表面,则得不到单一晶型。
②无水乙醇和乙二醇都可能含少量水。
回答下列问题:
(1)步骤①生成Sb2(OCH2CH2O)3,写出化学方程式
(2)仪器a的名称为
(3)洗涤时Sb2O3晶体洗净的判断标准是
(4)烘干时,晶体装在
(5)如果将乙二醇改为乙醇用上述同样方法制备,往往得到Sb2O3混晶,解释原因
(6)用
(7)取mg产品于锥形瓶中,用盐酸等试剂预处理后,用amol·L-1碘标准液滴定。接近终点时加入2滴淀粉溶液,继续滴定至终点,消耗碘标准液VmL。反应原理为
 。
。①滴定终点现象是
②产品中Sb元素的质量分数是
您最近一年使用:0次
2024-05-01更新
|
262次组卷
|
3卷引用:山西省平遥中学2023-2024学年高三二模考试化学试题
名校
解题方法
10 . 连二亚硫酸钠( )俗称保险粉,广泛用于纺织、医药、选矿、造纸工业。某实验小组拟用甲酸钠、烧碱、二氧化硫制备连二亚硫酸钠并测定其纯度。
)俗称保险粉,广泛用于纺织、医药、选矿、造纸工业。某实验小组拟用甲酸钠、烧碱、二氧化硫制备连二亚硫酸钠并测定其纯度。
查阅资料:连二亚硫酸钠是一种白色粉末,易溶于水,难溶于乙醇;加热到80℃以上分解并出二氧化硫气体;在空气中能被氧化,是一种强还原剂。
Ⅰ. 的制备
的制备 时选用上图所示装置中的
时选用上图所示装置中的________ (填标号)。选用以下试剂中的________ (填标号)。
A.铜粉 B. 固体 C.98%浓硫酸 D.70%浓硫酸 E.10%稀硫酸
固体 C.98%浓硫酸 D.70%浓硫酸 E.10%稀硫酸
Ⅱ. 的制备
的制备
制用如图所示实验装置(加热、搅拌及夹持装置省略)制备 ,实验步骤如下:
,实验步骤如下: 一段时间;
一段时间;
ii.然后持续通入 ,保持水浴温度75℃左右,反应20min;
,保持水浴温度75℃左右,反应20min;
iii.停止加热,冷却至50℃;
iv.拆卸装置,将d中的混合物进行过滤、洗涤,得到粗产品。
(2)步骤Ⅰ中先通入 的目的是
的目的是________ (答出两点)。
(3)装置d中发生的主要反应的化学方程式为________ 。
(4)步骤iv中“洗涤”时,洗涤剂为________ (填“水”或“乙醇”),进一步提纯 的方法为
的方法为________ 。
Ⅲ.产品纯度的测定
称取纯化后的产品mg溶于水,加入足量 溶液后配成250mL待测液,量取25.00mL待测液于锥形瓶中,滴入2~3滴指示剂亚甲基蓝溶液,用
溶液后配成250mL待测液,量取25.00mL待测液于锥形瓶中,滴入2~3滴指示剂亚甲基蓝溶液,用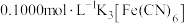 标准溶液进行滴定{已知滴定过程中
标准溶液进行滴定{已知滴定过程中 转化为
转化为 ,
, 转化为
转化为 ,杂质不参与反应},达到滴定终点时消耗标准溶液VmL。
,杂质不参与反应},达到滴定终点时消耗标准溶液VmL。
(5)滴定过程中发生反应的离子方程式为________ 。
(6)产品中 的质量分数为
的质量分数为________ 。
(7)下列情况会造成测定结果偏小的是________ (填标号)。
A.盛放待测液的锥形瓶内残留少量蒸馏水
B.未用 标准液润洗酸式滴定管
标准液润洗酸式滴定管
C.滴定终点时俯视读数
 )俗称保险粉,广泛用于纺织、医药、选矿、造纸工业。某实验小组拟用甲酸钠、烧碱、二氧化硫制备连二亚硫酸钠并测定其纯度。
)俗称保险粉,广泛用于纺织、医药、选矿、造纸工业。某实验小组拟用甲酸钠、烧碱、二氧化硫制备连二亚硫酸钠并测定其纯度。查阅资料:连二亚硫酸钠是一种白色粉末,易溶于水,难溶于乙醇;加热到80℃以上分解并出二氧化硫气体;在空气中能被氧化,是一种强还原剂。
Ⅰ.
 的制备
的制备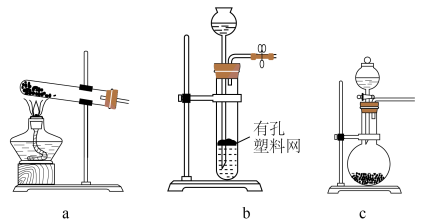
 时选用上图所示装置中的
时选用上图所示装置中的A.铜粉 B.
 固体 C.98%浓硫酸 D.70%浓硫酸 E.10%稀硫酸
固体 C.98%浓硫酸 D.70%浓硫酸 E.10%稀硫酸Ⅱ.
 的制备
的制备制用如图所示实验装置(加热、搅拌及夹持装置省略)制备
 ,实验步骤如下:
,实验步骤如下: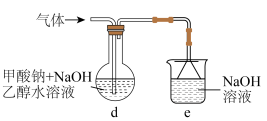
 一段时间;
一段时间;ii.然后持续通入
 ,保持水浴温度75℃左右,反应20min;
,保持水浴温度75℃左右,反应20min;iii.停止加热,冷却至50℃;
iv.拆卸装置,将d中的混合物进行过滤、洗涤,得到粗产品。
(2)步骤Ⅰ中先通入
 的目的是
的目的是(3)装置d中发生的主要反应的化学方程式为
(4)步骤iv中“洗涤”时,洗涤剂为
 的方法为
的方法为Ⅲ.产品纯度的测定
称取纯化后的产品mg溶于水,加入足量
 溶液后配成250mL待测液,量取25.00mL待测液于锥形瓶中,滴入2~3滴指示剂亚甲基蓝溶液,用
溶液后配成250mL待测液,量取25.00mL待测液于锥形瓶中,滴入2~3滴指示剂亚甲基蓝溶液,用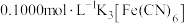 标准溶液进行滴定{已知滴定过程中
标准溶液进行滴定{已知滴定过程中 转化为
转化为 ,
, 转化为
转化为 ,杂质不参与反应},达到滴定终点时消耗标准溶液VmL。
,杂质不参与反应},达到滴定终点时消耗标准溶液VmL。(5)滴定过程中发生反应的离子方程式为
(6)产品中
 的质量分数为
的质量分数为(7)下列情况会造成测定结果偏小的是
A.盛放待测液的锥形瓶内残留少量蒸馏水
B.未用
 标准液润洗酸式滴定管
标准液润洗酸式滴定管C.滴定终点时俯视读数
您最近一年使用:0次
2024-04-16更新
|
333次组卷
|
2卷引用:2024届山西省朔州市怀仁市第一中学校等校高三下学期三模理综试题-高中化学



