名校
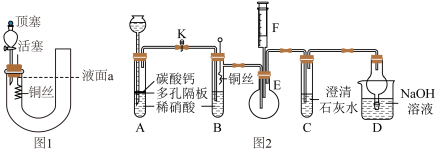
1 . 为了探究铜与稀硝酸反应产生的气体是NO,某课外活动小组设计了如下两套装置进行实验,请回答相关问题。
(1)如何检查该装置的气密性?___________ 。
(2)检验气密性后,重新组装好装置,打开分液漏斗的顶塞和活塞,从长管加入稀硝酸至液面到达a处,关闭活塞,微热短管,可观察到的实验现象为___________ 。
(二)乙同学设计了如图2所示装置(加热装置和固定装置均已略去)。装置气密性已检查,A中大理石,B、C、D中溶液均已装好,铜丝未浸入稀硝酸,止水夹K处于关闭状态,F是一半空的注射器。
(3)设计A装置的目的是___________ 。
(4)为达到上述目的应如何操作?___________ 。
(5)B装置中发生反应的离子方程式为___________ 。
(6)反应进行一段时间后,关闭止水夹K,将铜丝旋出稀硝酸液面。为验证铜和稀硝酸产生的气体是NO,应进行的操作和对应的现象是___________ 。
(1)如何检查该装置的气密性?
(2)检验气密性后,重新组装好装置,打开分液漏斗的顶塞和活塞,从长管加入稀硝酸至液面到达a处,关闭活塞,微热短管,可观察到的实验现象为
(二)乙同学设计了如图2所示装置(加热装置和固定装置均已略去)。装置气密性已检查,A中大理石,B、C、D中溶液均已装好,铜丝未浸入稀硝酸,止水夹K处于关闭状态,F是一半空的注射器。
(3)设计A装置的目的是
(4)为达到上述目的应如何操作?
(5)B装置中发生反应的离子方程式为
(6)反应进行一段时间后,关闭止水夹K,将铜丝旋出稀硝酸液面。为验证铜和稀硝酸产生的气体是NO,应进行的操作和对应的现象是
您最近一年使用:0次
名校
解题方法
2 . 土壤中的硝酸盐会被细菌分解。有一种脱氧硫杆菌能够利用土壤中的硫化物来分解硝酸盐,其主要化学原理为:
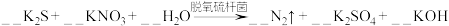 。
。
(1)配平上述反应方程式,并用单线桥标出电子转移的方向和数目___________ 。
(2)被氧化的元素是___________ 。
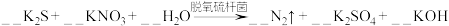 。
。(1)配平上述反应方程式,并用单线桥标出电子转移的方向和数目
(2)被氧化的元素是
您最近一年使用:0次
名校
3 . 元素周期表是指导我们系统学习化学的重要工具,下图是元素周期表的一部分。请回答以下问题:___________ 数相同,卤族元素处于同一纵行,是由于它们的___________ 数相同。
(2)碘元素在元素周期表中的位置是___________ ,它所在的周期共有___________ 种元素。
(3)根据同主族元素原子结构的相似性,可以推测磷元素气态氢化物的电子式为___________ 。
(4)某元素的原子L层电子数比K层电子数多 2个,与该元素同一主族的短周期元素是___________ (填元素符号)。
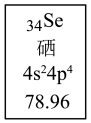
(5)硒元素在元素周期表中的具体信息如图所示,“78.96”的含义是___________ ,硒原子的结构示意图为___________ 。

(2)碘元素在元素周期表中的位置是
(3)根据同主族元素原子结构的相似性,可以推测磷元素气态氢化物的电子式为
(4)某元素的原子L层电子数比K层电子数多 2个,与该元素同一主族的短周期元素是
(5)硒元素在元素周期表中的具体信息如图所示,“78.96”的含义是
您最近一年使用:0次
名校
解题方法
4 . 硫化细菌是好氧菌,而反硫化细菌是厌氧菌,两类细菌参与了土壤中硫循环。___________ 剂(填“氧化”或“还原”)。
(2)“硫化细菌浸矿法”可将矿石中的CuS转化为可溶性铜盐,离子方程式是___________ 。
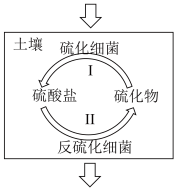
(2)“硫化细菌浸矿法”可将矿石中的CuS转化为可溶性铜盐,离子方程式是
您最近一年使用:0次
解题方法
5 . 下列关于NO、NO2的叙述正确的是
| A.都显红棕色 | B.都难溶于水 |
| C.都可由铜和硝酸反应制得 | D.都参与了自然界的氮循环 |
您最近一年使用:0次
6 . 含硫、氮物质的使用在为人类带来益处的同时,也给人们带来了一些困扰。利用化学原理处理含硫、氮的废气、废液等具有重要意义。二氧化氯(ClO2)可用于烟气中SO2和NO的脱除。研究发现ClO2氧化SO2和NO时涉及以下基元反应。
脱硝:
ⅰ
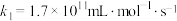
ⅱ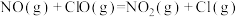
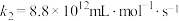
脱硫:
ⅲ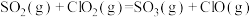

ⅳ
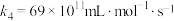
其中k为速率常数。对于基元反应: ,其速率方程表达式为
,其速率方程表达式为
实验测得:ClO2分别单独氧化纯SO2、纯NO以及同时氧化二者混合物的氧化率随时间(t)的变化情况如图所示。_______ 。
2.脱硝反应和脱硫反应哪个活化能更大?说明理由_______ 。
3.请结合ⅰ、ⅲ、ⅳ的速率常数,判断NO的存在是否会影响ClO2氧化SO2的速率并说明理由_______ 。
CO也可以与NO反应生成无污染物: 。
。
已知:
ⅰ 在浓度平衡常数表达式中,用相对分压代替浓度,可得到相对压力平衡常数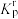 。
。
ⅱ 气体的相对分压等于其分压(单位为kPa)除以 (
(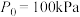 )。
)。
4.在某温度下,原料组成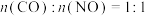 ,初始总压为100 kPa的恒容容器中进行上述反应,达到平衡时CO2的分压为40 kPa,则该反应的相对压力平衡常数
,初始总压为100 kPa的恒容容器中进行上述反应,达到平衡时CO2的分压为40 kPa,则该反应的相对压力平衡常数
_______ 。
5.该反应中,如果在恒压密闭容器中,仍保持原料组成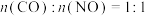 ,以下哪些条件可以判断反应达到平衡_______。
,以下哪些条件可以判断反应达到平衡_______。
脱硝:
ⅰ

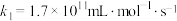
ⅱ
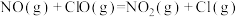
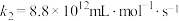
脱硫:
ⅲ
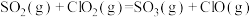

ⅳ

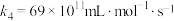
其中k为速率常数。对于基元反应:
 ,其速率方程表达式为
,其速率方程表达式为
实验测得:ClO2分别单独氧化纯SO2、纯NO以及同时氧化二者混合物的氧化率随时间(t)的变化情况如图所示。
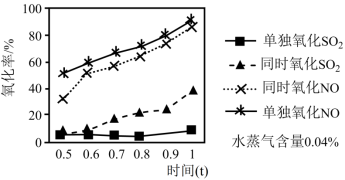
2.脱硝反应和脱硫反应哪个活化能更大?说明理由
3.请结合ⅰ、ⅲ、ⅳ的速率常数,判断NO的存在是否会影响ClO2氧化SO2的速率并说明理由
CO也可以与NO反应生成无污染物:
 。
。已知:
ⅰ 在浓度平衡常数表达式中,用相对分压代替浓度,可得到相对压力平衡常数
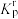 。
。ⅱ 气体的相对分压等于其分压(单位为kPa)除以
 (
(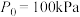 )。
)。4.在某温度下,原料组成
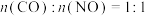 ,初始总压为100 kPa的恒容容器中进行上述反应,达到平衡时CO2的分压为40 kPa,则该反应的相对压力平衡常数
,初始总压为100 kPa的恒容容器中进行上述反应,达到平衡时CO2的分压为40 kPa,则该反应的相对压力平衡常数
5.该反应中,如果在恒压密闭容器中,仍保持原料组成
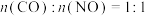 ,以下哪些条件可以判断反应达到平衡_______。
,以下哪些条件可以判断反应达到平衡_______。| A.CO的消耗速率等于NO的消耗速率 | B.容器内气体密度保持不变 |
| C.容器内平均相对分子质量保持不变 | D.CO的转化率保持不变 |
您最近一年使用:0次
解题方法
7 . 一种具有高弹性的自修复聚氨酯材料(TPU)结构如下:_______ 碳氮双键的键能。
A.大于 B.等于 C.小于
2.请写出TPU中元素的第一电离能的大小关系_______ 。

该聚合物由X( )和Y(
)和Y( )聚合而成。
)聚合而成。
A.大于 B.等于 C.小于
2.请写出TPU中元素的第一电离能的大小关系
您最近一年使用:0次
名校
解题方法
8 . 同周期的 A族和
A族和 A族的元素原子序数不可能相差
A族的元素原子序数不可能相差
 A族和
A族和 A族的元素原子序数不可能相差
A族的元素原子序数不可能相差| A.2 | B.12 | C.17 | D.26 |
您最近一年使用:0次
9 . 原子最外层有2个电子的元素不可能位于元素周期表的
A. A族 A族 | B.第15族 | C.副族 | D.0族 |
您最近一年使用:0次
名校
10 . 下列关于硝态氮肥和铵态氮肥的比较错误的是
| A.都易溶于水 | B.受热都容易分解 |
| C.都不能和碱性物质混运共施 | D.土壤胶粒对 的吸附效果更好 的吸附效果更好 |
您最近一年使用:0次



