解题方法
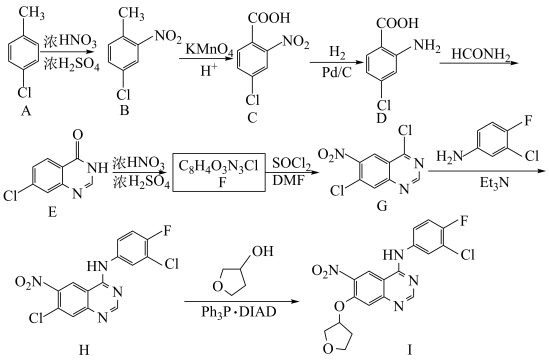
1 . 化合物I是制备抗肿瘤药物阿法替尼的重要中间体,化合物I的一种合成路线如图。
已知:RCH=NH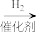 RCH2NH2
RCH2NH2
回答下列问题:
(1)C中含氧官能团的名称是_______ 。
(2)A的化学名称为_______ 。
(3)F的结构简式为_______ ,H→I的反应类型为_______ 。
(4)G→H的化学方程式为_______ 。
(5) 有多种同分异构体,符合下列条件的有
有多种同分异构体,符合下列条件的有_______ 种(不考虑立体异构),其中核磁共振氢谱有3组峰,其峰面积比为6:1:1的结构简式为_______ (写出一种)。
a.能发生银镜反应 b.不含醚键

已知:RCH=NH
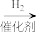 RCH2NH2
RCH2NH2回答下列问题:
(1)C中含氧官能团的名称是
(2)A的化学名称为
(3)F的结构简式为
(4)G→H的化学方程式为
(5)
 有多种同分异构体,符合下列条件的有
有多种同分异构体,符合下列条件的有a.能发生银镜反应 b.不含醚键
您最近一年使用:0次
2 . 研究金属腐蚀和防腐的原理很有现实意义。
(1)如图甲为人教版教材中探究钢铁的吸氧腐蚀的装置。某兴趣小组按该装置实验,导管中液柱上升缓慢,下列措施可以更快更清晰观察到水柱上升现象的有__________(填字母)。
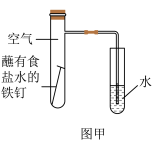
(2)该小组将甲图装置改进成乙图装置并进行实验,导管中红墨水液柱高度随时间的变化逐渐减慢,你认为影响因素为__________ 。

(3)为探究铁钉腐蚀实验a、b两点所发生的反应,进行以下实验,完成表格空白(已知铁氰化钾溶液遇亚铁离子生成蓝色沉淀,常用于亚铁离子的检验):
根据以上实验探究,试判断③______ (填“a”或“b”)为负极,该点腐蚀更严重。
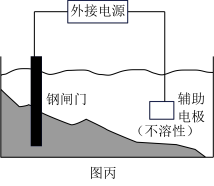
(4)图丙中钢闸门应与外接电源的__________ 相连(填“正极”或“负极”)钢闸门不会被腐蚀,属于__________ 保护法。
(1)如图甲为人教版教材中探究钢铁的吸氧腐蚀的装置。某兴趣小组按该装置实验,导管中液柱上升缓慢,下列措施可以更快更清晰观察到水柱上升现象的有__________(填字母)。

| A.用纯氧气代替试管内空气 | B.用酒精灯加热试管提高温度 |
| C.将铁钉换成铁粉和炭粉混合粉末 | D.换成更细的导管,水中滴加红墨水 |
(2)该小组将甲图装置改进成乙图装置并进行实验,导管中红墨水液柱高度随时间的变化逐渐减慢,你认为影响因素为

(3)为探究铁钉腐蚀实验a、b两点所发生的反应,进行以下实验,完成表格空白(已知铁氰化钾溶液遇亚铁离子生成蓝色沉淀,常用于亚铁离子的检验):
实验操作 | 实验现象 | 实验结论 |
向 溶液中滴加2~3滴酚酞指示剂 溶液中滴加2~3滴酚酞指示剂 | a点附近溶液出现红色 | a点电极反应为① |
然后再滴加2~3滴铁氰化钾溶液 | b点周围出现监色沉淀 | b点电极反应为② |
(4)图丙中钢闸门应与外接电源的

您最近一年使用:0次
3 . Ⅰ.氮的固定是几百年来科学家一直研究的课题。
(1)下表列举了不同温度下大气固氮和工业固氮的部分化学平衡常数K的值。.
①分析数据可知:大气固氮反应属于__________ (填“吸热”或“放热”)反应。
②分析数据可知:人类不适合大规模模拟大气固氮的原因:__________ 。
(2)工业固氮反应中,在其他条件相同时,分别测定 的平衡转化率在不同压强(
的平衡转化率在不同压强( 、
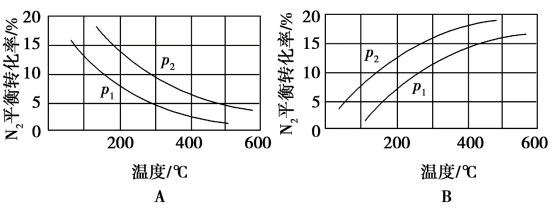
、 )下随温度变化的曲线,下图所示的图示中,正确的是
)下随温度变化的曲线,下图所示的图示中,正确的是______ (填“A”或“B”);比较 、
、 的大小关系:
的大小关系:__________ 。
Ⅱ.目前工业合成氨的原理是 。
。
(3)在一定温度下,将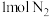 和
和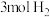 混合置于体积不变的密闭容器中发生反应。
混合置于体积不变的密闭容器中发生反应。
①下列描述能说明反应达到平衡状态的是__________ (填字母)。
A.单位时间内消耗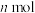 的
的 同时消耗
同时消耗 的
的
B. 、
、 、
、 的浓度相等
的浓度相等
C.混合气体的平均相对分子质量不变
D.混合气体的密度不变
②已知450℃时,某时刻测得 ,
, ,
, ,此时可逆反应
,此时可逆反应__________ 。
A.向正方向进行 B.向逆方向进行 C.处于平衡状态
(1)下表列举了不同温度下大气固氮和工业固氮的部分化学平衡常数K的值。.
| 反应 | 大气固氮 | 工业固氮 | |||
温度/℃ | 27 | 2000 | 25 | 400 | 450 |
平衡常数K |
| 0.1 |
| 0.507 | 0.152 |
②分析数据可知:人类不适合大规模模拟大气固氮的原因:
(2)工业固氮反应中,在其他条件相同时,分别测定
 的平衡转化率在不同压强(
的平衡转化率在不同压强( 、
、 )下随温度变化的曲线,下图所示的图示中,正确的是
)下随温度变化的曲线,下图所示的图示中,正确的是 、
、 的大小关系:
的大小关系:
Ⅱ.目前工业合成氨的原理是
 。
。(3)在一定温度下,将
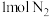 和
和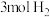 混合置于体积不变的密闭容器中发生反应。
混合置于体积不变的密闭容器中发生反应。①下列描述能说明反应达到平衡状态的是
A.单位时间内消耗
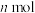 的
的 同时消耗
同时消耗 的
的
B.
 、
、 、
、 的浓度相等
的浓度相等C.混合气体的平均相对分子质量不变
D.混合气体的密度不变
②已知450℃时,某时刻测得
 ,
, ,
, ,此时可逆反应
,此时可逆反应A.向正方向进行 B.向逆方向进行 C.处于平衡状态
您最近一年使用:0次
4 . 回答下列问题。
(1)如图是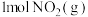 和
和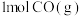 反应生成
反应生成 和
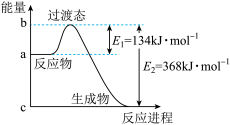
和 过程中的能量变化示意图。请写出
过程中的能量变化示意图。请写出 和
和 反应的热化学方程式
反应的热化学方程式__________ 。
(2)用如图所示装置进行中和热的测定实验。
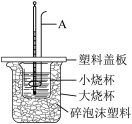
①仪器A的名称是__________ ,碎泡沫塑料的作用是__________ 。
②若实验过程中,未加塑料盖板,则实验测出的
__________ (填“偏大”或“偏小”或“无影响”)。
③理论上强酸强碱的中和热为 ,写出表示稀硫酸和稀
,写出表示稀硫酸和稀 溶液反应的中和热的热化学方程式
溶液反应的中和热的热化学方程式__________ 。
(3)甲醇是人们开发和利用的一种新能源。已知:


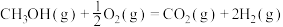
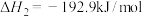
①甲醇蒸气完全燃烧生成二氧化碳气体和液态水的热化学方程式为__________ ;
② 的燃烧热为
的燃烧热为__________ 。
(1)如图是
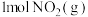 和
和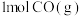 反应生成
反应生成 和
和 过程中的能量变化示意图。请写出
过程中的能量变化示意图。请写出 和
和 反应的热化学方程式
反应的热化学方程式
(2)用如图所示装置进行中和热的测定实验。

①仪器A的名称是
②若实验过程中,未加塑料盖板,则实验测出的

③理论上强酸强碱的中和热为
 ,写出表示稀硫酸和稀
,写出表示稀硫酸和稀 溶液反应的中和热的热化学方程式
溶液反应的中和热的热化学方程式(3)甲醇是人们开发和利用的一种新能源。已知:


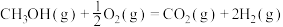
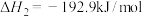
①甲醇蒸气完全燃烧生成二氧化碳气体和液态水的热化学方程式为
②
 的燃烧热为
的燃烧热为
您最近一年使用:0次
5 . 平衡有多种类型,如化学平衡、溶解平衡、电离平衡。下列不存在平衡的是(不考虑水的电离平衡)
| A.稀醋酸溶液中 | B.氯化银悬浊液中 |
| C.氮气与氢气反应的混合物中 | D.稀氯化钠水溶液中 |
您最近一年使用:0次
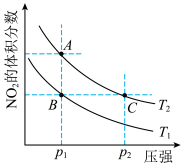
6 . 反应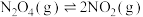
 ,在温度为
,在温度为 、
、 时,平衡体系中
时,平衡体系中 的体积分数随压强的变化曲线如图所示。下列说法正确的是。
的体积分数随压强的变化曲线如图所示。下列说法正确的是。
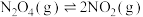
 ,在温度为
,在温度为 、
、 时,平衡体系中
时,平衡体系中 的体积分数随压强的变化曲线如图所示。下列说法正确的是。
的体积分数随压强的变化曲线如图所示。下列说法正确的是。
| A.A、C两点的反应速率:A>C |
| B.A、C两点气体的颜色:A深,C浅 |
| C.A、C两点气体的平均相对分子质量:A>C |
| D.由状态B到状态A,可以用加热的方法 |
您最近一年使用:0次
7 . 下列反应中属于吸热反应的是
| A.甲烷燃烧反应 | B. 与 与 反应 反应 |
| C.Zn与盐酸反应 | D.盐酸和 溶液反应 溶液反应 |
您最近一年使用:0次
8 . 下列能影响水的电离平衡,并使溶液中的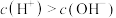 的操作是。
的操作是。
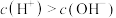 的操作是。
的操作是。| A.将纯水加热至100℃ | B.向水中加氢氧化钡固体 |
| C.向水中投入少量的钠 | D.向水中加入少量 |
您最近一年使用:0次
9 . 目前市场上有一种专门为婴幼儿设计的电解质饮料,适合在婴幼儿感冒、发烧时快速补充体内流失的电解质成分。下列物质可用作该饮料中的电解质的是。
A. | B.葡萄糖 | C.Fe | D. |
您最近一年使用:0次
名校
解题方法
10 . 我国科学家利用锰族催化剂(Mn4CaOx,x代表氧原子数)解密光合作用。锰簇在S3Yz·态的可逆结构异构化如图。
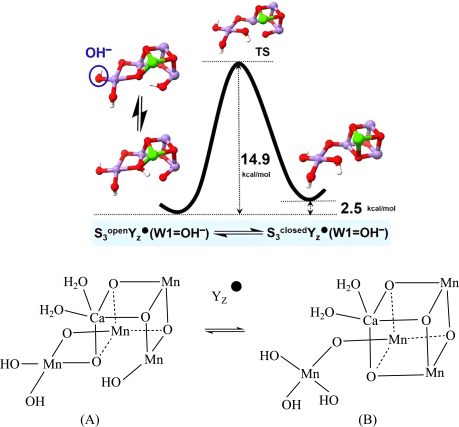
请回答下列问题:
(1)基态锰原子电子排布式为______ 。
(2)锰族催化剂Mn4CaOx中所含元素电负性由大到小的顺序为______ (用元素符号表示),Mn元素位于元素周期表第______ 周期第______ 族。
(3)根据上图可知,稳定性:A______ B(填“>”“<”或“=”)。
(4)1molA含______ molH-Oσ键。
(5)CaO晶胞与NaCl晶胞属于同种类型,如图所示。

①前者的熔点明显高于后者,其主要原因是______ 。
②该晶胞中含有Ca2+的数目为______ ,距离O2-最近的Ca2+的数目有______ 个。
③已知:Ca2+和O2-的核间距为apm,NA为阿伏加德罗常数的值。则CaO晶体密度为______ g/cm3.

请回答下列问题:
(1)基态锰原子电子排布式为
(2)锰族催化剂Mn4CaOx中所含元素电负性由大到小的顺序为
(3)根据上图可知,稳定性:A
(4)1molA含
(5)CaO晶胞与NaCl晶胞属于同种类型,如图所示。

①前者的熔点明显高于后者,其主要原因是
②该晶胞中含有Ca2+的数目为
③已知:Ca2+和O2-的核间距为apm,NA为阿伏加德罗常数的值。则CaO晶体密度为
您最近一年使用:0次
2024-03-29更新
|
256次组卷
|
2卷引用:2024届西藏自治区拉萨市高三上学期第一次模拟考试理综试题