解题方法
1 . 某学习小组探究FeCl3与Na2SO3之间的反应,设计了以下实验。下列说法错误的是
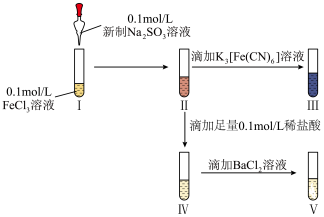
| A.Ⅱ中溶液颜色比Ⅰ中更深,是由于Fe3+水解程度增大 |
| B.Ⅲ中有深蓝色沉淀生成,无法证明FeCl3与Na2SO3发生了氧化还原反应 |
| C.从Ⅱ到Ⅳ滴加的溶液可改为0.05mol/L稀硫酸 |
| D.Ⅴ中有大量白色沉淀生成,证明FeCl3能氧化Na2SO3 |
您最近一年使用:0次
2024-05-07更新
|
166次组卷
|
2卷引用:江西省鹰潭市2024届高三下学期第二次模拟考试化学试卷
2 .  常用作橡胶的硫化剂,能改变生橡胶遇冷变硬的性质。
常用作橡胶的硫化剂,能改变生橡胶遇冷变硬的性质。 各原子最外层均达到8电子稳定结构,极易与水反应生成淡黄色沉淀和能使品红溶液褪色的气体。下列说法不正确的是
各原子最外层均达到8电子稳定结构,极易与水反应生成淡黄色沉淀和能使品红溶液褪色的气体。下列说法不正确的是
 常用作橡胶的硫化剂,能改变生橡胶遇冷变硬的性质。
常用作橡胶的硫化剂,能改变生橡胶遇冷变硬的性质。 各原子最外层均达到8电子稳定结构,极易与水反应生成淡黄色沉淀和能使品红溶液褪色的气体。下列说法不正确的是
各原子最外层均达到8电子稳定结构,极易与水反应生成淡黄色沉淀和能使品红溶液褪色的气体。下列说法不正确的是A. 中硫元素化合价是+1 中硫元素化合价是+1 |
B. 的结构式是 的结构式是 |
C. 与水反应时,氧化产物与还原产物的物质的量之比为 与水反应时,氧化产物与还原产物的物质的量之比为 |
D.向 中滴加 中滴加 溶液,有白色沉淀产生,则证明 溶液,有白色沉淀产生,则证明 中含有 中含有 |
您最近一年使用:0次
2023-07-08更新
|
148次组卷
|
4卷引用:江西省宜春市丰城市第九中学2023-2024学年高三上学期开学考化学试题
3 . 科学证明姜酮可以使人延年益寿,入伏吃姜效果最好,姜酮大量存在于姜皮中,其结构简式如图所示。下列说法错误的是
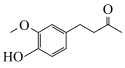
| A.分子中含有3种官能团 | B.能与FeCl3溶液发生显色反应 |
| C.苯环上一溴代物有2种 | D.1mol姜酮最多能与4molH2发生加成反应 |
您最近一年使用:0次
2023-09-24更新
|
61次组卷
|
2卷引用:江西红色十校2024届高三上学期9月联考化学试题
4 . 大气的成分在工业上有重要的应用。
I.
(1)在恒容密闭容器中,发生反应N2(g)+3H2(g)⇌2NH3(g),下列说法可以证明反应已达到平衡状态的是_______ (填序号)。
①单位时间内生成nmolN2的同时生成2nmolNH3
②1个N≡N键断裂的同时,有6个N—H键形成
③1个N≡N键断裂的同时,有3个H—H键形成
④混合气体的密度不再改变的状态
⑤混合气体的压强不再改变的状态
⑥混合气体的平均相对分子质量不再改变的状态
(2)为提高H2的转化率,实际生产中宜采取的措施是_______ (填字母)。
A.及时移出氨 B.适当增大压强 C.循环利用和不断补充氮气 D.减小压强 E.降低温度
II.中国科学家首次实现了以二氧化碳为原料,不依赖植物光合作用,直接人工合成淀粉。已知CO2经催化加氢可以生成多种低碳有机物。
已知:①CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH=-49.5kJ·mol-1
②CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH=+40.9kJ·mol-1
③CO(g)+2H2(g)⇌CH3OH(g) ΔH3
回答下列问题:
(3)反应③的ΔH3为_______ 。
(4)一定温度下,在一体积固定的密闭容器中进行反应①,测得CO2的物质的量浓度随反应时间的变化如图所示:则反应进行的前5分钟内,v(H2)=____ ;10min时,改变的外界条件可能是_____ 。
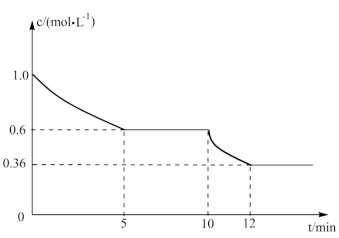
(5)已知一定温度下按照起始比 =2,在一密闭容器中进行反应③,保持总压为4MPa不变,达平衡时CO的平衡转化率为50%,则该条件下用平衡体系中各气体分压表示的平衡常数Kp=
=2,在一密闭容器中进行反应③,保持总压为4MPa不变,达平衡时CO的平衡转化率为50%,则该条件下用平衡体系中各气体分压表示的平衡常数Kp=_______ (各气体分压=平衡体系中各气体的体积分数×总压)。
I.
(1)在恒容密闭容器中,发生反应N2(g)+3H2(g)⇌2NH3(g),下列说法可以证明反应已达到平衡状态的是
①单位时间内生成nmolN2的同时生成2nmolNH3
②1个N≡N键断裂的同时,有6个N—H键形成
③1个N≡N键断裂的同时,有3个H—H键形成
④混合气体的密度不再改变的状态
⑤混合气体的压强不再改变的状态
⑥混合气体的平均相对分子质量不再改变的状态
(2)为提高H2的转化率,实际生产中宜采取的措施是
A.及时移出氨 B.适当增大压强 C.循环利用和不断补充氮气 D.减小压强 E.降低温度
II.中国科学家首次实现了以二氧化碳为原料,不依赖植物光合作用,直接人工合成淀粉。已知CO2经催化加氢可以生成多种低碳有机物。
已知:①CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH=-49.5kJ·mol-1
②CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH=+40.9kJ·mol-1
③CO(g)+2H2(g)⇌CH3OH(g) ΔH3
回答下列问题:
(3)反应③的ΔH3为
(4)一定温度下,在一体积固定的密闭容器中进行反应①,测得CO2的物质的量浓度随反应时间的变化如图所示:则反应进行的前5分钟内,v(H2)=

(5)已知一定温度下按照起始比
 =2,在一密闭容器中进行反应③,保持总压为4MPa不变,达平衡时CO的平衡转化率为50%,则该条件下用平衡体系中各气体分压表示的平衡常数Kp=
=2,在一密闭容器中进行反应③,保持总压为4MPa不变,达平衡时CO的平衡转化率为50%,则该条件下用平衡体系中各气体分压表示的平衡常数Kp=
您最近一年使用:0次
解题方法
5 . 下列关于钠及其化合物的说法中错误的是
| A.碳酸氢钠药片是抗酸药,服用时喝些醋能提高药效 |
B. 与 与 反应放出氧气,可用于制作呼吸面具 反应放出氧气,可用于制作呼吸面具 |
| C.分别将少量钠投入到盛有水和乙醇的烧杯中,可比较水与乙醇中氢的活泼性 |
D.用铂丝蘸取某溶液灼烧,火焰呈黄色,证明其中含有 |
您最近一年使用:0次
名校
解题方法
6 . 25°C时,下列说法不正确的是
| A.等体积Na2CO3和NaHCO3溶液,以甲基橙作指示剂,达滴定终点时,消耗等量的HCl标准液,则NaHCO3浓度更大 |
| B.欲证明HA为弱酸,可将pH=3的HA溶液稀释为原体积的10倍后,测定pH>4 |
C.均为0.10 mol·L-1的Na2CO3、Na2SO3、Na2SO4溶液中阴离子的浓度依次减小〔已知:Ka(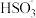 )=6.1×10-8;Ka( )=6.1×10-8;Ka( )=4.7×10-11〕 )=4.7×10-11〕 |
| D.常温下pH=11的纯碱溶液中水电离产生的n(H+)大于该溶液中n(H+) |
您最近一年使用:0次
2021-09-06更新
|
529次组卷
|
4卷引用:江西省南昌市2022届高三摸底考试化学试题
名校
解题方法
7 . 国际奥委会明令禁止运动员在体育竞技中服用兴奋剂.运动员服用兴奋剂,既有失公平,也败坏了体育道德.某种兴奋剂的结构简式如图所示.有关该物质的说法正确的是
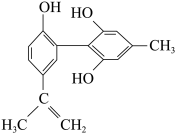

| A.1mol该物质分别与浓溴水和氢气反应时最多消耗Br2和H2的物质的量分别为4mol和7mol |
| B.滴入酸性高锰酸钾溶液,振荡,紫色褪去,能证明其结构中一定存在碳碳双键 |
| C.该有机物可以发生氧化反应,取代反应和消去反应 |
| D.该分子中的所有碳原子不可能共平面 |
您最近一年使用:0次
2021-04-08更新
|
807次组卷
|
6卷引用:江西省吉安市第一中学2022-2023学年高三上学期11月期中考试化学试题
名校
8 . 保险粉Na2S2O4大量用于印染业,并用来漂白纸张、纸浆和陶土等。某化学兴趣小组同学用甲酸法制取保险粉的装置如图所示(加持装置略去)。
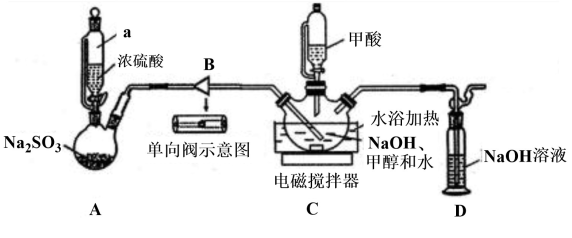
已知:保险粉易溶于水,不溶于甲醇,具有强还原性,在空气中易被氧化:2Na2S2O4+O2+2H2O=NaHSO3或Na2S2O4 +O2+H2O =NaHSO3+NaHSO4。实验时先把甲酸(HCOOH)与溶于甲醇和水混合溶剂的NaOH混合,再通入SO2气体。回答下列问题:
(1)仪器a的名称是______ ;装置B的作用是______ 。
(2)装置C中甲醇不参加反应,甲醇的作用是______ ;生成Na2S2O4的离子方程式为______ 。
(3)下列有关该实验的说法正确的是______ (填序号)。
A.可用硝酸和BaCl2溶液检验制得的Na2S2O4中是否混有NaHSO4
B.实验中甲酸和NaOH最合适的物质的量之比为1:1
C.用N2排尽装置内的空气,有利于提高 的Na2S2O4纯度
D.得到Na2S2O4固体后可用甲醇洗涤
(4)测定产品中Na2S2O4质量分数,其实验步骤如下,准确称取0.5000g产品放入锥形瓶中,加入适量水使其溶解。然后加入足量甲醛,充分反应,再滴加几滴指示剂,用0.2000mol·L-1的标准I2溶液滴定,至终点时,消耗25.00mL标准I2溶液。实验过程中涉及的反应:Na2S2O4+2HCHO+H2O =NaHSO3·HCHO+NaHSO2·HCHO;NaHSO2·HCHO+2I2+2H2O= NaHSO4+HCHO+4HI。该实验加入指示剂是______ ,产品Na2S2O4 (M=174g·mol-1)的质量分数为 ______ % (保留一位小数)。
(5)探究Na2S2O4的性质。隔绝空气加热Na2S2O4固体完全分解是到固体产物Na2SO3,Na2S2O3和SO2,但该兴趣小组没有做到完全隔绝空气,得到的固体产物中还含有Na2SO4。请设计实验证明该分解产物中含有Na2SO4。实验方案是______ 。(可选试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、KMnO4溶液)

已知:保险粉易溶于水,不溶于甲醇,具有强还原性,在空气中易被氧化:2Na2S2O4+O2+2H2O=NaHSO3或Na2S2O4 +O2+H2O =NaHSO3+NaHSO4。实验时先把甲酸(HCOOH)与溶于甲醇和水混合溶剂的NaOH混合,再通入SO2气体。回答下列问题:
(1)仪器a的名称是
(2)装置C中甲醇不参加反应,甲醇的作用是
(3)下列有关该实验的说法正确的是
A.可用硝酸和BaCl2溶液检验制得的Na2S2O4中是否混有NaHSO4
B.实验中甲酸和NaOH最合适的物质的量之比为1:1
C.用N2排尽装置内的空气,有利于提高 的Na2S2O4纯度
D.得到Na2S2O4固体后可用甲醇洗涤
(4)测定产品中Na2S2O4质量分数,其实验步骤如下,准确称取0.5000g产品放入锥形瓶中,加入适量水使其溶解。然后加入足量甲醛,充分反应,再滴加几滴指示剂,用0.2000mol·L-1的标准I2溶液滴定,至终点时,消耗25.00mL标准I2溶液。实验过程中涉及的反应:Na2S2O4+2HCHO+H2O =NaHSO3·HCHO+NaHSO2·HCHO;NaHSO2·HCHO+2I2+2H2O= NaHSO4+HCHO+4HI。该实验加入指示剂是
(5)探究Na2S2O4的性质。隔绝空气加热Na2S2O4固体完全分解是到固体产物Na2SO3,Na2S2O3和SO2,但该兴趣小组没有做到完全隔绝空气,得到的固体产物中还含有Na2SO4。请设计实验证明该分解产物中含有Na2SO4。实验方案是
您最近一年使用:0次
2020-12-21更新
|
1181次组卷
|
6卷引用:江西省南昌市第二中学2021-2022学年高三上学期第一次检测理综化学试题
江西省南昌市第二中学2021-2022学年高三上学期第一次检测理综化学试题四川省成都市第七中学2021届高三一诊模拟考试理综化学试题(已下线)培优01 无机制备类实验 基础训练-2021年高考化学大题培优练(新高考地区专用)(已下线)解密06 金属及其化合物(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密06 金属及其化合物(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练辽宁省沈阳市第一二〇中学2021-2022学年高三上学期第四次质量监测化学试题
名校
解题方法
9 . 辛烯醛是重要化工原料,某小组拟用正丁醛制备辛烯醛并探究其结构。
[制备实验]
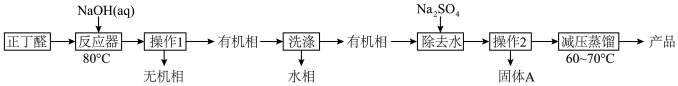
已知:①正丁醛的沸点为75.7℃。辛烯醛沸点为177℃,密度为0.848 g·cm-3,不溶于水。
②CH3CH2CH2CHO
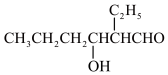

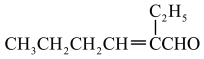
(1)在如图1三颈瓶中加入12.6 mL 2% NaOH溶液,在充分搅拌下,从恒压滴液漏斗慢慢滴入10 mL正丁醛。最适宜的加热方式是___________ ;使用冷凝管的目的是____________ 。
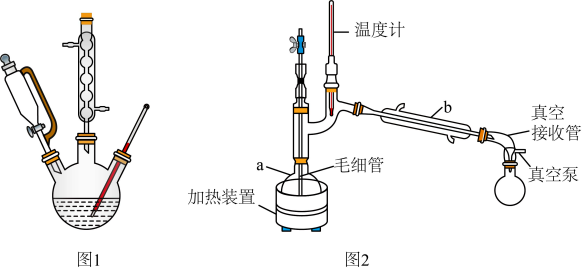
(2)操作1中使用的主要仪器名称是___________ ,有机相从___________ (填“上”或“下”)口取出。
(3)判断有机相已洗涤至中性的操作方法:___________ 。
(4)操作2的名称是_____________ ;固体A的摩尔质量为322 g·mol-1,固体A的化学式为___________ 。
(5)利用图2装置进行“减压蒸馏”。下列有关说法错误的是___________ 。(填选项)
A 温度计示数为177℃,指示馏分温度
B 随着温度计液泡高度的提升,所得液体的沸点升高
C 毛细管的作用和沸石相似,防止液体暴沸
D 实验结束后,应先关闭冷凝水,再关闭真空泵
[性质实验]
资料显示:醛类(RCHO)在常温下能与溴水、酸性高锰酸钾溶液反应;在加热条件下能与银氨溶液、新制氢氧化铜浊液反应。
(6)为了证明辛烯醛含有碳碳双键,设计如下方案,能达到实验目的的是________ 。(填选项)
a 取少量溴水,滴加辛烯醛,振荡,溶液褪色
b 取少量酸性高锰酸钾溶液,滴加辛烯醛,振荡,溶液褪色
c 取少量辛烯醛,加入足量的银氨溶液,水浴加热充分反应后,冷却,在上层清液中先滴加稀盐酸酸化,再滴加溴水,振荡
d 取少量辛烯醛,加入足量的新制Cu(OH)2浊液,加热充分反应后,冷却,在上层清液中先滴加稀盐酸酸化,再滴加溴水,振荡
[制备实验]

已知:①正丁醛的沸点为75.7℃。辛烯醛沸点为177℃,密度为0.848 g·cm-3,不溶于水。
②CH3CH2CH2CHO

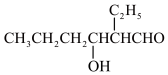

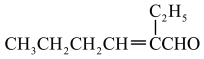
(1)在如图1三颈瓶中加入12.6 mL 2% NaOH溶液,在充分搅拌下,从恒压滴液漏斗慢慢滴入10 mL正丁醛。最适宜的加热方式是

(2)操作1中使用的主要仪器名称是
(3)判断有机相已洗涤至中性的操作方法:
(4)操作2的名称是
(5)利用图2装置进行“减压蒸馏”。下列有关说法错误的是
A 温度计示数为177℃,指示馏分温度
B 随着温度计液泡高度的提升,所得液体的沸点升高
C 毛细管的作用和沸石相似,防止液体暴沸
D 实验结束后,应先关闭冷凝水,再关闭真空泵
[性质实验]
资料显示:醛类(RCHO)在常温下能与溴水、酸性高锰酸钾溶液反应;在加热条件下能与银氨溶液、新制氢氧化铜浊液反应。
(6)为了证明辛烯醛含有碳碳双键,设计如下方案,能达到实验目的的是
a 取少量溴水,滴加辛烯醛,振荡,溶液褪色
b 取少量酸性高锰酸钾溶液,滴加辛烯醛,振荡,溶液褪色
c 取少量辛烯醛,加入足量的银氨溶液,水浴加热充分反应后,冷却,在上层清液中先滴加稀盐酸酸化,再滴加溴水,振荡
d 取少量辛烯醛,加入足量的新制Cu(OH)2浊液,加热充分反应后,冷却,在上层清液中先滴加稀盐酸酸化,再滴加溴水,振荡
您最近一年使用:0次
2020-07-09更新
|
398次组卷
|
3卷引用:江西省2020届高三下学期调研考试(三) 化学
名校
10 . 钟南山院士指出,实验证明中药连花清瘟胶囊对治疗新冠肺炎有明显疗效,G是其有效药理成分之一,存在如图转化关系:
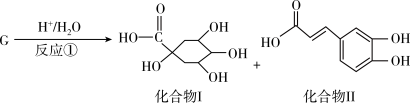
下列有关说法正确的是

下列有关说法正确的是
| A.化合物Ⅱ中所有碳原子可能都共面 |
| B.化合物Ⅰ分子中有3个手性碳原子 |
| C.化合物G、Ⅰ、Ⅱ均能发生氧化反应、取代反应、消去反应 |
| D.若在反应中,G与水按1:1发生反应,则G的分子式为C16H20O10 |
您最近一年使用:0次
2020-06-09更新
|
301次组卷
|
5卷引用:江西省金溪县第一中学2023届高三上学期第一次月考化学试题
江西省金溪县第一中学2023届高三上学期第一次月考化学试题山东省淄博市部分学校2020届高三6月阶段性诊断考试(二模)化学试题(已下线)热点题型特训 新情境迁移考查有机化合物的结构和性质(已下线)【浙江新东方】高中化学20210621-005【2021】【高二下】广东省肇庆市第一中学2020--2021学年高二下学期期中考试化学试题



