名校
1 . Ⅰ.几种短周期元素的原子半径及主要化合价如下表:已知X是短周期中最活泼的金属,且与R同周期。
(1)M在元素周期表中的位置为________________ 。
(2)X与Y按原子个数比2∶1构成的物质的电子式为________________ ;所含化学键类型_________ 。
(3)X+、 Y2-、M2-离子半径大小顺序为_____________________________________ 。
(4)将YM2通入FeCl3溶液中的离子方程式:______________________________________ 。
Ⅱ.如下图转化关系: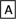
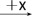
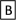
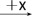
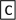
(1)若B为白色胶状不溶物,则A与C反应的离子方程式为_______________________ 。
(2)若向B溶液中滴加铁氰化钾溶液会产生特征蓝色沉淀,则A与C反应的离子方程式为___________ 。
| 元素代号 | X | Y | Z | M | R |
| 原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
| 主要化合价 | +1 | +6 -2 | +5 -3 | -2 | +3 |
(2)X与Y按原子个数比2∶1构成的物质的电子式为
(3)X+、 Y2-、M2-离子半径大小顺序为
(4)将YM2通入FeCl3溶液中的离子方程式:
Ⅱ.如下图转化关系:
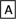
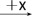
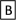
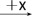
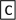
(1)若B为白色胶状不溶物,则A与C反应的离子方程式为
(2)若向B溶液中滴加铁氰化钾溶液会产生特征蓝色沉淀,则A与C反应的离子方程式为
您最近一年使用:0次
2018-11-16更新
|
376次组卷
|
2卷引用:江西省安远县第一中学2020届高三上学期第三次月考化学试题
2 . I.元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3:4,M原子的最外层电子数与次外层电子数之比为3 :4,且M原子的质子数是Y原子的2倍;N-、Z+、X+离子半径逐渐减小;化合物XN常温下为气体,请回答下列问题:
(1)写出Y、Z、N按原子个数之比1 :1:1形成的化合物的电子式_______________ 。
(2)写出由X、Y、Z、M、N中某些原子形成的18电子分子和18电子离子发生氧化还原反应的离子方程式:_________________ 。
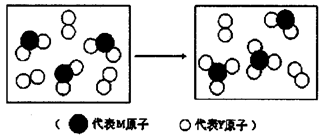
(3)上图表示由上述两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,请写出该转化过程的化学方程式:________________ 。
Ⅱ.A、B、C、D是原子序数均小于20的四种元素。A与B同主族,且能形成BA2、BA3的型分子。B、C、D所形成的简单离子电子层结构相同,且B、C、D离子半径依次减小。请回答下列问题:
(4)D元素在元素周期表中的位置是_____ 。B与D所形成的化合物的化学键类型为______ 。
(5)将C单质的水溶液滴加到B与D所形成化合物的水溶液中,其反应的离子方程式为_________ 。
(1)写出Y、Z、N按原子个数之比1 :1:1形成的化合物的电子式
(2)写出由X、Y、Z、M、N中某些原子形成的18电子分子和18电子离子发生氧化还原反应的离子方程式:

(3)上图表示由上述两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,请写出该转化过程的化学方程式:
Ⅱ.A、B、C、D是原子序数均小于20的四种元素。A与B同主族,且能形成BA2、BA3的型分子。B、C、D所形成的简单离子电子层结构相同,且B、C、D离子半径依次减小。请回答下列问题:
(4)D元素在元素周期表中的位置是
(5)将C单质的水溶液滴加到B与D所形成化合物的水溶液中,其反应的离子方程式为
您最近一年使用:0次
解题方法
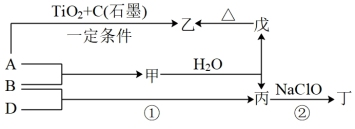
3 . 已知A、B、D为中学常见的单质,甲、乙、丙、丁、戊为短周期元素组成的化合物。其中,丙是一种能使湿润的红色石蕊试纸变蓝的无色气体;丁是一种高能燃料,其组成元素与丙相同,且为18电子微粒;戊是一种难溶于水的白色胶状物质,既能与强酸反应,也能与强碱反应,具有净水作用。各物质间的转化关系如图所示(某些条件已略去)。请用化学用语回答下列问题:
(1)A在元素周期表中的位置________
A、B单质对应元素的简单离子半径由大到小的顺序为____________________ 。
(2)丙的电子式为____________ ,丁中所包含的化学键类型有_____________ (填字母序号)。
a.离子键 b.极性共价键 c.非极性共价键
(3)甲和水反应生成戊和丙的化学方程式为_______________________ 。
(4)一定条件下,A与TiO2、C(石墨)反应只生成乙和碳化钛(TiC)。已知该反应生成1mol乙时放出536kJ热量,其热化学方程式为_______________________ 。
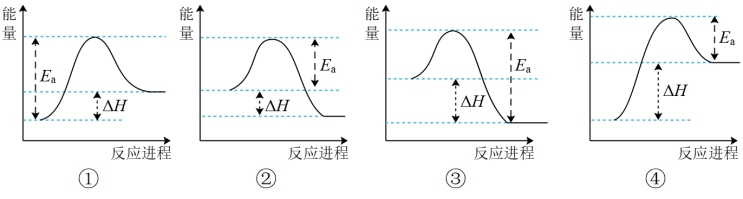
(5)已知另有物质己为中学常见黑色磁性氧化物,能够与A在一定条件下发生反应,实验测得与A反应的焓变(△H)和活化能(Ea)。下列能量关系图合理的是__________ (填写序号)。
(6)资料显示物质己可用于除去地下水中的TcO4— (99Tc具有放射性)。在弱酸性条件下,物质已将TcO4— 转化为难溶于水的TcO2,同时得到一种难溶于水的弱碱,该反应的离子方程式为___________________________ 。

(1)A在元素周期表中的位置
A、B单质对应元素的简单离子半径由大到小的顺序为
(2)丙的电子式为
a.离子键 b.极性共价键 c.非极性共价键
(3)甲和水反应生成戊和丙的化学方程式为
(4)一定条件下,A与TiO2、C(石墨)反应只生成乙和碳化钛(TiC)。已知该反应生成1mol乙时放出536kJ热量,其热化学方程式为
(5)已知另有物质己为中学常见黑色磁性氧化物,能够与A在一定条件下发生反应,实验测得与A反应的焓变(△H)和活化能(Ea)。下列能量关系图合理的是

(6)资料显示物质己可用于除去地下水中的TcO4— (99Tc具有放射性)。在弱酸性条件下,物质已将TcO4— 转化为难溶于水的TcO2,同时得到一种难溶于水的弱碱,该反应的离子方程式为
您最近一年使用:0次
4 . 下图是一些常见的单质和化合物之间的转化关系图,有些反应中的部分物质被略去。常温常压下,A为无色有毒气体,B为红棕色粉末,C、E为生活中最常用的金属单质,J为红褐色固体,L为两性氢氧化物。反应①、②均为工业上的重要反应。
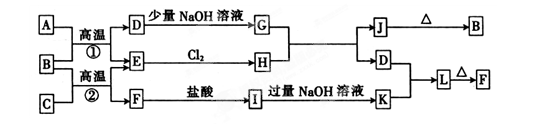
请回答下列问题:
⑴写出B的化学式为__________ ;D的电子式为____________ 。
⑵组成单质C的元素在元素周期表中的位置为_____________ ;
⑶写出向I溶液中加入过量NaOH溶液时发生反应的离子方程式:_____________ 。
⑷写出向Na2SiO3溶液中通入少量D时发生反应的离子方程式:______________ 。

请回答下列问题:
⑴写出B的化学式为
⑵组成单质C的元素在元素周期表中的位置为
⑶写出向I溶液中加入过量NaOH溶液时发生反应的离子方程式:
⑷写出向Na2SiO3溶液中通入少量D时发生反应的离子方程式:
您最近一年使用:0次
5 . 化合物M由两种短周期主族元素组成,在一定条件下可以发生下列转化:
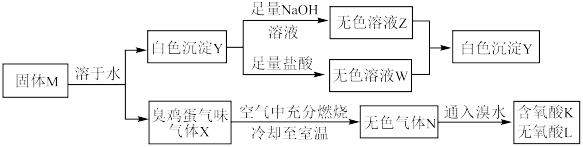
请回答下列问题:
(1)固体M的化学式为___________ 。
(2)无氧酸L中阴离子对应元素在元素周期表中的位置为___________ ,其基态原子中电子的空间运动状态有___________ 种。
(3)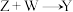 的化学方程式为
的化学方程式为___________ 。
(4)上述流程的反应中涉及的短周期非金属元素的电负性由大到小的顺序为___________ 。
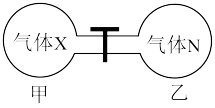
(5)如图所示,在室温下向甲、乙两相同密闭容器中,分别充入等物质的量气体X和气体N。
①反应前两容器中的气体密度: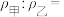
___________ 。
②打开活塞,使气体充分反应,则反应前后的压强: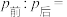
___________ 。
(6)将无色气体N通入到浓硝酸中,有红棕色气体冒出,在反应中n(氧化剂):n(还原剂)=___________ 。

请回答下列问题:
(1)固体M的化学式为
(2)无氧酸L中阴离子对应元素在元素周期表中的位置为
(3)
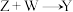 的化学方程式为
的化学方程式为(4)上述流程的反应中涉及的短周期非金属元素的电负性由大到小的顺序为
(5)如图所示,在室温下向甲、乙两相同密闭容器中,分别充入等物质的量气体X和气体N。

①反应前两容器中的气体密度:
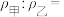
②打开活塞,使气体充分反应,则反应前后的压强:
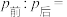
(6)将无色气体N通入到浓硝酸中,有红棕色气体冒出,在反应中n(氧化剂):n(还原剂)=
您最近一年使用:0次
2023-11-22更新
|
88次组卷
|
2卷引用:江西省2024届高三上学期11 月一轮总复习调研测试化学试题
解题方法
6 . 以苯为原料合成F,转化关系如下:

F是一种具有重要工业价值的芳香化合物,含有C、H、O、N 四种元素,其蒸气密度是相同状况下氢气密度的74.5倍,分子中有两个互为对位的取代基。C能与碳酸氢钠反应,试剂②为Fe/HCl。已知:
①
② 苯胺:弱碱性,易氧化
苯胺:弱碱性,易氧化
③RCOCl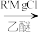 RCOR'
RCOR'
请回答下列问题:
(1)反应① 为加成反应,写出A的化学式_________ 。
(2)B中所含官能团的名称为_______ ;生成B时,常伴有附反应发生,反应所得产物除B外可能还含有____________ (写出一种的结构简式)。
(3)试剂①是指_________ ;试剂①和试剂②的顺序能否互换________ ;为什么?________ 。
(4)E生成F的化学方程式___________________ 。
(5)参照上述合成路线,以(CH3)2CHCHO为原料(无机试剂任选),设计制备(CH3)2CHCOCH3的合成路线。________________ 。

F是一种具有重要工业价值的芳香化合物,含有C、H、O、N 四种元素,其蒸气密度是相同状况下氢气密度的74.5倍,分子中有两个互为对位的取代基。C能与碳酸氢钠反应,试剂②为Fe/HCl。已知:
①

②
 苯胺:弱碱性,易氧化
苯胺:弱碱性,易氧化③RCOCl
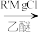 RCOR'
RCOR'请回答下列问题:
(1)反应① 为加成反应,写出A的化学式
(2)B中所含官能团的名称为
(3)试剂①是指
(4)E生成F的化学方程式
(5)参照上述合成路线,以(CH3)2CHCHO为原料(无机试剂任选),设计制备(CH3)2CHCOCH3的合成路线。
您最近一年使用:0次
名校
解题方法
7 . 碲(Te)广泛用于太阳能、电子、医药等领域,对碲的综合回收利用尤为重要。工业上,从含碲化亚铜的废渣(主要成分Cu2Te,还有少量的Ag、Cu)中提取碲的流程如图:

回答下列问题:
(1)写出碲元素在元素周期表中的位置____ 。
(2)“酸浸”过程中生成TeOSO4的离子方程式为____ 。
(3)已知:Ksp(Ag2SO4)=7.70×10-5,Ksp(AgCl)=1.8×10-10。向含Ag2SO4滤渣中加入浓盐酸,Ag2SO4能否充分转化为AgCl?通过计算说明____ 。
(4)电解除铜时,铜、碲沉淀的关系如表。
①电解初始阶段阴极的电极反应式是____ 。
②最佳电解时间为30min,原因是____ 。
(5)向“滤液II”中通入SO2反应一段时间后,Te(IV)的浓度从5.0g/L下降到0.2g/L,写出TeOSO4生成Te的化学方程式____ ,其中Te元素的回收率为____ (忽略溶液体积变化,结果用百分数表示,保留二位有效数字)。
(6)整个过程中可循环利用的物质为____ (填化学式)。

回答下列问题:
(1)写出碲元素在元素周期表中的位置
(2)“酸浸”过程中生成TeOSO4的离子方程式为
(3)已知:Ksp(Ag2SO4)=7.70×10-5,Ksp(AgCl)=1.8×10-10。向含Ag2SO4滤渣中加入浓盐酸,Ag2SO4能否充分转化为AgCl?通过计算说明
(4)电解除铜时,铜、碲沉淀的关系如表。
| 电解时间(min) | 铜沉淀率 | 碲沉淀率 |
| 10 | 25% | 0.1% |
| 20 | 40% | 0.2% |
| 30 | 62% | 0.4% |
| 40 | 65% | 2.0% |
②最佳电解时间为30min,原因是
(5)向“滤液II”中通入SO2反应一段时间后,Te(IV)的浓度从5.0g/L下降到0.2g/L,写出TeOSO4生成Te的化学方程式
(6)整个过程中可循环利用的物质为
您最近一年使用:0次
2022-05-05更新
|
668次组卷
|
3卷引用:江西省重点中学盟校2022届高三下学期5月第二次联考理综化学试题
江西省重点中学盟校2022届高三下学期5月第二次联考理综化学试题(已下线)微专题28 有关工艺流程和实验探究方程式的书写-备战2023年高考化学一轮复习考点微专题陕西师范大学附属中学、渭北中学等2022-2023学年高三上学期期初检测化学联考试题
8 . A是化合物,B是金属单质,它们之间相互反应以及生成物之间的转化关系如图所示:
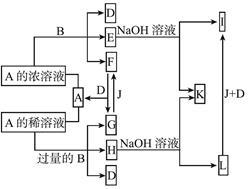
(1)金属B在元素周期表中的位置是________ ,B和A的浓溶液反应的条件是________ 。写出少量B与A的稀溶液反应的离子方程式:__________________________ 。
(2)常温下0.1 mol/L E的水溶液中各离子浓度大小关系为________________ 。
(3)L转化为I的现象是________ 。写出有关的化学方程式:____________________ 。
(4)如何检测H溶液中阳离子的存在,写出实验操作方法、现象、结论:________________________ 。
(5)已知25 ℃时Fe(OH)3的Ksp=3.5×10-39,现将4.0×10-8 mol/L E溶液与2.0×10-8 mol/L NaOH溶液等体积混合(忽略溶液混合时体积的变化),通过列式计算说明是否有沉淀产生:____________________ 。

(1)金属B在元素周期表中的位置是
(2)常温下0.1 mol/L E的水溶液中各离子浓度大小关系为
(3)L转化为I的现象是
(4)如何检测H溶液中阳离子的存在,写出实验操作方法、现象、结论:
(5)已知25 ℃时Fe(OH)3的Ksp=3.5×10-39,现将4.0×10-8 mol/L E溶液与2.0×10-8 mol/L NaOH溶液等体积混合(忽略溶液混合时体积的变化),通过列式计算说明是否有沉淀产生:
您最近一年使用:0次
9 . 已知一个碳原子上连有两个羟基时,易发生下列转化:
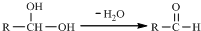 .请根据如图回答:
.请根据如图回答:

(1)A中所含官能团的名称为___________ 。
(2)质谱仪分析发现B的最大质荷比为208;红外光谱显示B分子中含有苯环结构和两个酯基;核磁共振氢谱中有五个吸收峰,其峰值比为2:2:2:3:3,其中苯环上的一氯代物只有两种。则B的结构简式为____________ 。
(3)写出下列反应方程式:①_____________ ;②____________ 。
(4)符合下列条件的B的同分异构体共有________ 种。
①属于芳香族化合物
②含有三个取代基,其中只有一个羟基,另两个取代基相同且处于相同的位置
③能发生水解反应和银镜反应
(5)已知: 。
。
请以G为唯一有机试剂合成乙酰乙酸乙酯(CH3COCH2COOC2H5),设计合成路线(其他试剂任选)。__________________________________
合成路线流程图示例: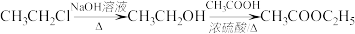 。
。
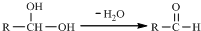 .请根据如图回答:
.请根据如图回答:
(1)A中所含官能团的名称为
(2)质谱仪分析发现B的最大质荷比为208;红外光谱显示B分子中含有苯环结构和两个酯基;核磁共振氢谱中有五个吸收峰,其峰值比为2:2:2:3:3,其中苯环上的一氯代物只有两种。则B的结构简式为
(3)写出下列反应方程式:①
(4)符合下列条件的B的同分异构体共有
①属于芳香族化合物
②含有三个取代基,其中只有一个羟基,另两个取代基相同且处于相同的位置
③能发生水解反应和银镜反应
(5)已知:
 。
。请以G为唯一有机试剂合成乙酰乙酸乙酯(CH3COCH2COOC2H5),设计合成路线(其他试剂任选)。
合成路线流程图示例:
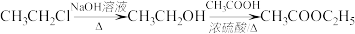 。
。
您最近一年使用:0次
2016-12-09更新
|
353次组卷
|
3卷引用:2017届江西省吉安一中高三上学期第一次段考化学卷
名校
解题方法
10 . 聚戊二酸丙二醇酯(PPG)是一种可降解的聚酯类高分子材料,在材料的生物相容性方面有很好的应用前景。PPG的一种合成路线如下:
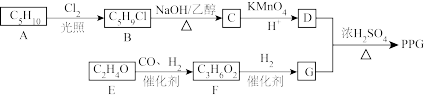
已知:①A、E的核磁共振氢谱显示只有一种化学环境的氢;
②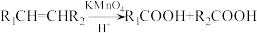
③R1CHO+R2CH2CHO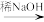

④F能发生银镜反应,也能被氧化成丙二醛。
回答下列问题:
(1)A的结构简式为___________ ,F中官能团名称为___________ 。
(2)由B生成C的化学方程式为___________ 。
(3)由D和G生成PPG的反应类型为___________ 。
(4)D的同分异构体中能同时满足下列条件的共有___________ 种(不含立体异构):
①能与饱和NaHCO3溶液反应产生气体;②既能发生银镜反应,又能发生水解反应;其中核磁共振氢谱显示为3组峰,且峰面积比为6:1:1的是___________ (写结构简式)。
(5)以乙醇、甲醛为起始原料,选用必要的无机试剂合成G,写出合成路线(用结构简式表示有机物)用箭头表示转化关系,箭头上注明试剂和反应条件。___________
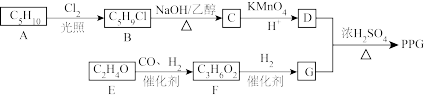
已知:①A、E的核磁共振氢谱显示只有一种化学环境的氢;
②
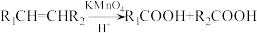
③R1CHO+R2CH2CHO
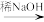

④F能发生银镜反应,也能被氧化成丙二醛。
回答下列问题:
(1)A的结构简式为
(2)由B生成C的化学方程式为
(3)由D和G生成PPG的反应类型为
(4)D的同分异构体中能同时满足下列条件的共有
①能与饱和NaHCO3溶液反应产生气体;②既能发生银镜反应,又能发生水解反应;其中核磁共振氢谱显示为3组峰,且峰面积比为6:1:1的是
(5)以乙醇、甲醛为起始原料,选用必要的无机试剂合成G,写出合成路线(用结构简式表示有机物)用箭头表示转化关系,箭头上注明试剂和反应条件。
您最近一年使用:0次
2021-09-06更新
|
477次组卷
|
3卷引用:江西省南昌市2022届高三摸底考试化学试题



