名校
解题方法
1 . 乙二胺四乙酸铁钠可用于感光材料冲洗药品及漂白剂,化学式为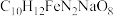 ;工业上可用EDTA与
;工业上可用EDTA与 、NaOH溶液发生反应进行制备,合成路线如下:
、NaOH溶液发生反应进行制备,合成路线如下:
(1)基态氯原子的价层电子排布图为___________ 。
(2)下列氮原子能量最高的是___________(填标号)。
(3)EDTA的组成元素中C、N、O的第一电离能由大到小顺序为___________ (填元素符号)。碳原子的杂化轨道类型为___________ 。
(4)NH3中N—H键的键角小于CH4中C—H键的键角,其原因为___________ 。
(5)某种Fe、N组成的磁性化合物的结构如图1所示,N随机排列在Fe构成的正八面体的空隙中。该磁性化合物的化学式为___________ 。___________ 区(填“s”“p”“d”或“ds”)。铁的某种晶胞沿面对角线的位置切下之后可以得到如图2所示的截面。假设铁的原子半径为a nm,则该铁晶体的密度为___________  (列出计算式,设
(列出计算式,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
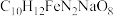 ;工业上可用EDTA与
;工业上可用EDTA与 、NaOH溶液发生反应进行制备,合成路线如下:
、NaOH溶液发生反应进行制备,合成路线如下: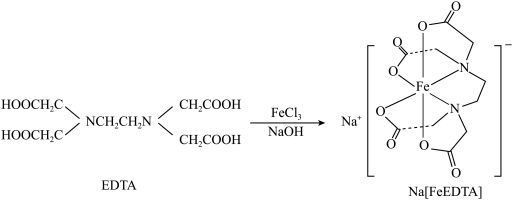
(1)基态氯原子的价层电子排布图为
(2)下列氮原子能量最高的是___________(填标号)。
A.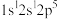 | B. | C. | D.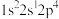 |
(4)NH3中N—H键的键角小于CH4中C—H键的键角,其原因为
(5)某种Fe、N组成的磁性化合物的结构如图1所示,N随机排列在Fe构成的正八面体的空隙中。该磁性化合物的化学式为
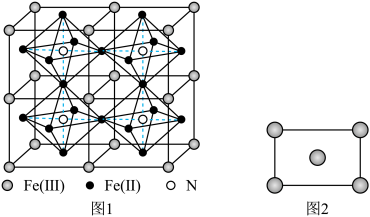
 (列出计算式,设
(列出计算式,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
2023-04-23更新
|
906次组卷
|
8卷引用:北京市首都师范大学附属中学2023-2024学年高三下学期3月月考化学试题
北京市首都师范大学附属中学2023-2024学年高三下学期3月月考化学试题福建省百校联盟2023届高三第三次模拟考试化学试题福建省百校联盟2023届高三下学期第三次模拟考试化学试题(已下线)押题密卷 02-【热题狂飙】2023年高考化学样卷(全国卷专用)广西壮族自治区南宁市第二中学2023届高三下学期收网考理科综合化学试题(已下线)专题16 物质结构与性质综合题-2023年高考化学真题题源解密(全国通用)北京市第二中学2022-2023学年高二下学期期末考试化学试题2023届广西钦州市灵山县那隆中学高三下学期5月考前冲刺保温卷理综试卷-高中化学
2010·北京西城·二模
2 . 化合物A是制玻璃的主要原料之一。常温下,化合物B、H、I为气体,B不溶于水,H、I易溶于水,H的水溶液呈碱性,I的水溶液呈酸性。D元素是地壳中含量仅次于氧的非金属元素。化合物J是一种可用于制造发动机的新型无机非金属材料,其相对分子质量为140,其中D元素的质量分数为60%。上述物质间的转化关系如下图所示。
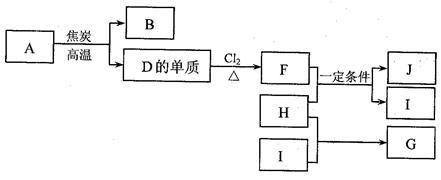
(1)除A外,制玻璃的主要原料还有物质(填化学式)_______ 、_______ 。
盛放NaOH溶液的试剂瓶不能用玻璃塞,原因是(用化学方程式表示)_______ 。
(2)D元素在元素周期表中的位置是___________ 。
(3)H的电子式是_________ 。
(4)F和H反应生成J和I反应的化学方程式是___________ 。
(5)下列说法正确的是(填选项序号)______ 。
a.上述由A生成D的单质的反应属于置换反应
b. D元素在自然界中主要以单质形式存在
c. G是含有极性共价键的离子化合物
d. I是强电解质,G是弱电解质,二者的水溶液都显酸性

(1)除A外,制玻璃的主要原料还有物质(填化学式)
盛放NaOH溶液的试剂瓶不能用玻璃塞,原因是(用化学方程式表示)
(2)D元素在元素周期表中的位置是
(3)H的电子式是
(4)F和H反应生成J和I反应的化学方程式是
(5)下列说法正确的是(填选项序号)
a.上述由A生成D的单质的反应属于置换反应
b. D元素在自然界中主要以单质形式存在
c. G是含有极性共价键的离子化合物
d. I是强电解质,G是弱电解质,二者的水溶液都显酸性
您最近一年使用:0次
3 . 硒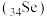 是一种应用广泛的元素。
是一种应用广泛的元素。
Ⅰ.检测细胞体内的
风湿性关节炎与细胞体内产生的 有关。一种含
有关。一种含 的荧光探针分子
的荧光探针分子 检测
检测 及再生的转化如图。
及再生的转化如图。 位于元素周期表中
位于元素周期表中_____________ 区(填“ ”“
”“ ”“
”“ ”或“
”或“ ”)。
”)。
② 的结构式是
的结构式是_____________ 。
(2)在 中,
中,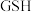 转化为
转化为 。
。 ”在
”在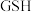 中标出所有的手性碳原子
中标出所有的手性碳原子__________ 。
② 中,
中,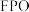 与
与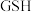 的物质的量之比为
的物质的量之比为_________________ 。
Ⅱ.应用于光电领域
 可作为新型镁电池的正极材料,其晶胞结构如图所示。
可作为新型镁电池的正极材料,其晶胞结构如图所示。_________________ 。
②晶胞中“ ”表示
”表示_________________ (填离子符号)。
(4)新型镁电池放电时,图1晶胞中 位置不变,
位置不变, 嵌入的同时
嵌入的同时 被挤出。生成的
被挤出。生成的 晶体结构与
晶体结构与 晶体相似,其中
晶体相似,其中 位于图1晶胞的
位于图1晶胞的_____________________ (填序号)。
 .棱心
.棱心  .面心
.面心  .体心
.体心  .顶点
.顶点
 是一种应用广泛的元素。
是一种应用广泛的元素。Ⅰ.检测细胞体内的

风湿性关节炎与细胞体内产生的
 有关。一种含
有关。一种含 的荧光探针分子
的荧光探针分子 检测
检测 及再生的转化如图。
及再生的转化如图。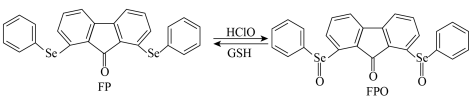
 位于元素周期表中
位于元素周期表中 ”“
”“ ”“
”“ ”或“
”或“ ”)。
”)。②
 的结构式是
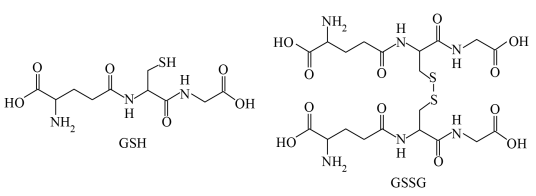
的结构式是(2)在
 中,
中, 转化为
转化为 。
。
 ”在
”在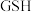 中标出所有的手性碳原子
中标出所有的手性碳原子②
 中,
中,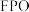 与
与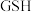 的物质的量之比为
的物质的量之比为Ⅱ.应用于光电领域
 可作为新型镁电池的正极材料,其晶胞结构如图所示。
可作为新型镁电池的正极材料,其晶胞结构如图所示。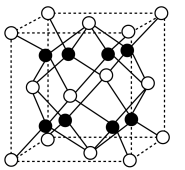
②晶胞中“
 ”表示
”表示(4)新型镁电池放电时,图1晶胞中
 位置不变,
位置不变, 嵌入的同时
嵌入的同时 被挤出。生成的
被挤出。生成的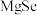 晶体结构与
晶体结构与 晶体相似,其中
晶体相似,其中 位于图1晶胞的
位于图1晶胞的 .棱心
.棱心  .面心
.面心  .体心
.体心  .顶点
.顶点
您最近一年使用:0次
4 . 金属镓有“电子工业脊梁”的美誉,镓及其化合物应用广泛。
(1) 镓(Ga)的原子结构示意图为 ,镓元素在周期表中的位置是
,镓元素在周期表中的位置是_______ 。
(2)镓能与沸水剧烈反应生成氢气和氢氧化镓,该反应的化学方程式是______________ 。
(3)氮化镓在电和光的转化方面性能突出,是迄今理论上光电转化效率最高的材料。
资料:镓的熔点较低(29.8℃),沸点很高(2403℃)。
①传统的氮化镓(GaN)制备方法是采用GaCl3与NH3在一定条件下反应,该反应的化学方程式是____________________ 。
②当代工业上固态氮化镓(GaN)的制备方法是利用镓与NH3在1000℃高温下合成,同时生成氢气,每生成l mol H2时放出10.27 kJ热量。该可逆反应的热化学方程式是____________________________________ 。
③在密闭容器中,充入一定量的Ga与NH3发生上述反应,实验测得反应平衡体系中NH3的体积分数与压强P和温度T的关系曲线如图1所示。

图中A点和C点化学平衡常数的关系是:KA_____ KC (填“>”“=”或“<”),理由是_____________________________ 。
(4)电解法可以提纯粗镓,具体原理如图2所示:
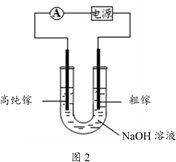
①粗镓与电源____ 极相连。(填“正”或“负”)
②镓在阳极溶解生成的Ga3+与NaOH溶液反应生成GaO2-,GaO2-在阴极放电的电极反应式是
_____________________________ 。
(1) 镓(Ga)的原子结构示意图为
 ,镓元素在周期表中的位置是
,镓元素在周期表中的位置是(2)镓能与沸水剧烈反应生成氢气和氢氧化镓,该反应的化学方程式是
(3)氮化镓在电和光的转化方面性能突出,是迄今理论上光电转化效率最高的材料。
资料:镓的熔点较低(29.8℃),沸点很高(2403℃)。
①传统的氮化镓(GaN)制备方法是采用GaCl3与NH3在一定条件下反应,该反应的化学方程式是
②当代工业上固态氮化镓(GaN)的制备方法是利用镓与NH3在1000℃高温下合成,同时生成氢气,每生成l mol H2时放出10.27 kJ热量。该可逆反应的热化学方程式是
③在密闭容器中,充入一定量的Ga与NH3发生上述反应,实验测得反应平衡体系中NH3的体积分数与压强P和温度T的关系曲线如图1所示。

图中A点和C点化学平衡常数的关系是:KA
(4)电解法可以提纯粗镓,具体原理如图2所示:

①粗镓与电源
②镓在阳极溶解生成的Ga3+与NaOH溶液反应生成GaO2-,GaO2-在阴极放电的电极反应式是
您最近一年使用:0次
解题方法
5 . 有效控制大气温室气体浓度,推动绿色低碳发展,是人类可持续发展的重要战略之一,因此捕集、利用CO2始终是科学研究的热点。
(1)新的研究表明,可以将CO2转化为炭黑回收利用,反应原理如图所示。
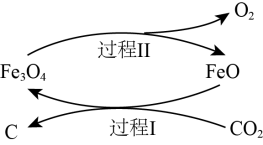
①碳在元素周期表中的位置是_______________ 。
②整个过程中FeO的作用是__________________ 。
③写出CO2转化为炭黑的总反应化学方程式__________________ 。
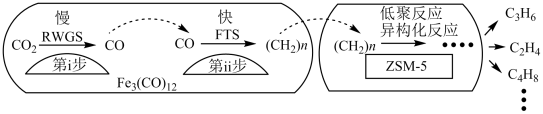
(2)我国科学家用Fe3(CO)12/ZSM-5催化CO2加氢合成低碳烯烃反应,所得产物含CH4、C3H6、C4H8等副产物,反应过程如图。
催化剂中添加Na、K、Cu助剂后(助剂也起催化作用)可改变反应的选择性,在其他条件相同时,添加不同助剂,经过相同时间后测得CO2转化率和各产物的物质的量分数如下表。
①欲提高单位时间内乙烯的产量,在Fe3(CO)12/ZSM-5中添加____________ 助剂效果最好;
②加入助剂能提高单位时间内乙烯产量的根本原因是____________ 。
(3)电解法转化CO2可实现CO2资源化利用。电解CO2制HCOOH的原理如右图所示。
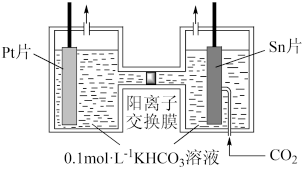
①写出阴极CO2还原为HCOO−的电极反应式:________________________ 。
②电解一段时间后,阳极区的KHCO3溶液浓度降低,其原因是_____________________ 。
(1)新的研究表明,可以将CO2转化为炭黑回收利用,反应原理如图所示。

①碳在元素周期表中的位置是
②整个过程中FeO的作用是
③写出CO2转化为炭黑的总反应化学方程式
(2)我国科学家用Fe3(CO)12/ZSM-5催化CO2加氢合成低碳烯烃反应,所得产物含CH4、C3H6、C4H8等副产物,反应过程如图。

催化剂中添加Na、K、Cu助剂后(助剂也起催化作用)可改变反应的选择性,在其他条件相同时,添加不同助剂,经过相同时间后测得CO2转化率和各产物的物质的量分数如下表。
助剂 | CO2转化率 (%) | 各产物在所有产物中的占比(%) | ||
C2H4 | C3H6 | 其他 | ||
Na | 42.5 | 35.9 | 39.6 | 24.5 |
K | 27.2 | 75.6 | 22.8 | 1.6 |
Cu | 9.8 | 80.7 | 12.5 | 6.8 |
①欲提高单位时间内乙烯的产量,在Fe3(CO)12/ZSM-5中添加
②加入助剂能提高单位时间内乙烯产量的根本原因是
(3)电解法转化CO2可实现CO2资源化利用。电解CO2制HCOOH的原理如右图所示。

①写出阴极CO2还原为HCOO−的电极反应式:
②电解一段时间后,阳极区的KHCO3溶液浓度降低,其原因是
您最近一年使用:0次
6 . W、X、Y、Z为同一周期的四种主族元素,原子序数依次增大。基态Y原子的价电子排布为3s23p4,X的电离能数据如下表所示。
(1)基态X原子的电子排布式_____ ,X在元素周期表中的位置是_____ ,_____ 区。
(2)用电子式表示WZ的形成过程:_____ 。
(3)下列事实能用元素周期律解释的是_____ (填字母序号)。
a.W可用于制备活泼金属钾
b.Y的气态氢化物的稳定性小于H2O
c.将Z单质通入Na2S溶液中,溶液变浑浊
d.Y的氧化物对应的水化物H2YO3的酸性比H2SiO3强
(4)为了进一步研究最高价氧化物对应水化物的酸碱性与元素金属性、非金属性的关系,查阅如下资料。
ⅰ.某元素最高价氧化物对应的水化物脱水前的化学式通常可以表示为M(OH)n,该水化物中的M-O-H结构有两种断键方式,断M-O键在水中电离出OH-,断O-H键则在水中电离出H+。
ⅱ.在水等强极性溶剂中,成键原子电负性的差异是影响化学键断裂难易程度的原因之一。水化物的M-O-H结构中,成键原子电负性差异越大,所成化学键越容易断裂。
①已知:O、H元素的电负性数值分别为3.5和2.1,若元素M的电负性数值为2.5,且电负性差异是影响M-O-H中化学键断裂难易程度的主要原因。该元素最高价氧化物对应的水化物呈_____ (填“酸”或“碱”)性,依据是_____ 。
②W和X的最高价氧化物对应的水化物中,碱性较强的是_____ (写化学式),结合资料说明理由:_____ 。
| 电离能 | I1 | I2 | I3 | I4 | … |
| Ia/kJ•mol-1 | 738 | 1451 | 7733 | 10540 | … |
(2)用电子式表示WZ的形成过程:
(3)下列事实能用元素周期律解释的是
a.W可用于制备活泼金属钾
b.Y的气态氢化物的稳定性小于H2O
c.将Z单质通入Na2S溶液中,溶液变浑浊
d.Y的氧化物对应的水化物H2YO3的酸性比H2SiO3强
(4)为了进一步研究最高价氧化物对应水化物的酸碱性与元素金属性、非金属性的关系,查阅如下资料。
ⅰ.某元素最高价氧化物对应的水化物脱水前的化学式通常可以表示为M(OH)n,该水化物中的M-O-H结构有两种断键方式,断M-O键在水中电离出OH-,断O-H键则在水中电离出H+。
ⅱ.在水等强极性溶剂中,成键原子电负性的差异是影响化学键断裂难易程度的原因之一。水化物的M-O-H结构中,成键原子电负性差异越大,所成化学键越容易断裂。
①已知:O、H元素的电负性数值分别为3.5和2.1,若元素M的电负性数值为2.5,且电负性差异是影响M-O-H中化学键断裂难易程度的主要原因。该元素最高价氧化物对应的水化物呈
②W和X的最高价氧化物对应的水化物中,碱性较强的是
您最近一年使用:0次
7 . 为纪念元素周期表诞生 150 周年,IUPAC 等从世界范围征集优秀青年化学家为化学元素代言,我国有8 位化学家成为硫(S)等元素的代言人。回答下列问题:
(1)S 在周期表中的位置是___________
(2)下列有关性质的比较,能用元素周期律解释的是___________ (填字母序号)
a.非金属性:O>S b.离子半径:S2->Cl- c.酸性:H2SO4>H2SO3 d.酸性:H2SO4>H3PO4
(3)Se 与 S 位于同一主族,二者氢化物稳定性较强的是:___________ (用化学式表示),用原子结构解释原因___________
(4)某同学用如下装置探究不同价态硫元素之间的转化。培养皿中 A、B、C 三个塑料瓶盖内盛有不同物质。向 Na2SO3 固体上滴加 70%硫酸,迅速用玻璃片将培养皿盖严,实验记录如下。
能够说明硫元素由+4 价转化为+6 价的证据是___________
(1)S 在周期表中的位置是
(2)下列有关性质的比较,能用元素周期律解释的是
a.非金属性:O>S b.离子半径:S2->Cl- c.酸性:H2SO4>H2SO3 d.酸性:H2SO4>H3PO4
(3)Se 与 S 位于同一主族,二者氢化物稳定性较强的是:
(4)某同学用如下装置探究不同价态硫元素之间的转化。培养皿中 A、B、C 三个塑料瓶盖内盛有不同物质。向 Na2SO3 固体上滴加 70%硫酸,迅速用玻璃片将培养皿盖严,实验记录如下。
| 实验装置 | 瓶盖 | 物质 | 实验现象 |
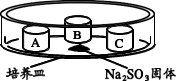 | A | 蘸有品红溶液的棉花 | 品红溶液褪色 |
| B | HCl、BaCl2 的混合溶液 | 无明显变化 | |
| C | HCl、BaCl2、FeCl3 的混合溶液 | 产生白色沉淀 |
能够说明硫元素由+4 价转化为+6 价的证据是
您最近一年使用:0次
2021-02-21更新
|
289次组卷
|
2卷引用:北京市房山区2021届高三上学期期末考试化学试题
名校
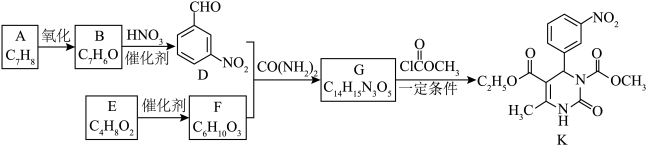
8 . 化合物K有抗高血压活性,其合成路线如下。___________ 。
(2)B→D的化学方程式是___________ 。
(3)G的结构简式是___________ 。
(4)E属于酯,E的结构简式是___________ 。
(5)K中能与 溶液反应的官能团有
溶液反应的官能团有___________ 。
a.碳碳双键 b.酯基 c.酰胺基
(6)D也可由间硝基甲苯通过电解法制得,主要物质转化关系如下。 的定义:
的定义: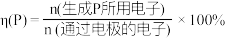
①Ⅱ中,生成Q的离子方程式是___________ 。
②若电解产生的 使间硝基甲苯通过两步氧化完全转化为D,当电极通过
使间硝基甲苯通过两步氧化完全转化为D,当电极通过 ,生成amol D时,
,生成amol D时,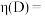
___________ 。
(7)以D、F和 为原料,“一锅法”合成G的转化过程如下。
为原料,“一锅法”合成G的转化过程如下。___________ ,M→N的反应类型是___________ 。
已知:
(2)B→D的化学方程式是
(3)G的结构简式是
(4)E属于酯,E的结构简式是
(5)K中能与
 溶液反应的官能团有
溶液反应的官能团有a.碳碳双键 b.酯基 c.酰胺基
(6)D也可由间硝基甲苯通过电解法制得,主要物质转化关系如下。
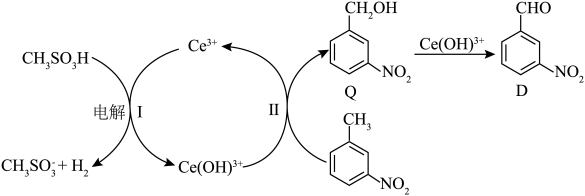
 的定义:
的定义: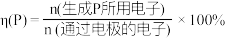
①Ⅱ中,生成Q的离子方程式是
②若电解产生的
 使间硝基甲苯通过两步氧化完全转化为D,当电极通过
使间硝基甲苯通过两步氧化完全转化为D,当电极通过 ,生成amol D时,
,生成amol D时,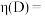
(7)以D、F和
 为原料,“一锅法”合成G的转化过程如下。
为原料,“一锅法”合成G的转化过程如下。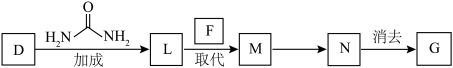
您最近一年使用:0次
2024-04-10更新
|
492次组卷
|
2卷引用:北京市西城区2024届高三统一测试(一模)化学试题
9 . W、X、Y、Z为同一周期的四种主族元素,原子序数依次增大。基态Y原子的价电子排布为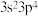 ,X的电离能数据如下表所示。
,X的电离能数据如下表所示。
(1)X在元素周期表中的位置是___________ 。
(2)用电子式表示WZ的形成过程:___________ 。
(3)下列事实能用元素周期律解释的是___________(填字母序号)。
(4)为了进一步研究最高价氧化物对应水化物的酸碱性与元素金属性、非金属性的关系,查阅如下资料。
i.某元素最高价氧化物对应的水化物脱水前的化学式通常可以表示为 ,该水化物中的
,该水化物中的 结构有两种断键方式:断
结构有两种断键方式:断 键在水中电离出
键在水中电离出 ;断
;断 键在水中电离出
键在水中电离出 。
。
ⅱ.在水等强极性溶剂中,成键原子电负性的差异是影响化学键断裂难易程度的原因之一、水化物的 结构中,成键原子电负性差异越大,所形成的化学键越容易断裂。
结构中,成键原子电负性差异越大,所形成的化学键越容易断裂。
①已知:O、H元素的电负性数值分别为3.5和2.1;某元素M的电负性数值为2.5,且电负性差异是影响 中化学键断裂难易程度的主要原因。该元素最高价氧化物对应的水化物呈
中化学键断裂难易程度的主要原因。该元素最高价氧化物对应的水化物呈___________ (填“酸”或“碱”)性,依据是___________ 。
②W和X的最高价氧化物对应的水化物中,碱性较强的是___________ (写化学式),结合资料说明理由:___________ 。
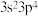 ,X的电离能数据如下表所示。
,X的电离能数据如下表所示。| 电离能 |  |  |  |  |  |
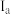 / / | 738 | 1451 | 7733 | 10540 |  |
(2)用电子式表示WZ的形成过程:
(3)下列事实能用元素周期律解释的是___________(填字母序号)。
| A.W可用于制备活泼金属钾 |
B.Y的气态氢化物的稳定性小于 |
C.将Z单质通入 溶液中,溶液变浑浊 溶液中,溶液变浑浊 |
D.Y的氧化物对应的水化物 的酸性比 的酸性比 强 强 |
i.某元素最高价氧化物对应的水化物脱水前的化学式通常可以表示为
 ,该水化物中的
,该水化物中的 结构有两种断键方式:断
结构有两种断键方式:断 键在水中电离出
键在水中电离出 ;断
;断 键在水中电离出
键在水中电离出 。
。ⅱ.在水等强极性溶剂中,成键原子电负性的差异是影响化学键断裂难易程度的原因之一、水化物的
 结构中,成键原子电负性差异越大,所形成的化学键越容易断裂。
结构中,成键原子电负性差异越大,所形成的化学键越容易断裂。①已知:O、H元素的电负性数值分别为3.5和2.1;某元素M的电负性数值为2.5,且电负性差异是影响
 中化学键断裂难易程度的主要原因。该元素最高价氧化物对应的水化物呈
中化学键断裂难易程度的主要原因。该元素最高价氧化物对应的水化物呈②W和X的最高价氧化物对应的水化物中,碱性较强的是
您最近一年使用:0次
名校
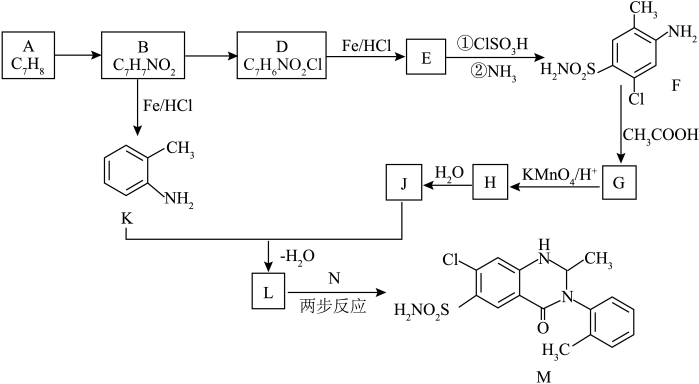
10 . 某研究小组以甲苯为起始原料,按下列路线合成某利尿药物 。
。 的化学方程式为
的化学方程式为_______ 。
(2) 的反应试剂及条件为
的反应试剂及条件为_______ 。
(3) 的反应类型为
的反应类型为_______ 。
(4)下列说法正确的是_______ 。
 的一氯代物共有3种
的一氯代物共有3种
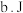 在一定条件下可以生成高分子化合物
在一定条件下可以生成高分子化合物
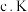 的核磁共振氢谱共有6个峰
的核磁共振氢谱共有6个峰
(5) 两步反应的设计目的是
两步反应的设计目的是_______ 。
(6)已知 的转化过程分两步,转化关系如图所示。
的转化过程分两步,转化关系如图所示。 和
和 的结构简式:
的结构简式:_______ 、_______ 。
 。
。
已知: (
( 代表烃基或
代表烃基或 原子)
原子)
 的化学方程式为
的化学方程式为(2)
 的反应试剂及条件为
的反应试剂及条件为(3)
 的反应类型为
的反应类型为(4)下列说法正确的是
 的一氯代物共有3种
的一氯代物共有3种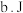 在一定条件下可以生成高分子化合物
在一定条件下可以生成高分子化合物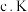 的核磁共振氢谱共有6个峰
的核磁共振氢谱共有6个峰(5)
 两步反应的设计目的是
两步反应的设计目的是(6)已知
 的转化过程分两步,转化关系如图所示。
的转化过程分两步,转化关系如图所示。
 和
和 的结构简式:
的结构简式:
您最近一年使用:0次
2024-04-01更新
|
232次组卷
|
3卷引用:北京市门头沟区2023-2024学年高三下学期一模化学试题



