名校
解题方法
1 . 乙二胺四乙酸铁钠可用于感光材料冲洗药品及漂白剂,化学式为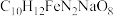 ;工业上可用EDTA与
;工业上可用EDTA与 、NaOH溶液发生反应进行制备,合成路线如下:
、NaOH溶液发生反应进行制备,合成路线如下:
(1)基态氯原子的价层电子排布图为___________ 。
(2)下列氮原子能量最高的是___________(填标号)。
(3)EDTA的组成元素中C、N、O的第一电离能由大到小顺序为___________ (填元素符号)。碳原子的杂化轨道类型为___________ 。
(4)NH3中N—H键的键角小于CH4中C—H键的键角,其原因为___________ 。
(5)某种Fe、N组成的磁性化合物的结构如图1所示,N随机排列在Fe构成的正八面体的空隙中。该磁性化合物的化学式为___________ 。___________ 区(填“s”“p”“d”或“ds”)。铁的某种晶胞沿面对角线的位置切下之后可以得到如图2所示的截面。假设铁的原子半径为a nm,则该铁晶体的密度为___________  (列出计算式,设
(列出计算式,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
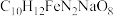 ;工业上可用EDTA与
;工业上可用EDTA与 、NaOH溶液发生反应进行制备,合成路线如下:
、NaOH溶液发生反应进行制备,合成路线如下: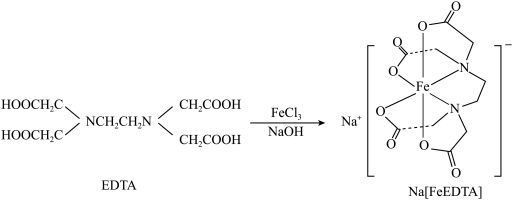
(1)基态氯原子的价层电子排布图为
(2)下列氮原子能量最高的是___________(填标号)。
A.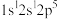 | B. | C. | D.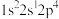 |
(4)NH3中N—H键的键角小于CH4中C—H键的键角,其原因为
(5)某种Fe、N组成的磁性化合物的结构如图1所示,N随机排列在Fe构成的正八面体的空隙中。该磁性化合物的化学式为
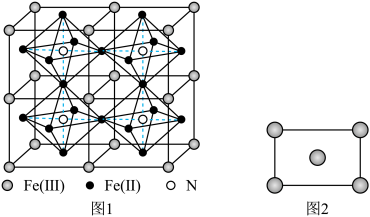
 (列出计算式,设
(列出计算式,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
2023-04-23更新
|
906次组卷
|
8卷引用:广西壮族自治区南宁市第二中学2023届高三下学期收网考理科综合化学试题
广西壮族自治区南宁市第二中学2023届高三下学期收网考理科综合化学试题2023届广西钦州市灵山县那隆中学高三下学期5月考前冲刺保温卷理综试卷-高中化学福建省百校联盟2023届高三第三次模拟考试化学试题福建省百校联盟2023届高三下学期第三次模拟考试化学试题(已下线)押题密卷 02-【热题狂飙】2023年高考化学样卷(全国卷专用)(已下线)专题16 物质结构与性质综合题-2023年高考化学真题题源解密(全国通用)北京市首都师范大学附属中学2023-2024学年高三下学期3月月考化学试题北京市第二中学2022-2023学年高二下学期期末考试化学试题
名校
解题方法
2 . 药物M可用于治疗动脉硬化,其合成路线如下。
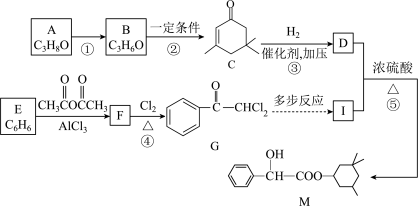
已知:i.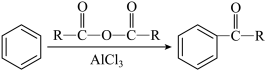
ii.B的核磁共振氢谱只有一组峰
回答下列问题:
(1)M的官能团名称为___________ 。
(2)有机物A的名称为___________ 。
(3)C的分子式为___________ 。
(4)反应④的反应类型是___________ 。
(5)写出反应⑤的化学方程式为___________ 。
(6)写出满足下列条件的G的所有同分异构体的结构简式___________ 。
①结构中含有酚羟基 ②苯环上只有两个取代基且位于间位
(7)已知: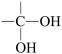 →
→ 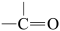 +H2O ,以G为原料,选择必要的无机试剂合成I,设计合成路线
+H2O ,以G为原料,选择必要的无机试剂合成I,设计合成路线___________ (用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。

已知:i.

ii.B的核磁共振氢谱只有一组峰
回答下列问题:
(1)M的官能团名称为
(2)有机物A的名称为
(3)C的分子式为
(4)反应④的反应类型是
(5)写出反应⑤的化学方程式为
(6)写出满足下列条件的G的所有同分异构体的结构简式
①结构中含有酚羟基 ②苯环上只有两个取代基且位于间位
(7)已知:
 →
→ 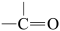 +H2O ,以G为原料,选择必要的无机试剂合成I,设计合成路线
+H2O ,以G为原料,选择必要的无机试剂合成I,设计合成路线
您最近一年使用:0次
3 . 亚硒酸钠(Na2SeO3)为无色晶体,在空气中稳定,溶于水不溶于醇。如图是氧气氧化法制备亚硒酸钠的生产工序,请回答下列问题∶

(1)硒与硫是同主族的相邻元素,亚硒酸钠中硒的化合价为_________ ,在周期表中的位置是_________ 。
(2)搅拌槽中加入氢氧化钠合成亚硒酸钠溶液并调整pH值为7~14,pH值调到7~ 14的原因是____________ 。
(3)操作①的名称是_______ ;流程图中真空干燥箱的作用是_____________ 。
(4)操作②为_____________ 、结晶、过滤、洗涤,然后用离心机甩掉结晶残液即得带有结晶水的亚硒酸钠。其中所用洗涤剂最好是______ (填序号)。
a.稀硫酸b.氢氧化钠稀溶液c.水d.乙醇
(5)现在常用以单质硒为原料,在氢氧化钠水溶液中通入高压氧气的方法来获得亚硒酸钠。写出制备亚硒酸钠的化学反应方程式:____________________ 。
(6)已知在上述合成路线中粗硒在转化为二氧化硒时损失2%,搅拌槽中二氧化硒的利用率为95%,其他损耗忽略不计,试计算利用1t含硒79%的粗硒最终可生产______ t(精确到0.1t)含亚硒酸钠95%的产品。

(1)硒与硫是同主族的相邻元素,亚硒酸钠中硒的化合价为
(2)搅拌槽中加入氢氧化钠合成亚硒酸钠溶液并调整pH值为7~14,pH值调到7~ 14的原因是
(3)操作①的名称是
(4)操作②为
a.稀硫酸b.氢氧化钠稀溶液c.水d.乙醇
(5)现在常用以单质硒为原料,在氢氧化钠水溶液中通入高压氧气的方法来获得亚硒酸钠。写出制备亚硒酸钠的化学反应方程式:
(6)已知在上述合成路线中粗硒在转化为二氧化硒时损失2%,搅拌槽中二氧化硒的利用率为95%,其他损耗忽略不计,试计算利用1t含硒79%的粗硒最终可生产
您最近一年使用:0次
4 . 相对分子质量为92的某芳香烃X是一种重要的有机化工原料,研究部门以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去)。其中A是一氯代物,H是一种功能高分子,链节组成为C7H5NO。
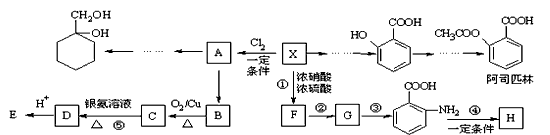
已知:
Ⅰ.
Ⅱ.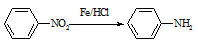 (苯胺、易被氧化)
(苯胺、易被氧化)
请根据所学知识与本题所给信息回答下列问题:
(1)X的分子式是__________ ;C的名称是___________ 。
(2)H的结构简式是_____________ 。
(3)反应②、④的类型是__________ 。
(4)反应⑤的化学方程式是____________ ;
(5)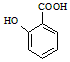 有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有
有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有_______ 种。
(6)请用合成反应流程图表示出由A和其他无机物(溶剂任选)合成 最合理的方案。
最合理的方案。
示例如下:
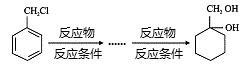
____________

已知:
Ⅰ.

Ⅱ.
 (苯胺、易被氧化)
(苯胺、易被氧化)请根据所学知识与本题所给信息回答下列问题:
(1)X的分子式是
(2)H的结构简式是
(3)反应②、④的类型是
(4)反应⑤的化学方程式是
(5)
 有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有
有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有(6)请用合成反应流程图表示出由A和其他无机物(溶剂任选)合成
 最合理的方案。
最合理的方案。示例如下:

您最近一年使用:0次
名校
解题方法
5 . 医用麻醉药苄佐卡因E和食品防腐剂J的合成路线如下:
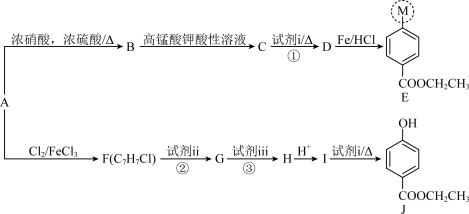
已知:I.M代表E分子结构中的一部分
II.
请回答下列问题:
(1)A属于芳香烃,分子式为C7H8 ,其名称是_______ ,A到B的反应类型是______________________ 。
(2)E中所含含氧官能团的名称是_______ ,M的结构简式是__________ 。
(3)C能与NaHCO3溶液反应,则反应①的化学方程式是_____________ 。
(4)反应②、③中试剂ii和试剂iii依次是_______ 。(填序号)
a.高锰酸钾酸性溶液、氢氧化钠溶液
b.氢氧化钠溶液、高锰酸钾酸性溶液
(5)H的结构简式是_______ 。
(6)J有多种同分异构体,其中符合下列条件的同分异构体有______ 种,写出其中任一种同分异构体的结构简式:____ 。
a.为苯的二元取代物
b.遇到FeCl3溶液显紫色,能发生水解反应且能发生银镜反应
(7)以A为起始原料,选用必要的无机试剂合成涂改液的主要成分亚甲基环己烷(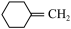 ),写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭 头上注明试剂和反应条件):
),写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭 头上注明试剂和反应条件):_____________

已知:I.M代表E分子结构中的一部分
II.

请回答下列问题:
(1)A属于芳香烃,分子式为C7H8 ,其名称是
(2)E中所含含氧官能团的名称是
(3)C能与NaHCO3溶液反应,则反应①的化学方程式是
(4)反应②、③中试剂ii和试剂iii依次是
a.高锰酸钾酸性溶液、氢氧化钠溶液
b.氢氧化钠溶液、高锰酸钾酸性溶液
(5)H的结构简式是
(6)J有多种同分异构体,其中符合下列条件的同分异构体有
a.为苯的二元取代物
b.遇到FeCl3溶液显紫色,能发生水解反应且能发生银镜反应
(7)以A为起始原料,选用必要的无机试剂合成涂改液的主要成分亚甲基环己烷(
 ),写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭 头上注明试剂和反应条件):
),写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭 头上注明试剂和反应条件):
您最近一年使用:0次
名校
6 . A是五元环状化合物,相对分子质量为98,其中氧元素的质量分数为49%,其核磁共振氢谱只有一个峰;反应⑤是加成反应;G是一种合成橡胶和树脂的重要原料。有关物质的转化关系如图所示:

已知:(其中R是烃基)
①
 2RCOOH ②RCOOH
2RCOOH ②RCOOH RCH2OH
RCH2OH
请回答以下问题:
(1)G的名称为____________________ 。
(2)B中官能团的名称是______________ ,④的反应类型是_______________ 。
(3)E可在一定条件下生成高分子化合物,写出该高分子化合物可能的结构简式:_______________ 。
(4)F属于酯类,反应⑥的化学方程式为_____________________________ 。
(5)有机物Y与E互为同分异构体,且具有相同的官能团种类和数目,写出所有符合条件的Y的结构简式___________________ 。
(6)写出由G合成2-氯-1,3-丁二烯的合成路线(无机试剂任选):__________________________ 。

已知:(其中R是烃基)
①

 2RCOOH ②RCOOH
2RCOOH ②RCOOH RCH2OH
RCH2OH请回答以下问题:
(1)G的名称为
(2)B中官能团的名称是
(3)E可在一定条件下生成高分子化合物,写出该高分子化合物可能的结构简式:
(4)F属于酯类,反应⑥的化学方程式为
(5)有机物Y与E互为同分异构体,且具有相同的官能团种类和数目,写出所有符合条件的Y的结构简式
(6)写出由G合成2-氯-1,3-丁二烯的合成路线(无机试剂任选):
您最近一年使用:0次
7 . 赫克反应(Heckreaction)在有机化学反应中有较广泛的应用,通式可表示为:R-X+R'-CH=CH2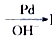 R'-CH=CH-R+HX(R-X中的R通常是不饱和烃基或苯环,R'-CH=CH2通常是丙烯酸酯或丙烯腈等)
R'-CH=CH-R+HX(R-X中的R通常是不饱和烃基或苯环,R'-CH=CH2通常是丙烯酸酯或丙烯腈等)
已知A是最简单,最基本的芳香烃,现A、B、C、D等有机化合物有如下转化关系(部分反应物、生成物、反应条件已省略):

请回答下列问题。
(1)反应I的反应类型是______ ,化合物C的名称是______ 。
(2)写出B催化加氢反应的化学方程式__________ 。
(3)写出D的结构简式(不考虑立体异构):________________ ,生成D的反应中需要加入K2CO3而不是加入KOH,其目的是_______________ 。
(4)写出符合限定条件(既具有酸性又能使溴的四氯化碳溶液褪色)的C的同分异构体的结构简式(不考虑立体异构):_______________ 。
(5)苯甲酸苯甲酯既可以用作香料、食品添加剂及一些香料的溶剂,也可以用作塑料、涂料的增塑剂,还可以用来治疗疥疮。写出由A的最简单的同系物制备苯甲酸苯甲酯(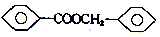 )的合成路线,所需的其他试剂均为简单的无机物。(合成路线常用的表示方式为
)的合成路线,所需的其他试剂均为简单的无机物。(合成路线常用的表示方式为 )
)__________________________
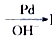 R'-CH=CH-R+HX(R-X中的R通常是不饱和烃基或苯环,R'-CH=CH2通常是丙烯酸酯或丙烯腈等)
R'-CH=CH-R+HX(R-X中的R通常是不饱和烃基或苯环,R'-CH=CH2通常是丙烯酸酯或丙烯腈等)已知A是最简单,最基本的芳香烃,现A、B、C、D等有机化合物有如下转化关系(部分反应物、生成物、反应条件已省略):

请回答下列问题。
(1)反应I的反应类型是
(2)写出B催化加氢反应的化学方程式
(3)写出D的结构简式(不考虑立体异构):
(4)写出符合限定条件(既具有酸性又能使溴的四氯化碳溶液褪色)的C的同分异构体的结构简式(不考虑立体异构):
(5)苯甲酸苯甲酯既可以用作香料、食品添加剂及一些香料的溶剂,也可以用作塑料、涂料的增塑剂,还可以用来治疗疥疮。写出由A的最简单的同系物制备苯甲酸苯甲酯(
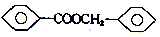 )的合成路线,所需的其他试剂均为简单的无机物。(合成路线常用的表示方式为
)的合成路线,所需的其他试剂均为简单的无机物。(合成路线常用的表示方式为 )
)
您最近一年使用:0次
8 . 相对分子质量为92的某芳香烃X是一种重要的有机化工原料,研究部门以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去)。其中A是一氯代物,H是一种功能高分子。
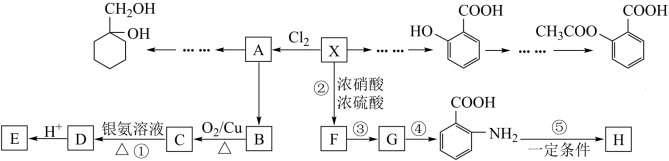
已知:
I、
II、 (苯胺,易被氧化)
(苯胺,易被氧化)
请根据所学知识与本题所给信息回答下列问题:
(1)反应③ 的类型是_______ ;
(2)写出反应① 的化学方程式_______ ;
(3)写出反应② 的化学方程式_______ ;
(4) 有多种同分异构体,写出符合下列条件的所有结构简式:
有多种同分异构体,写出符合下列条件的所有结构简式:_______ ;
(i)能发生银镜反应
(ii)遇FeC13溶液呈紫色
(iii)属于芳香族化合物,且苯环上一氯代物只有2 种
(5)参照上述合成路线图,设计由A 到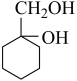 的合成路线(无机试剂任选)
的合成路线(无机试剂任选) _______ 。

已知:
I、

II、
 (苯胺,易被氧化)
(苯胺,易被氧化)请根据所学知识与本题所给信息回答下列问题:
(1)反应③ 的类型是
(2)写出反应① 的化学方程式
(3)写出反应② 的化学方程式
(4)
 有多种同分异构体,写出符合下列条件的所有结构简式:
有多种同分异构体,写出符合下列条件的所有结构简式:(i)能发生银镜反应
(ii)遇FeC13溶液呈紫色
(iii)属于芳香族化合物,且苯环上一氯代物只有2 种
(5)参照上述合成路线图,设计由A 到
 的合成路线(无机试剂任选)
的合成路线(无机试剂任选)
您最近一年使用:0次
14-15高三上·广西桂林·阶段练习
解题方法
9 . 已知 +HCN→
+HCN→
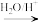
 ,CO和H2按物质的量之比1∶2可以制得G,有机玻璃可按如图路线合成:
,CO和H2按物质的量之比1∶2可以制得G,有机玻璃可按如图路线合成:

(1)A、E的结构简式分别为:_______ 、_______ ;
(2)B→C、E→F的反应类型分别为:_______ 、_______ ;
(3)写出下列转化的化学方程式:C→D_______ ;G+F→H_______ ;
(4)要检验B中的Br元素,可用的操作和现象为_______ 。
(5)写出符合下列要求的H的同分异构体①有一个支链②能使溴的四氯化碳溶液褪色③跟NaHCO3反应生成CO2_______ ,_______ 。(只要求写出2个)
 +HCN→
+HCN→
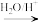
 ,CO和H2按物质的量之比1∶2可以制得G,有机玻璃可按如图路线合成:
,CO和H2按物质的量之比1∶2可以制得G,有机玻璃可按如图路线合成:
(1)A、E的结构简式分别为:
(2)B→C、E→F的反应类型分别为:
(3)写出下列转化的化学方程式:C→D
(4)要检验B中的Br元素,可用的操作和现象为
(5)写出符合下列要求的H的同分异构体①有一个支链②能使溴的四氯化碳溶液褪色③跟NaHCO3反应生成CO2
您最近一年使用:0次
名校
解题方法
10 . 研究碳、氮、硫等元素化合物的性质或转化对建设生态文明,美丽中国具有重要意义。
(1)海水中无机碳的存在形式及分布如图所示:
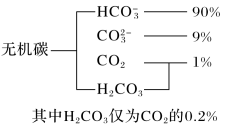
用离子方程式表示海水呈弱碱性的原因__ 。已知春季海水pH=8.1,预测夏季海水碱性将会__ (填“增强”或“减弱”)
(2)工业上以CO和H2为原料合成甲醇的反应:CO(g)+2H2(g)⇌CH3OH(g) ΔH<0,在容积为1L的恒容容器中,分别在T1、T2、T3三种温度下合成甲醇。如图是上述三种温度下不同H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。下列说法正确的是__ (填字母)。
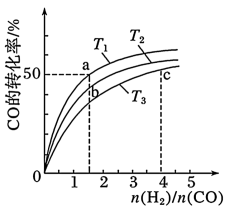
A.a、b、c三点H2转化率:c>a>b
B.上述三种温度之间关系为T1>T2>T3
C.a点状态下再通入0.5molCO和0.5molCH3OH,平衡不移动
D.c点状态下再通入1molCO和4molH2,新平衡中H2的体积分数增大
(3)NO加速臭氧层被破坏,其反应过程如图所示:
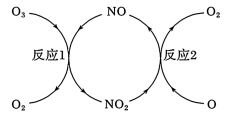
①NO的作用是__ 。
②已知:
O3(g)+O(g)=2O2(g) ΔH=-143kJ·mol-1
反应1:O3(g)+NO(g)=NO2(g)+O2(g) ΔH1=-200.2kJ·mol-1。
反应2:热化学方程式为__ 。
(4)若将CO和NO按不同比例投入一密闭容器中发生反应:2CO(g)+2NO(g) N2(g)+2CO2(g) ΔH=-759.8kJ·mol-1,反应达到平衡时,N2的体积分数随
N2(g)+2CO2(g) ΔH=-759.8kJ·mol-1,反应达到平衡时,N2的体积分数随 的变化曲线如图。
的变化曲线如图。
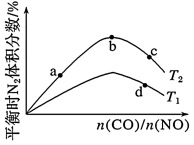
①b点时,平衡体系中C、N原子个数之比接近___ 。
②a、b、c三点CO的转化率从大到小的顺序为__ ;a、c、d三点的平衡常数从大到小的顺序为___ 。
③若 =0.8,反应达平衡时,N2的体积分数为20%,则CO的转化率为
=0.8,反应达平衡时,N2的体积分数为20%,则CO的转化率为___ 。
(1)海水中无机碳的存在形式及分布如图所示:

用离子方程式表示海水呈弱碱性的原因
(2)工业上以CO和H2为原料合成甲醇的反应:CO(g)+2H2(g)⇌CH3OH(g) ΔH<0,在容积为1L的恒容容器中,分别在T1、T2、T3三种温度下合成甲醇。如图是上述三种温度下不同H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。下列说法正确的是

A.a、b、c三点H2转化率:c>a>b
B.上述三种温度之间关系为T1>T2>T3
C.a点状态下再通入0.5molCO和0.5molCH3OH,平衡不移动
D.c点状态下再通入1molCO和4molH2,新平衡中H2的体积分数增大
(3)NO加速臭氧层被破坏,其反应过程如图所示:

①NO的作用是
②已知:
O3(g)+O(g)=2O2(g) ΔH=-143kJ·mol-1
反应1:O3(g)+NO(g)=NO2(g)+O2(g) ΔH1=-200.2kJ·mol-1。
反应2:热化学方程式为
(4)若将CO和NO按不同比例投入一密闭容器中发生反应:2CO(g)+2NO(g)
 N2(g)+2CO2(g) ΔH=-759.8kJ·mol-1,反应达到平衡时,N2的体积分数随
N2(g)+2CO2(g) ΔH=-759.8kJ·mol-1,反应达到平衡时,N2的体积分数随 的变化曲线如图。
的变化曲线如图。
①b点时,平衡体系中C、N原子个数之比接近
②a、b、c三点CO的转化率从大到小的顺序为
③若
 =0.8,反应达平衡时,N2的体积分数为20%,则CO的转化率为
=0.8,反应达平衡时,N2的体积分数为20%,则CO的转化率为
您最近一年使用:0次



