1 . 通过对模型、图形、图表的观察,获取有关信息是化学学习的一种重要能力。请按要求回答下列问题:
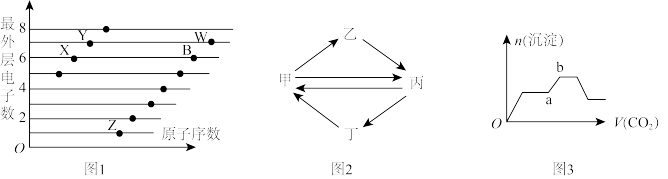
(1)图1是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图。
①Y元素在元素周期表中的位置为_______________ 。
②气态氢化物的稳定性:X_____ (填“>”“<”)Y。
③这五种元素形成的简单离子中,离子半径最大的是_______ (填离子符号)。
④Z的氢化物ZH可以和水发生氧化还原反应,其反应方程式为_________________ 。
(2)图2是甲、乙、丙、丁四种物质的转化关系,其中每一步都能一步实现的是__________
(3)图3表示将足量的CO2不断通入NaOH、Ba(OH)2、NaAlO2的混合溶液中,生成沉淀与通入CO2的量的关系,则ab段发生反应的离子方程式为_______________________________

(1)图1是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图。
①Y元素在元素周期表中的位置为
②气态氢化物的稳定性:X
③这五种元素形成的简单离子中,离子半径最大的是
④Z的氢化物ZH可以和水发生氧化还原反应,其反应方程式为
(2)图2是甲、乙、丙、丁四种物质的转化关系,其中每一步都能一步实现的是
| 甲 | 乙 | 丙 | 丁 | |
| A | FeCl3 | FeCl2 | Fe2O3 | Fe(OH)3 |
| B | Cu | CuO | CuSO4 | CuCl2 |
| C | NO | HNO3 | NO2 | NH3 |
| D | Si | Na2SiO3 | SiO2 | SiF4 |
您最近一年使用:0次
2 . X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。X、Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素。请回答下列问题:
(1)Y在元素周期表中的位置为________________。
(2)五种元素原子半径由大到小的顺序是(写元素符号)_________________________。
(3)QX的电子式为___________;QX与水反应放出气体的化学方程式为____________。
(4)X、Z两元素能形成两种化合物的电子式分别为 和 。
(5)由以上某些元素组成的化合物A、B、C、D有如下转化关系:

其中C是溶于水显酸性的气体;D是淡黄色固体。
①写出C的结构式__________________;
②如果A、B均由三种元素组成,B为两性不溶物,由A转化为B的离子方程式_______。
(1)Y在元素周期表中的位置为________________。
(2)五种元素原子半径由大到小的顺序是(写元素符号)_________________________。
(3)QX的电子式为___________;QX与水反应放出气体的化学方程式为____________。
(4)X、Z两元素能形成两种化合物的电子式分别为 和 。
(5)由以上某些元素组成的化合物A、B、C、D有如下转化关系:

其中C是溶于水显酸性的气体;D是淡黄色固体。
①写出C的结构式__________________;
②如果A、B均由三种元素组成,B为两性不溶物,由A转化为B的离子方程式_______。
您最近一年使用:0次
名校
解题方法
3 . 某废催化剂主要成分为镍、钒、铁、铝及其硫化物,为实现金属资源的再利用,对其处理的流程如下图所示。

按要求回答下列问题:
(1)Ni在元素周期表中的位置为___________ 。聚合氯化铁的化学式为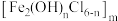 ,其中铁元素的化合价为
,其中铁元素的化合价为___________ 。
(2)“滤液”的处理
①“滤液”中,阴离子主要有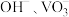 和
和___________ 。
②从“滤液”中获取钒单质的流程如下图所示,其中“离子交换”和“洗脱”可简单表示为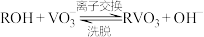 (其中ROH为离子交换树脂)。
(其中ROH为离子交换树脂)。
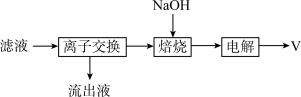
向流出液中通入过量 可得到沉淀,该沉淀的化学式为
可得到沉淀,该沉淀的化学式为___________ 。“电解”时阴极的电极反应为___________ ,阴极可能产生的气体副产物为___________ 。
(3)聚合氯化铁的制备
①“转化”过程中,实际加入 的量远大于按方程式计算所需的量,其原因为
的量远大于按方程式计算所需的量,其原因为___________ 。
②“转化”过程中,溶液的 必须控制在一定的范围内。
必须控制在一定的范围内。 偏小时
偏小时___________ , 偏大时则形成
偏大时则形成 沉淀。
沉淀。
(4)氯化镍晶体 (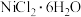 )纯度的测定(杂质不含氯元素)
)纯度的测定(杂质不含氯元素)
ⅰ.用适量蒸馏水溶解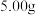 样品,再稀释至
样品,再稀释至 。
。
ⅱ.取 待测液,加入指示剂,用
待测液,加入指示剂,用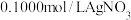 标准液滴定,多次平行实验情况如下表和下图所示。
标准液滴定,多次平行实验情况如下表和下图所示。

ⅲ.另取 蒸馏水,进行空白对照实验,消耗标准液的平均用量为
蒸馏水,进行空白对照实验,消耗标准液的平均用量为 。
。
① 标准液滴定溶液中的
标准液滴定溶液中的 ,采用
,采用 为指示剂,利用
为指示剂,利用 与
与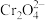 生成砖红色沉淀,指示达到终点。当达到滴定终点时,溶液中的
生成砖红色沉淀,指示达到终点。当达到滴定终点时,溶液中的 恰好沉淀完全(浓度为
恰好沉淀完全(浓度为 ),此时溶液中
),此时溶液中
___________  。[已知:
。[已知: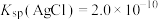 ,
, 。]
。]
②氯化镍晶体的纯度为___________ %。

按要求回答下列问题:
(1)Ni在元素周期表中的位置为
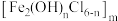 ,其中铁元素的化合价为
,其中铁元素的化合价为(2)“滤液”的处理
①“滤液”中,阴离子主要有
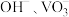 和
和②从“滤液”中获取钒单质的流程如下图所示,其中“离子交换”和“洗脱”可简单表示为
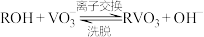 (其中ROH为离子交换树脂)。
(其中ROH为离子交换树脂)。
向流出液中通入过量
 可得到沉淀,该沉淀的化学式为
可得到沉淀,该沉淀的化学式为(3)聚合氯化铁的制备
①“转化”过程中,实际加入
 的量远大于按方程式计算所需的量,其原因为
的量远大于按方程式计算所需的量,其原因为②“转化”过程中,溶液的
 必须控制在一定的范围内。
必须控制在一定的范围内。 偏小时
偏小时 偏大时则形成
偏大时则形成 沉淀。
沉淀。(4)氯化镍晶体 (
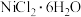 )纯度的测定(杂质不含氯元素)
)纯度的测定(杂质不含氯元素)ⅰ.用适量蒸馏水溶解
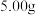 样品,再稀释至
样品,再稀释至 。
。ⅱ.取
 待测液,加入指示剂,用
待测液,加入指示剂,用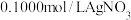 标准液滴定,多次平行实验情况如下表和下图所示。
标准液滴定,多次平行实验情况如下表和下图所示。
| 滴定次数 | 标准液体积 | |
滴定前的刻度 | 滴定终点的刻度 | |
| 第1次 | 2.35 |  |
| 第2次 | 0.70 | 20.85 |
| 第3次 | 0.75 | 22.90 |
 蒸馏水,进行空白对照实验,消耗标准液的平均用量为
蒸馏水,进行空白对照实验,消耗标准液的平均用量为 。
。①
 标准液滴定溶液中的
标准液滴定溶液中的 ,采用
,采用 为指示剂,利用
为指示剂,利用 与
与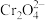 生成砖红色沉淀,指示达到终点。当达到滴定终点时,溶液中的
生成砖红色沉淀,指示达到终点。当达到滴定终点时,溶液中的 恰好沉淀完全(浓度为
恰好沉淀完全(浓度为 ),此时溶液中
),此时溶液中
 。[已知:
。[已知: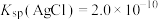 ,
, 。]
。]②氯化镍晶体的纯度为
您最近一年使用:0次
名校
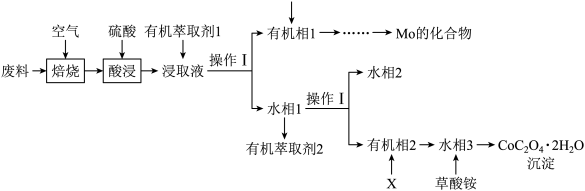
4 . 工业上用废料制备 的工艺流程如图所示:
的工艺流程如图所示:
已知:①废料中主要含有 、
、 、
、 ,其他杂质不参与反应;
,其他杂质不参与反应;
②焙烧时,Mo元素转化为 ;
;
③浸取液中金属离子以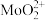 、
、 、
、 形式存在;
形式存在;
④25℃时, 的
的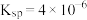 。
。
回答下列问题:
(1)Co元素在元素周期表中的位置是___________ 。已知Mo的核电荷数为42,Mo(IV)离子的价层电子排布式是___________ 。
(2)焙烧时,发生氧化反应的元素有___________ (填元素符号)。标准状况下33.6L 参与焙烧,完全反应时转移的电子的物质的量为
参与焙烧,完全反应时转移的电子的物质的量为___________ 。
(3)酸浸时,所用硫酸过量,则Mo元素发生转化的离子方程式为___________ 。
(4)在实验室进行操作I,所用到的玻璃仪器有___________ 。
(5)萃取 “的原理是“
“的原理是“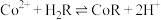 ”,水相2中存在的主要阳离子有
”,水相2中存在的主要阳离子有___________ ,加入试剂X是___________ (填名称),假定水相3中 的浓度为c mo/L,且沉钴过程中加入沉淀剂固体后不考虑溶液体积变化,并忽略盐类的水解,当
的浓度为c mo/L,且沉钴过程中加入沉淀剂固体后不考虑溶液体积变化,并忽略盐类的水解,当 沉淀完全时,溶液中
沉淀完全时,溶液中 最小值的计算式为
最小值的计算式为___________ mol/L(用含c的计算式表示)。
(6)在空气中加热10.98g ,受热过程中不同温度范围内分别得到一种固体物质,其质量如下表。经测定,加热到210~320℃过程中的生成物只有
,受热过程中不同温度范围内分别得到一种固体物质,其质量如下表。经测定,加热到210~320℃过程中的生成物只有 和钴的氧化物,此过程发生反应的化学方程式为
和钴的氧化物,此过程发生反应的化学方程式为___________ 。
 的工艺流程如图所示:
的工艺流程如图所示:
已知:①废料中主要含有
 、
、 、
、 ,其他杂质不参与反应;
,其他杂质不参与反应;②焙烧时,Mo元素转化为
 ;
;③浸取液中金属离子以
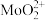 、
、 、
、 形式存在;
形式存在;④25℃时,
 的
的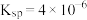 。
。回答下列问题:
(1)Co元素在元素周期表中的位置是
(2)焙烧时,发生氧化反应的元素有
 参与焙烧,完全反应时转移的电子的物质的量为
参与焙烧,完全反应时转移的电子的物质的量为(3)酸浸时,所用硫酸过量,则Mo元素发生转化的离子方程式为
(4)在实验室进行操作I,所用到的玻璃仪器有
(5)萃取
 “的原理是“
“的原理是“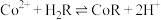 ”,水相2中存在的主要阳离子有
”,水相2中存在的主要阳离子有 的浓度为c mo/L,且沉钴过程中加入沉淀剂固体后不考虑溶液体积变化,并忽略盐类的水解,当
的浓度为c mo/L,且沉钴过程中加入沉淀剂固体后不考虑溶液体积变化,并忽略盐类的水解,当 沉淀完全时,溶液中
沉淀完全时,溶液中 最小值的计算式为
最小值的计算式为(6)在空气中加热10.98g
 ,受热过程中不同温度范围内分别得到一种固体物质,其质量如下表。经测定,加热到210~320℃过程中的生成物只有
,受热过程中不同温度范围内分别得到一种固体物质,其质量如下表。经测定,加热到210~320℃过程中的生成物只有 和钴的氧化物,此过程发生反应的化学方程式为
和钴的氧化物,此过程发生反应的化学方程式为| 温度范围/℃ | 固体质量/g |
| 150~210 | 8.82 |
| 210~320 | 4.82 |
| 890~920 | 4.50 |
您最近一年使用:0次
2022-09-25更新
|
403次组卷
|
2卷引用:重庆市巴蜀中学校2022-2023学年高三上学期适应性月考卷(二)化学试题
名校
解题方法
5 . 钼酸锂(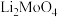 )主要用于电极材料、金属陶瓷、电阻器材料等领域,通过如图流程,以钼矿(主要成分是
)主要用于电极材料、金属陶瓷、电阻器材料等领域,通过如图流程,以钼矿(主要成分是 ,还有杂质CuO、FeO)为原料可制备钼酸锂。
,还有杂质CuO、FeO)为原料可制备钼酸锂。

回答下列问题:
(1)已知基态Mo的价层电子排布式为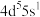 ,则Mo位于元素周期表第
,则Mo位于元素周期表第_______ 周期第_______ 族。
(2)写出焙烧过程中发生的主要反应的化学方程式_______ 。
(3)“碱浸”前需对粗 进行粉碎,这一操作的目的是
进行粉碎,这一操作的目的是_______ ,该操作过程中测定浸取率与温度的关系数据如表:
从浸取率和经济角度考虑,选取的合适温度是_______ ℃。
(4)“转化”操作中加入双氧水的目的是将其中少量的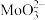 氧化为
氧化为 ,该反应的离子方程式是
,该反应的离子方程式是_______ 。
(5)“合成”的温度是1000~1200℃,则气体Y中含有 、
、_______ (填化学式)。
(6)电解硝酸工业的尾气NO可制备 ,其工作原理如图所示:
,其工作原理如图所示:

①阴极的电极反应式为_______ 。
②将电解生成的 全部转化为
全部转化为 ,则通入的
,则通入的 与实际参加反应的NO的物质的量之比至少为
与实际参加反应的NO的物质的量之比至少为_______ 。
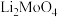 )主要用于电极材料、金属陶瓷、电阻器材料等领域,通过如图流程,以钼矿(主要成分是
)主要用于电极材料、金属陶瓷、电阻器材料等领域,通过如图流程,以钼矿(主要成分是 ,还有杂质CuO、FeO)为原料可制备钼酸锂。
,还有杂质CuO、FeO)为原料可制备钼酸锂。
回答下列问题:
(1)已知基态Mo的价层电子排布式为
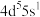 ,则Mo位于元素周期表第
,则Mo位于元素周期表第(2)写出焙烧过程中发生的主要反应的化学方程式
(3)“碱浸”前需对粗
 进行粉碎,这一操作的目的是
进行粉碎,这一操作的目的是| 温度/℃ | 40 | 50 | 60 | 70 | 80 | 90 |
| 浸取率/% | 85.5 | 88.5 | 95.3 | 95.7 | 96.0 | 89.5 |
从浸取率和经济角度考虑,选取的合适温度是
(4)“转化”操作中加入双氧水的目的是将其中少量的
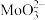 氧化为
氧化为 ,该反应的离子方程式是
,该反应的离子方程式是(5)“合成”的温度是1000~1200℃,则气体Y中含有
 、
、(6)电解硝酸工业的尾气NO可制备
 ,其工作原理如图所示:
,其工作原理如图所示:
①阴极的电极反应式为
②将电解生成的
 全部转化为
全部转化为 ,则通入的
,则通入的 与实际参加反应的NO的物质的量之比至少为
与实际参加反应的NO的物质的量之比至少为
您最近一年使用:0次
6 . 短周期元素W、X、Y和Z在元素周期表中的相对位置如表所示,这四种元素原子的最外层电子数之和为21。下列关系正确的是
| W | X | |||
| Y | Z |
| A.氢化物沸点:W>X |
| B.简单离子的半径:Y<X |
| C.化合物熔点:Y2X3<YZ3 |
| D.氧化物对应水化物的酸性:Y>W |
您最近一年使用:0次
2021-01-22更新
|
430次组卷
|
4卷引用:重庆市垫江第五中学2021届高三下学期4月月考化学试题
重庆市垫江第五中学2021届高三下学期4月月考化学试题北京市丰台区2021届高三上学期期末考试化学试题天津市河东区2021届高三一模考试化学试题(已下线)第16讲 元素周期律和元素周期表(精讲)-2022年一轮复习讲练测
名校
7 . 阿司匹林( )是一种用途很广的消炎镇痛药物。可以通过以下方法合成:
)是一种用途很广的消炎镇痛药物。可以通过以下方法合成:

已知:
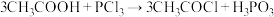 。
。
请回答下列问题:
(1)阿司匹林中的含氧官能团有___________ (写名称),反应①的反应类型为___________ 。
(2)通过水杨酸还可制得香料E和高分子化合物G,转化关系如图。

①请写出A→E的化学方程式:___________ 。
②已知G是一种聚酯,请写出其结构简式:___________ 。
(3)水杨酸所有属于芳香酯的同分异构体中,苯环上有两个对位取代基的结构简式为_______ 。
(4)结合题中信息,以苯酚、异丁烯为原料(其他无机原料自选)合成聚合物 的流程路线如下:
的流程路线如下:

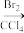 ………
………



请完善上述合成流程路线中的省略部分___________ 。
 )是一种用途很广的消炎镇痛药物。可以通过以下方法合成:
)是一种用途很广的消炎镇痛药物。可以通过以下方法合成:
已知:

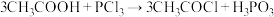 。
。请回答下列问题:
(1)阿司匹林中的含氧官能团有
(2)通过水杨酸还可制得香料E和高分子化合物G,转化关系如图。

①请写出A→E的化学方程式:
②已知G是一种聚酯,请写出其结构简式:
(3)水杨酸所有属于芳香酯的同分异构体中,苯环上有两个对位取代基的结构简式为
(4)结合题中信息,以苯酚、异丁烯为原料(其他无机原料自选)合成聚合物
 的流程路线如下:
的流程路线如下:
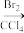 ………
………



请完善上述合成流程路线中的省略部分
您最近一年使用:0次
名校
解题方法
8 . 化合物G是一种药物中间体,其合成路线如图所示:
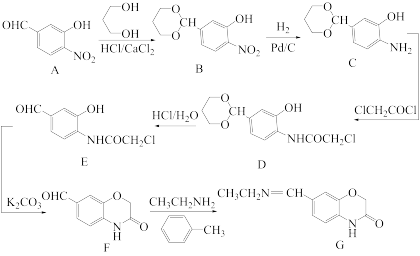
(1)A的分子式为___________ ,物质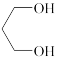 的化学名称为
的化学名称为___________ (系统命名法)。
(2)A→B的反应需经历A→X→B的过程,X的化学式为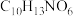 ,则推测X的结构简式为
,则推测X的结构简式为___________ 。
(3)B→C、C→D的反应类型分别为___________ 、___________ 。
(4)写出E→F反应的化学方程式:___________ 。
(5)C有多种同分异构体,写出满足以下要求的同分异构体的结构简式:___________ (只写一种)。
①能与 溶液发生显色反应;
溶液发生显色反应;
②核磁共振氢谱显示四组峰,且峰面积之比为6:3:2:2。
(6)参照题干中的合成路线及信息,以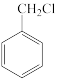 、
、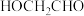 和苯酚为有机原料制备
和苯酚为有机原料制备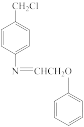 ,设计合成路线图
,设计合成路线图_______ (无机试剂任选,用箭头表示转化关系,箭头上注明试剂和反应条件)。

(1)A的分子式为
 的化学名称为
的化学名称为(2)A→B的反应需经历A→X→B的过程,X的化学式为
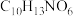 ,则推测X的结构简式为
,则推测X的结构简式为(3)B→C、C→D的反应类型分别为
(4)写出E→F反应的化学方程式:
(5)C有多种同分异构体,写出满足以下要求的同分异构体的结构简式:
①能与
 溶液发生显色反应;
溶液发生显色反应;②核磁共振氢谱显示四组峰,且峰面积之比为6:3:2:2。
(6)参照题干中的合成路线及信息,以
 、
、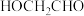 和苯酚为有机原料制备
和苯酚为有机原料制备 ,设计合成路线图
,设计合成路线图
您最近一年使用:0次
2022-09-25更新
|
359次组卷
|
3卷引用:重庆市巴蜀中学校2022-2023学年高三上学期适应性月考卷(二)化学试题
名校
解题方法
9 . (Te)与氧元素同族,在元素周期表中与硒(Se)相邻,位于硒(Se)的下方。含元素碲(Te)的几种物质存在如图所示转化关系。下列说法错误的是
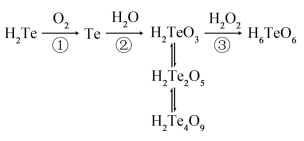

A.反应①利用了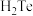 的还原性 的还原性 |
| B.碲(Te)位于元素周期表中第五周期第ⅥA族 |
C.反应③利用了 的氧化性 的氧化性 |
| D.H2Te2O5转化为H2Te4O9发生了氧化还原反应 |
您最近一年使用:0次
名校
解题方法
10 . 从钒铬锰矿渣(主要成分为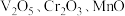 )中提铬的一种工艺流程如下:
)中提铬的一种工艺流程如下:
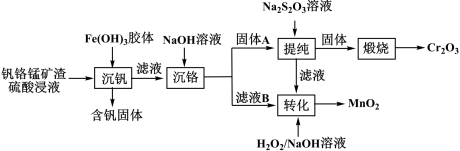
已知: 较大时,二价锰
较大时,二价锰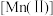 在空气中易被氧化。回答下列问题:
在空气中易被氧化。回答下列问题:
(1) 元素在周期表中的位置是
元素在周期表中的位置是___________ 。
(2)常温下,各种形态五价钒粒子总浓度的对数 与
与 关系如图1,已知钒铬锰矿渣硫酸浸液中
关系如图1,已知钒铬锰矿渣硫酸浸液中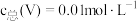 ,“沉钒”过程控制
,“沉钒”过程控制 ,则与胶体共沉降的五价钒粒子的存在形态为
,则与胶体共沉降的五价钒粒子的存在形态为___________ (填化学式)。
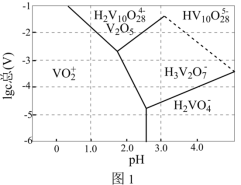
(3)某温度下,Cr(Ⅲ)、Mn(Ⅱ)的沉淀率与pH关系如图2,“沉铬”过程最佳pH为_____ (填标号);
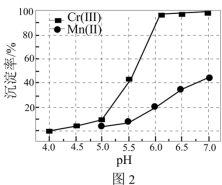
a.4.0 b.5.0 c.6.0
在该条件下滤液B中
______  [
[ 近似为
近似为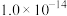 ,
, 的
的 近似为
近似为 ]。
]。
(4)“转化”过程中生成 的离子方程式为
的离子方程式为_________ 。
(5)“提纯”过程中 的作用为
的作用为________ 。
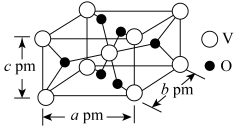
(6)一种含钒的氧化物晶胞结构如图所示,已知NA表示阿伏加德罗常数的值,则该晶体密度为_______ g•cm-3 (列出计算式即可)。
 )中提铬的一种工艺流程如下:
)中提铬的一种工艺流程如下:
已知:
 较大时,二价锰
较大时,二价锰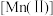 在空气中易被氧化。回答下列问题:
在空气中易被氧化。回答下列问题:(1)
 元素在周期表中的位置是
元素在周期表中的位置是(2)常温下,各种形态五价钒粒子总浓度的对数
 与
与 关系如图1,已知钒铬锰矿渣硫酸浸液中
关系如图1,已知钒铬锰矿渣硫酸浸液中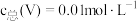 ,“沉钒”过程控制
,“沉钒”过程控制 ,则与胶体共沉降的五价钒粒子的存在形态为
,则与胶体共沉降的五价钒粒子的存在形态为
(3)某温度下,Cr(Ⅲ)、Mn(Ⅱ)的沉淀率与pH关系如图2,“沉铬”过程最佳pH为

a.4.0 b.5.0 c.6.0
在该条件下滤液B中

 [
[ 近似为
近似为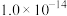 ,
, 的
的 近似为
近似为 ]。
]。(4)“转化”过程中生成
 的离子方程式为
的离子方程式为(5)“提纯”过程中
 的作用为
的作用为(6)一种含钒的氧化物晶胞结构如图所示,已知NA表示阿伏加德罗常数的值,则该晶体密度为

您最近一年使用:0次



