2022高三·全国·专题练习
1 . 化合物F是制备某种改善睡眠药物的中间体,其合成路线如下:

回答下列问题:
(1) 的反应类型是
的反应类型是___________ 。
(2)化合物B核磁共振氢谱的吸收峰有___________ 组。
(3)化合物C的结构简式为___________ 。
(4) 的过程中,被还原的官能团是
的过程中,被还原的官能团是___________ ,被氧化的官能团是___________ 。
(5)若只考虑氟的位置异构,则化合物F的同分异构体有___________ 种。
(6)已知 、
、 和
和 的产率分别为70%、82%和80%,则
的产率分别为70%、82%和80%,则 的总产率为
的总产率为___________ 。
(7) 配合物可催化
配合物可催化 转化中
转化中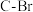 键断裂,也能催化反应①:
键断裂,也能催化反应①:
反应①: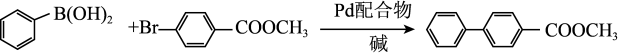
为探究有机小分子催化反应①的可能性,甲、乙两个研究小组分别合成了有机小分子 (结构如下图所示)。在合成
(结构如下图所示)。在合成 的过程中,甲组使用了
的过程中,甲组使用了 催化剂,并在纯化过程中用沉淀剂除
催化剂,并在纯化过程中用沉淀剂除 ;乙组未使用金属催化剂。研究结果显示,只有甲组得到的产品能催化反应①。
;乙组未使用金属催化剂。研究结果显示,只有甲组得到的产品能催化反应①。
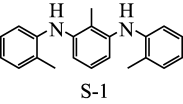
根据上述信息,甲、乙两组合成的 产品催化性能出现差异的原因是
产品催化性能出现差异的原因是___________ 。

回答下列问题:
(1)
 的反应类型是
的反应类型是(2)化合物B核磁共振氢谱的吸收峰有
(3)化合物C的结构简式为
(4)
 的过程中,被还原的官能团是
的过程中,被还原的官能团是(5)若只考虑氟的位置异构,则化合物F的同分异构体有
(6)已知
 、
、 和
和 的产率分别为70%、82%和80%,则
的产率分别为70%、82%和80%,则 的总产率为
的总产率为(7)
 配合物可催化
配合物可催化 转化中
转化中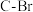 键断裂,也能催化反应①:
键断裂,也能催化反应①:反应①:
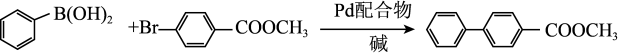
为探究有机小分子催化反应①的可能性,甲、乙两个研究小组分别合成了有机小分子
 (结构如下图所示)。在合成
(结构如下图所示)。在合成 的过程中,甲组使用了
的过程中,甲组使用了 催化剂,并在纯化过程中用沉淀剂除
催化剂,并在纯化过程中用沉淀剂除 ;乙组未使用金属催化剂。研究结果显示,只有甲组得到的产品能催化反应①。
;乙组未使用金属催化剂。研究结果显示,只有甲组得到的产品能催化反应①。
根据上述信息,甲、乙两组合成的
 产品催化性能出现差异的原因是
产品催化性能出现差异的原因是
您最近一年使用:0次
2022-07-12更新
|
9062次组卷
|
15卷引用:新疆乌鲁木齐市第四十中学2023-2024学年高三上学期11月月考化学试题
新疆乌鲁木齐市第四十中学2023-2024学年高三上学期11月月考化学试题(已下线)专题18 有机化学基础(综合题)-2022年高考真题模拟题分项汇编2022年湖北省高考真题化学试题(已下线)2022年湖北省高考真题变式题16-19(已下线)考点45 有机化合物的合成-备战2023年高考化学一轮复习考点帮(全国通用)湖北省武汉市第一中学2022-2023学年高三上学期9月开学考试化学试题陕西师范大学附属中学、渭北中学等2022-2023学年高三上学期期初检测化学联考试题陕西师范大学附属中学、渭北中学等2023届高三上学期期初检测联考化学试题(已下线)第35讲 生物大分子与合成高分子(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)热点情景汇编-专题十一 有机推断中的新发展(已下线)第一部分 二轮专题突破 大题突破5 有机综合推断(选考)(已下线)专题21 有机推断题(已下线)专题21 有机推断题(已下线)专题16 有机合成与推断-2023年高考化学真题题源解密(新高考专用)(已下线)考点39 有机推断(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
名校
2 . 具有抗菌作用的白头翁素衍生物H的合成路线如下图所示:

已知:
ⅰ. RCH2Br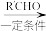

ⅱ.

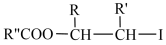
ⅲ. 2

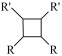 (以上R、R’、R”代表氢、或烃基等)
(以上R、R’、R”代表氢、或烃基等)
(1)A属于芳香烃,名称是________ ,由B生成C的反应类型是________ 。
(2)试剂a是________ ,HCHO的电子式是________ 。
(3)E的结构简式是________ 。
(4)由F生成G的化学方程式是_______ 。
(5)二取代芳香化合物W是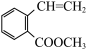 同分异构体,能使溴的四氯化碳溶液反应,能发生银镜反应,能发生水解反应,W共有
同分异构体,能使溴的四氯化碳溶液反应,能发生银镜反应,能发生水解反应,W共有______ 种(不含立体结构)。其中核磁共振氢谱为五组峰的结构简式为________ 。
(6)以乙醇为起始原料,结合已知信息选用必要的无机试剂合成 ,写出合成路线(用简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
,写出合成路线(用简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)___________ 。

已知:
ⅰ. RCH2Br
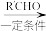

ⅱ.



ⅲ. 2


 (以上R、R’、R”代表氢、或烃基等)
(以上R、R’、R”代表氢、或烃基等)(1)A属于芳香烃,名称是
(2)试剂a是
(3)E的结构简式是
(4)由F生成G的化学方程式是
(5)二取代芳香化合物W是
 同分异构体,能使溴的四氯化碳溶液反应,能发生银镜反应,能发生水解反应,W共有
同分异构体,能使溴的四氯化碳溶液反应,能发生银镜反应,能发生水解反应,W共有(6)以乙醇为起始原料,结合已知信息选用必要的无机试剂合成
 ,写出合成路线(用简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
,写出合成路线(用简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
您最近一年使用:0次
名校
解题方法
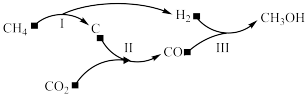
3 . 以天然气为原料经由合成气(CO、H2)制化学品是目前天然气转化利用的主导技术路线。制备 的反应转化关系如图所示。设NA为阿伏加德罗常数的值,下列说法正确的是
的反应转化关系如图所示。设NA为阿伏加德罗常数的值,下列说法正确的是
 的反应转化关系如图所示。设NA为阿伏加德罗常数的值,下列说法正确的是
的反应转化关系如图所示。设NA为阿伏加德罗常数的值,下列说法正确的是
A.用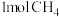 理论上能生产的 理论上能生产的 中含有极性键的数目为4 NA 中含有极性键的数目为4 NA |
B.等物质的量的 和 和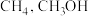 的质子数比 的质子数比 多8 NA 多8 NA |
C.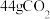 气体和 气体和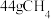 与 与 的混合气体,所含C原子数均为NA 的混合气体,所含C原子数均为NA |
D.用 制备合成气的反应中,若生成 制备合成气的反应中,若生成 ,反应转移电子数为3 NA ,反应转移电子数为3 NA |
您最近一年使用:0次
2021-11-30更新
|
542次组卷
|
3卷引用:新疆疏附县第一中学2021-2022学年高三上学期第二次月考化学试题
解题方法
4 . 2023年3月,我国科学家发现了世界首例具有本征相干性的光阴极量子材料一钛酸锶(SrTiO3),其性能远超传统的光阴极材料。一种“溶胶-沉淀”一步法合成钛酸锶纳米粉体的工艺流程如图所示。
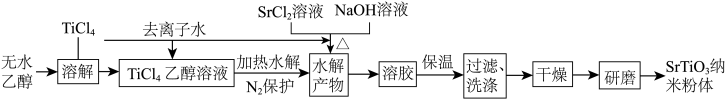
已知:i.TiCl4易溶于无水乙醇;
ii.Ti4+加热水解生成TiO2•xH2O;
iii.SrSO4在1580℃以上分解。
回答下列问题:
(1)钛元素位于元素周期表第四周期_______ 族。SrTiO3中Sr的化合价为_______ 。
(2)由水解产物生成SrTiO3溶胶的化学方程式为_______ 。
(3)对SrTiO3溶胶进行保温的目的是_______ 。
(4)检验SrTiO3沉淀是否洗涤干净的操作为_______ 。
(5)NaOH溶液的浓度、钛液浓度、反应时间对w(TiO2)、产物纯度的影响如表所示。
合成高纯SrTiO3纳米粉体的最佳工艺条件为_______ 。
(6)钛酸锶中钛锶比的测定。
①测定TiO2的含量:称取mg样品,经一系列处理除去Sr后,配制成250mL溶液。移取25.00mL溶液于锥形瓶中,准确加入V1mLc1mol•L-1EDTA标准溶液(过量),充分反应后,加入指示剂,用c2mol•L-1ZnSO4溶液滴定,滴定至终点时消耗V2mLZnSO4溶液。则钛酸锶中TiO2的质量分数为_______ (列出计算式即可,已知滴定计量关系:EDTA-Ti4+,EDTA~Zn2+)。
②测定SrO的含量:称取mg样品,用硫酸铵和浓硫酸处理,再用乙醇-水稀释成100mL溶液,用氨水调节溶液pH=4,完全沉淀后过滤得到SrSO4沉淀,于850℃时灼烧至恒重,质量为m1g。则钛酸锶中钛锶比为_______ [钛锶比= =
=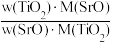 ]。
]。

已知:i.TiCl4易溶于无水乙醇;
ii.Ti4+加热水解生成TiO2•xH2O;
iii.SrSO4在1580℃以上分解。
回答下列问题:
(1)钛元素位于元素周期表第四周期
(2)由水解产物生成SrTiO3溶胶的化学方程式为
(3)对SrTiO3溶胶进行保温的目的是
(4)检验SrTiO3沉淀是否洗涤干净的操作为
(5)NaOH溶液的浓度、钛液浓度、反应时间对w(TiO2)、产物纯度的影响如表所示。
| 反应条件 | c(NaOH)/(mol•L-1) | 钛液浓度/(mol•L-1) | 反应时间/h | ||||||
| 3.30 | 5.30 | 7.30 | 1.60 | 2.20 | 2.80 | 4 | 5 | 6 | |
| w(TiO2)/% | 32.31 | 32.79 | 33.34 | 32.33 | 32.79 | 33.34 | 32.07 | 33.34 | 32.35 |
| 产物纯度/% | 94.69 | 96.36 | 97.69 | 92.77 | 97.00 | 97.69 | 95.12 | 97.69 | 97.52 |
(6)钛酸锶中钛锶比的测定。
①测定TiO2的含量:称取mg样品,经一系列处理除去Sr后,配制成250mL溶液。移取25.00mL溶液于锥形瓶中,准确加入V1mLc1mol•L-1EDTA标准溶液(过量),充分反应后,加入指示剂,用c2mol•L-1ZnSO4溶液滴定,滴定至终点时消耗V2mLZnSO4溶液。则钛酸锶中TiO2的质量分数为
②测定SrO的含量:称取mg样品,用硫酸铵和浓硫酸处理,再用乙醇-水稀释成100mL溶液,用氨水调节溶液pH=4,完全沉淀后过滤得到SrSO4沉淀,于850℃时灼烧至恒重,质量为m1g。则钛酸锶中钛锶比为
 =
=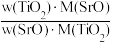 ]。
]。
您最近一年使用:0次
解题方法
5 . 广谱抗真菌药G的一种合成路线如下:

已知: ,R3MgBr为格氏试剂
,R3MgBr为格氏试剂
回答下列问题:
(1)A的化学名称为___________ ,B中所含的官能团的名称为___________ 。
(2)由D生成E的化学方程式为___________ 。
(3)已知F仅含三种元素,则F的结构简式为___________
(4)E,F生成G的反应类型为___________
(5)E的同分异构体有多种,写出一种含有手性碳原子的同分异构体结构简式(并用※标出手性碳原子的位置)______
(6)结合题中所给信息。写出用CH3CH2OH为原料(无机试剂、格氏试剂任选),制备叔丁醇 ((CH3)3C-OH)的合成路线______ 。

已知:
 ,R3MgBr为格氏试剂
,R3MgBr为格氏试剂回答下列问题:
(1)A的化学名称为
(2)由D生成E的化学方程式为
(3)已知F仅含三种元素,则F的结构简式为
(4)E,F生成G的反应类型为
(5)E的同分异构体有多种,写出一种含有手性碳原子的同分异构体结构简式(并用※标出手性碳原子的位置)
(6)结合题中所给信息。写出用CH3CH2OH为原料(无机试剂、格氏试剂任选),制备叔丁醇 ((CH3)3C-OH)的合成路线
您最近一年使用:0次
6 . 硫、氮元素形成的有毒有害气体对大气造成严重污染,研究它们的转化关系对消除污染有重要指导作用。已知:标准生成焓是指298K,100kPa条件下,由最稳定的单质生成单位物质的量的纯物质的热效应,△H=生成物标准生成焓总和﹣反应物标准生成焓总和。
(1)写出NO2氧化SO2的热化学方程式___________ 。(已知NO2自身被还原为NO)
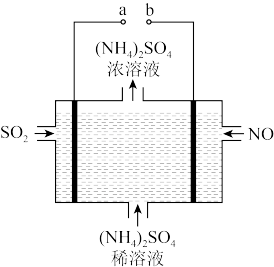
(2)可用如图电解装置将雾霾中的NO、SO2转化为(NH4)2SO4,则a接电源的___________ 极,阴极的电极反应式为___________ 。
(3)按投料比n(NO):n(Cl2)=2:1将NO和Cl2加入到恒压密闭容器中,发生反应2NO(g)+Cl2(g)⇌2NOCl(g),平衡时NO的转化率与温度的关系如图所示。
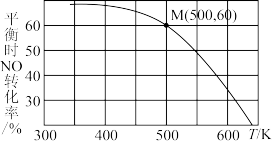
①反应的△H___________ 0。(填“>”或“<”)
②已知总压pMPa,M点时容器内Cl2的转化率为___________ 。M点的平衡常数Kp=___________ MPa﹣1(Kp为以平衡分压表示的平衡常数:平衡分压=总压×体积分数)。
(4)利用现代传感技术探究压强对2NO2(g)⇌N2O4(g)平衡移动的影响。在恒定温度和标准压强条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。
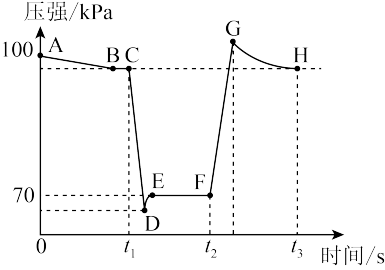
①B、E两点对应的反应速率大小为vB(逆)___________ vE(正)(填“>”、“<”或“=”)。
②F、H两点对应气体的平均相对分子质量较小的点为___________ 。(填字母序号)
| 物质 | 标准生成焓(kJ/mol) | 物质 | 标准生成焓(kJ/mol) |
| O2(g) | 0 | SO2(g) | ﹣296.9 |
| N2(g) | 0 | SO3(g) | ﹣395.2 |
| S(斜方硫,s) | 0 | NO(g) | 89.9 |
| NO2(g) | 33.9 |
(2)可用如图电解装置将雾霾中的NO、SO2转化为(NH4)2SO4,则a接电源的

(3)按投料比n(NO):n(Cl2)=2:1将NO和Cl2加入到恒压密闭容器中,发生反应2NO(g)+Cl2(g)⇌2NOCl(g),平衡时NO的转化率与温度的关系如图所示。

①反应的△H
②已知总压pMPa,M点时容器内Cl2的转化率为
(4)利用现代传感技术探究压强对2NO2(g)⇌N2O4(g)平衡移动的影响。在恒定温度和标准压强条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。

①B、E两点对应的反应速率大小为vB(逆)
②F、H两点对应气体的平均相对分子质量较小的点为
您最近一年使用:0次
名校
7 . 生活中常用的某种香料X的结构简式为: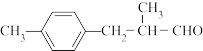
已知:
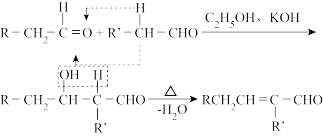
香料X的合成路线如下:

(1)A的结构简式是________________ 。
(2)检验有机物C中含有碳碳双键所需用的试剂_____________ 。
a.银氨溶液 b.酸性高锰酸钾溶液
c.溴水 d.氢氧化钠溶液
(3)D→X的化学方程式为____________________________ 。
(4)有机物B的某种同分异构体E,具有如下性质:
a.与浓溴水反应生成白色沉淀,且1 mol E最多能与4 mol Br2反应
b.红外光谱显示该有机物中存在碳碳双键
则E的结构简式为________________ 。
(5)糠叉丙酮(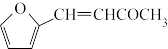 )是一种重要的医药中间体,请参考上述合成路线,设计一条由丙烯[CH3CH=CH2]和糠醛(
)是一种重要的医药中间体,请参考上述合成路线,设计一条由丙烯[CH3CH=CH2]和糠醛(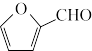 )为原料制备糠叉丙酮的合成路线(无机试剂任用,用结构简式表示有机物),用箭头表示转化关系,箭头上注明试剂和反应条件)
)为原料制备糠叉丙酮的合成路线(无机试剂任用,用结构简式表示有机物),用箭头表示转化关系,箭头上注明试剂和反应条件)____________________ 。
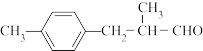
已知:

香料X的合成路线如下:

(1)A的结构简式是
(2)检验有机物C中含有碳碳双键所需用的试剂
a.银氨溶液 b.酸性高锰酸钾溶液
c.溴水 d.氢氧化钠溶液
(3)D→X的化学方程式为
(4)有机物B的某种同分异构体E,具有如下性质:
a.与浓溴水反应生成白色沉淀,且1 mol E最多能与4 mol Br2反应
b.红外光谱显示该有机物中存在碳碳双键
则E的结构简式为
(5)糠叉丙酮(
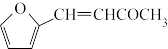 )是一种重要的医药中间体,请参考上述合成路线,设计一条由丙烯[CH3CH=CH2]和糠醛(
)是一种重要的医药中间体,请参考上述合成路线,设计一条由丙烯[CH3CH=CH2]和糠醛( )为原料制备糠叉丙酮的合成路线(无机试剂任用,用结构简式表示有机物),用箭头表示转化关系,箭头上注明试剂和反应条件)
)为原料制备糠叉丙酮的合成路线(无机试剂任用,用结构简式表示有机物),用箭头表示转化关系,箭头上注明试剂和反应条件)
您最近一年使用:0次
2018-05-06更新
|
260次组卷
|
3卷引用:新疆克孜勒苏柯尔克孜自治州阿克陶县2022-2023学年高三上学期11月期中考试化学试题
新疆克孜勒苏柯尔克孜自治州阿克陶县2022-2023学年高三上学期11月期中考试化学试题【全国百强校】江西省南昌市十中2017-2018学年高二下学期期中考试化学试题(已下线)【南昌新东方】2018 南昌十中高二(下) 期中考试 009
8 . 元素周期表中第ⅦA族元素的单质及其化合物的用途广泛。
(1)Cl2的电子式是_______ 。新制的氯水可用于漂白,工业上将氯气制成漂白粉的目的是_________ ,漂白粉是一种_______ (填“混合物”或“纯净物”)。
(2)碘元素在元素周期表中的位置是_________________ ;为防缺碘,食盐中常添加碘酸钾,该物质内存在_________ 键(填化学键类型)。
(3)溴单质是唯一常温下呈液态的非金属单质,液溴的保存通常采取的方法是_______ 。
(4)已知:X2(g)+H2(g) 2HX(g) (X2表示Cl2、Br2和I2)。下图表示平衡常数K与温度T的关系。
2HX(g) (X2表示Cl2、Br2和I2)。下图表示平衡常数K与温度T的关系。
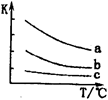
① H表示X2与H2反应的晗变,H
H表示X2与H2反应的晗变,H____ 0。(填“>”、“<”或“=”)
②曲线a表示的是________ (填“Cl2”、“Br2”或“I2”)与H2反应时K与T的关系。
(1)Cl2的电子式是
(2)碘元素在元素周期表中的位置是
(3)溴单质是唯一常温下呈液态的非金属单质,液溴的保存通常采取的方法是
(4)已知:X2(g)+H2(g)
 2HX(g) (X2表示Cl2、Br2和I2)。下图表示平衡常数K与温度T的关系。
2HX(g) (X2表示Cl2、Br2和I2)。下图表示平衡常数K与温度T的关系。
①
 H表示X2与H2反应的晗变,H
H表示X2与H2反应的晗变,H②曲线a表示的是
您最近一年使用:0次
9 . 由简单的烃可合成多种有机物
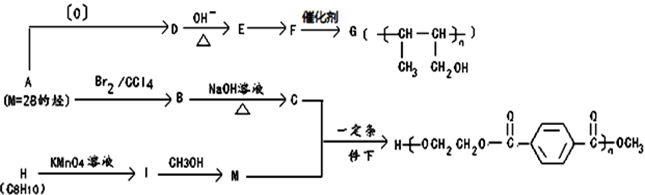
已知: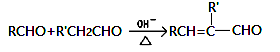 ,
, 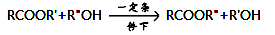 。
。
(1)A的结构简式为________________ ;
(2)D所含的官能团名称为_______ ,B→C的反应类型_____________ ;
(3)已知1mol E在一定条件下和1mol H2反应生成F,写出E→F的化学方程式_____________ ;
(4)E的顺式结构简式为_____________________ ;
(5)关于I的说法正确的是______________________ ;
A.能与溴水发生加成反应 B.能发生酯化反应
C.核磁共振氢谱有3组吸收峰 D.能与NaHCO3溶液反应
(6)写出C与M反应的化学方程式_______________________________ ;
(7)以CH3CHO为有机原料,选用必要的无机试剂合成CH3CHOHCHOHCH2OH,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)____________ 。

已知:
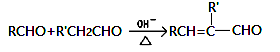 ,
, 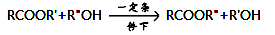 。
。(1)A的结构简式为
(2)D所含的官能团名称为
(3)已知1mol E在一定条件下和1mol H2反应生成F,写出E→F的化学方程式
(4)E的顺式结构简式为
(5)关于I的说法正确的是
A.能与溴水发生加成反应 B.能发生酯化反应
C.核磁共振氢谱有3组吸收峰 D.能与NaHCO3溶液反应
(6)写出C与M反应的化学方程式
(7)以CH3CHO为有机原料,选用必要的无机试剂合成CH3CHOHCHOHCH2OH,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
您最近一年使用:0次
2018-03-27更新
|
302次组卷
|
2卷引用:【全国百强校】新疆兵团第二师华山中学2019届高三上学期学前考试化学试题
解题方法
10 . 氮和氮的化合物在国防建设、工农业生产和生活中都有极其广泛的用途。请回答下列与氮元素有关的问题:
(1)NaCN广泛用于电镀工业上,实验测得浓度相同的NaCN溶液和NaHCO3溶液,前者的pH大,则酸性:HCN___________ H2CO3(填“强于”或“弱于”)。
(2)亚硝酰氯(结构式为Cl-N=O)是有机合成中的重要试剂。它可由C12和NO在通常条件下反应制得,反应方程式为:2NO(g)+Cl2(g) 2ClNO(g)。已知几种化学键的键能数据如下表:
2ClNO(g)。已知几种化学键的键能数据如下表:
当Cl2与NO反应生成ClNO的过程中转移了5mol电子,理论上热量变化为___________ kJ。
(3)在一个恒容密闭容器中充入2 mol NO(g)和1molCl2(g)发生(2)中反应,在温度分别为T1、T2时测得NO的物质的量(单位:mol)与时间的关系如下表所示:
①若容器容积为1L,温度为T1℃时,反应开始到5min时,C12的平均反应速率为_______ 。
②在T1条件下,反应进行到13min时,反应的正反应速率____________ 逆反应速率(填“大于”、“等于”或“小于”),请解释原因:________________________________ 。
③温度为T2℃时,起始时容器内的压强为p0,则该反应的压强平衡常数Kp=_____ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4)近年来,地下水中的氮污染已成为一个世界性的环境问题。在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的H2可高效转化酸性溶液中的硝态氮(NO3-),其工作原理如图所示:
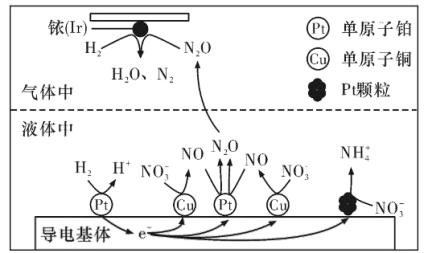
①Ir表面发生反应的方程式为___________ 。
②若导电基体上的Pt颗粒增多,造成的结果是___________ 。
(1)NaCN广泛用于电镀工业上,实验测得浓度相同的NaCN溶液和NaHCO3溶液,前者的pH大,则酸性:HCN
(2)亚硝酰氯(结构式为Cl-N=O)是有机合成中的重要试剂。它可由C12和NO在通常条件下反应制得,反应方程式为:2NO(g)+Cl2(g)
 2ClNO(g)。已知几种化学键的键能数据如下表:
2ClNO(g)。已知几种化学键的键能数据如下表:| 化学键 | Cl—Cl | Cl—N | N=O | N O(NO) O(NO) |
| 键能(kJ/mol) | 243 | 200 | 607 | 630 |
当Cl2与NO反应生成ClNO的过程中转移了5mol电子,理论上热量变化为
(3)在一个恒容密闭容器中充入2 mol NO(g)和1molCl2(g)发生(2)中反应,在温度分别为T1、T2时测得NO的物质的量(单位:mol)与时间的关系如下表所示:
| 温度/℃ | 0min | 5min | 8min | 13min |
| T1 | 2 | 1.5 | 1.3 | 1.0 |
| T2 | 2 | 1.15 | 1.0 | 1.0 |
①若容器容积为1L,温度为T1℃时,反应开始到5min时,C12的平均反应速率为
②在T1条件下,反应进行到13min时,反应的正反应速率
③温度为T2℃时,起始时容器内的压强为p0,则该反应的压强平衡常数Kp=
(4)近年来,地下水中的氮污染已成为一个世界性的环境问题。在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的H2可高效转化酸性溶液中的硝态氮(NO3-),其工作原理如图所示:

①Ir表面发生反应的方程式为
②若导电基体上的Pt颗粒增多,造成的结果是
您最近一年使用:0次



