解题方法
1 . 氧钒(Ⅳ)碱式碳酸铵晶体{(NH4)5[CVO)6(CO3)4(OH)9]•10H2O}是制备多种含钒产品和催化剂的基础原料和前驱体。
已知:①氧钒(Ⅳ)碱式碳酸铵晶体呈紫红色,难溶于水和乙醇;
②VO2+有较强还原性,易被氧化。
实验室以V2O5为原料制备该晶体的流程如图:
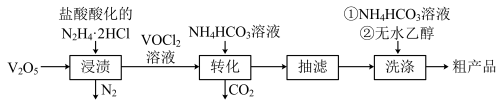
请回答下列问题:
(1)“浸渍”时反应的化学方程式为___________ 。
(2)“转化”时需要在CO2氛围中进行的原因是___________ 。
(3)“转化”可在下图装置中进行:
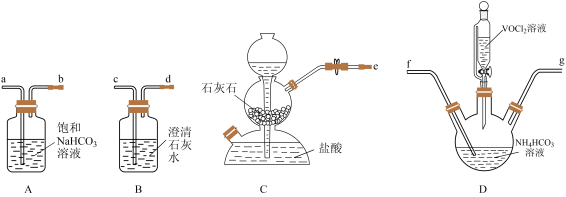
①上述装置连接的合理顺序为e→___________ (按气流方向,用小写字母表示)。
②写出装置D中生成氧钮(Ⅳ)碱式碳酸铵晶体的化学方程式___________ 。
(4)“抽滤”装置如图所示,抽滤原理是___________ 。

(5)“洗涤”时用饱和NH4HCO3溶液洗涤晶体,检验晶体已洗涤干净的操作是___________ 。
(6)为测定粗产品中钒元素的含量,称取l.0g粗产品于锥形瓶中,用20mL蒸馏水与30mL稀硫酸溶解后加入0.01mol/LKMnO4溶液至稍过量,充分反应后继续滴加2%的NaNO2溶液至稍过量,再用尿素除去过量的NaNO2,滴入几滴铁氰化钾K3[Fe(CN)6]溶液,最后用0.2mol/L(NH4)2Fe(SO4)2标准溶液滴定,滴定终点消耗标准溶液的体积为20.00mL。(已知粗产品中杂质不含钒,也不参与反应;滴定反应为
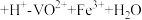 )
)
①滴定终点时的现象为___________ 。
②粗产品中钒元素的质量分数为___________ %。
已知:①氧钒(Ⅳ)碱式碳酸铵晶体呈紫红色,难溶于水和乙醇;
②VO2+有较强还原性,易被氧化。
实验室以V2O5为原料制备该晶体的流程如图:

请回答下列问题:
(1)“浸渍”时反应的化学方程式为
(2)“转化”时需要在CO2氛围中进行的原因是
(3)“转化”可在下图装置中进行:

①上述装置连接的合理顺序为e→
②写出装置D中生成氧钮(Ⅳ)碱式碳酸铵晶体的化学方程式
(4)“抽滤”装置如图所示,抽滤原理是

(5)“洗涤”时用饱和NH4HCO3溶液洗涤晶体,检验晶体已洗涤干净的操作是
(6)为测定粗产品中钒元素的含量,称取l.0g粗产品于锥形瓶中,用20mL蒸馏水与30mL稀硫酸溶解后加入0.01mol/LKMnO4溶液至稍过量,充分反应后继续滴加2%的NaNO2溶液至稍过量,再用尿素除去过量的NaNO2,滴入几滴铁氰化钾K3[Fe(CN)6]溶液,最后用0.2mol/L(NH4)2Fe(SO4)2标准溶液滴定,滴定终点消耗标准溶液的体积为20.00mL。(已知粗产品中杂质不含钒,也不参与反应;滴定反应为

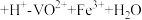 )
)①滴定终点时的现象为
②粗产品中钒元素的质量分数为
您最近一年使用:0次
名校
解题方法
2 .  是一种重要的化工产品。以菱锰矿(主要成分为
是一种重要的化工产品。以菱锰矿(主要成分为 ,还含有
,还含有 、FeO、CoO等)为原料制备
、FeO、CoO等)为原料制备 的工艺流程如下图。
的工艺流程如下图。
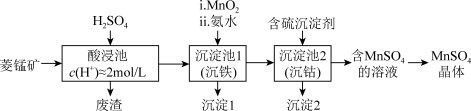
资料:金属离子沉淀的pH
(1)酸浸后所得溶液的金属阳离子包括 、
、 、
、_______ 。
(2)沉淀池1中,先加 充分反应后再加氨水,写出加
充分反应后再加氨水,写出加 时发生反应的离子方程式:
时发生反应的离子方程式:_______ 。
(3)沉淀池2中,不能用NaOH代替含硫沉淀剂,原因是_______ 。
(4)图为 和
和 的溶解度曲线。从“含
的溶解度曲线。从“含 的溶液”中提取“
的溶液”中提取“ 晶体”的操作为
晶体”的操作为_______ 、洗涤、干燥。
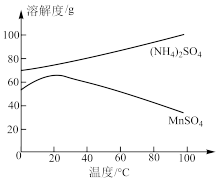
(5)受实际条件限制,“酸浸池”所得的废渣中还含有锰元素,其含量测定方法如下。
i.称取a g废渣,加酸将锰元素全部溶出成 ,过滤,将滤液定容于100mL容量瓶中;
,过滤,将滤液定容于100mL容量瓶中;
ii.取25.00 mL溶液于锥形瓶中,加入少量催化剂和过量 溶液,加热、充分反应后,煮沸溶液使过量的
溶液,加热、充分反应后,煮沸溶液使过量的 分解。
分解。
iii.加入指示剂,用b mol/L 溶液滴定,滴定至终点时消耗
溶液滴定,滴定至终点时消耗 溶液的体积为c mL ,
溶液的体积为c mL , 重新变成
重新变成 。
。
①补全步骤ⅱ中反应的离子方程式:_______ 。
 +
+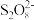 +_______
+_______
 +_______+_______
+_______+_______
②废渣中锰元素的质量分数为_______ 。
 是一种重要的化工产品。以菱锰矿(主要成分为
是一种重要的化工产品。以菱锰矿(主要成分为 ,还含有
,还含有 、FeO、CoO等)为原料制备
、FeO、CoO等)为原料制备 的工艺流程如下图。
的工艺流程如下图。
资料:金属离子沉淀的pH
| 金属离子 | Fe3+ | Fe2+ | Co2+ | Mn2+ |
| 开始沉淀 | 1.5 | 6.3 | 7.4 | 7.6 |
| 完全沉淀 | 2.8 | 8.3 | 9.4 | 10.2 |
 、
、 、
、(2)沉淀池1中,先加
 充分反应后再加氨水,写出加
充分反应后再加氨水,写出加 时发生反应的离子方程式:
时发生反应的离子方程式:(3)沉淀池2中,不能用NaOH代替含硫沉淀剂,原因是
(4)图为
 和
和 的溶解度曲线。从“含
的溶解度曲线。从“含 的溶液”中提取“
的溶液”中提取“ 晶体”的操作为
晶体”的操作为
(5)受实际条件限制,“酸浸池”所得的废渣中还含有锰元素,其含量测定方法如下。
i.称取a g废渣,加酸将锰元素全部溶出成
 ,过滤,将滤液定容于100mL容量瓶中;
,过滤,将滤液定容于100mL容量瓶中;ii.取25.00 mL溶液于锥形瓶中,加入少量催化剂和过量
 溶液,加热、充分反应后,煮沸溶液使过量的
溶液,加热、充分反应后,煮沸溶液使过量的 分解。
分解。iii.加入指示剂,用b mol/L
 溶液滴定,滴定至终点时消耗
溶液滴定,滴定至终点时消耗 溶液的体积为c mL ,
溶液的体积为c mL , 重新变成
重新变成 。
。①补全步骤ⅱ中反应的离子方程式:
 +
+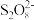 +_______
+_______
 +_______+_______
+_______+_______②废渣中锰元素的质量分数为
您最近一年使用:0次
2023-04-15更新
|
268次组卷
|
3卷引用: 山东省青岛第十七中学2020-2021学年高三下学期期中考试化学试题
名校
解题方法
3 . 炼铁的矿石主要有赤铁矿、磁铁矿和菱铁矿等。在测定磁铁矿中铁的含量前,通常要对矿石进行预处理。对矿样进行预处理后,用重铬酸钾标准溶液可测定铁矿石的含铁量,现有两种对矿样进行预处理的方法如下:

已知:
I.Sn、Hg、Ti在溶液中可存在的形式有 (无色)、
(无色)、 (无色)、
(无色)、 、
、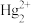 、
、 (紫色)、
(紫色)、 (无色),
(无色), 能与
能与 反应,且
反应,且 也能与
也能与 反应,氯化汞溶于水,氯化亚汞是白色难溶固体;
反应,氯化汞溶于水,氯化亚汞是白色难溶固体;
II.钨酸钠 可作指示剂,若+6价钨被还原为+5价钨,溶液由无色变为蓝色;
可作指示剂,若+6价钨被还原为+5价钨,溶液由无色变为蓝色;
III. 和
和 均具有还原性,氧化性:
均具有还原性,氧化性: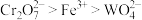 ;
;
IV.二苯胺硫磺钠本身无色,被氧化后呈现紫红色
请回答下列问题:
(1)反应②后得到的悬浊液中固体物质为_______ (写化学式)。
(2)过程①发生反应的离子方程式为_______ 。
(3)反应③中含铁元素的离子发生的反应:_______ ;反应(3)中溶液变蓝,说明_______ 。
(4)矿样预处理后,加入 混酸溶液,以二苯胺硫磺钠为指示剂,用重铬酸钾标准溶液可测定铁矿石的含铁量,当
混酸溶液,以二苯胺硫磺钠为指示剂,用重铬酸钾标准溶液可测定铁矿石的含铁量,当_______ 现象,说明达到了滴定终点。
(5)现称取 矿样进行实验,最终消耗
矿样进行实验,最终消耗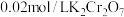 标准溶液
标准溶液 ,则矿样中含铁的质量分数为
,则矿样中含铁的质量分数为_______ 。

已知:
I.Sn、Hg、Ti在溶液中可存在的形式有
 (无色)、
(无色)、 (无色)、
(无色)、 、
、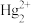 、
、 (紫色)、
(紫色)、 (无色),
(无色), 能与
能与 反应,且
反应,且 也能与
也能与 反应,氯化汞溶于水,氯化亚汞是白色难溶固体;
反应,氯化汞溶于水,氯化亚汞是白色难溶固体;II.钨酸钠
 可作指示剂,若+6价钨被还原为+5价钨,溶液由无色变为蓝色;
可作指示剂,若+6价钨被还原为+5价钨,溶液由无色变为蓝色;III.
 和
和 均具有还原性,氧化性:
均具有还原性,氧化性: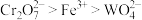 ;
;IV.二苯胺硫磺钠本身无色,被氧化后呈现紫红色
请回答下列问题:
(1)反应②后得到的悬浊液中固体物质为
(2)过程①发生反应的离子方程式为
(3)反应③中含铁元素的离子发生的反应:
(4)矿样预处理后,加入
 混酸溶液,以二苯胺硫磺钠为指示剂,用重铬酸钾标准溶液可测定铁矿石的含铁量,当
混酸溶液,以二苯胺硫磺钠为指示剂,用重铬酸钾标准溶液可测定铁矿石的含铁量,当(5)现称取
 矿样进行实验,最终消耗
矿样进行实验,最终消耗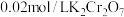 标准溶液
标准溶液 ,则矿样中含铁的质量分数为
,则矿样中含铁的质量分数为
您最近一年使用:0次
2022-11-10更新
|
172次组卷
|
2卷引用:山东省菏泽市2022-2023学年高三上学期期中联考化学(A卷)试题
名校
解题方法
4 . 五氧化二氮(N2O5)是有机合成中常用的绿色硝化剂。N2O5常温下为白色固体,可溶于CH2Cl2等氯代烃溶剂,微溶于水且与水反应生成强酸,高于室温时不稳定。
(1)某化学兴趣小组设计臭氧(O3)氧化法制备N2O5,反应原理为N2O4+O3=N2O5+O2。实验装置如图,回答下列问题:

①装置C的名称______ ,装置D的作用是______ ;装置E的作用是_____ 。
②写出装置A中发生反应的离子方程式______ 。
③实验时,将装置C浸入______ (填“热水”或“冰水”)中,打开装置A中分液漏斗的活塞,一段时间后C中液体变为红棕色。关闭分液漏斗的活塞,打开活塞K,通过臭氧发生器向装置C中通入含有臭氧的氧气。
(2)判断C中反应已结束的现象是_____ 。
(3)用滴定法测定N2O5粗产品中N2O4的含量。取2.0g粗产品,加入20.00mL0.1250mol·L-1酸性高锰酸钾溶液。充分反应后,用0.1000mol·L-1H2O2溶液滴定剩余的高锰酸钾,达到滴定终点时,消耗H2O2溶液17.50mL。(已知:H2O2与HNO3不反应且不考虑其分解)
①产品中N2O4与KMnO4发生反应的离子方程式为_____ 。
②判断滴定达到终点的现象是______ 。
③产品中N2O4的质量分数为_____ (保留到小数点后两位)。
(1)某化学兴趣小组设计臭氧(O3)氧化法制备N2O5,反应原理为N2O4+O3=N2O5+O2。实验装置如图,回答下列问题:

①装置C的名称
②写出装置A中发生反应的离子方程式
③实验时,将装置C浸入
(2)判断C中反应已结束的现象是
(3)用滴定法测定N2O5粗产品中N2O4的含量。取2.0g粗产品,加入20.00mL0.1250mol·L-1酸性高锰酸钾溶液。充分反应后,用0.1000mol·L-1H2O2溶液滴定剩余的高锰酸钾,达到滴定终点时,消耗H2O2溶液17.50mL。(已知:H2O2与HNO3不反应且不考虑其分解)
①产品中N2O4与KMnO4发生反应的离子方程式为
②判断滴定达到终点的现象是
③产品中N2O4的质量分数为
您最近一年使用:0次
名校
解题方法
5 . 某实验小组以BaS溶液为原料制备 ,并用重量法测定产品中
,并用重量法测定产品中 的含量。设计了如下实验方案:
的含量。设计了如下实验方案:
可选用试剂:NaCl晶体、BaS溶液、浓 、稀
、稀 、
、 溶液、蒸馏水
溶液、蒸馏水
步骤1. 的制备
的制备
按如图所示装置进行实验,得到 溶液,经一系列步骤获得
溶液,经一系列步骤获得 产品。
产品。

步骤2,产品中 的含量测定
的含量测定
①称取产品0.5000g,用100mL水溶解,酸化,加热至近沸;
②在不断搅拌下,向①所得溶液逐滴加入热的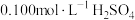 溶液;
溶液;
③沉淀完全后,60℃水浴40分钟,经过滤、洗涤、烘干等步骤,称量白色固体,质量为0.4660g。
回答下列问题:
(1)Ⅰ是制取___________ 气体的装置,Ⅰ中b仪器的作用是___________ ;Ⅲ中的试剂应选用___________ 。
(2)Ⅱ中发生主要反应的化学方程式为___________ ;
(3)如何对装置Ⅰ进行气密性检验___________ ;
(4)沉淀过程中需加入过量的 溶液,原因是
溶液,原因是___________ ;
(5)在过滤操作中,下列仪器不需要用到的是___________ (填名称);

(6)产品中 的质量分数为
的质量分数为___________ (保留三位有效数字)。
 ,并用重量法测定产品中
,并用重量法测定产品中 的含量。设计了如下实验方案:
的含量。设计了如下实验方案:可选用试剂:NaCl晶体、BaS溶液、浓
 、稀
、稀 、
、 溶液、蒸馏水
溶液、蒸馏水步骤1.
 的制备
的制备按如图所示装置进行实验,得到
 溶液,经一系列步骤获得
溶液,经一系列步骤获得 产品。
产品。
步骤2,产品中
 的含量测定
的含量测定①称取产品0.5000g,用100mL水溶解,酸化,加热至近沸;
②在不断搅拌下,向①所得溶液逐滴加入热的
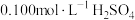 溶液;
溶液;③沉淀完全后,60℃水浴40分钟,经过滤、洗涤、烘干等步骤,称量白色固体,质量为0.4660g。
回答下列问题:
(1)Ⅰ是制取
(2)Ⅱ中发生主要反应的化学方程式为
(3)如何对装置Ⅰ进行气密性检验
(4)沉淀过程中需加入过量的
 溶液,原因是
溶液,原因是(5)在过滤操作中,下列仪器不需要用到的是

(6)产品中
 的质量分数为
的质量分数为
您最近一年使用:0次
解题方法
6 . 氧钒(IV)碱式碳酸铵晶体难溶于水,其化学式为(NH4)5[(VO)6(CO3)4(OH)9]·10H2O。实验室以V2O5为原料制备氧钒(IV)碱式碳酸铵晶体,过程如图:
V2O5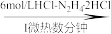 VOCl2溶液
VOCl2溶液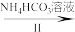 (NH4)5[(VO)6(CO3)4(OH)9]·10H2O
(NH4)5[(VO)6(CO3)4(OH)9]·10H2O
已知:①氧化性:V2O5>Cl2;②VO2+能被O2氧化。
(1)步骤I不选用盐酸,而选用盐酸一盐酸肼(HCl—N2H4·2HCl),可以防止生成____ ,保护环境。
(2)步骤II可在如图装置中进行:

①上述装置依次连接的合理顺序为c→____ (按气流方向,用小写字母表示)。
②连接好装置,检查气密性良好后,加入试剂,开始实验,先____ (填实验操作),当C中溶液变浑浊,____ (填实验操作),进行实验。
③装置D中每生成1mol氧钒(IV)碱式碳酸铵晶体,需要消耗____ molNH4HCO3。
(3)加入VOCl2溶液使反应完全,取下恒压滴液漏斗,立即塞上橡胶塞,将三颈烧瓶置于CO2保护下的干燥器中,静置,得到紫色晶体,过滤。接下来的操作是____ ,最后用乙醚洗涤2-3次,干燥后称重。(必须用到的药品为:饱和NH4HCO3溶液,无水乙醇)。
(4)测定粗产品中钒的含量。实验步骤如下:
称量ag产品于锥形瓶中,用20mL蒸馏水与30mL稀硫酸溶解后,加入0.02mol·L-1KMnO4溶液至稍过量,充分反应后继续滴加1%的NaNO2溶液至稍过量,再用尿素除去过量NaNO2,最后用cmol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗标准溶液的体积为bmL。NaNO2溶液的作用是____ (用离子方程式表示),粗产品中钒的质量分数表达式为____ (以VO2+计)。若(NH4)2Fe(SO4)2标准溶液部分变质,则测定结果____ (填“偏高”、“偏低”或“无影响”)。已知:VO +Fe2++2H+=VO2++Fe3++H2O。
+Fe2++2H+=VO2++Fe3++H2O。
V2O5
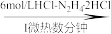 VOCl2溶液
VOCl2溶液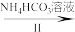 (NH4)5[(VO)6(CO3)4(OH)9]·10H2O
(NH4)5[(VO)6(CO3)4(OH)9]·10H2O已知:①氧化性:V2O5>Cl2;②VO2+能被O2氧化。
(1)步骤I不选用盐酸,而选用盐酸一盐酸肼(HCl—N2H4·2HCl),可以防止生成
(2)步骤II可在如图装置中进行:

①上述装置依次连接的合理顺序为c→
②连接好装置,检查气密性良好后,加入试剂,开始实验,先
③装置D中每生成1mol氧钒(IV)碱式碳酸铵晶体,需要消耗
(3)加入VOCl2溶液使反应完全,取下恒压滴液漏斗,立即塞上橡胶塞,将三颈烧瓶置于CO2保护下的干燥器中,静置,得到紫色晶体,过滤。接下来的操作是
(4)测定粗产品中钒的含量。实验步骤如下:
称量ag产品于锥形瓶中,用20mL蒸馏水与30mL稀硫酸溶解后,加入0.02mol·L-1KMnO4溶液至稍过量,充分反应后继续滴加1%的NaNO2溶液至稍过量,再用尿素除去过量NaNO2,最后用cmol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗标准溶液的体积为bmL。NaNO2溶液的作用是
 +Fe2++2H+=VO2++Fe3++H2O。
+Fe2++2H+=VO2++Fe3++H2O。
您最近一年使用:0次
名校
7 . 三氯氧磷(POCl3)可用作半导体掺杂剂及光导纤维原料,是能推进中国半导体产业链发展壮大的一种重要的化工原料。工业上可以直接氧化PCl3制备POCl3,反应原理为:P4(白磷)+6Cl2=4PCl3,2PCl3+O2=2POCl3。
已知:PCl3、POCl3的部分性质如下:
某化学兴趣小组模拟该工艺设计实验装置如图(某些夹持装置和加热装置已略去):
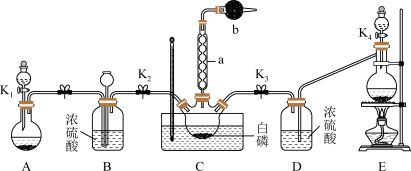
(1)检查装置气密性并加入纯净的白磷,先制取一种气体,缓慢地通入C中,直至C中的白磷完全消失后,再通入另一种气体。仪器a的名称为_______ ,b中盛放的药品是_______ 。
(2)装置E反应的离子方程式为_______ 。
(3)C反应温度控制在60~65℃,不能过高或过低的原因是_______ 。分离提纯获得POCl3的实验方法是_______ 。
(4)通过测定三氯氧磷产品中氯元素含量,可进一步计算产品的纯度,实验步骤如下:
①取ag产品置于盛50.00mL蒸馏水的水解瓶中,摇动至完全水解,将水解液配成100.00mL溶液,预处理排除含磷粒子的影响。
②取10.00mL溶液于锥形瓶中,向其中加入Comol/L-1的AgNO3溶液V0mL,使Cl-完全沉淀,再加入20mL硝基苯,振荡,使沉淀表面被有机物覆盖;然后选择Fe(NO3),指示剂,用c1mol/L-1NH4SCN溶液滴定过量Ag+至终点,记下所用体积为V1mL。
[已知:Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2.0×10-12]
滴定终点的现象:_______ 。实验过程中加入硝基苯的目的是_______ ,若无此操作,则所测POCI3的含量将_______ (填“偏高”“偏低”或“不变”)。
(5)产品中POCl3的质量分数为_______ 。
已知:PCl3、POCl3的部分性质如下:
| 熔点/℃ | 沸点/℃ | 相对分子质量 | 其它 | |
| PCl3 | -112 | 75.5 | 137.5 | 遇水生成H3PO3和HCl |
| POCl3 | 2 | 105.3 | 153.5 | 遇水生成H3PO4和HCl |

(1)检查装置气密性并加入纯净的白磷,先制取一种气体,缓慢地通入C中,直至C中的白磷完全消失后,再通入另一种气体。仪器a的名称为
(2)装置E反应的离子方程式为
(3)C反应温度控制在60~65℃,不能过高或过低的原因是
(4)通过测定三氯氧磷产品中氯元素含量,可进一步计算产品的纯度,实验步骤如下:
①取ag产品置于盛50.00mL蒸馏水的水解瓶中,摇动至完全水解,将水解液配成100.00mL溶液,预处理排除含磷粒子的影响。
②取10.00mL溶液于锥形瓶中,向其中加入Comol/L-1的AgNO3溶液V0mL,使Cl-完全沉淀,再加入20mL硝基苯,振荡,使沉淀表面被有机物覆盖;然后选择Fe(NO3),指示剂,用c1mol/L-1NH4SCN溶液滴定过量Ag+至终点,记下所用体积为V1mL。
[已知:Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2.0×10-12]
滴定终点的现象:
(5)产品中POCl3的质量分数为
您最近一年使用:0次
2022-05-17更新
|
1542次组卷
|
7卷引用:山东省枣庄市第三中学2022-2023学年高三上学期期中考试化学试题
山东省枣庄市第三中学2022-2023学年高三上学期期中考试化学试题陕西省西安市临潼区2022届高三下学期第二次模拟考试理综化学试题(已下线)专题17化学实验综合题-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题16化学实验综合题-2022年高考真题+模拟题汇编(全国卷)(已下线)专题17化学实验综合题-五年(2018~2022)高考真题汇编(全国卷)(已下线)2022年全国甲卷高考真题变式题(非选择题)(已下线)2022年全国乙卷高考变式题(非选择题)
名校
8 . FeCO3可用于制备补血剂。某研究小组制备FeCO3,并对FeCO3的性质和应用进行探究。
已知:①FeCO3是白色固体,难溶于水
②Fe2++6SCN- Fe(SCN)
Fe(SCN) (无色)
(无色)
Ⅰ.FeCO3的制取(夹持装置略)
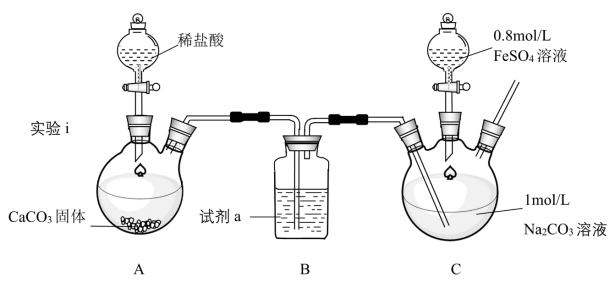
装置C中,向Na2CO3溶液(pH=11.9)通入一段时间CO2至其pH为7,滴加一定量FeSO4溶液,产生白色沉淀,过滤、洗涤、干燥,得到FeCO3固体。
(1)试剂a是_______ 。
(2)向Na2CO3溶液通入CO2的目的是_______ 。
(3)C装置中制取FeCO3的离子方程式为_______ 。
(4)有同学认为C中出现白色沉淀之后应继续通CO2,你认为是否合理?说明理由_______ 。
Ⅱ.FeCO3的性质探究

(5)对比实验ⅱ和ⅲ,得出的实验结论是_______ 。(写2个)
(6)依据实验ⅱ的现象,写出加入10%H2O2溶液的离子方程式_______ 。
Ⅲ.FeCO3的应用
(7)FeCO3溶于乳酸[CH3CH(OH)COOH]能制得可溶性乳酸亚铁补血剂。该实验小组用KMnO4测定补血剂中亚铁含量进而计算乳酸亚铁的质量分数,发现乳酸亚铁的质量分数总是大于100%,其原因是_______ (不考虑操作不当引起的误差)。
已知:①FeCO3是白色固体,难溶于水
②Fe2++6SCN-
 Fe(SCN)
Fe(SCN) (无色)
(无色)Ⅰ.FeCO3的制取(夹持装置略)

装置C中,向Na2CO3溶液(pH=11.9)通入一段时间CO2至其pH为7,滴加一定量FeSO4溶液,产生白色沉淀,过滤、洗涤、干燥,得到FeCO3固体。
(1)试剂a是
(2)向Na2CO3溶液通入CO2的目的是
(3)C装置中制取FeCO3的离子方程式为
(4)有同学认为C中出现白色沉淀之后应继续通CO2,你认为是否合理?说明理由
Ⅱ.FeCO3的性质探究

(5)对比实验ⅱ和ⅲ,得出的实验结论是
(6)依据实验ⅱ的现象,写出加入10%H2O2溶液的离子方程式
Ⅲ.FeCO3的应用
(7)FeCO3溶于乳酸[CH3CH(OH)COOH]能制得可溶性乳酸亚铁补血剂。该实验小组用KMnO4测定补血剂中亚铁含量进而计算乳酸亚铁的质量分数,发现乳酸亚铁的质量分数总是大于100%,其原因是
您最近一年使用:0次
2022-04-20更新
|
1076次组卷
|
6卷引用:化学-2022年高考押题预测卷02(山东卷)
(已下线)化学-2022年高考押题预测卷02(山东卷)湖南省大联考雅礼十六校2021-2022学年高三第二次联考化学试题(已下线)化学-2022年高考考前押题密卷(天津卷)(已下线)考点53 化学实验方案设计与评价-备战2023年高考化学一轮复习考点帮(全国通用)湖北省襄阳市第五中学2022届高三适应性考试(一)化学试题(已下线)考点48 实验方案设计与评价(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
名校
9 . 过硼酸钠(NaBO3·4H2O)可用于漂白剂及杀菌消毒。由硼镁矿(Mg2B2O5·H2O)制取过硼酸钠的过程及装置如下:

已知:I.过硼酸钠微溶于水,热水中不稳定;硼砂(Na2B4O7·10H2O)溶于水吸热,在水中的溶解度如图1所示。

Ⅱ.当pH高于10时,硼元素以BO 形式存在;当pH在9左右时,以
形式存在;当pH在9左右时,以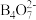 形式存在。
形式存在。
回答下列问题:
(1)步骤I中的化学方程式为___________ ;步骤II中通入CO2的目的是___________ ,操作②获得硼砂Na2B4O7·10H2O的方法是___________ ,过滤。
(2)步骤III回流反应时所进行的操作为:按图2组装好装置→___________ (填序号,下同)→打开磁力搅拌器→打开冷凝水→___________ 。

①用纸槽向c处加入硼砂;②打开a处旋塞加入双氧水;③c处加入氢氧化钠溶液④调低恒温水浴温度;⑤调高恒温水浴温度
(3)步骤IV中洗涤时选用乙醇,原因是___________ 。
(4)活性氧含量的高低直接决定产品的质量,合格产品中活性氧的含量≥10%(1mol H2O2相当于1 mol活性氧原子)。已知:KMnO4不与H3BO3反应。为了确定所得产品是否合格,进行如下实验:称取0.2g干燥样品置于锥形瓶中,加少量水润湿,加入3mol·L-1 25.0 mL稀硫酸使试样全部溶解,产生过氧化氢,摇匀。用0.100mol·L-1高锰酸钾标准溶液滴定溶液的H2O2至终点,发生的反应为:KMnO4+H2O2+H2SO4→K2SO4+MnSO4+H2O+O2↑,三次滴定平均消耗KMnO4溶液6.40mL。配制100mL 0.100mol·L-1高锰酸钾标准溶液,用到的玻璃仪器除玻璃棒、胶头滴管和烧杯外,还有___________ ,若滴定前滴定管尖嘴处无气泡,滴定后出现气泡,会使测得的活性氧含量___________ (填“偏高”“偏低”或“不变”),活性氧的质量分数为___________ %(保留一位小数)。

已知:I.过硼酸钠微溶于水,热水中不稳定;硼砂(Na2B4O7·10H2O)溶于水吸热,在水中的溶解度如图1所示。

Ⅱ.当pH高于10时,硼元素以BO
 形式存在;当pH在9左右时,以
形式存在;当pH在9左右时,以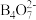 形式存在。
形式存在。回答下列问题:
(1)步骤I中的化学方程式为
(2)步骤III回流反应时所进行的操作为:按图2组装好装置→

①用纸槽向c处加入硼砂;②打开a处旋塞加入双氧水;③c处加入氢氧化钠溶液④调低恒温水浴温度;⑤调高恒温水浴温度
(3)步骤IV中洗涤时选用乙醇,原因是
(4)活性氧含量的高低直接决定产品的质量,合格产品中活性氧的含量≥10%(1mol H2O2相当于1 mol活性氧原子)。已知:KMnO4不与H3BO3反应。为了确定所得产品是否合格,进行如下实验:称取0.2g干燥样品置于锥形瓶中,加少量水润湿,加入3mol·L-1 25.0 mL稀硫酸使试样全部溶解,产生过氧化氢,摇匀。用0.100mol·L-1高锰酸钾标准溶液滴定溶液的H2O2至终点,发生的反应为:KMnO4+H2O2+H2SO4→K2SO4+MnSO4+H2O+O2↑,三次滴定平均消耗KMnO4溶液6.40mL。配制100mL 0.100mol·L-1高锰酸钾标准溶液,用到的玻璃仪器除玻璃棒、胶头滴管和烧杯外,还有
您最近一年使用:0次
2022-06-02更新
|
1616次组卷
|
3卷引用:山东省实验中学2022届高三打靶化学试题
解题方法
10 .  (三草酸合铁酸钾)易溶于水,难溶于乙醇,常用作有机反应的催化剂。某同学利用下图装置制备
(三草酸合铁酸钾)易溶于水,难溶于乙醇,常用作有机反应的催化剂。某同学利用下图装置制备 ,然后再制备三草酸合铁酸钾。
,然后再制备三草酸合铁酸钾。
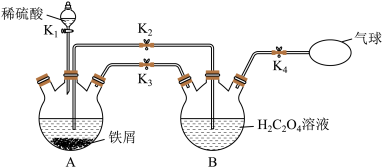
回答下列问题:
(1)打开 、
、 和
和 ,关闭
,关闭 ,制备
,制备 。为使生成的
。为使生成的 溶液与
溶液与 溶液接触,应进行的操作为
溶液接触,应进行的操作为___________ ,B中生成 沉淀的离子方程式为
沉淀的离子方程式为___________ 。
(2)向 中加入过量饱和
中加入过量饱和 溶液,水浴加热并缓慢滴加
溶液,水浴加热并缓慢滴加 溶液,制得
溶液,制得 ,同时有红褐色沉淀生成,该反应的化学方程式为
,同时有红褐色沉淀生成,该反应的化学方程式为___________ ;将上述混合物煮沸,加入饱和 溶液,充分反应后缓慢加入乙醇,结晶、抽滤、洗涤、干燥得到目标产物。将混合物煮沸的目的是
溶液,充分反应后缓慢加入乙醇,结晶、抽滤、洗涤、干燥得到目标产物。将混合物煮沸的目的是___________ ; 的作用是
的作用是___________ 。
(3)制备的 中可能含有
中可能含有 ,采用
,采用 滴定法测定产品纯度,实验步骤如下。
滴定法测定产品纯度,实验步骤如下。
I.取a g样品于锥形瓶中,加入稀 溶解,水浴加热至75℃。用
溶解,水浴加热至75℃。用 的
的 溶液趁热滴定,消耗
溶液趁热滴定,消耗 溶液
溶液 。
。
II.向上述溶液中加入适量还原剂将 完全还原为
完全还原为 ,加入稀
,加入稀 酸化后,在75℃继续用
酸化后,在75℃继续用 溶液滴定,又消耗
溶液滴定,又消耗 溶液
溶液 。
。
若省略步骤II,能否测定 的质量分数
的质量分数___________ (若能,写出表达式;若不能,说明原因);若样品中不含 ,则
,则 与
与 的关系为
的关系为___________ ;若步骤I中滴入 不足,则测得样品中Fe元素含量
不足,则测得样品中Fe元素含量___________ (填“偏高”、“偏低”或“不变”)。
 (三草酸合铁酸钾)易溶于水,难溶于乙醇,常用作有机反应的催化剂。某同学利用下图装置制备
(三草酸合铁酸钾)易溶于水,难溶于乙醇,常用作有机反应的催化剂。某同学利用下图装置制备 ,然后再制备三草酸合铁酸钾。
,然后再制备三草酸合铁酸钾。
回答下列问题:
(1)打开
 、
、 和
和 ,关闭
,关闭 ,制备
,制备 。为使生成的
。为使生成的 溶液与
溶液与 溶液接触,应进行的操作为
溶液接触,应进行的操作为 沉淀的离子方程式为
沉淀的离子方程式为(2)向
 中加入过量饱和
中加入过量饱和 溶液,水浴加热并缓慢滴加
溶液,水浴加热并缓慢滴加 溶液,制得
溶液,制得 ,同时有红褐色沉淀生成,该反应的化学方程式为
,同时有红褐色沉淀生成,该反应的化学方程式为 溶液,充分反应后缓慢加入乙醇,结晶、抽滤、洗涤、干燥得到目标产物。将混合物煮沸的目的是
溶液,充分反应后缓慢加入乙醇,结晶、抽滤、洗涤、干燥得到目标产物。将混合物煮沸的目的是 的作用是
的作用是(3)制备的
 中可能含有
中可能含有 ,采用
,采用 滴定法测定产品纯度,实验步骤如下。
滴定法测定产品纯度,实验步骤如下。I.取a g样品于锥形瓶中,加入稀
 溶解,水浴加热至75℃。用
溶解,水浴加热至75℃。用 的
的 溶液趁热滴定,消耗
溶液趁热滴定,消耗 溶液
溶液 。
。II.向上述溶液中加入适量还原剂将
 完全还原为
完全还原为 ,加入稀
,加入稀 酸化后,在75℃继续用
酸化后,在75℃继续用 溶液滴定,又消耗
溶液滴定,又消耗 溶液
溶液 。
。若省略步骤II,能否测定
 的质量分数
的质量分数 ,则
,则 与
与 的关系为
的关系为 不足,则测得样品中Fe元素含量
不足,则测得样品中Fe元素含量
您最近一年使用:0次



