名校
解题方法
1 . FeSO4溶液放置在空气中容易变质,因此为了方便使用 Fe2+,实验室中常保存硫酸亚铁铵晶体[俗称“摩尔盐”,化学式为(NH4)2Fe(SO4)2•6H2O],它比绿矾或绿矾溶液更稳定。(稳定是指物质放置 在空气中不易发生各种化学反应而变质)
I.硫酸亚铁铵晶体的制备与检验
(1)某兴趣小组设计实验制备硫酸亚铁铵晶体。
本实验中,配制溶液以及后续使用到的蒸馏水都必须煮沸、冷却后再使用,这样处理蒸馏水的目的是_______ 。向 FeSO4溶液中加入饱和(NH4)2SO4溶液,经过操作_______ 、冷却结晶、过滤、洗涤和干燥后得到一 种浅蓝绿色的晶体。
(2)该小组同学继续设计实验证明所制得晶体的成分。
①如图所示实验的目的是_______ ,C 装置的作用是_______ 。
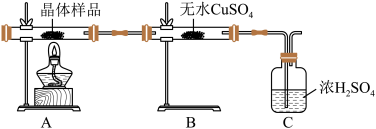
取少量晶体溶于水,得淡绿色待测液。
②取少量待测液,_______ (填操作与现象),证明所制得的晶体中有 Fe2+。
③取少量待测液,经其它实验证明晶体中有NH4+和SO42-
II.实验探究影响溶液中 Fe2+稳定性的因素
(3)配制 0.8 mol/L 的 FeSO4溶液(pH=4.5)和 0.8 mol/L 的(NH4)2Fe(SO4)2溶液(pH=4.0),各取 2 ml 上述溶液于两支试管中,刚开始两种溶液都是浅绿色,分别同时滴加 2 滴 0.01mol/L 的 KSCN 溶液,15 分钟后观察可见:(NH4)2Fe(SO4)2溶液仍然为浅绿色透明澄清溶液;FeSO4溶液则出现淡黄色浑浊。
【资料 1】
①请用离子方程式解释 FeSO4溶液产生淡黄色浑浊的原因_______ 。
②讨论影响 Fe2+稳定性的因素,小组同学提出以下 3 种假设:
假设 1:其它条件相同时,NH4+的存在使(NH4)2Fe(SO4)2溶液中 Fe2+稳定性较好。
假设 2:其它条件相同时,在一定 pH 范围内,溶液 pH 越小 Fe2+稳定性越好。
假设 3:_______ 。
(4)小组同学用如图装置(G为灵敏电流计),滴入适量的硫酸溶液分 别控制溶液 A(0.2 mol/L NaCl)和溶液 B(0.1mol/L FeSO4)为不同的 pH,
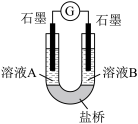
观察记录电流计读数,对假设 2 进行实验研究,实验结果如表所示。
【资料 2】原电池装置中,其它条件相同时,负极反应物的还原性越强或正极反应物的氧化性越强,该原 电池的电流越大。
【资料 3】常温下,0.1mol/L pH=1 的 FeSO4溶液比 pH=5 的 FeSO4溶液稳定性更好。 根据以上实验结果和资料信息,经小组讨论可以得出以下结论:
①U 形管中左池的电极反应式____________ 。
②对比实验 1 和 2(或 3 和 4) ,在一定 pH 范围内,可得出的结论为____________ 。
③对比实验____________ 和____________ ,还可得出在一定pH 范围内溶液酸碱性变化对 O2氧化性强弱的影响因素。
④ 对【资料 3】实验事实的解释为____________ 。
I.硫酸亚铁铵晶体的制备与检验
(1)某兴趣小组设计实验制备硫酸亚铁铵晶体。
本实验中,配制溶液以及后续使用到的蒸馏水都必须煮沸、冷却后再使用,这样处理蒸馏水的目的是
(2)该小组同学继续设计实验证明所制得晶体的成分。
①如图所示实验的目的是

取少量晶体溶于水,得淡绿色待测液。
②取少量待测液,
③取少量待测液,经其它实验证明晶体中有NH4+和SO42-
II.实验探究影响溶液中 Fe2+稳定性的因素
(3)配制 0.8 mol/L 的 FeSO4溶液(pH=4.5)和 0.8 mol/L 的(NH4)2Fe(SO4)2溶液(pH=4.0),各取 2 ml 上述溶液于两支试管中,刚开始两种溶液都是浅绿色,分别同时滴加 2 滴 0.01mol/L 的 KSCN 溶液,15 分钟后观察可见:(NH4)2Fe(SO4)2溶液仍然为浅绿色透明澄清溶液;FeSO4溶液则出现淡黄色浑浊。
【资料 1】
| 沉淀 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 7.6 | 2.7 |
| 完全沉淀pH | 9.6 | 3.7 |
②讨论影响 Fe2+稳定性的因素,小组同学提出以下 3 种假设:
假设 1:其它条件相同时,NH4+的存在使(NH4)2Fe(SO4)2溶液中 Fe2+稳定性较好。
假设 2:其它条件相同时,在一定 pH 范围内,溶液 pH 越小 Fe2+稳定性越好。
假设 3:
(4)小组同学用如图装置(G为灵敏电流计),滴入适量的硫酸溶液分 别控制溶液 A(0.2 mol/L NaCl)和溶液 B(0.1mol/L FeSO4)为不同的 pH,

观察记录电流计读数,对假设 2 进行实验研究,实验结果如表所示。
| 序号 | A:0.2mol·L-1NaCl | B:0.1mol·L-1FeSO4 | 电流计读数 |
| 实验1 | pH=1 | pH=5 | 8.4 |
| 实验2 | pH=1 | pH=1 | 6.5 |
| 实验3 | pH=6 | pH=5 | 7.8 |
| 实验4 | pH=6 | pH=1 | 5.5 |
【资料 3】常温下,0.1mol/L pH=1 的 FeSO4溶液比 pH=5 的 FeSO4溶液稳定性更好。 根据以上实验结果和资料信息,经小组讨论可以得出以下结论:
①U 形管中左池的电极反应式
②对比实验 1 和 2(或 3 和 4) ,在一定 pH 范围内,可得出的结论为
③对比实验
④ 对【资料 3】实验事实的解释为
您最近一年使用:0次
2020-04-16更新
|
458次组卷
|
2卷引用:山东省济宁市嘉祥县第一中学2020届高三下学期第三次质量检测化学试题
名校
2 . 过碳酸钠( ,相对分子质量为314)俗名固体双氧水,是一种新型家用清洁剂和消毒剂,具有碳酸钠和双氧水的双重性质,其3%水溶液显碱性。工业上利用
,相对分子质量为314)俗名固体双氧水,是一种新型家用清洁剂和消毒剂,具有碳酸钠和双氧水的双重性质,其3%水溶液显碱性。工业上利用 和
和 采用“醇析法”制取过碳酸钠晶体的工艺流程如下:
采用“醇析法”制取过碳酸钠晶体的工艺流程如下: 极易溶于水,难溶于乙醇。
极易溶于水,难溶于乙醇。
回答下列问题:
(1)“控温 反应”目的是防止过碳酸钠受热分解,写出过碳酸钠受热分解的化学方程式
反应”目的是防止过碳酸钠受热分解,写出过碳酸钠受热分解的化学方程式___________ 。
(2)“操作a”的名称是___________ ,完成此操作需要的玻璃仪器有烧杯、玻璃棒和___________ ;“洗涤”所用试剂为___________ 。
(3)查阅资料知过碳酸钠在水溶液中氧化性更强,原因是 与
与 反应转化为氧化性更强的
反应转化为氧化性更强的 。写出过碳酸钠溶液中产生
。写出过碳酸钠溶液中产生 的离子方程式
的离子方程式___________ 。
(4)市售过碳酸钠一般都含有碳酸钠,现用以下方案测定某过碳酸钠样品的纯度:称量 样品;全部溶于水中并加入足量稀盐酸充分反应;加热蒸发结晶;称量所得固体质量为
样品;全部溶于水中并加入足量稀盐酸充分反应;加热蒸发结晶;称量所得固体质量为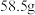 。
。
①“全部溶于水中并加入足量稀盐酸”产生两种无色无味的气体,写出该反应的化学方程式___________ ;
②该样品中过碳酸钠的质量分数为___________ (保留小数点后一位)。
 ,相对分子质量为314)俗名固体双氧水,是一种新型家用清洁剂和消毒剂,具有碳酸钠和双氧水的双重性质,其3%水溶液显碱性。工业上利用
,相对分子质量为314)俗名固体双氧水,是一种新型家用清洁剂和消毒剂,具有碳酸钠和双氧水的双重性质,其3%水溶液显碱性。工业上利用 和
和 采用“醇析法”制取过碳酸钠晶体的工艺流程如下:
采用“醇析法”制取过碳酸钠晶体的工艺流程如下: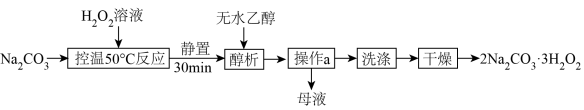
 极易溶于水,难溶于乙醇。
极易溶于水,难溶于乙醇。回答下列问题:
(1)“控温
 反应”目的是防止过碳酸钠受热分解,写出过碳酸钠受热分解的化学方程式
反应”目的是防止过碳酸钠受热分解,写出过碳酸钠受热分解的化学方程式(2)“操作a”的名称是
(3)查阅资料知过碳酸钠在水溶液中氧化性更强,原因是
 与
与 反应转化为氧化性更强的
反应转化为氧化性更强的 。写出过碳酸钠溶液中产生
。写出过碳酸钠溶液中产生 的离子方程式
的离子方程式(4)市售过碳酸钠一般都含有碳酸钠,现用以下方案测定某过碳酸钠样品的纯度:称量
 样品;全部溶于水中并加入足量稀盐酸充分反应;加热蒸发结晶;称量所得固体质量为
样品;全部溶于水中并加入足量稀盐酸充分反应;加热蒸发结晶;称量所得固体质量为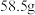 。
。①“全部溶于水中并加入足量稀盐酸”产生两种无色无味的气体,写出该反应的化学方程式
②该样品中过碳酸钠的质量分数为
您最近一年使用:0次
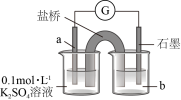
3 . 资料显示, 可以将
可以将 氧化为
氧化为 。某小组同学设计实验探究
。某小组同学设计实验探究 被
被 氧化的产物及铜元素的价态。已知:
氧化的产物及铜元素的价态。已知: 易溶于
易溶于 溶液,发生反应
溶液,发生反应 (红棕色);
(红棕色); 和
和 氧化性几乎相同。
氧化性几乎相同。
将等体积的 溶液加入到n
溶液加入到n 铜粉和m
铜粉和m
 (
( )的固体混合物中,振荡。
)的固体混合物中,振荡。
实验记录如下:
(1)基态 的电子排布式
的电子排布式___________ 。
(2)实验Ⅲ所得溶液中,被氧化的铜元素的可能存在形式有 (蓝色)或
(蓝色)或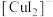 (无色),进行以下实验探究:
(无色),进行以下实验探究:
步骤a.取实验Ⅲ的深红棕色溶液,加入 ,多次萃取、分液。
,多次萃取、分液。
步骤b.取分液后的无色水溶液,滴入浓氨水。溶液颜色变浅蓝色,并逐渐变深。
i.步骤a除去 的原理是
的原理是___________ 。
ii.查阅资料, (无色)容易被空气氧化,用两个离子方程式解释步骤b的溶液中发生的变化:
(无色)容易被空气氧化,用两个离子方程式解释步骤b的溶液中发生的变化:___________ ,___________ 。
(3)上述实验推测实验Ⅰ和Ⅱ中的白色沉淀可能是 ,分别取实验Ⅰ和Ⅱ充分反应后的固体,洗涤后得到白色沉淀,加入
,分别取实验Ⅰ和Ⅱ充分反应后的固体,洗涤后得到白色沉淀,加入 溶液,
溶液,___________ (填实验现象)。实验Ⅲ中铜被氧化的化学方程式是___________ 。
(4)上述实验结果, 仅将
仅将 氧化为+1价。在隔绝空气的条件下进行电化学实验,证实了
氧化为+1价。在隔绝空气的条件下进行电化学实验,证实了 能将
能将 氧化为
氧化为 。装置如图所示,a物质为
。装置如图所示,a物质为___________ ,b试剂为___________ 。
 可以将
可以将 氧化为
氧化为 。某小组同学设计实验探究
。某小组同学设计实验探究 被
被 氧化的产物及铜元素的价态。已知:
氧化的产物及铜元素的价态。已知: 易溶于
易溶于 溶液,发生反应
溶液,发生反应 (红棕色);
(红棕色); 和
和 氧化性几乎相同。
氧化性几乎相同。将等体积的
 溶液加入到n
溶液加入到n 铜粉和m
铜粉和m
 (
( )的固体混合物中,振荡。
)的固体混合物中,振荡。实验记录如下:
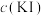 | 实验现象 | |
| 实验Ⅰ | 0.01 | 极少量 溶解,溶液为淡红色;充分反应后,红色的铜粉转化为白色沉淀,溶液仍为淡红色 溶解,溶液为淡红色;充分反应后,红色的铜粉转化为白色沉淀,溶液仍为淡红色 |
| 实验Ⅱ | 0.1 | 部分 溶解,溶液为红棕色;充分反应后,红色的铜粉转化为白色沉淀,溶液仍为红棕色 溶解,溶液为红棕色;充分反应后,红色的铜粉转化为白色沉淀,溶液仍为红棕色 |
| 实验Ⅲ | 4 |  完全溶解,溶液为深红棕色;充分反应后,红色的铜粉完全溶解,溶液为深红棕色 完全溶解,溶液为深红棕色;充分反应后,红色的铜粉完全溶解,溶液为深红棕色 |
 的电子排布式
的电子排布式(2)实验Ⅲ所得溶液中,被氧化的铜元素的可能存在形式有
 (蓝色)或
(蓝色)或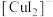 (无色),进行以下实验探究:
(无色),进行以下实验探究:步骤a.取实验Ⅲ的深红棕色溶液,加入
 ,多次萃取、分液。
,多次萃取、分液。步骤b.取分液后的无色水溶液,滴入浓氨水。溶液颜色变浅蓝色,并逐渐变深。
i.步骤a除去
 的原理是
的原理是ii.查阅资料,
 (无色)容易被空气氧化,用两个离子方程式解释步骤b的溶液中发生的变化:
(无色)容易被空气氧化,用两个离子方程式解释步骤b的溶液中发生的变化:(3)上述实验推测实验Ⅰ和Ⅱ中的白色沉淀可能是
 ,分别取实验Ⅰ和Ⅱ充分反应后的固体,洗涤后得到白色沉淀,加入
,分别取实验Ⅰ和Ⅱ充分反应后的固体,洗涤后得到白色沉淀,加入 溶液,
溶液,(4)上述实验结果,
 仅将
仅将 氧化为+1价。在隔绝空气的条件下进行电化学实验,证实了
氧化为+1价。在隔绝空气的条件下进行电化学实验,证实了 能将
能将 氧化为
氧化为 。装置如图所示,a物质为
。装置如图所示,a物质为
您最近一年使用:0次
2023-11-03更新
|
276次组卷
|
2卷引用:山东省青岛市第十九中学2023-2024学年高二上学期化学期末试卷
名校
4 . 三氯化铬(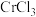 )是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。实验室制取
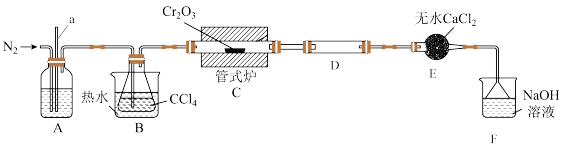
)是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。实验室制取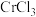 的装置如图所示:
的装置如图所示:
已知:碱性条件下, 可将
可将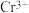 氧化
氧化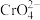 (黄色);酸性条件下,
(黄色);酸性条件下, 可将
可将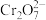 (橙色)还原为
(橙色)还原为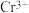 (绿色)。
(绿色)。
回答下列问题:
(1)基态Cr原子的核外电子排布式为_______ 。
(2)装置B中热水的作用是_______ ;实验进行一段时间后,发现导管a中的液面在不断上升,出现该现象的可能原因是_______ ,改进的措施是_______ 。
(3)对于装置C中发生的反应,甲、乙分别提出了两种不同的观点,甲认为发生的反应是 ;乙认为发生的反应是
;乙认为发生的反应是 。
。
Ⅰ.查阅资料知: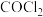 (俗称光气)有毒,遇潮湿的空气马上生成两种酸性气体,该反应的化学方程式为
(俗称光气)有毒,遇潮湿的空气马上生成两种酸性气体,该反应的化学方程式为_______ 。
Ⅱ.设计实验验证装置C中发生的反应;反应结束后,静置,待装置F中溶液分层后,取适量上层溶液于试管中,_______ ,证明甲的观点正确,
(4)测定某样品中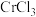 的质量分数的实验步骤如下:
的质量分数的实验步骤如下:
Ⅰ.取5.0g该样品,在强碱性条件下·加入过量30% 溶液,小火加热使
溶液,小火加热使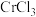 完全转化为
完全转化为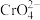 ,再继续加热一段时间。
,再继续加热一段时间。
Ⅱ.冷却后,滴入适量的稀硫酸和浓磷酸(浓磷酸的作用是防止指示剂提前变色),使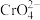 转化为
转化为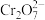 ,再加适量的蒸馏水将溶液稀释至100mL
,再加适量的蒸馏水将溶液稀释至100mL
Ⅲ.取25.00mL溶液,加入适量浓 混合均匀,滴入的3滴试亚铁灵作指示剂,用新配制的
混合均匀,滴入的3滴试亚铁灵作指示剂,用新配制的 的
的 标准溶液滴定,溶液由黄色经蓝绿色变为红褐色即为终点,重复2~3次,平均消耗
标准溶液滴定,溶液由黄色经蓝绿色变为红褐色即为终点,重复2~3次,平均消耗 标准溶液21.00mL(滴定中
标准溶液21.00mL(滴定中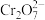 被
被 还原为
还原为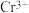 )。
)。
①步骤Ⅰ中完全转化时发生反应的离子方程式为_______ 。
②该样品中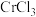 的质量分数为
的质量分数为_______ 。
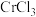 )是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。实验室制取
)是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。实验室制取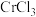 的装置如图所示:
的装置如图所示:
已知:碱性条件下,
 可将
可将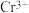 氧化
氧化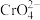 (黄色);酸性条件下,
(黄色);酸性条件下, 可将
可将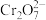 (橙色)还原为
(橙色)还原为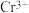 (绿色)。
(绿色)。回答下列问题:
(1)基态Cr原子的核外电子排布式为
(2)装置B中热水的作用是
(3)对于装置C中发生的反应,甲、乙分别提出了两种不同的观点,甲认为发生的反应是
 ;乙认为发生的反应是
;乙认为发生的反应是 。
。Ⅰ.查阅资料知:
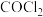 (俗称光气)有毒,遇潮湿的空气马上生成两种酸性气体,该反应的化学方程式为
(俗称光气)有毒,遇潮湿的空气马上生成两种酸性气体,该反应的化学方程式为Ⅱ.设计实验验证装置C中发生的反应;反应结束后,静置,待装置F中溶液分层后,取适量上层溶液于试管中,
(4)测定某样品中
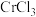 的质量分数的实验步骤如下:
的质量分数的实验步骤如下:Ⅰ.取5.0g该样品,在强碱性条件下·加入过量30%
 溶液,小火加热使
溶液,小火加热使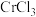 完全转化为
完全转化为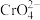 ,再继续加热一段时间。
,再继续加热一段时间。Ⅱ.冷却后,滴入适量的稀硫酸和浓磷酸(浓磷酸的作用是防止指示剂提前变色),使
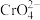 转化为
转化为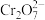 ,再加适量的蒸馏水将溶液稀释至100mL
,再加适量的蒸馏水将溶液稀释至100mLⅢ.取25.00mL溶液,加入适量浓
 混合均匀,滴入的3滴试亚铁灵作指示剂,用新配制的
混合均匀,滴入的3滴试亚铁灵作指示剂,用新配制的 的
的 标准溶液滴定,溶液由黄色经蓝绿色变为红褐色即为终点,重复2~3次,平均消耗
标准溶液滴定,溶液由黄色经蓝绿色变为红褐色即为终点,重复2~3次,平均消耗 标准溶液21.00mL(滴定中
标准溶液21.00mL(滴定中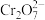 被
被 还原为
还原为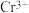 )。
)。①步骤Ⅰ中完全转化时发生反应的离子方程式为
②该样品中
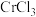 的质量分数为
的质量分数为
您最近一年使用:0次
2022-10-12更新
|
487次组卷
|
5卷引用:山东省枣庄市2022-2023学年高三下学期二模考试化学试题变式题(实验综合题)
(已下线)山东省枣庄市2022-2023学年高三下学期二模考试化学试题变式题(实验综合题)广东省部分学校2022-2023学年高三上学期10月联考化学试题江西省赣州市五校联考2022-2023学年高三上学期期中考试化学试题湖南省邵东市第一中学2022-2023学年高二上学期期中考试化学试题安徽省滁州市实验中学等2校2022-2023学年高二上学期1月期末考试化学试题
名校
5 . 微量元素体检报告单显示,某儿童体内铁元素含量偏低。
(1)服用维生素C可使食物中的 转化为
转化为 。在这个过程中体现维生素C的
。在这个过程中体现维生素C的_______ (填“氧化性”或“还原性”)。缺铁性贫血患者应补充 ,一些补铁剂用硫酸亚铁制成药片时,外表包有一层特殊的糖衣,推测糖衣的作用是
,一些补铁剂用硫酸亚铁制成药片时,外表包有一层特殊的糖衣,推测糖衣的作用是_______ 。
(2)硫酸亚铁晶体 在医药上用作补血剂.某课外小组设计实验测定该补血剂中铁元素的含量,并检验该补血剂是否变质.实验步骤如下:
在医药上用作补血剂.某课外小组设计实验测定该补血剂中铁元素的含量,并检验该补血剂是否变质.实验步骤如下:
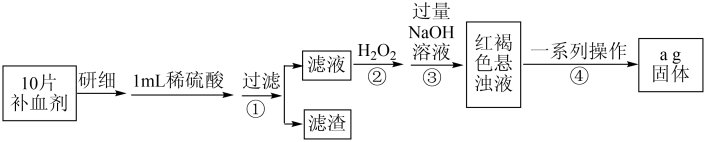
请回答下列问题:
i.取步骤①的滤液滴加 溶液后变为红色,说明滤液中含有
溶液后变为红色,说明滤液中含有_______ (填离子符号),加入 粉后红色褪去,写出加入铁粉时反应的离子方程式:
粉后红色褪去,写出加入铁粉时反应的离子方程式:_______ 。
ii.另取步骤①的滤液,检验其中是否存在 的试剂为
的试剂为_______ 。
iii.步骤②加入过量 的目的是
的目的是_______ 。
iv.一系列操作包括过滤、洗涤、灼烧,最后所得固体为_______ (写化学式)。
v.假设实验中的损耗忽略不计,若1片补血剂的质量为 ,则补血剂中铁元素的质量分数为
,则补血剂中铁元素的质量分数为_______ 。
(1)服用维生素C可使食物中的
 转化为
转化为 。在这个过程中体现维生素C的
。在这个过程中体现维生素C的 ,一些补铁剂用硫酸亚铁制成药片时,外表包有一层特殊的糖衣,推测糖衣的作用是
,一些补铁剂用硫酸亚铁制成药片时,外表包有一层特殊的糖衣,推测糖衣的作用是(2)硫酸亚铁晶体
 在医药上用作补血剂.某课外小组设计实验测定该补血剂中铁元素的含量,并检验该补血剂是否变质.实验步骤如下:
在医药上用作补血剂.某课外小组设计实验测定该补血剂中铁元素的含量,并检验该补血剂是否变质.实验步骤如下:
请回答下列问题:
i.取步骤①的滤液滴加
 溶液后变为红色,说明滤液中含有
溶液后变为红色,说明滤液中含有 粉后红色褪去,写出加入铁粉时反应的离子方程式:
粉后红色褪去,写出加入铁粉时反应的离子方程式:ii.另取步骤①的滤液,检验其中是否存在
 的试剂为
的试剂为iii.步骤②加入过量
 的目的是
的目的是iv.一系列操作包括过滤、洗涤、灼烧,最后所得固体为
v.假设实验中的损耗忽略不计,若1片补血剂的质量为
 ,则补血剂中铁元素的质量分数为
,则补血剂中铁元素的质量分数为
您最近一年使用:0次
2022-01-24更新
|
327次组卷
|
3卷引用:山东省济宁市2021-2022学年高一上学期期末考试化学试题
名校
解题方法
6 . 利用如图装置进行浓硫酸与蔗糖反应的实验,敞口瓶中的蔗糖滴有少量水,将注射器中的浓硫酸注入其中,反应一段时间后,下列说法正确的是
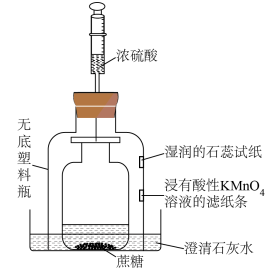
| A.湿润石蕊试纸变红,说明SO2属于酸性氧化物 |
| B.浸有酸性KMnO4溶液的滤纸条褪色,说明SO2具有还原性 |
| C.澄清石灰水变浑浊,说明反应有CO2产生 |
| D.该实验只体现了浓硫酸的吸水性和强氧化性 |
您最近一年使用:0次
2023-12-04更新
|
345次组卷
|
6卷引用:山东省青岛平度市第一中学2023-2024学年高一上学期迎元旦月考化学试题
7 . Na2O2具有强氧化性,H2具有还原性,某同学根据氧化还原反应的知识推测Na2O2与H2能发生反应。为了验证此推测结果,该同学设计并进行了如图所示实验。
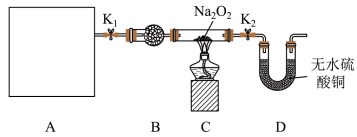
Ⅰ.实验探究
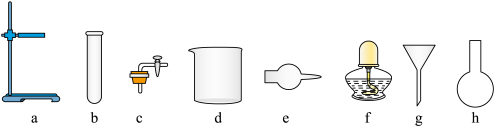
(1)图A是制取氢气的装置,从下图中所给仪器中选择一部分组装成一套能随开随停的发生装置,选择的仪器是_______ (填编号)。
(2)装置A中用粗锌和稀盐酸制取氢气,B装置的名称是______ ;里面所盛放的试剂是______ ,其作用是_____ 。
(3)下面是实验过程中的重要操作,正确的顺序是______ (填序号)。
A.加热至Na2O2逐渐熔化,反应一段时间
B.用小试管收集气体并检验其纯度
C.打开K1、K2,通入氢气
D.停止加热,充分冷却,关闭K1、K2
(4)实验过程中观察到淡黄色粉末慢慢变成白色固体,无水硫酸铜未变蓝色。由此可推出Na2O2与H2反应的化学方程式为________ 。
Ⅱ.数据处理。实验结束后,该同学欲测定C装置硬质玻璃管内白色固体中未反应完的Na2O2含量。其操作流程如图:

①测定过程中需要的仪器除固定、夹持仪器外,还有电子天平、烧杯、酒精灯、蒸发皿和________ ,操作2的名称是________ 。
②在转移溶液时,若溶液转移不完全,则测得的Na2O2质量分数________ (填“偏大”“偏小”或“不变”)。

Ⅰ.实验探究
(1)图A是制取氢气的装置,从下图中所给仪器中选择一部分组装成一套能随开随停的发生装置,选择的仪器是

(2)装置A中用粗锌和稀盐酸制取氢气,B装置的名称是
(3)下面是实验过程中的重要操作,正确的顺序是
A.加热至Na2O2逐渐熔化,反应一段时间
B.用小试管收集气体并检验其纯度
C.打开K1、K2,通入氢气
D.停止加热,充分冷却,关闭K1、K2
(4)实验过程中观察到淡黄色粉末慢慢变成白色固体,无水硫酸铜未变蓝色。由此可推出Na2O2与H2反应的化学方程式为
Ⅱ.数据处理。实验结束后,该同学欲测定C装置硬质玻璃管内白色固体中未反应完的Na2O2含量。其操作流程如图:

①测定过程中需要的仪器除固定、夹持仪器外,还有电子天平、烧杯、酒精灯、蒸发皿和
②在转移溶液时,若溶液转移不完全,则测得的Na2O2质量分数
您最近一年使用:0次
解题方法
8 . 连二亚硫酸钠(Na2S2O4)俗称保险粉,有极强的还原性。难溶于乙醇,可溶于氢氧化钠水溶液并稳定存在。广泛用于纺织工业的还原性染色、清洗、印花、脱色以及织物的漂白等。
(1)制备二氧化硫。若使用如图所示装置制备干燥的SO2气体,回答以下问题:
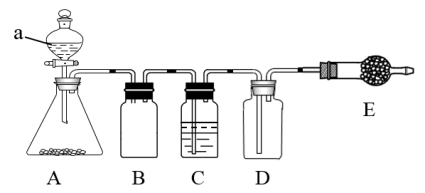
①A中盛液体的玻璃仪器a的名称是___ 。
②B装置的作用是___ ;E中固体试为___ 。
(2)锌粉法制备保险粉。锌粉法制备Na2S2O4的工艺流程如图所示:

①工业上常将锌块进行预处理得到锌粉—水悬浊液,其目的是__ 。
②在步骤I制取Na2S2O4过程中发生了氧化还原反应,SO2表现了___ (填“氧化性”、“还原性”或“酸性”);生成1molNa2S2O4转移电子____ mol。
③在步骤Ⅲ中分离产品Na2S2O4时应选用下列装置___ (填甲、乙、丙、丁)。

(3)保险粉的性质。①保险粉不稳定,容易分解生成甲、乙、丙三种化合物。若将甲、乙两种物质分别配成溶液,在甲溶液中加入稀硫酸,则有淡黄色沉淀和气体丙产生;乙溶液中加入BaCl2溶液和稀盐酸,有气体丙产生,但无白色沉淀。保险粉分解的化学方程式为:___ 。
②保险粉在空气中容易吸收氧气而发生氧化,其方程式为,甲:2Na2S2O4+O2+2H2O=4NaHSO3或乙:Na2S2O4+O2+H2O=NaHSO3+NaHSO4。请设计实验证明氧化时发生的是反应乙:___ 。
(1)制备二氧化硫。若使用如图所示装置制备干燥的SO2气体,回答以下问题:

①A中盛液体的玻璃仪器a的名称是
②B装置的作用是
(2)锌粉法制备保险粉。锌粉法制备Na2S2O4的工艺流程如图所示:

①工业上常将锌块进行预处理得到锌粉—水悬浊液,其目的是
②在步骤I制取Na2S2O4过程中发生了氧化还原反应,SO2表现了
③在步骤Ⅲ中分离产品Na2S2O4时应选用下列装置

(3)保险粉的性质。①保险粉不稳定,容易分解生成甲、乙、丙三种化合物。若将甲、乙两种物质分别配成溶液,在甲溶液中加入稀硫酸,则有淡黄色沉淀和气体丙产生;乙溶液中加入BaCl2溶液和稀盐酸,有气体丙产生,但无白色沉淀。保险粉分解的化学方程式为:
②保险粉在空气中容易吸收氧气而发生氧化,其方程式为,甲:2Na2S2O4+O2+2H2O=4NaHSO3或乙:Na2S2O4+O2+H2O=NaHSO3+NaHSO4。请设计实验证明氧化时发生的是反应乙:
您最近一年使用:0次
9 . 某学习小组对SO2使溶液褪色的机理进行探究。
I.SO2气体的制备和性质初探

(1)装置A中发生反应的化学方程式____________ 。
(2)装置B中的试剂x是____________ 。
(3)小组同学观察到C、D中溶液均褪色,通过检验C溶液中有SO42-,得出C中溶液褪色的原因是____________ 。
II.小组同学通过实验继续对D中品红溶液褪色进行探究。
(4)探究使品红褪色的主要微粒(分别取2 mL试剂a,滴加2滴品红溶液)
①实验 iii中Na2SO3溶液显碱性的原因_____________ (结合化学用语分析解释)。
②对比实验iii 和v,可以排除在该实验条件下OH-对品红褪色的影响,则试剂a可能
是__________ 溶液。
查阅资料:品红与SO2水溶液、NaHSO3溶液、Na2SO3溶液反应前后物质如下:
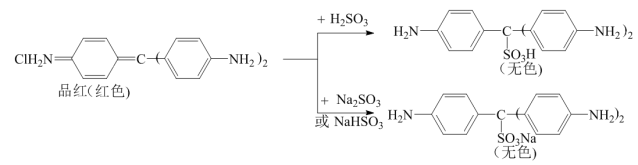
③通过上述实验探究并结合资料,小组同学得出结论:一是使品红溶液褪色的主要微粒是________ ;二是品红溶液中颜色变化主要与其分子中的________ 结构有关。
(5)验证SO2使品红褪色反应的可逆性
①甲同学加热实验i褪色后的溶液,产生刺激性气味气体,红色恢复,从化学平衡移动 角度解释红色恢复的原因__________ 。
②乙同学向实验i褪色后的溶液中滴入Ba(OH)2溶液至pH=10,生成白色沉淀,溶液变红。写出生成白色沉淀的离子方程式___________ 。
③丙同学利用SO2的还原性,运用本题所用试剂 ,设计了如下实验,证实了SO2使品红褪色反应的可逆:则试剂Y是__________ 。

I.SO2气体的制备和性质初探

(1)装置A中发生反应的化学方程式
(2)装置B中的试剂x是
(3)小组同学观察到C、D中溶液均褪色,通过检验C溶液中有SO42-,得出C中溶液褪色的原因是
II.小组同学通过实验继续对D中品红溶液褪色进行探究。
(4)探究使品红褪色的主要微粒(分别取2 mL试剂a,滴加2滴品红溶液)
| 装置 | 序号 | 试剂a | 实验现象 |
 | i | 0.1 mol/L SO2溶液(pH=2) | 红色逐渐变浅,之后完全褪色 |
| ii | 0.1 mol/L NaHSO3溶液(pH=5 ) | 红色立即变浅,之后完全褪色 | |
| iii | 0.1 mol/L Na2SO3溶液( pH=10) | 红色立即褪色 | |
| iv | pH=2H2SO4溶液 | 红色无明显变化 | |
| v | 试剂a | 红色无明显变化 |
②对比实验iii 和v,可以排除在该实验条件下OH-对品红褪色的影响,则试剂a可能
是
查阅资料:品红与SO2水溶液、NaHSO3溶液、Na2SO3溶液反应前后物质如下:

③通过上述实验探究并结合资料,小组同学得出结论:一是使品红溶液褪色的主要微粒是
(5)验证SO2使品红褪色反应的可逆性
①甲同学加热实验i褪色后的溶液,产生刺激性气味气体,红色恢复,从
②乙同学向实验i褪色后的溶液中滴入Ba(OH)2溶液至pH=10,生成白色沉淀,溶液变红。写出生成白色沉淀的离子方程式
③丙同学利用SO2的还原性,

您最近一年使用:0次
2020-05-22更新
|
526次组卷
|
3卷引用:山东师范大学附属中学2020届普通高等学校招生全国统一考试化学试题(模拟一)
名校
10 . 查找资料得知:溴水 显橙黄色,碘水
显橙黄色,碘水 显棕黄色;还原性:
显棕黄色;还原性: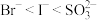 ,
, 在溶液中被氧化时一般生成
在溶液中被氧化时一般生成 。有一无色未知溶液可能含有
。有一无色未知溶液可能含有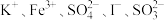 中的一种或者几种,现做以下实验。
中的一种或者几种,现做以下实验。
①取部分溶液加入少量溴水,振荡,溶液呈无色;
②向①的溶液中加入过量氯化钡溶液,产生白色沉淀,再加过量稀硝酸沉淀不溶解;
③取少量②的溶液滴入足量 溶液,有沉淀生成。
溶液,有沉淀生成。
下列关于无色溶液组成的判断正确的是
 显橙黄色,碘水
显橙黄色,碘水 显棕黄色;还原性:
显棕黄色;还原性: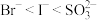 ,
, 在溶液中被氧化时一般生成
在溶液中被氧化时一般生成 。有一无色未知溶液可能含有
。有一无色未知溶液可能含有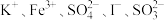 中的一种或者几种,现做以下实验。
中的一种或者几种,现做以下实验。①取部分溶液加入少量溴水,振荡,溶液呈无色;
②向①的溶液中加入过量氯化钡溶液,产生白色沉淀,再加过量稀硝酸沉淀不溶解;
③取少量②的溶液滴入足量
 溶液,有沉淀生成。
溶液,有沉淀生成。下列关于无色溶液组成的判断正确的是
A.肯定含有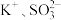 ,可能含有 ,可能含有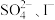 ,肯定不含 ,肯定不含 |
B.肯定不含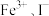 ,肯定含有 ,肯定含有 ,可能含有 ,可能含有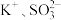 |
C.肯定不含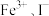 ,肯定含有 ,肯定含有 ,可能含有 ,可能含有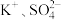 |
D.肯定含有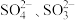 ,可能含有 ,可能含有 ,肯定不含 ,肯定不含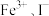 |
您最近一年使用:0次
2022-01-27更新
|
2295次组卷
|
6卷引用:山东省济南市章丘区2021-2022学年高一下学期期中考试化学试题



