解题方法
1 . 下表是元素周期表中的一部分。
根据A~J在周期表中的位置,用元素符号或化学式回答下列问题:
(1)化学性质最不活泼的元素是___________ ,氧化性最强的单质是___________ ,还原性最强的单质是___________ 。
(2)最高价氧化物对应的水化物中,碱性最强的是___________ ,酸性最强的是___________
(3)A分别与E、F、G、H、I形成的化合物中,最稳定的是___________ 。
(4)在B、C、D、G、I中,离子半径最大的是___________ 。
(5)元素C与I形成的化合物的电子式是___________ 。
(6)53号元素在元素周期表中的位置___________ 。
(7)D单质与B的最高价氧化物对应水化物反应的离子方程式___________
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | E | F | H | J | ||||
| 3 | B | C | D | G | I |
(1)化学性质最不活泼的元素是
(2)最高价氧化物对应的水化物中,碱性最强的是
(3)A分别与E、F、G、H、I形成的化合物中,最稳定的是
(4)在B、C、D、G、I中,离子半径最大的是
(5)元素C与I形成的化合物的电子式是
(6)53号元素在元素周期表中的位置
(7)D单质与B的最高价氧化物对应水化物反应的离子方程式
您最近一年使用:0次
名校
2 . 某小组在实验室用NaClO溶液和NH3反应制备N2H4,并进行相关的性质探究实验。
Ⅰ.制备N2H4
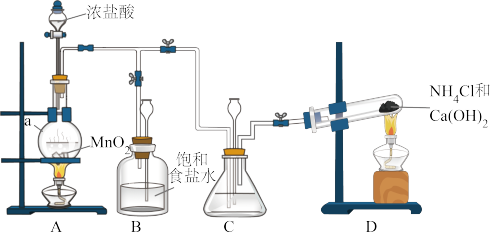
(1)仪器a的名称是___________ 。
(2)装置C中盛放的试剂是___________ 。装置B的作用是___________ 。
(3)制备N2H4的离子方程式为___________ 。
Ⅱ.测定产品中水合肼(N2H4 · H2O)的含量
(4)称取产品6.0 g,加入适量NaHCO3固体(滴定过程中,调节溶液的pH保持在6.5左右), 加水配成250 mL溶液,移取25.00 mL置于锥形瓶中,并滴加2 ~ 3滴淀粉溶液,用 0.3000 mol • L-1的碘标准溶液滴定(已知:N2H4·H2O+2I2 =N2↑ +4HI+H2O)。
①滴定到达终点的现象是___________ 。
②实验测得消耗碘标准溶液的平均值为20.00 mL,产品中水合腓的质量分数为___________ 。
Ⅲ.探究的还原性与碱性。将制得的耕分离提纯后,进行如图实验。

【查阅资料]AgOH在溶液中不稳定,易分解生成黑色的Ag2O,Ag2O可溶于氨水。
【提出假设】黑色固体可能是Ag、Ag2O中的一种或两种。
【实验验证】设计如下方案,进行实验。
(5)请完成表中的空白部分:①___________ ;②___________ 。
(6)实验表明,黑色固体主要成分是Ag,还有少量氧化银,请解释原因:___________ 。
Ⅰ.制备N2H4

(1)仪器a的名称是
(2)装置C中盛放的试剂是
(3)制备N2H4的离子方程式为
Ⅱ.测定产品中水合肼(N2H4 · H2O)的含量
(4)称取产品6.0 g,加入适量NaHCO3固体(滴定过程中,调节溶液的pH保持在6.5左右), 加水配成250 mL溶液,移取25.00 mL置于锥形瓶中,并滴加2 ~ 3滴淀粉溶液,用 0.3000 mol • L-1的碘标准溶液滴定(已知:N2H4·H2O+2I2 =N2↑ +4HI+H2O)。
①滴定到达终点的现象是
②实验测得消耗碘标准溶液的平均值为20.00 mL,产品中水合腓的质量分数为
Ⅲ.探究的还原性与碱性。将制得的耕分离提纯后,进行如图实验。

【查阅资料]AgOH在溶液中不稳定,易分解生成黑色的Ag2O,Ag2O可溶于氨水。
【提出假设】黑色固体可能是Ag、Ag2O中的一种或两种。
【实验验证】设计如下方案,进行实验。
| 操作 | 现象 | 实验结论 |
| i.取少量黑色固体于试管中,加入适量①_________ | 黑色固体部分溶解 | 黑色固体有Ag2O |
| ii.取少量黑色固体于试管中加入足量稀硝酸,振荡 | ②_________ | 黑色固体是Ag和Ag2O |
(6)实验表明,黑色固体主要成分是Ag,还有少量氧化银,请解释原因:
您最近一年使用:0次
2022-03-29更新
|
833次组卷
|
6卷引用:四川省绵阳南山中学2022-2023学年高三上学期入学考试理综化学试题
四川省绵阳南山中学2022-2023学年高三上学期入学考试理综化学试题四川省绵阳市高中2022-2023学年高二下学期理科突击班6月月考化学试题山西省太原市2022届高三下学期模拟考试(一模)理科综合化学试题(已下线)专题17化学实验综合题-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题16化学实验综合题-2022年高考真题+模拟题汇编(全国卷)(已下线)专题17化学实验综合题-五年(2018~2022)高考真题汇编(全国卷)
3 . 高铁酸钾(K2FeO4)是一种新型绿色、高效的水处理剂,对病毒的去除率可达99.95%。已知K2FeO4在低于常温的碱性环境中稳定,酸性条件下,其氧化性强于KMnO4、Cl2等。某小组设计制备K2FeO4并测定其纯度的实验步骤如下:
I.制备次氯酸钾。在搅拌和冰水浴条件下,将Cl2通入浓KOH溶液,同时补加一定量KOH,产生了大量白色沉淀,抽滤后得到浓KClO滤液。
II.制备高铁酸钾(装置如图)
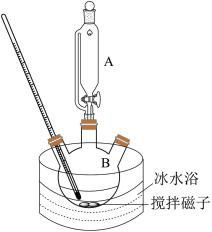
碱性条件下,向如图装置加入上述浓KClO 溶液与冰水浴磁子搅拌Fe(NO3)3;饱和溶液,反应一段时间,得到紫黑色溶液和大量白色沉淀,抽滤分离,用冰盐浴进一步冷却滤液得到K2FeO4粗品。
III.测定高铁酸钾样品的纯度。取0.300g上述步骤制备的K2FeO4样品于锥形瓶,在强碱性溶液中,用过量CrO2-与FeO42-反应生成 CrO42-和Fe(OH)3。稀硫酸酸化后加入指示剂,以0.150mol/L(NH)2Fe(SO4)2标准溶液滴定 Cr(VI)至 Cr3+,终点消耗 20.0mL。
(1)步骤I制备次氯酸钾的化学方程式为_____ ;“补加一定量KOH”的目的除了与过量Cl2继续反应生成更多KClO外,还在步骤II中起到___________ 的作用。
(2)根据 K2FeO4理论合成产率与合成条件响应曲面投影图(见图,虚线上的数据表示K2FeO4的理论合成产率),步骤II中控制的条件应是:温度______ (序号,下同),反应时间_____________ 。
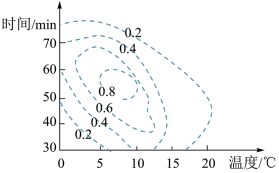
a.0.0~5.0℃ b.5.0~10℃ c.10~15℃ d.40~50 min e.50~60 min f.60~70 min
(3)步骤II中,为了避免副产物K3FeO4的产生,Fe(NO3)3饱和溶液应放在仪器A中,A的名称是________ ;写出实验刚开始时生成FeO42-的离子方程式________ 。
(4)根据步骤皿I的测定数据,计算高铁酸钾样品纯度为_____ (保留3位有效数字)。
(5)为探究酸性条件下FeO42-氧化性强弱,甲同学取步骤II所得K2FeO4粗品加入到少量盐酸中,观察到产生黄绿色气体,经检验气体为Cl2。该现象能否证明“酸性条件下FeO42-氧化性强于Cl2”,并说明理由_______________________________ 。
I.制备次氯酸钾。在搅拌和冰水浴条件下,将Cl2通入浓KOH溶液,同时补加一定量KOH,产生了大量白色沉淀,抽滤后得到浓KClO滤液。
II.制备高铁酸钾(装置如图)

碱性条件下,向如图装置加入上述浓KClO 溶液与冰水浴磁子搅拌Fe(NO3)3;饱和溶液,反应一段时间,得到紫黑色溶液和大量白色沉淀,抽滤分离,用冰盐浴进一步冷却滤液得到K2FeO4粗品。
III.测定高铁酸钾样品的纯度。取0.300g上述步骤制备的K2FeO4样品于锥形瓶,在强碱性溶液中,用过量CrO2-与FeO42-反应生成 CrO42-和Fe(OH)3。稀硫酸酸化后加入指示剂,以0.150mol/L(NH)2Fe(SO4)2标准溶液滴定 Cr(VI)至 Cr3+,终点消耗 20.0mL。
(1)步骤I制备次氯酸钾的化学方程式为
(2)根据 K2FeO4理论合成产率与合成条件响应曲面投影图(见图,虚线上的数据表示K2FeO4的理论合成产率),步骤II中控制的条件应是:温度

a.0.0~5.0℃ b.5.0~10℃ c.10~15℃ d.40~50 min e.50~60 min f.60~70 min
(3)步骤II中,为了避免副产物K3FeO4的产生,Fe(NO3)3饱和溶液应放在仪器A中,A的名称是
(4)根据步骤皿I的测定数据,计算高铁酸钾样品纯度为
(5)为探究酸性条件下FeO42-氧化性强弱,甲同学取步骤II所得K2FeO4粗品加入到少量盐酸中,观察到产生黄绿色气体,经检验气体为Cl2。该现象能否证明“酸性条件下FeO42-氧化性强于Cl2”,并说明理由
您最近一年使用:0次
解题方法
4 . 为了探究乙二酸的不稳定性、弱酸性和还原性,某化学兴趣小组设计如下实验。
[查阅资料]乙二酸俗称草酸,草酸晶体(H2C2O4·2H2O)在100℃时开始升华,157℃时大量升华并开始分解;草酸蒸气在低温下迅速冷凝为固体;草酸钙不溶于水,草酸蒸气能使澄清石灰水变浑浊。
I.乙二酸的不稳定性:根据草酸晶体的组成,猜想其受热分解产物为CO、CO2和H2O。
(1)请用下列装置组成一套探究并验证其产物的实验装置。请回答下列问题:

①装置的连接顺序为:A→D→B→G→_______ →_______ →C→G。
②装置中冰水混合物的作用是_______ 。
③整套装置存在不合理之处_______ 。
II.乙二酸的弱酸性:该小组同学为验证草酸性质需0.1mol/L的草酸溶液480mL。
(2)配制该溶液需要的玻璃仪器有量筒、烧杯、玻璃棒、_______ 、_______ 。
(3)为验证草酸具有弱酸性设计了下列实验,其中能达到实验目的的是_______ 。
A.将草酸晶体溶于含酚酞的NaOH溶液中,溶液褪色
B.测定0.1mol/L草酸溶液的pH
C.将草酸溶液加入Na2CO3溶液中,有CO2放出
(4)该小组同学将0.1mol/L草酸溶液和0.1mol/L的NaOH溶液等体积混合后,测定反应后溶液呈酸性,则所得溶液中各离子浓度由大到小的顺序为_______ 。
III.乙二酸的还原性:
(5)该小组同学向用硫酸酸化的KMnO4溶液中滴入过量的草酸溶液,发现酸性KMnO4溶液褪色,从而判断草酸具有较强的还原性。该反应的离子方程式为_______ 。
[查阅资料]乙二酸俗称草酸,草酸晶体(H2C2O4·2H2O)在100℃时开始升华,157℃时大量升华并开始分解;草酸蒸气在低温下迅速冷凝为固体;草酸钙不溶于水,草酸蒸气能使澄清石灰水变浑浊。
I.乙二酸的不稳定性:根据草酸晶体的组成,猜想其受热分解产物为CO、CO2和H2O。
(1)请用下列装置组成一套探究并验证其产物的实验装置。请回答下列问题:

①装置的连接顺序为:A→D→B→G→
②装置中冰水混合物的作用是
③整套装置存在不合理之处
II.乙二酸的弱酸性:该小组同学为验证草酸性质需0.1mol/L的草酸溶液480mL。
(2)配制该溶液需要的玻璃仪器有量筒、烧杯、玻璃棒、
(3)为验证草酸具有弱酸性设计了下列实验,其中能达到实验目的的是
A.将草酸晶体溶于含酚酞的NaOH溶液中,溶液褪色
B.测定0.1mol/L草酸溶液的pH
C.将草酸溶液加入Na2CO3溶液中,有CO2放出
(4)该小组同学将0.1mol/L草酸溶液和0.1mol/L的NaOH溶液等体积混合后,测定反应后溶液呈酸性,则所得溶液中各离子浓度由大到小的顺序为
III.乙二酸的还原性:
(5)该小组同学向用硫酸酸化的KMnO4溶液中滴入过量的草酸溶液,发现酸性KMnO4溶液褪色,从而判断草酸具有较强的还原性。该反应的离子方程式为
您最近一年使用:0次
解题方法
5 . 亚硝酸钠(NaNO2)是一种常 见的食品添加剂,使用时必须严格控制其用量。某兴趣小组用下图所示装置制备NaNO2并进行纯度测定(夹持装置及A中加热装置已略去)。

已知:①2NO+Na2O2=2NaNO2;
②NO能被酸性KMnO4溶液氧化成NO , MnO
, MnO 被还原为Mn2+。
被还原为Mn2+。
③在酸性条件下NaNO2能把I-氧化为I2; S2O 能把I2还原为I-。
能把I2还原为I-。
(1)装置A中盛装浓HNO3的仪器名称为_______ ,三领烧瓶中发生反应的化学方程式为_______ 。
(2)二氧化氮在装置B中与水反应转化为一氧化氮, 其中铜发生反应的离子方程式为_______ 。
(3)为保证制得的亚硝酸钠的纯度,C装置中盛放的试剂可能是_______(填序号)。
(4)E装置的作用是_______ ,若撤去装置E中试管,则导管口可能看到的现象为_______ 。
(5)利用滴定的方法进行纯度测定。
可供选择的试剂有: A.稀硫酸 B.稀硝酸 C.c1mol·L-1KI溶液 D.淀粉溶液 E. c2mol·L -1Na2S2O3溶液 F. c3 mol·L-1酸性KMnO4溶液
①利用NaNO2的还原性来测定其纯度,须选用的试剂是_______ (填序号),滴定终点的现象为_______ 。
②利用NaNO2的氧化性来测定其纯度,须选用的试剂有_______ (填序号)。

已知:①2NO+Na2O2=2NaNO2;
②NO能被酸性KMnO4溶液氧化成NO
 , MnO
, MnO 被还原为Mn2+。
被还原为Mn2+。③在酸性条件下NaNO2能把I-氧化为I2; S2O
 能把I2还原为I-。
能把I2还原为I-。(1)装置A中盛装浓HNO3的仪器名称为
(2)二氧化氮在装置B中与水反应转化为一氧化氮, 其中铜发生反应的离子方程式为
(3)为保证制得的亚硝酸钠的纯度,C装置中盛放的试剂可能是_______(填序号)。
| A.P2O5 | B.碱石灰 | C.无水CaCl2 | D.氧化钙 |
(5)利用滴定的方法进行纯度测定。
可供选择的试剂有: A.稀硫酸 B.稀硝酸 C.c1mol·L-1KI溶液 D.淀粉溶液 E. c2mol·L -1Na2S2O3溶液 F. c3 mol·L-1酸性KMnO4溶液
①利用NaNO2的还原性来测定其纯度,须选用的试剂是
②利用NaNO2的氧化性来测定其纯度,须选用的试剂有
您最近一年使用:0次
6 . 某化学兴趣小组的同学,都利用如图所示的仪器来完成各自设计的实验。回答下列问题:

(1)甲同学在仪器A中加入H2O2溶液,若X是能使带火星的木条复燃的气体,则B中所盛固体是___________ (填化学式),A的名称是___________ 。
(2)乙同学验证SO2具有还原性和弱氧化性。制备SO2的反应为Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O
①若C中盛装酸性KMnO4稀溶液,打开仪器A的活塞,一段时间后C中观察到的现象是___________ ,该反应证明了SO2具有___________ 性。
②若C中盛装Na2S溶液,C中观察到的现象是___________ ,该实验检验SO2的___________ 性。
(3)丙同学用KMnO4与浓盐酸制氯气,C中装H2O得到新制氯水,再取氯水进行下表所列实验操作。
(4)丁同学验证酸性强弱H2SO4> H2CO3>H2SiO3,则C中发生反应的离子方程式为___________ 。

(1)甲同学在仪器A中加入H2O2溶液,若X是能使带火星的木条复燃的气体,则B中所盛固体是
(2)乙同学验证SO2具有还原性和弱氧化性。制备SO2的反应为Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O
①若C中盛装酸性KMnO4稀溶液,打开仪器A的活塞,一段时间后C中观察到的现象是
②若C中盛装Na2S溶液,C中观察到的现象是
(3)丙同学用KMnO4与浓盐酸制氯气,C中装H2O得到新制氯水,再取氯水进行下表所列实验操作。
| 实验 | 操作 | 现象/离子方程式或化学方程式 |
| ① | 把氯水滴在蓝色石蕊试纸上 | 现象: |
| ② | 向氯水中滴加硝酸银溶液,不断振荡 | 离子方程式: |
| ③ | 向氯水中滴加碳酸钠溶液,不断振荡 | 现象: |
| ④ | 向氯水中通入SO2气体 | 化学方程式: |
您最近一年使用:0次
名校
解题方法
7 .  为无色结晶,有毒;水中的溶解度为35.7g(20℃)、58.7g(100℃)。实验室用毒重石(主要含
为无色结晶,有毒;水中的溶解度为35.7g(20℃)、58.7g(100℃)。实验室用毒重石(主要含 ,及少量
,及少量 、
、 、
、 等杂质)经过加工处理,可制得
等杂质)经过加工处理,可制得 晶体。其实验步骤如下:
晶体。其实验步骤如下:
I.样品分解:称取a g毒重石矿粉于烧杯中,加入稍过量的 溶液,90℃下加热搅拌2h,待充分反应后,冷却,过滤。
溶液,90℃下加热搅拌2h,待充分反应后,冷却,过滤。
II.除 :向滤液中加入一定量的BaS溶液,有黑色沉淀生成,过滤。
:向滤液中加入一定量的BaS溶液,有黑色沉淀生成,过滤。
III.结晶:将步骤II的 滤液经过___________,___________,抽滤,用冷水和乙醇各洗涤晶体2~3次,自然晾干。
滤液经过___________,___________,抽滤,用冷水和乙醇各洗涤晶体2~3次,自然晾干。
回答下列问题:
(1)步骤I中,观察到的实验现象有___________ 。
(2)步骤II检验 是否完全沉淀的方法是
是否完全沉淀的方法是___________ ;在过滤中,下列仪器必需用到的是___________ (填仪器名称),与普通过滤相比,步骤III抽滤的优点是___________ 。___________ ,___________ ,抽滤”。
(4)样品分解时,不选用酸性更强且等量的盐酸溶液替代 溶液,可能的原因是
溶液,可能的原因是___________ 。
(5) 纯度的测定
纯度的测定
某学生查阅资料: ,X代表
,X代表 ,
, 、
、 等,
等, 代表
代表 的阴离子,设计如下纯度测量方案:
的阴离子,设计如下纯度测量方案:
步骤I.准确称取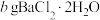 粗品并用20.0mL水溶解。
粗品并用20.0mL水溶解。
步骤II.用 的
的 标准溶液滴定其中的
标准溶液滴定其中的
步骤III.重复滴定2~3次,记录每次消耗 标准溶液的体积
标准溶液的体积
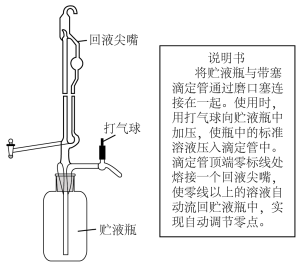
①滴定时采用下图所示的侧边自动定零位滴定管,结合该装置的使用说明书分析其优点___________ 。 含量的测定值偏高的是
含量的测定值偏高的是___________ (填序号)。
a.未干燥锥形瓶 b. 标准溶液久置部分失效
标准溶液久置部分失效
c.滴定终点时滴定管尖嘴中产生气泡 d.杂质可与 反应
反应
 为无色结晶,有毒;水中的溶解度为35.7g(20℃)、58.7g(100℃)。实验室用毒重石(主要含
为无色结晶,有毒;水中的溶解度为35.7g(20℃)、58.7g(100℃)。实验室用毒重石(主要含 ,及少量
,及少量 、
、 、
、 等杂质)经过加工处理,可制得
等杂质)经过加工处理,可制得 晶体。其实验步骤如下:
晶体。其实验步骤如下:I.样品分解:称取a g毒重石矿粉于烧杯中,加入稍过量的
 溶液,90℃下加热搅拌2h,待充分反应后,冷却,过滤。
溶液,90℃下加热搅拌2h,待充分反应后,冷却,过滤。II.除
 :向滤液中加入一定量的BaS溶液,有黑色沉淀生成,过滤。
:向滤液中加入一定量的BaS溶液,有黑色沉淀生成,过滤。III.结晶:将步骤II的
 滤液经过___________,___________,抽滤,用冷水和乙醇各洗涤晶体2~3次,自然晾干。
滤液经过___________,___________,抽滤,用冷水和乙醇各洗涤晶体2~3次,自然晾干。回答下列问题:
(1)步骤I中,观察到的实验现象有
(2)步骤II检验
 是否完全沉淀的方法是
是否完全沉淀的方法是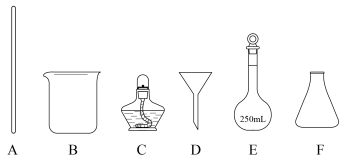
(4)样品分解时,不选用酸性更强且等量的盐酸溶液替代
 溶液,可能的原因是
溶液,可能的原因是(5)
 纯度的测定
纯度的测定某学生查阅资料:
 ,X代表
,X代表 ,
, 、
、 等,
等, 代表
代表 的阴离子,设计如下纯度测量方案:
的阴离子,设计如下纯度测量方案:步骤I.准确称取
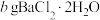 粗品并用20.0mL水溶解。
粗品并用20.0mL水溶解。步骤II.用
 的
的 标准溶液滴定其中的
标准溶液滴定其中的
步骤III.重复滴定2~3次,记录每次消耗
 标准溶液的体积
标准溶液的体积①滴定时采用下图所示的侧边自动定零位滴定管,结合该装置的使用说明书分析其优点
 含量的测定值偏高的是
含量的测定值偏高的是a.未干燥锥形瓶 b.
 标准溶液久置部分失效
标准溶液久置部分失效c.滴定终点时滴定管尖嘴中产生气泡 d.杂质可与
 反应
反应
您最近一年使用:0次
2024-03-29更新
|
241次组卷
|
3卷引用:2024届四川省雅安市、遂宁市、眉山市高三第二次诊断性考试理科综合试题-高中化学
2024届四川省雅安市、遂宁市、眉山市高三第二次诊断性考试理科综合试题-高中化学四川省乐山市2024届高三第二次调查研究考试理科综合-化学试题(已下线)湖南省长沙市第一中学2023-2024学年高三下学期三模化学试题
名校
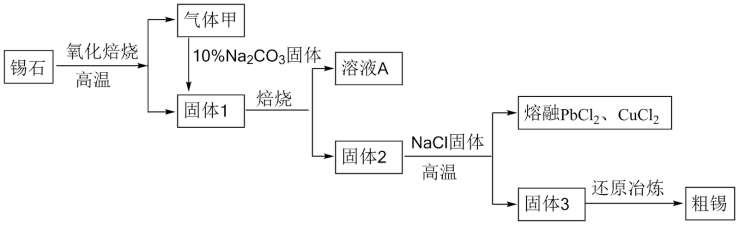
8 . 锡、钨、锦和稀土并称为中国的四大战略资源,工业上主要以锡石(主要成分为 ,还含有
,还含有 、
、 、S、Cu、Pb、Fe等杂质)为原料制备金属锡,其主要工艺流程如下:
、S、Cu、Pb、Fe等杂质)为原料制备金属锡,其主要工艺流程如下:
查阅资料可知:钨酸钙( )难溶于水,Sn、Pb在化合物中主要呈现+2、+4两种化合价。
)难溶于水,Sn、Pb在化合物中主要呈现+2、+4两种化合价。
回答下列问题:
(1)氧化焙烧时加快反应速率的方法有___________ (任填一种),气体甲的主要成分是___________ (填化学式)。
(2)在固体1中加入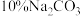 溶液并进行熔烧,其目的是将W元素转化为可溶性盐分离出来,已知该过程中不涉及氧化还原反应,则溶液A中含W元素的溶液的溶质是
溶液并进行熔烧,其目的是将W元素转化为可溶性盐分离出来,已知该过程中不涉及氧化还原反应,则溶液A中含W元素的溶液的溶质是___________ (填化学式);固体2中Pb元素的化合价为___________ 。
(3)固体3通过还原冶炼可得到粗锡,若使用焦炭在高温条件下进行,其反应原理与二氧化硅和碳反应相似,则还原制得锡的化学方程式为___________ 。
(4) 具有强还原性,在酸性条件易被空气中的
具有强还原性,在酸性条件易被空气中的 氧化,其反应的离子方程式为
氧化,其反应的离子方程式为___________ 。
(5)通过下列过程可以测定粗锡中锡的纯度:将粗锡样品溶于盐酸中得到 溶液,再加入过量的
溶液,再加入过量的 溶液转化为
溶液转化为 ,然后用已知浓度的
,然后用已知浓度的 溶液去滴定生成的
溶液去滴定生成的 。现有粗锡样品0.613g,经上述各步反应后,共用去
。现有粗锡样品0.613g,经上述各步反应后,共用去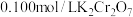 溶液16.0mL,则该粗锡样品中锡的质量分数为
溶液16.0mL,则该粗锡样品中锡的质量分数为___________ (假设杂质不参与反应)。
 ,还含有
,还含有 、
、 、S、Cu、Pb、Fe等杂质)为原料制备金属锡,其主要工艺流程如下:
、S、Cu、Pb、Fe等杂质)为原料制备金属锡,其主要工艺流程如下:
查阅资料可知:钨酸钙(
 )难溶于水,Sn、Pb在化合物中主要呈现+2、+4两种化合价。
)难溶于水,Sn、Pb在化合物中主要呈现+2、+4两种化合价。回答下列问题:
(1)氧化焙烧时加快反应速率的方法有
(2)在固体1中加入
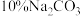 溶液并进行熔烧,其目的是将W元素转化为可溶性盐分离出来,已知该过程中不涉及氧化还原反应,则溶液A中含W元素的溶液的溶质是
溶液并进行熔烧,其目的是将W元素转化为可溶性盐分离出来,已知该过程中不涉及氧化还原反应,则溶液A中含W元素的溶液的溶质是(3)固体3通过还原冶炼可得到粗锡,若使用焦炭在高温条件下进行,其反应原理与二氧化硅和碳反应相似,则还原制得锡的化学方程式为
(4)
 具有强还原性,在酸性条件易被空气中的
具有强还原性,在酸性条件易被空气中的 氧化,其反应的离子方程式为
氧化,其反应的离子方程式为(5)通过下列过程可以测定粗锡中锡的纯度:将粗锡样品溶于盐酸中得到
 溶液,再加入过量的
溶液,再加入过量的 溶液转化为
溶液转化为 ,然后用已知浓度的
,然后用已知浓度的 溶液去滴定生成的
溶液去滴定生成的 。现有粗锡样品0.613g,经上述各步反应后,共用去
。现有粗锡样品0.613g,经上述各步反应后,共用去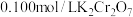 溶液16.0mL,则该粗锡样品中锡的质量分数为
溶液16.0mL,则该粗锡样品中锡的质量分数为
您最近一年使用:0次
2021-07-22更新
|
173次组卷
|
2卷引用:四川省成都市龙泉驿区2020-2021学年高一下学期末学业质量监测联考化学试题
解题方法
9 . 人类的农业生产离不开氯肥,几乎所有的氨肥都以氨为原料生产,某化学兴趣小组利用如图装置制备氨气并探究相关性质

(1)该实验中A装置制备 的化学方程式
的化学方程式_______ ,装置D的作用:_______ 。
(2)甲同学认为该实验装置不严谨,应在装置D后再连接一个装有 固体的球形干燥管,其目的是:
固体的球形干燥管,其目的是:_______ 。
(3)实验开始时,先点燃装置_______ (填“A”或“C”)的酒精灯,一段时间后再点燃另一装置酒精灯。
(4)实验结束发现:C中粉末完全变红,D中无水硫酸铜变蓝,还产生一种单质气体。为进一步确定红色固体物质,参阅资料:Cu、 均为红色固体,其中
均为红色固体,其中 能溶于氨水,生成无色溶液,在空气中立即氧化成蓝色
能溶于氨水,生成无色溶液,在空气中立即氧化成蓝色 ,而Cu不与氨水反应。
,而Cu不与氨水反应。
乙同学提出假设:①红色固体为Cu单质;
②红色固体为 ;
;
③_______
设计实验操作:i.取反应后的红色固体物质于洁净试管中
ii.向其中滴加足量氨水,并充分振荡
iii.观察到溶液变为蓝色,固体有剩余
丙同学为验证乙同学的假设,取CuO固体4.0g重复上述加热实验,反应后装置C中得红色固体3.52g。
请结合上述信息,写出 与CuO反应的化学方程式:
与CuO反应的化学方程式:_______ 。
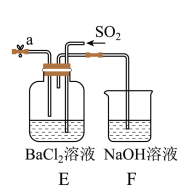
(5)已知,将 通入
通入 溶液中,无明显现象。如图,若将上述实验生成的
溶液中,无明显现象。如图,若将上述实验生成的 与
与 同时通入
同时通入 溶液中,产生白色沉淀:若向a处分别通入
溶液中,产生白色沉淀:若向a处分别通入_______ (填下列气体编号),在E中也能产生白色沉淀,其白色沉淀为_______ 。
A. B.
B. C.
C. D.
D.

(1)该实验中A装置制备
 的化学方程式
的化学方程式(2)甲同学认为该实验装置不严谨,应在装置D后再连接一个装有
 固体的球形干燥管,其目的是:
固体的球形干燥管,其目的是:(3)实验开始时,先点燃装置
(4)实验结束发现:C中粉末完全变红,D中无水硫酸铜变蓝,还产生一种单质气体。为进一步确定红色固体物质,参阅资料:Cu、
 均为红色固体,其中
均为红色固体,其中 能溶于氨水,生成无色溶液,在空气中立即氧化成蓝色
能溶于氨水,生成无色溶液,在空气中立即氧化成蓝色 ,而Cu不与氨水反应。
,而Cu不与氨水反应。乙同学提出假设:①红色固体为Cu单质;
②红色固体为
 ;
;③
设计实验操作:i.取反应后的红色固体物质于洁净试管中
ii.向其中滴加足量氨水,并充分振荡
iii.观察到溶液变为蓝色,固体有剩余
丙同学为验证乙同学的假设,取CuO固体4.0g重复上述加热实验,反应后装置C中得红色固体3.52g。
请结合上述信息,写出
 与CuO反应的化学方程式:
与CuO反应的化学方程式:(5)已知,将
 通入
通入 溶液中,无明显现象。如图,若将上述实验生成的
溶液中,无明显现象。如图,若将上述实验生成的 与
与 同时通入
同时通入 溶液中,产生白色沉淀:若向a处分别通入
溶液中,产生白色沉淀:若向a处分别通入
A.
 B.
B. C.
C. D.
D.
您最近一年使用:0次
名校
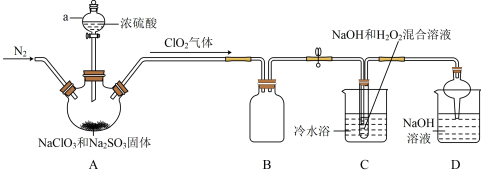
10 . 新冠疫情期间使用了大量的消毒剂,其中二氧化氯(ClO2)与亚氯酸钠(NaClO2)都具有强氧化性。两者作漂白剂时,不伤害织物;作饮用水消毒剂时,不残留异味。某研究性学习小组利用如下装置由二氧化氯制备NaClO2·3H2O,并探究其性质。
I.查阅资料:
①ClO2易与碱溶液反应生成等物质的量的两种盐,其中一种为氯酸盐。
②NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·3H2O,高于38℃时析出的晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
Ⅱ.制备与分离:
(1)实验加药品前应进行的实验操作是____ 。
(2)盛放NaClO3和Na2SO3固体的仪器名称是____ 。
(3)装置A中参加反应的氧化剂与还原剂的物质的量之比为____ 。
(4)B装置的作用是____ 。
(5)若要从装置C反应后的溶液获得无水NaClO2晶体的操作步骤如下,请完成下列操作步骤②的内容。
①减压,55℃蒸发结晶; ②____ ;
③用38℃~60℃热水洗涤; ④在38℃~60℃间进行干燥,得到成品。
(6)装置D是处理尾气,反应的化学方程式____ 。
(7)实验结束后,继续通入一段时间N2的目的是____ 。
Ⅲ.测量与计算:
(8)利用题中原理制备出NaClO2·3H2O晶体的样品,可以用“间接碘量法”测定样品(杂质与I-不发生反应)的纯度,过程如下:取样品1.4450g配制成250mL溶液,从中取出25.00mL,加入足量KI固体和适量稀H2SO4,再滴加几滴淀粉溶液,(已知:ClO +4I-+4H+=2H2O+2I2+Cl-),然后用cmol·L-1 Na2S2O3标准溶液滴定至终点,重复2次,测得消耗标准溶液的体积平均值为vmL(已知:I2+2S2O
+4I-+4H+=2H2O+2I2+Cl-),然后用cmol·L-1 Na2S2O3标准溶液滴定至终点,重复2次,测得消耗标准溶液的体积平均值为vmL(已知:I2+2S2O =S4O
=S4O +2I-)。
+2I-)。
①滴定终点的现象是____ 。
②下列滴定操作会导致测量结果偏低的是____ (填字母)。
a 锥形瓶洗涤后没有干燥 b 滴定时锥形瓶中有液体溅出
c 滴定终点时俯视读数 d 滴定管滴定前有气泡,滴定后气泡消失
③样品中NaClO2·3H2O的纯度为____ %(用含c、v的代数式表示)。

I.查阅资料:
①ClO2易与碱溶液反应生成等物质的量的两种盐,其中一种为氯酸盐。
②NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·3H2O,高于38℃时析出的晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
Ⅱ.制备与分离:
(1)实验加药品前应进行的实验操作是
(2)盛放NaClO3和Na2SO3固体的仪器名称是
(3)装置A中参加反应的氧化剂与还原剂的物质的量之比为
(4)B装置的作用是
(5)若要从装置C反应后的溶液获得无水NaClO2晶体的操作步骤如下,请完成下列操作步骤②的内容。
①减压,55℃蒸发结晶; ②
③用38℃~60℃热水洗涤; ④在38℃~60℃间进行干燥,得到成品。
(6)装置D是处理尾气,反应的化学方程式
(7)实验结束后,继续通入一段时间N2的目的是
Ⅲ.测量与计算:
(8)利用题中原理制备出NaClO2·3H2O晶体的样品,可以用“间接碘量法”测定样品(杂质与I-不发生反应)的纯度,过程如下:取样品1.4450g配制成250mL溶液,从中取出25.00mL,加入足量KI固体和适量稀H2SO4,再滴加几滴淀粉溶液,(已知:ClO
 +4I-+4H+=2H2O+2I2+Cl-),然后用cmol·L-1 Na2S2O3标准溶液滴定至终点,重复2次,测得消耗标准溶液的体积平均值为vmL(已知:I2+2S2O
+4I-+4H+=2H2O+2I2+Cl-),然后用cmol·L-1 Na2S2O3标准溶液滴定至终点,重复2次,测得消耗标准溶液的体积平均值为vmL(已知:I2+2S2O =S4O
=S4O +2I-)。
+2I-)。①滴定终点的现象是
②下列滴定操作会导致测量结果偏低的是
a 锥形瓶洗涤后没有干燥 b 滴定时锥形瓶中有液体溅出
c 滴定终点时俯视读数 d 滴定管滴定前有气泡,滴定后气泡消失
③样品中NaClO2·3H2O的纯度为
您最近一年使用:0次
2020-11-20更新
|
1050次组卷
|
3卷引用:四川省遂宁市2021届高三零诊考试理综化学试题



