名校
解题方法
1 . 下列装置用于实验室制氨气或验证氨气的化学性质,其中能达到实验目的的是
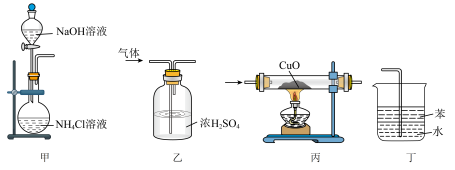
| A.用装置甲制取氨气 | B.用装置乙除去氨气中的水蒸气 |
| C.用装置丙验证氨气具有还原性 | D.用装置丁吸收尾气 |
您最近一年使用:0次
2024-05-05更新
|
305次组卷
|
13卷引用:四川省什邡中学2022-2023学年高一下学期第一次月考化学试题
四川省什邡中学2022-2023学年高一下学期第一次月考化学试题四川省射洪中学校2023-2024学年高一下学期4月第一次月考化学试题云南省开远市第一中学校2022-2023学年高一下学期期中考试化学试题江苏省泰州市2023-2024学年高一上学期1月期末化学试题(已下线)专题03 常见气体的实验室制取(考点清单)(讲+练)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)湖北省武汉市第十二中学2023-2024学年高一下学期3月月考化学试题广东省潮州市饶平县第二中学2023-2024学年高一下学期第一次月考化学试题江西省南昌十九中2022-2023学年高一下学期3月第一次月考化学试卷山东省济宁市微山县第二中学2023-2024学年高一下学期第一次月考化学试题江苏省扬州中学2023-2024学年高一下学期4月期中考试化学试题安徽省淮南市第二中2023-2024学年高一下学期第一次月考化学试题北京市育英学校2023-2024学年高一上学期期末考试化学试题湖北省咸宁市崇阳县第二高级中学2023-2024学年高一下学期3月月考化学试题
名校
解题方法
2 . 将 通入
通入 溶液至饱和的过程中,始终未观察到溶液中出现浑浊,若再通入另一种气体
溶液至饱和的过程中,始终未观察到溶液中出现浑浊,若再通入另一种气体 ,则产生白色沉淀,制备气体
,则产生白色沉淀,制备气体 的试剂不能是
的试剂不能是
 通入
通入 溶液至饱和的过程中,始终未观察到溶液中出现浑浊,若再通入另一种气体
溶液至饱和的过程中,始终未观察到溶液中出现浑浊,若再通入另一种气体 ,则产生白色沉淀,制备气体
,则产生白色沉淀,制备气体 的试剂不能是
的试剂不能是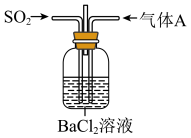
A. 和 和 | B.大理石和稀盐酸 |
C. 和浓硝酸 和浓硝酸 | D. 和浓盐酸 和浓盐酸 |
您最近一年使用:0次
2024-04-27更新
|
61次组卷
|
13卷引用:【全国百强校】四川省成都外国语学校2018-2019学年高一下学期入学考试化学试题
【全国百强校】四川省成都外国语学校2018-2019学年高一下学期入学考试化学试题四川省威远中学2018-2019学年高一下学期期中考试化学试题【区级联考】北京市西城区2018-2019学年高一第一学期期末考试化学试题河北安平中学2020届高三上学期第二次月考化学试题鲁科版(2019)高一必修第一册第三章B 素养拓展区 过综合 章末素养综合检测(已下线)小题必刷19 硫及其化合物——2021年高考化学一轮复习小题必刷(通用版)江西省上饶市铅山县第一中学2020-2021学年上学期高一联考(自招班)化学试题(已下线)化学(上海A卷)-学易金卷:2023年高考第一次模拟考试卷山西省阳泉市第一中学校2022-2023学年高一下学期期中考试化学试题(已下线)专题突破卷04?非金属及其化合物?-2024年高考化学一轮复习考点通关卷(新教材新高考) 天津市滨海新区田家炳中学2023-2024学年高三上学期第二次月考化学试题安徽省淮北市第一中学2023-2024学年高一下学期3月月考化学试题云南省大理白族自治州祥云祥华中学2023-2024学年高一下学期3月月考化学试题
解题方法
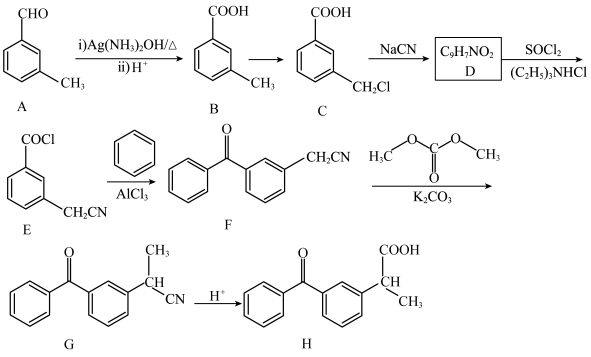
3 . H是合成某药物的中间体。H的一种合成路线如下:
(1)H中所含官能团名称为___________ ,A的化学名称为___________ 。
(2)B→C的反应试剂和条件是___________ 。
(3)C→D的反应类型是___________ 。
(4)写出E→F的化学方程式:___________ 。
(5)苯的二元取代物T是H的同分异构体,则符合下列条件的T有___________ 种(不包含立体异构)。
①分子中含有两个苯环,且每个苯环上的两个取代基均在对位;
②遇 溶液显紫色且能发生银镜反应;
溶液显紫色且能发生银镜反应;
③1molT可消耗3molNaOH。
写出其中一种不能与溴水发生加成反应的同分异构体的结构简式:___________ 。
(6)设计以甲苯和苯为原料制备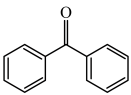 的合成路线:
的合成路线:___________ (其他试剂任选)。
(1)H中所含官能团名称为
(2)B→C的反应试剂和条件是
(3)C→D的反应类型是
(4)写出E→F的化学方程式:
(5)苯的二元取代物T是H的同分异构体,则符合下列条件的T有
①分子中含有两个苯环,且每个苯环上的两个取代基均在对位;
②遇
 溶液显紫色且能发生银镜反应;
溶液显紫色且能发生银镜反应;③1molT可消耗3molNaOH。
写出其中一种不能与溴水发生加成反应的同分异构体的结构简式:
(6)设计以甲苯和苯为原料制备
 的合成路线:
的合成路线:
您最近一年使用:0次
4 . 某团队报道了高温富水环境下,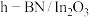 催化丙烷氧化脱氢原理,涉及反应如下:
催化丙烷氧化脱氢原理,涉及反应如下:
i.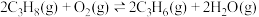

ii.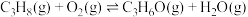

回答下列问题:
(1)上述反应过程中涉及的C、N、O元素可以组成多种配体,如CO、 、
、 等,CO、
等,CO、 的配位原子是C,而
的配位原子是C,而 的配位原子是N,简述其原因
的配位原子是N,简述其原因___________ 。
(2)已知:丙烷、丙烯的燃烧热分别为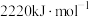 、
、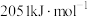 。18g液态水变为
。18g液态水变为 吸收热量44kJ。则
吸收热量44kJ。则
___________  。下列关于反应i自发性判断正确的是
。下列关于反应i自发性判断正确的是___________ (填标号)。
A.任何温度都能自发进行 B.任何温度都不能自发进行
C.在较高温度下能自发进行 D.在较低温度下能自发进行
(3)已知反应i速率方程为 (k为速率常数只与温度、催化剂有关;α、β、γ、δ为反应级数,可以为正数、负数或分数)。
(k为速率常数只与温度、催化剂有关;α、β、γ、δ为反应级数,可以为正数、负数或分数)。
①一定温度下,反应速率与浓度( )关系如下表所示:
)关系如下表所示:
根据数据计算,α+β+γ+δ=___________ 。
②速率常数与温度、活化能关系式为 (R、C为常数,T为温度,
(R、C为常数,T为温度, 为活化能且不随温度变化而变化)。在不同催化剂Cat1、Cat2作用下,Ink与
为活化能且不随温度变化而变化)。在不同催化剂Cat1、Cat2作用下,Ink与 关系如图:
关系如图:___________ (填“Cat1”或“Cat2”)。
(4)在密闭容器中充入 和
和 ,仅发生上述反应i和ii,测得丙烷的平衡转化率与温度、压强关系如图所示:
,仅发生上述反应i和ii,测得丙烷的平衡转化率与温度、压强关系如图所示:___________ 。
② 下,A点丙烯的选择性为80%(选择性等于丙烯的物质的量与丙烷转化的总物质的量之比)。B点时,反应ii的压强平衡常数
下,A点丙烯的选择性为80%(选择性等于丙烯的物质的量与丙烷转化的总物质的量之比)。B点时,反应ii的压强平衡常数
___________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(5)在熔融碳酸钠中,丙烷-空气燃料电池的放电效率高。该燃料电池放电时,负极的电极反应式为___________ 。
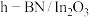 催化丙烷氧化脱氢原理,涉及反应如下:
催化丙烷氧化脱氢原理,涉及反应如下:i.
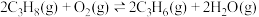

ii.
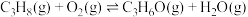

回答下列问题:
(1)上述反应过程中涉及的C、N、O元素可以组成多种配体,如CO、
 、
、 等,CO、
等,CO、 的配位原子是C,而
的配位原子是C,而 的配位原子是N,简述其原因
的配位原子是N,简述其原因(2)已知:丙烷、丙烯的燃烧热分别为
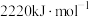 、
、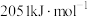 。18g液态水变为
。18g液态水变为 吸收热量44kJ。则
吸收热量44kJ。则
 。下列关于反应i自发性判断正确的是
。下列关于反应i自发性判断正确的是A.任何温度都能自发进行 B.任何温度都不能自发进行
C.在较高温度下能自发进行 D.在较低温度下能自发进行
(3)已知反应i速率方程为
 (k为速率常数只与温度、催化剂有关;α、β、γ、δ为反应级数,可以为正数、负数或分数)。
(k为速率常数只与温度、催化剂有关;α、β、γ、δ为反应级数,可以为正数、负数或分数)。①一定温度下,反应速率与浓度(
 )关系如下表所示:
)关系如下表所示:| 序号 |  | 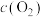 | 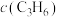 | 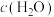 | v |
| Ⅰ | 0.1 | 0.1 | 0.1 | 0.1 | k |
| Ⅱ | 0.2 | 0.1 | 0.1 | 0.1 | 4k |
| Ⅲ | 0.2 | 0.4 | 0.1 | 0.1 | 8k |
| Ⅳ | 0.4 | 0.1 | 0.2 | 0.1 | 8k |
| Ⅴ | 0.4 | 0.4 | 0.1 | 0.2 | 16k |
②速率常数与温度、活化能关系式为
 (R、C为常数,T为温度,
(R、C为常数,T为温度, 为活化能且不随温度变化而变化)。在不同催化剂Cat1、Cat2作用下,Ink与
为活化能且不随温度变化而变化)。在不同催化剂Cat1、Cat2作用下,Ink与 关系如图:
关系如图: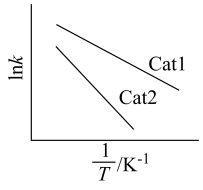
(4)在密闭容器中充入
 和
和 ,仅发生上述反应i和ii,测得丙烷的平衡转化率与温度、压强关系如图所示:
,仅发生上述反应i和ii,测得丙烷的平衡转化率与温度、压强关系如图所示: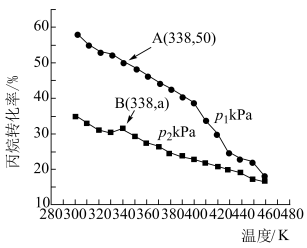
②
 下,A点丙烯的选择性为80%(选择性等于丙烯的物质的量与丙烷转化的总物质的量之比)。B点时,反应ii的压强平衡常数
下,A点丙烯的选择性为80%(选择性等于丙烯的物质的量与丙烷转化的总物质的量之比)。B点时,反应ii的压强平衡常数
(5)在熔融碳酸钠中,丙烷-空气燃料电池的放电效率高。该燃料电池放电时,负极的电极反应式为
您最近一年使用:0次
解题方法
5 . 近日,某科研小组制备了新型锂离子电池电极材料——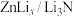 。该小组以废旧锌锰电池为原料合成
。该小组以废旧锌锰电池为原料合成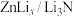 ,简易流程如下:
,简易流程如下: 、Fe、
、Fe、 等)。
等)。
② 在酸性条件下转化成
在酸性条件下转化成 和
和 ;
; 的沸点为78.8℃。
的沸点为78.8℃。
③已知几种金属离子沉淀的pH如表所示:
回答下列问题:
(1)滤渣1的主要成分是___________ (填化学式)。“氧化”步骤除氧化 外还氧化
外还氧化___________ (填微粒符号)。
(2)“调pH”中发生反应的总离子方程式为___________ 。“调pH”最低为___________ 。
(3)“系列操作”是___________ 、___________ 、过滤、洗涤、干燥等。
(4) 的作用是
的作用是___________ (用化学方程式表示)。
(5)合成产品时要隔离空气,在下列___________(填标号)气氛中加热。
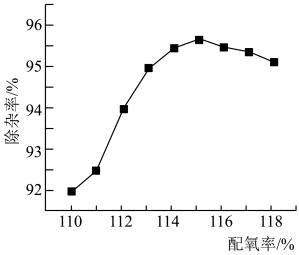
(6)工业生产中,氧化剂的实际用量和理论计算量之间的比值称为配氧率。如图是“氧化”中除杂率与配氧率关系。配氧率选择115时除杂率最高的原因是___________ 。
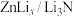 。该小组以废旧锌锰电池为原料合成
。该小组以废旧锌锰电池为原料合成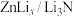 ,简易流程如下:
,简易流程如下: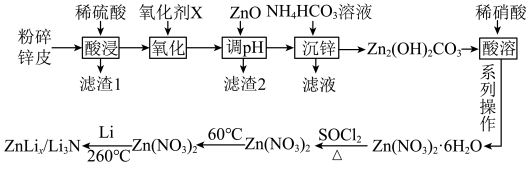
 、Fe、
、Fe、 等)。
等)。②
 在酸性条件下转化成
在酸性条件下转化成 和
和 ;
; 的沸点为78.8℃。
的沸点为78.8℃。③已知几种金属离子沉淀的pH如表所示:
| 金属氢氧化物 |  |  |  |  |
| 开始沉淀的pH | 2.7 | 7.6 | 8.1 | 6.2 |
| 完全沉淀的pH | 3.7 | 9.6 | 10.1 | 8.2 |
(1)滤渣1的主要成分是
 外还氧化
外还氧化(2)“调pH”中发生反应的总离子方程式为
(3)“系列操作”是
(4)
 的作用是
的作用是(5)合成产品时要隔离空气,在下列___________(填标号)气氛中加热。
A. | B. | C.Ar | D. |
(6)工业生产中,氧化剂的实际用量和理论计算量之间的比值称为配氧率。如图是“氧化”中除杂率与配氧率关系。配氧率选择115时除杂率最高的原因是
您最近一年使用:0次
解题方法
6 . 铬酰氯( )常作有机合成的氯化剂。它的部分性质如下表所示:
)常作有机合成的氯化剂。它的部分性质如下表所示:
某小组设计如图装置利用 和HCl迅速反应制备铬酰氯。
和HCl迅速反应制备铬酰氯。
(1)装浓盐酸的仪器名称是___________ ,B装置作用是___________ 。
(2)A中可能看到的现象是___________ ,利用浓硫酸的性质是___________ 。
(3)C中反应的化学方程式是___________ 。
(4)有人认为,E装置可以用盛装NaOH溶液的洗气瓶替代,是否合理:___________ (填“是”或“否”),请解释原因:___________ 。
(5)利用如图装置测定铬酰氯中氯元素含量(杂质不参与反应)。 溶液,过滤,用稀硝酸酸化滤液,再加入
溶液,过滤,用稀硝酸酸化滤液,再加入 溶液,最后用
溶液,最后用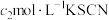 溶液滴定过量的
溶液滴定过量的 ,消耗溶液
,消耗溶液 。
。
该样品中氯元素质量分数为___________ 。如果滴定管没有润洗,测得结果会___________ (填“偏高”“偏低”或“无影响”)。
已知:常温下, ,
,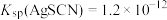 ,
,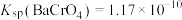 。
。
 )常作有机合成的氯化剂。它的部分性质如下表所示:
)常作有机合成的氯化剂。它的部分性质如下表所示:| 物理性质 | 化学性质 |
| 熔点:-96.5℃,沸点:117℃ | 放置在空气中会迅速挥发并水解 |
 和HCl迅速反应制备铬酰氯。
和HCl迅速反应制备铬酰氯。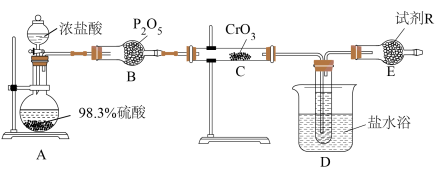
(1)装浓盐酸的仪器名称是
(2)A中可能看到的现象是
(3)C中反应的化学方程式是
(4)有人认为,E装置可以用盛装NaOH溶液的洗气瓶替代,是否合理:
(5)利用如图装置测定铬酰氯中氯元素含量(杂质不参与反应)。
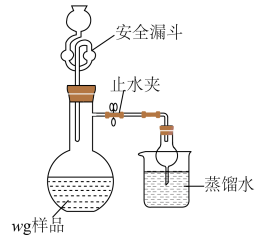
 溶液,过滤,用稀硝酸酸化滤液,再加入
溶液,过滤,用稀硝酸酸化滤液,再加入 溶液,最后用
溶液,最后用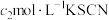 溶液滴定过量的
溶液滴定过量的 ,消耗溶液
,消耗溶液 。
。该样品中氯元素质量分数为
已知:常温下,
 ,
,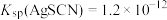 ,
,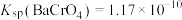 。
。
您最近一年使用:0次
解题方法
7 . 甲醇( )作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。以
)作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。以 为催化剂在水溶液中电催化二氧化碳还原为
为催化剂在水溶液中电催化二氧化碳还原为 和
和 的能量变化如图所示:
的能量变化如图所示:
 )作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。以
)作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。以 为催化剂在水溶液中电催化二氧化碳还原为
为催化剂在水溶液中电催化二氧化碳还原为 和
和 的能量变化如图所示:
的能量变化如图所示: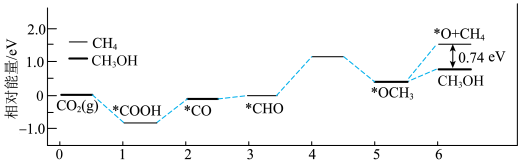
A.生成甲醇反应的决速步为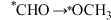 |
| B.两反应只涉及极性键的断裂和生成 |
| C.通过上图分析:甲烷比甲醇稳定 |
D.用 作催化剂可提高甲醇的选择性 作催化剂可提高甲醇的选择性 |
您最近一年使用:0次
8 . 铌镍合金材料在生产中有广泛应用,它的晶胞如图所示。已知: 为阿伏加德罗常数的值,铌(Nb)和钒位于同族且与钒相邻,但是基态Nb原子最外层只有1个电子。下列叙述正确的是
为阿伏加德罗常数的值,铌(Nb)和钒位于同族且与钒相邻,但是基态Nb原子最外层只有1个电子。下列叙述正确的是
 为阿伏加德罗常数的值,铌(Nb)和钒位于同族且与钒相邻,但是基态Nb原子最外层只有1个电子。下列叙述正确的是
为阿伏加德罗常数的值,铌(Nb)和钒位于同族且与钒相邻,但是基态Nb原子最外层只有1个电子。下列叙述正确的是
A.基态Nb原子价层电子排布式为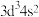 |
| B.镍、铌元素都位于周期表ds区 |
| C.晶胞中Nb、Ni原子数之比为3:1 |
D.晶体密度为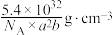 |
您最近一年使用:0次
解题方法
9 . 其他条件不变时,向1L刚性密闭容器中充入 。假定只发生下列三个反应:
。假定只发生下列三个反应:
①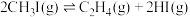

②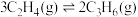

③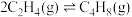

体系中 、
、 、
、 所占物质的量分数与温度关系如图所示:
所占物质的量分数与温度关系如图所示:
 。假定只发生下列三个反应:
。假定只发生下列三个反应:①
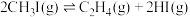

②
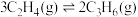

③
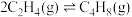

体系中
 、
、 、
、 所占物质的量分数与温度关系如图所示:
所占物质的量分数与温度关系如图所示: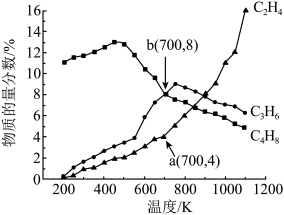
A.根据图像可判断: , , |
| B.升温,反应②和③只向正反应方向移动 |
C.700K时, 转化率为80% 转化率为80% |
D.若700K时反应①处于平衡状态,则其物质的量分数平衡常数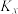 为6.4 为6.4 |
您最近一年使用:0次
10 . 近日,中科院上海硅酸盐研究所施剑林团队报道了MnOOH催化谷胱甘肽自氧化产生活性氧。某小组以菱锰矿(主要成分为 ,含少量
,含少量 、FeO、CoO、
、FeO、CoO、 、
、 等)为原料制备高纯度MnOOH,流程如下:
等)为原料制备高纯度MnOOH,流程如下:
②几种金属离子沉淀的pH如表所示:
下列叙述正确的是
 ,含少量
,含少量 、FeO、CoO、
、FeO、CoO、 、
、 等)为原料制备高纯度MnOOH,流程如下:
等)为原料制备高纯度MnOOH,流程如下: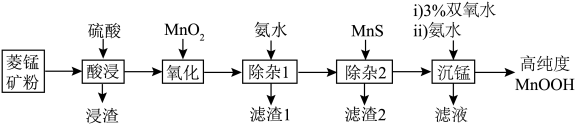
②几种金属离子沉淀的pH如表所示:
| 金属氢氧化物 |  |  |  |  |  |
| 开始沉淀的pH | 2.7 | 7.6 | 4.0 | 7.6 | 8.1 |
| 完全沉淀的pH | 3.7 | 9.6 | 5.2 | 9.2 | 10.1 |
A.滤渣1的成分是 和 和 |
B.“氧化”反应的离子方程式为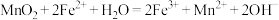 |
C.“除杂2”的原理是 |
D.双氧水氧化 ,滤液一定显酸性 ,滤液一定显酸性 |
您最近一年使用:0次



