名校
解题方法
1 . 某同学在实验室模拟工业制备H2SO4,再用制得的浓H2SO4制备C2H4气体,并设计实验检验气体产物。
Ⅰ.制备H2SO4的重要一步是制SO3(熔点:16.8℃,沸点:44.8℃)
某同学在实验室中根据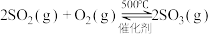 ,设计如图1所示实验装置来制备SO3固体。回答下列问题:
,设计如图1所示实验装置来制备SO3固体。回答下列问题:______ ;A装置中加入Na2SO3固体的同时,还需加几滴水,然后再滴加浓硫酸。加几滴水的作用是____________________ 。
②装置D盛放的是______ 溶液,其作用是____________________ 。
③实验开始时的操作顺序为______ 。(选填“a”或“b”)
a.先点燃E处的酒精灯后将混合气体通入E。
b.先将混合气体通入E后点燃E处的酒精灯。
Ⅱ.制取乙烯
图2是实验室制乙烯的发生装置,根据图示回答下列问题:____________________ 。操作中应迅速升温至______ ℃。
(3)反应前在②中放入几块碎瓷片的目的是____________________ 。
Ⅲ.检验产物
(4)为检验上述实验收集到的产物,该小组同学进行了如下实验并得出相应结论。
实验①~③中的结论不合理的是______ (填序号),原因是____________________ 。
Ⅰ.制备H2SO4的重要一步是制SO3(熔点:16.8℃,沸点:44.8℃)
某同学在实验室中根据
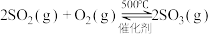 ,设计如图1所示实验装置来制备SO3固体。回答下列问题:
,设计如图1所示实验装置来制备SO3固体。回答下列问题: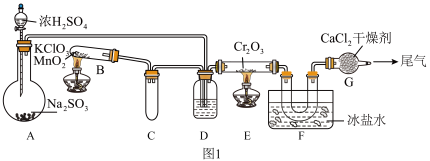
②装置D盛放的是
③实验开始时的操作顺序为
a.先点燃E处的酒精灯后将混合气体通入E。
b.先将混合气体通入E后点燃E处的酒精灯。
Ⅱ.制取乙烯
图2是实验室制乙烯的发生装置,根据图示回答下列问题:

(3)反应前在②中放入几块碎瓷片的目的是
Ⅲ.检验产物
(4)为检验上述实验收集到的产物,该小组同学进行了如下实验并得出相应结论。
实验序号 | 检验试剂和反应条件 | 现象 | 结论 |
① | 酸性KMnO4溶液 | 紫红色褪去 | 产物含有乙烯 |
② | 澄清 | 变浑浊 | 产物含有CO2 |
③ | 通过品红溶液 | 红色褪去 | 产物含有SO2 |
您最近一年使用:0次
名校
2 . 回答下列问题
(1)基态Cu的价电子排布式为______ 。 是一种配离子,中心离子的配位数为
是一种配离子,中心离子的配位数为______ ,配体为______ ,配位体所含元素中,电负性最大的是______ ,第一电离能最大的元素是______ 。
(2) 中心原子的价层电子对数目为
中心原子的价层电子对数目为______ ;叠氮酸根 的几何构型为
的几何构型为______ 。
(3)对羟基苯甲醛( )的沸点明显高于邻羟基苯甲醛(
)的沸点明显高于邻羟基苯甲醛( )的沸点,主要原因是
)的沸点,主要原因是______ 。
(4)BaCO3、CaCO3都属于离子晶体,它们的分解反应均属于吸热反应,热分解的能量关系如下(M=Mg或Ca或Ba):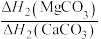
______ 1(选填“>”、“<”或“=”,下同);
②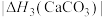
______ 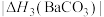 。
。
(5)二硒键、二硫键是重要的光响应动态共价键。在光照条件下,含二硒键(-Se-Se-)、二硫键(-S-S-)的化合物可以发生共价交换反应,其光响应原理可用如图表示,则图中实现光响应的最大波长:
______  (选填“>”或“<”或“=”),其原因是
(选填“>”或“<”或“=”),其原因是______ 。______ 。
②阿伏加德罗常数的值为 ,该晶体的摩尔体积为
,该晶体的摩尔体积为______  (列出计算式)。
(列出计算式)。
(1)基态Cu的价电子排布式为
 是一种配离子,中心离子的配位数为
是一种配离子,中心离子的配位数为(2)
 中心原子的价层电子对数目为
中心原子的价层电子对数目为 的几何构型为
的几何构型为(3)对羟基苯甲醛(
 )的沸点明显高于邻羟基苯甲醛(
)的沸点明显高于邻羟基苯甲醛( )的沸点,主要原因是
)的沸点,主要原因是(4)BaCO3、CaCO3都属于离子晶体,它们的分解反应均属于吸热反应,热分解的能量关系如下(M=Mg或Ca或Ba):

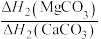
②
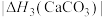
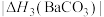 。
。(5)二硒键、二硫键是重要的光响应动态共价键。在光照条件下,含二硒键(-Se-Se-)、二硫键(-S-S-)的化合物可以发生共价交换反应,其光响应原理可用如图表示,则图中实现光响应的最大波长:

 (选填“>”或“<”或“=”),其原因是
(选填“>”或“<”或“=”),其原因是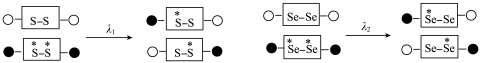
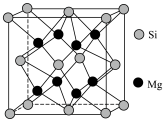
②阿伏加德罗常数的值为
 ,该晶体的摩尔体积为
,该晶体的摩尔体积为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
名校
解题方法
3 . 铜及其化合物在工业生产上有许多用途。某工厂以辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)为原料制备不溶于水的碱式碳酸铜的流程如图。
②
(1)加快“浸取”速率,除将辉铜矿粉碎外,还可采取的措施有______ 。(任写一种),除铁时溶液的pH值调控范围为:______ 。
(2)滤渣Ⅰ中的主要成分是MnO2、S、SiO2,请写出“浸取”反应中生成S单质的离子方程式:____________________ 。
(3)常温下“除铁”时加入的试剂A可用______ ,若加A后溶液的pH调为5,则溶液中 的浓度为
的浓度为______  。
。
(4)沉锰的离子方程式为:____________________ 。滤液Ⅱ经蒸发结晶得到的盐主要是______ 。(写化学式)
(5)过滤Ⅱ得到的沉淀经过洗涤、干燥可以得到碱式碳酸铜,判断沉淀是否洗净的操作是______ 。
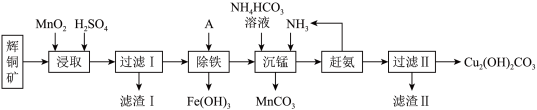
金属离子 |
|
|
|
|
开始沉淀 | 7.5 | 2.7 | 5.6 | 8.3 |
完全沉淀 | 9.0 | 3.7 | 6.7 | 9.8 |

(1)加快“浸取”速率,除将辉铜矿粉碎外,还可采取的措施有
(2)滤渣Ⅰ中的主要成分是MnO2、S、SiO2,请写出“浸取”反应中生成S单质的离子方程式:
(3)常温下“除铁”时加入的试剂A可用
 的浓度为
的浓度为 。
。(4)沉锰的离子方程式为:
(5)过滤Ⅱ得到的沉淀经过洗涤、干燥可以得到碱式碳酸铜,判断沉淀是否洗净的操作是
您最近一年使用:0次
名校
4 . 利用CH4与CO2进行催化重整,对温室气体的减排具有重要意义,催化重整时发生的反应: ,得到合成气(CO和H2),为化工生产提供了廉价原料,同时,CH4、CO2的资源化利用也是实现“碳达峰”、“碳中和”的有效措施。请结合题意,回答下列问题:
,得到合成气(CO和H2),为化工生产提供了廉价原料,同时,CH4、CO2的资源化利用也是实现“碳达峰”、“碳中和”的有效措施。请结合题意,回答下列问题:
(1)已知: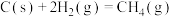
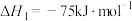

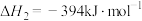
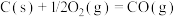
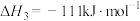
催化重整反应 的
的
______  。
。
(2)某温度下,向1 L的密闭容器中充入0.2 mol CH4与0.2 mol CO2,发生 催化重整反应,
催化重整反应, ;10 min时达到平衡,测得平衡混合物中CH4(g)的体积分数为12.5%,则CO2的平衡转化率为
;10 min时达到平衡,测得平衡混合物中CH4(g)的体积分数为12.5%,则CO2的平衡转化率为______ ;用H2表示的反应速率为______  。
。
(3)已知:常温下CH3COOH的电离常数 。常温下,在三元弱酸H3R的水溶液中H3R、
。常温下,在三元弱酸H3R的水溶液中H3R、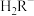 、
、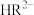 、
、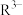 的分布分数δ(含R元素微粒占全部含R粒子的物质的量分数)随pH的变化如下图所示,其三级电离常数分别表示为:
的分布分数δ(含R元素微粒占全部含R粒子的物质的量分数)随pH的变化如下图所示,其三级电离常数分别表示为: 、
、 、
、 。则:Na2HR溶液显
。则:Na2HR溶液显______ 性(选填“酸”或“碱”或“中”),常温下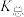 的数量级为
的数量级为______ 。 (
( 、
、 、
、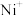 等)与O3反应可得
等)与O3反应可得 。
。 与CH4反应能高选择性地生成甲醇。总反应为:
与CH4反应能高选择性地生成甲醇。总反应为: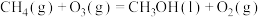 ;
;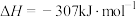 。分别在300K和310K下(其他反应条件相同)进行反应
。分别在300K和310K下(其他反应条件相同)进行反应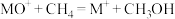 ,结果如下图(见下图1)所示。图中300K的曲线是
,结果如下图(见下图1)所示。图中300K的曲线是______ (填“a”或“b”)。300K、60 s时 的转化率为
的转化率为______ (列出算式)。 、
、 和
和 在水中达沉淀溶解平衡时的
在水中达沉淀溶解平衡时的 关系图(见上图2)(
关系图(见上图2)(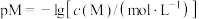 ;
; 可认为
可认为 离子沉淀完全)。则:
离子沉淀完全)。则:
______ 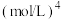 。
。
 ,得到合成气(CO和H2),为化工生产提供了廉价原料,同时,CH4、CO2的资源化利用也是实现“碳达峰”、“碳中和”的有效措施。请结合题意,回答下列问题:
,得到合成气(CO和H2),为化工生产提供了廉价原料,同时,CH4、CO2的资源化利用也是实现“碳达峰”、“碳中和”的有效措施。请结合题意,回答下列问题:(1)已知:
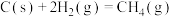
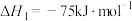

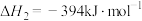
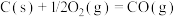
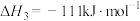
催化重整反应
 的
的
 。
。(2)某温度下,向1 L的密闭容器中充入0.2 mol CH4与0.2 mol CO2,发生
 催化重整反应,
催化重整反应, ;10 min时达到平衡,测得平衡混合物中CH4(g)的体积分数为12.5%,则CO2的平衡转化率为
;10 min时达到平衡,测得平衡混合物中CH4(g)的体积分数为12.5%,则CO2的平衡转化率为 。
。(3)已知:常温下CH3COOH的电离常数
 。常温下,在三元弱酸H3R的水溶液中H3R、
。常温下,在三元弱酸H3R的水溶液中H3R、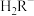 、
、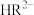 、
、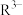 的分布分数δ(含R元素微粒占全部含R粒子的物质的量分数)随pH的变化如下图所示,其三级电离常数分别表示为:
的分布分数δ(含R元素微粒占全部含R粒子的物质的量分数)随pH的变化如下图所示,其三级电离常数分别表示为: 、
、 、
、 。则:Na2HR溶液显
。则:Na2HR溶液显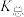 的数量级为
的数量级为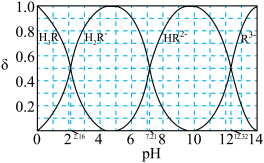
 (
( 、
、 、
、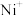 等)与O3反应可得
等)与O3反应可得 。
。 与CH4反应能高选择性地生成甲醇。总反应为:
与CH4反应能高选择性地生成甲醇。总反应为: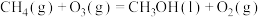 ;
;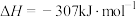 。分别在300K和310K下(其他反应条件相同)进行反应
。分别在300K和310K下(其他反应条件相同)进行反应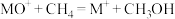 ,结果如下图(见下图1)所示。图中300K的曲线是
,结果如下图(见下图1)所示。图中300K的曲线是 的转化率为
的转化率为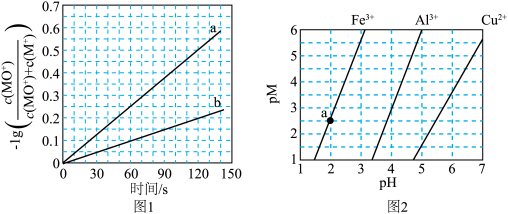
 、
、 和
和 在水中达沉淀溶解平衡时的
在水中达沉淀溶解平衡时的 关系图(见上图2)(
关系图(见上图2)(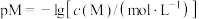 ;
; 可认为
可认为 离子沉淀完全)。则:
离子沉淀完全)。则:
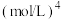 。
。
您最近一年使用:0次
名校
5 . 科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z为同一短周期元素,Z核外最外层电子数是X核外电子数的一半。下列叙述正确的是
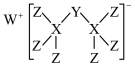
| A.WZ属于离子化合物,其水溶液呈碱性,图中阴离子含非极性键 |
| B.元素X、Y、Z的非金属性顺序为:X>Y>Z |
| C.Y的最高价氧化物的水化物是强酸 |
| D.该化合物中Y原子的价层满足8电子稳定结构 |
您最近一年使用:0次
名校
6 . 图(Ⅰ)和图(Ⅱ)分别为二元酸H2A和乙二胺(H2NCH2CH2NH2)溶液中各微粒的百分含量δ(即物质的量百分数)随溶液pH的变化曲线(25℃)。下列说法正确的是

| A.[H3NCH2CH2NH3]A溶液显碱性 |
B.[H3NCH2CH2NH2]HA溶液中存在关系式: 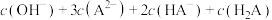 |
C.[H3NCH2CH2NH2][HA]溶液中各离子浓度大小关系为: |
D.向[H3NCH2CH2NH2][HA]溶液中通入一定量的HCl气体,则 可能增大也可能减小 可能增大也可能减小 |
您最近一年使用:0次
名校
7 . 工业上,从有机催化剂(主要含钴和锌)回收金属的简易流程如下:
(1)“灼烧”的目的是___________ 。“酸浸”时加入稀硫酸,浸出液含有 、
、 、
、 、
、 、
、 等,检验
等,检验 的试剂是
的试剂是___________ (填化学式)。
(2)“净化”中加入 ,生成
,生成 和
和 。书写离子方程式:
。书写离子方程式:___________ 。
(3) (已知其中硫为+6价)中含
(已知其中硫为+6价)中含___________ mol过氧键 ,“沉钴”中加入
,“沉钴”中加入 ,还原产物为
,还原产物为 。
。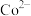 转化成
转化成 ,理论上消耗
,理论上消耗___________ mol 。
。
(4)“沉钴”的 不能太高,原因是
不能太高,原因是___________ 。
(5)“沉锌”加入 ,反应的离子方程式为
,反应的离子方程式为___________ ;沉锌的温度不能太高,原因是___________ 。
(6)“沉钴”中, 时
时 的数量级为
的数量级为___________ 。

(1)“灼烧”的目的是
 、
、 、
、 、
、 、
、 等,检验
等,检验 的试剂是
的试剂是(2)“净化”中加入
 ,生成
,生成 和
和 。书写离子方程式:
。书写离子方程式:(3)
 (已知其中硫为+6价)中含
(已知其中硫为+6价)中含 ,“沉钴”中加入
,“沉钴”中加入 ,还原产物为
,还原产物为 。
。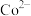 转化成
转化成 ,理论上消耗
,理论上消耗 。
。(4)“沉钴”的
 不能太高,原因是
不能太高,原因是(5)“沉锌”加入
 ,反应的离子方程式为
,反应的离子方程式为(6)“沉钴”中,
 时
时 的数量级为
的数量级为
您最近一年使用:0次
8 . 藿香蓟具有清热解毒功效,其有效成分结构如下。下列有关该物质的说法错误的是

| A.可以和NaOH溶液发生反应 | B.有四种不同的官能团 |
| C.可以使酸性高锰酸钾溶液和溴水褪色 | D.分子中所有碳原子不可能共面 |
您最近一年使用:0次
名校
9 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.25℃,101 kPa下,28 L氢气中质子的数目为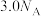 |
B.2.0 L 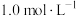 AlCl3溶液中, AlCl3溶液中, 的数目为 的数目为 |
C.0.20 mol苯甲酸(C7H6O2)充分燃烧,生成CO2的数目为 |
D.电解熔融CuCl2,阴极增重6.4 g,外电路中通过电子的数目为 |
您最近一年使用:0次
名校
10 . 化学与生产、生活密切相关,下列叙述错误的是
| A.浓硫酸具有强氧化性,不可用铁槽车储运浓硫酸 |
| B.通过红外光谱分析可以区分乙醇与乙酸乙酯 |
| C.二氧化硅在高温下用焦炭还原可制得粗硅 |
| D.太阳能在催化剂参与下分解水制氢是把光能转化为化学能的绿色化学方法 |
您最近一年使用:0次

 溶液
溶液


