名校
解题方法
1 . 下列离子方程式正确的是
A.用过量的 溶液吸收 溶液吸收 尾气: 尾气: |
B.铜丝插入浓硫酸中:Cu+H2SO4(浓)=Cu2++SO +H2↑ +H2↑ |
C.向 溶液中加过量的 溶液中加过量的 溶液并加热: 溶液并加热: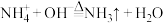 |
D.Fe溶于足量稀 : :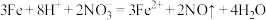 |
您最近一年使用:0次
名校
解题方法
2 . 化学与生产、生活息息相关,下列叙述正确的是
| A.SO2有毒,故不能作食品添加剂 |
| B.医疗上,BaCO3可用作消化系统X射线检查的内服药剂 |
| C.浓硫酸具有很强的吸水性,可用来干燥氨气 |
| D.NH3沸点低,易液化,工业上常用液氨作制冷剂 |
您最近一年使用:0次
解题方法
3 . 下列对硅及其化合物的有关叙述正确的是
| A.二氧化硅与烧碱溶液和氢氟酸均能反应,故其是两性氧化物 |
| B.晶体硅的化学性质不活泼,常温下不与任何物质发生反应 |
| C.硅酸钠的水溶液俗称水玻璃,可用作黏合剂和防火剂 |
| D.氮化硅熔点高,硬度大,可导电,化学性质稳定,是优异的非金属材料 |
您最近一年使用:0次
解题方法
4 . 某化学反应中的能量变化如图所示。下列说法正确的是
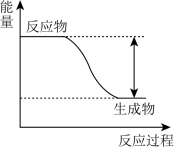
| A.该反应一定可以设计成原电池 |
| B.该反应不需要加热就一定可以发生 |
| C.该图像可以表示中和反应的能量变化 |
| D.反应中断键吸收的能量大于形成化学键放出的能量 |
您最近一年使用:0次
5 . 氮氧化物是主要的大气污染物之一,可用一氧化碳或活性炭还原氮氧化物,减少大气污染。回答下列问题:
(1)一定条件下,CO与NO反应生成两种无污染的气体,反应的化学方程式为2CO(g)+2NO(g)=N2(g)+2CO2(g),生成1mol N2(g),转移电子的物质的量为___________ mol,为提高该反应的化学反应速率,下列措施可行的是 ___________ (填字母)。
A.压缩容器体积 B.降低温度 C.使用合适催化剂 D.恒温恒容充入稀有气体
(2)两个10L的密闭容器中分别都加入活性炭(足量)和1.0mol NO,发生反应:C(s)+2NO(g)=N2(g)+CO2(g)。实验测得,两容器中在不同温度下NO和N2的物质的量变化见下表:
①T1℃时,0~5min内,反应速率v(CO2)=___________ mol•L-1•min-1。
②T2℃时,按表中数据,反应一定达到化学平衡状态的时间段是___________ min~10min,此时,容器中CO2的物质的量浓度是___________ mol•L-1,NO的平衡转化率为___________ 。
③两容器中温度关系为T1___________ (填“>”“<”或“=”)T2。
(1)一定条件下,CO与NO反应生成两种无污染的气体,反应的化学方程式为2CO(g)+2NO(g)=N2(g)+2CO2(g),生成1mol N2(g),转移电子的物质的量为
A.压缩容器体积 B.降低温度 C.使用合适催化剂 D.恒温恒容充入稀有气体
(2)两个10L的密闭容器中分别都加入活性炭(足量)和1.0mol NO,发生反应:C(s)+2NO(g)=N2(g)+CO2(g)。实验测得,两容器中在不同温度下NO和N2的物质的量变化见下表:
| 物质的量/mol | 容器1(T1/℃) | 容器2(T2/℃) | |||||||
| 0 | 5min | 9min | 10min | 12min | 0 | 5min | 9min | 10min | |
| NO | 1.0 | 0.58 | 0.42 | 0.40 | 0.40 | 1.0 | 0.50 | 0.34 | 0.34 |
| N2 | 0 | 0.21 | 0.29 | 0.30 | 0.30 | 0 | 0.25 | 0.33 | 0.33 |
②T2℃时,按表中数据,反应一定达到化学平衡状态的时间段是
③两容器中温度关系为T1
您最近一年使用:0次
6 . NA表示阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,11.2LSO2含质子数为16NA |
| B.1molN2与3molH2充分反应,生成NH3分子数目为2NA |
| C.64gCu与足量浓硫酸反应,被还原H2SO4数目为2NA |
| D.1molNH4HCO3与足量NaOH溶液充分反应,消耗OH﹣的数目为NA |
您最近一年使用:0次
解题方法
7 . 电池在日常生活中使用越来越广泛。回答下列问题:
(1)燃料电池是一种高效、环境友好的供电装置,如图为氢氧燃料电池的工作原理示意图,a、b均为惰性电极。___________ (填“A”或“B”)口通入。
②b极的电极反应式为___________ 。
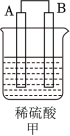
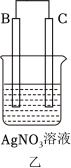
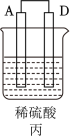
(2) A、B、C、D四种金属按下表中装置进行实验。
①装置甲溶液中的阴离子移向 ___________ (填“A”或“B”)极。
②装置乙中正极的电极反应式为___________ 。
③四种金属活动性由强到弱的顺序是___________ 。
(3)锌电池有望代替铅蓄电池,它的构成材料是锌、空气、某种电解质溶液,发生的总反应方程式是2Zn+O2=2ZnO。则该电池的负极材料是___________ ;当导线中有0.4mol电子通过时,理论上消耗的O2在标准状况下的体积是 ___________ L。
(1)燃料电池是一种高效、环境友好的供电装置,如图为氢氧燃料电池的工作原理示意图,a、b均为惰性电极。
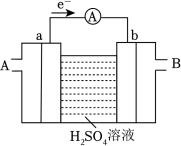
②b极的电极反应式为
(2) A、B、C、D四种金属按下表中装置进行实验。
| 装置 |
|
|
|
| 现象 | B表面产生气泡 | C质量增加 | D极不断溶解 |
②装置乙中正极的电极反应式为
③四种金属活动性由强到弱的顺序是
(3)锌电池有望代替铅蓄电池,它的构成材料是锌、空气、某种电解质溶液,发生的总反应方程式是2Zn+O2=2ZnO。则该电池的负极材料是
您最近一年使用:0次
解题方法
8 . 利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系。回答下列问题:___________ (填“只有氧化性”“只有还原性”或“既有氧化性又有还原性”)。
(2)实验室通常用Na2SO3与Z反应制取气体Y,反应的化学方程式为___________ 。将Y通入紫色石蕊试液中,可观察到的现象是 ___________ 。
(3)若将Y与Cl2按体积比1:1通入水中,充分振荡,再将所得溶液滴入品红试液,品红溶液___________ (填“褪色”或“不褪色”),理由是___________ 。
(4)工业上由S制取Z时,一般分三步:①由S生成Y;②由Y生成SO3;③由SO3生成Z,写出步骤②反应的化学方程式:___________ ,步骤③应用 ___________ (填试剂)吸收SO3。
(5)Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是 ___________(填字母)。

(2)实验室通常用Na2SO3与Z反应制取气体Y,反应的化学方程式为
(3)若将Y与Cl2按体积比1:1通入水中,充分振荡,再将所得溶液滴入品红试液,品红溶液
(4)工业上由S制取Z时,一般分三步:①由S生成Y;②由Y生成SO3;③由SO3生成Z,写出步骤②反应的化学方程式:
(5)Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是 ___________(填字母)。
| A.Na2S+S | B.Na2SO3+S | C.SO2+Na2SO4 | D.Na2SO3+Na2SO4 |
您最近一年使用:0次
解题方法
9 . 食品添加剂的使用满足了人们对食品多样化的需求.下列食品添加剂与化学反应速率有关的是
| 选项 | 食品添加剂 | 添加剂分类 |
| A | 食品中添加味精 | 增味剂 |
| B | 水果罐头中添加维生素C | 抗氧化剂 |
| C | 制造豆腐时添加葡萄糖酸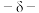 内酯 内酯 | 凝固剂 |
| D | 奶粉中添加硫酸亚铁和硫酸锌 | 营养强化剂 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 在一定条件下,氯酸钾和碘按下式发生反应:2KClO3+I2=2KIO3+Cl2,由此推断下列相应的结论不正确的是
| A.氧化性I2>Cl2 | B.该反应中Cl2是还原产物 |
| C.KClO3中Cl元素的化合价为+5 | D.KClO3是氧化剂 |
您最近一年使用:0次