名校
1 . 油酸甘油酯和硬脂酸甘油酯均是天然油脂的成分。它们的结构简式如图所示。
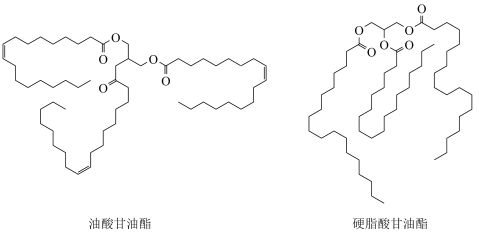
| A.油酸的分子式为C18H34O2 |
| B.1 mol油酸甘油酯与3 mol H2发生加成反应得到硬脂酸甘油酯 |
| C.天然油脂都能在NaOH溶液中发生取代反应 |
| D.将油酸甘油酯硬化可以降低其熔、沸点 |
您最近一年使用:0次
名校
解题方法
2 . 已知:①通常Br2与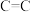 键可发生加成反应,但高温下,Br2易取代与
键可发生加成反应,但高温下,Br2易取代与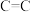 键直接相连的
键直接相连的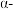 碳原子上的氢原子,如
碳原子上的氢原子,如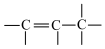
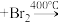
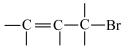
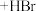 。②与苯环直接相连的支链碳原子上的氢原子也易被溴取代:
。②与苯环直接相连的支链碳原子上的氢原子也易被溴取代: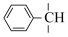
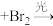
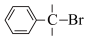
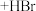 根据上述信息,结合所学知识,由丙苯(
根据上述信息,结合所学知识,由丙苯(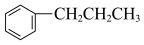 )制取1-苯基丙三醇(
)制取1-苯基丙三醇(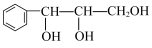 ),经历的化学反应类型依次为
),经历的化学反应类型依次为
| A.取代反应、消去反应、加成反应、加成反应、取代反应 |
| B.取代反应、消去反应、加成反应、取代反应、取代反应 |
| C.取代反应、加成反应、消去反应、加成反应、取代反应 |
| D.取代反应、消去反应、取代反应、加成反应、取代反应 |
您最近一年使用:0次
名校
3 . 根据如图所示装置 部分仪器已略去
部分仪器已略去 回答下列有关问题。
回答下列有关问题。

(1)实验甲在加热过程中能观察到产生白色沉淀的烧杯是___________ (填“Ⅰ”或“Ⅱ”),对应的试管中发生反应的化学方程式为___________ ;
(2)实验乙用来探究Na2O2与CO2的反应,观察到的实验现象为包有Na2O2的棉花燃烧。写出Na2O2与CO2反应的化学方程式,并用单线桥法标出电子转移的方向和数目:___________ ;
(3)取10g碳酸钠和碳酸氢钠的混合物充分加热,将生成的CO2气体通入足量的澄清石灰水中,测得生成沉淀的质量为4.0g。则原混合物中碳酸钠的质量分数为___________ 。
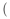 部分仪器已略去
部分仪器已略去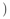 回答下列有关问题。
回答下列有关问题。 
(1)实验甲在加热过程中能观察到产生白色沉淀的烧杯是
(2)实验乙用来探究Na2O2与CO2的反应,观察到的实验现象为包有Na2O2的棉花燃烧。写出Na2O2与CO2反应的化学方程式,并用单线桥法标出电子转移的方向和数目:
(3)取10g碳酸钠和碳酸氢钠的混合物充分加热,将生成的CO2气体通入足量的澄清石灰水中,测得生成沉淀的质量为4.0g。则原混合物中碳酸钠的质量分数为
您最近一年使用:0次
名校
解题方法
4 . 已知某NaOH试样中含有NaCl杂质,为测定试样中NaOH的质量分数,进行如下实验:
①称量1.00g样品溶于水,配成250mL溶液;
②用碱式滴定管准确量取25.00mL所配溶液于锥形瓶中,滴加2~3滴酚酞溶液;
③用 的标准盐酸滴定并重复三次,每次实验数据记录如下:
的标准盐酸滴定并重复三次,每次实验数据记录如下:
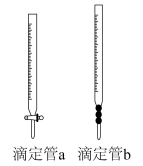
(1)盐酸溶液应装在如图滴定管___________ (填a或b)中。
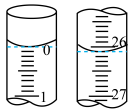
(2)若滴定开始和结束时,酸式滴定管中的液面如图所示所用盐酸的体积为___________ mL。
(3)①达到滴定终点的标志是___________ 。
②若出现下列情况,测定结果偏高的是___________ (填字母)。
a.滴定前用蒸馏水冲洗锥形瓶
b.滴定过程中振荡锥形瓶时不慎将瓶内溶液溅出
c.滴定过程中不慎将数滴盐酸滴在锥形瓶外
d.酸式滴定管在滴定前有气泡,滴定后气泡消失在上述实验中
(4)通过计算可知该烧碱样品的纯度为___________ 。
①称量1.00g样品溶于水,配成250mL溶液;
②用碱式滴定管准确量取25.00mL所配溶液于锥形瓶中,滴加2~3滴酚酞溶液;
③用
 的标准盐酸滴定并重复三次,每次实验数据记录如下:
的标准盐酸滴定并重复三次,每次实验数据记录如下:| 滴定序号 | 待测液体积/mL | 所消耗盐酸标准溶液的体积/mL | |
| 滴定前 | 滴定后 | ||
| 1 | 25.00 | 0.50 | 20.60 |
| 2 | 25.00 | 6.00 | 26.00 |
| 3 | 25.00 | 1.10 | 21.00 |
(1)盐酸溶液应装在如图滴定管

(2)若滴定开始和结束时,酸式滴定管中的液面如图所示所用盐酸的体积为

(3)①达到滴定终点的标志是
②若出现下列情况,测定结果偏高的是
a.滴定前用蒸馏水冲洗锥形瓶
b.滴定过程中振荡锥形瓶时不慎将瓶内溶液溅出
c.滴定过程中不慎将数滴盐酸滴在锥形瓶外
d.酸式滴定管在滴定前有气泡,滴定后气泡消失在上述实验中
(4)通过计算可知该烧碱样品的纯度为
您最近一年使用:0次
2023-11-22更新
|
244次组卷
|
2卷引用:重庆市长寿区八校联考2023-2024学年高二上学期1月期末化学试题
5 . 化学与生活息息相关,下列有关说法正确的是
| A.烟火五彩缤纷的颜色来自于不同金属元素的焰色 |
| B.二氧化硫有毒,严禁将其添加到任何食品和饮料中 |
| C.在元素周期表的副族元素中寻找半导体材料 |
| D.在医学检查中,重晶石和芒硝均可以用作钡餐 |
您最近一年使用:0次
名校
解题方法
6 . 已知稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,下列说法正确的是
| A.实验室中和反应反应热的测定,由Q=m·c·Δt算出的值即为中和反应的反应热 |
| B.1 mol H2SO4与足量的NaOH溶液反应,放出的热量为57.3kJ |
| C.稀盐酸与稀Ba(OH)2溶液反应生成1 mol H2O,放出的热量为57.3kJ |
| D.稀NaOH与98%浓硫酸反应生成1 mol H2O,放出的热量为57.3kJ |
您最近一年使用:0次
7 . 下列与化学反应能量变化相关的叙述正确的是
| A.焓变是指1 mol物质参加反应时的能量变化 |
| B.在一个化学反应中,当反应物总焓小于生成物的总焓时,ΔH为负值 |
| C.应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| D.同温同压下,H2(g) +Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH不同 |
您最近一年使用:0次
2023-08-31更新
|
266次组卷
|
2卷引用:重庆市长寿中学校2022-2023学年高二上学期10月期中考试化学试题
名校
8 . 下列各组物质性质的比较,结论正确的是
A.在水中的溶解度: |
B.溶液酸性: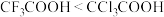 |
| C.晶体熔点:碳化硅<晶体硅 |
D.沸点: > > |
您最近一年使用:0次
名校
解题方法
9 . 葡酚酮是由葡萄籽提取的一种花青素类衍生物(结构简式如图)具有良好的抗氧化活性。下列关于葡酚酮叙述错误的是


| A.基态氧原子的电子有5种空间运动状态 |
| B.分子中含有两种杂化轨道类型的碳原子 |
| C.分子中含有2个手性碳原子 |
| D.该分子可形成分子间氢键 |
您最近一年使用:0次
2023-08-29更新
|
257次组卷
|
2卷引用:重庆市长寿中学校2022-2023学年高二下学期4月期中考试化学试题
名校
解题方法
10 . 已知:Q、R、X、Y、Z五种元素的原子序数依次递增,Z元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,其余均为短周期主族元素,Y原子价层电子排布式为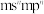 ,Q、X原子p轨道的电子数分别为2和4。下列说法中正确的是。
,Q、X原子p轨道的电子数分别为2和4。下列说法中正确的是。
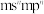 ,Q、X原子p轨道的电子数分别为2和4。下列说法中正确的是。
,Q、X原子p轨道的电子数分别为2和4。下列说法中正确的是。| A.元素的第一电离能:X>R>Q |
| B.Z位于元素周期表d区 |
| C.原子半径:Y>X>R>Q |
| D.Q、Y形成的最高价氧化物的水化物的酸性:Q>Y |
您最近一年使用:0次
2023-08-29更新
|
255次组卷
|
3卷引用:重庆市长寿中学校2022-2023学年高二下学期4月期中考试化学试题



