解题方法
1 . 下列各组实验操作规范,且能达到实验目的是


A.配制 的硫酸溶液 的硫酸溶液 | B.用乙醇萃取碘水中的碘单质 |
| C.检验乙醛中的醛基 | D.制备乙酸乙酯 |
您最近一年使用:0次
名校
解题方法
2 . 碳铂(结构简式如图)是一种广谱抗癌药物。下列关于碳铂的说法错误的是


| A.中心原子的配位数为4 | B. 和 和 杂化的碳原子数之比为 杂化的碳原子数之比为 |
C.分子中σ键与π键的数目之比为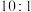 | D.分子中含有极性键、非极性键和配位键 |
您最近一年使用:0次
2024-02-10更新
|
215次组卷
|
7卷引用:山东省枣庄市2021-2022学年高三高考适应性练习(一)化学试题
山东省枣庄市2021-2022学年高三高考适应性练习(一)化学试题(已下线)微专题50 分子的立体结构的判断-备战2023年高考化学一轮复习考点微专题湖南省张家界市慈利县第一中学2022-2023学年高三上学期第四次月考化学试卷山东省淄博实验中学2022-2023学年高二下学期3月月考化学试题新疆乌鲁木齐市第六十八中学2023-2024学年高三上学期1月月考化学试题陕西省咸阳市实验中学2023-2024学年高二上学期段性检测(一)化学试题(已下线)3.4.1 配合物与超分子(基础)
名校
解题方法
3 . 下列物质的检验中,其结论一定正确的是
A.向某溶液中加入 溶液,产生白色沉淀,加入稀 溶液,产生白色沉淀,加入稀 后,白色沉淀不溶解,也无其他现象,说明原溶液中一定含有 后,白色沉淀不溶解,也无其他现象,说明原溶液中一定含有 |
B.向某溶液中加入盐酸产生无色气体,该气体能使澄清的石灰水变浑浊,说明该溶液中一定含有 或 或 |
C.取少量久置的 样品于试管中加水溶解,若加足量盐酸时有气体产生,再加 样品于试管中加水溶解,若加足量盐酸时有气体产生,再加 溶液时有白色沉淀产生,则说明 溶液时有白色沉淀产生,则说明 样品已部分被氧化 样品已部分被氧化 |
D.将某气体通入品红溶液中,品红溶液褪色,该气体一定是 |
您最近一年使用:0次
2024-01-15更新
|
371次组卷
|
20卷引用:陕西省西安高级中学2021-2022学年高三第一次适应性考试化学试题
陕西省西安高级中学2021-2022学年高三第一次适应性考试化学试题陕西省西安高级中学2021-2022学年高三第一次适应性考试化学试题上海市十二校2016届高三3月联考化学试题江西省丰城市第九中学2022-2023学年高三上学期入学考化学试题2016届甘肃省兰州第一中学高三9月月考化学试卷2017届河北省望都中学高三8月月考化学试卷2017届天津一中高三上第一次月考化学试卷2017届甘肃省兰州一中高三上学期9月月考化学试卷甘肃省兰州市第二十七中学2022届高三上学期8月月考化学试题(已下线)5.1.2 硫酸、含硫化合物的相互转化——同步学习必备知识(已下线)第四章 非金属及其化合物 第21练 硫酸 含硫物质的转化西安市第八十三中学2022-2023学年高一下学期第一次月考化学试题(已下线)专题01 硫及其化合物的性质及转化(专题过关)-2022-2023学年高一化学下学期期中期末考点大串讲(人教版2019必修第二册)四川省达州市达川区2022-2023学年高一下学期4月期中考试化学试题江西省宜春市宜丰中学2022-2023学年高一下学期3月月考化学试题上海市上海中学2023-2024学年高一上学期期末考试化学试卷湖北省襄阳市第一中学2023-2024学年高一下学期3月月考化学试题天津市滨海新区田家炳中学2023-2024学年高一下学期第一次月考化学试题山东省济宁市微山县第二中学2023-2024学年高一下学期第一次月考化学试题河南省焦作市博爱县第一中学2023-2024学年高一下学期4月期中考试化学试题
11-12高一·广东惠州·阶段练习
4 . 日常生活中的许多现象与化学反应有关,下列现象与氧化还原反应无关的是
A.铜器出现铜绿 | B.铁制菜刀生锈 |
| C.大理石雕像被酸雨腐蚀毁坏 | D.铝锅表面生成致密的薄膜 |
您最近一年使用:0次
2023-10-13更新
|
355次组卷
|
84卷引用:必刷卷03-2022年高考化学考前信息必刷卷(山东专用)
(已下线)必刷卷03-2022年高考化学考前信息必刷卷(山东专用)【全国百强校】甘肃省静宁县第一中学2019届高三上学期第一次模拟考试化学试题(已下线)上海市闸北区2010届高三第二次模拟考试化学试题广东省湛江市2021-2022学年高一上学期期末调研考试化学试题(已下线)基础卷04-【新高考新题型】2022年高考化学选择题标准化练习20卷(山东专用)黑龙江省齐齐哈尔市恒昌中学校2022-2023学年高一上学期第一次月考化学试题河北省秦皇岛市青龙满族自治县2022-2023学年高一上学期10月月考化学试题重庆市大足中学2022-2023学年高一上学期第一次月考化学试题(已下线)2011-2012学年广东省惠阳高级中学高一第二次段考化学试卷(已下线)2012-2013学年辽宁朝阳县柳城高级中学高一上学期期末考试化学试卷(已下线)2012-2013学年福建省清流一中高一第三阶段试化学试卷2015-2016学年湖北省宜昌市葛洲坝中学高一上学期期中测试化学试卷2015-2016学年河北省唐山一中高一上第一次月考化学试卷2015-2016学年四川省雅安天全中学高一上学期11月月考化学试卷2015-2016学年安徽省合肥一中等三校高一上期末化学试卷2015-2016学年贵州省毕节地区大方一中高一上学期期末化学试卷2015-2016学年西藏日喀则高级中学高一下4月月考化学卷2016-2017学年湖北省宜昌市葛洲坝中学高一上期中化学卷2016-2017学年吉林长春十一高中等两校高一上期末化学卷河北省衡水市安平中学2017-2018学年高一上学期第三次月考化学试题1湖南省浏阳二中、五中、六中三校2017-2018学年高一期中联考化学试题浙江省温州市2018届高三上学期期中考试化学试题河北省邢台市第一中学2017-2018学年高一上学期第三次月考化学试题辽宁省辽阳2017-2018学年高一化学期末考试题(已下线)【艺体生百日捷进提升系列-技能方法】专题3.06 氧化还原反应方面试题的解题方法与技巧人教版2017-2018学年高一化学必修1:2.3 氧化还原反应 同步测试【全国百强校】河北省辛集中学2018-2019学年高一上学期期中考试化学试题【校级联考】湖南省浏阳市六校联考2018-2019学年高一上学期期中考试化学试题云南省玉溪市江川区第二中学2018-2019学年高一上学期期末考试化学试题云南省新平一中2018-2019学年高一6月月考化学试题云南省鹤庆三中2018-2019学年高一下学期期末考试化学试题江苏省苏州市吴江区汾湖中学2019-2020学年高一上学期第一次月考化学试题内蒙古包头市第四中学2019-2020学年高一上学期期中考试化学试题广西桂林市第十八中学2019-2020学年高二上学期期中考试化学(文)试题山西省长治市第二中学2019-2020学年高一上学期12月月考化学试题河北省秦皇岛市昌黎县第八中学2019-2020学年高一上学期12月月考化学考试题重庆市第三十中学2019-2020学年高一10月月考化学试题云南省玉溪市元江民族中学2019-2020学年高一12月月考化学试题云南省玉溪市元江县一中2019-2020学年高一12月月考化学试题广西隆林县第二中学2019-2020学年高一上学期期末考试化学试题河北省唐山遵化市2019-2020学年高一上学期期中考试化学试题新疆伊犁哈萨克自治州伊宁市第八中学2019-2020学年高一上学期期中考试化学试题(已下线)2.3.1 认识氧化还原反应 氧化剂和还原剂练习(2)——《高中新教材同步备课》(鲁科版 必修第一册)四川省自贡市旭川中学2020-2021学年高一上学期开学考试化学试题(已下线)1.3.1 氧化还原反应(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版2019必修第一册)(已下线)第二章 化学物质及其变化(基础过关)-2020-2021学年高一化学单元测试定心卷(人教版必修1)黑龙江省齐齐哈尔市第八中学2020-2021学年高一上学期9月月考化学试题浙江省诸暨中学2020-2021学年高一上学期10月阶段性考试化学(实验班)试题(已下线)2.3.1 氧化还原反应(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版)河北省元氏县第四中学2020-2021学年高一10月月考化学试题(已下线)【浙江新东方】1宁夏银川一中2020-2021学年高一上学期期中考试化学试题吉林省汪清县第六中学2021届高三第三次月考模拟化学试题北京市第一五九中学2020-2021学年高一上学期期中考试化学试题(已下线)【浙江新东方】双师(27)四川省广元市川师大万达中学2020-2021学年高一上学期期中考试化学试题广西壮族自治区桂林市七星区桂林市第十八中学2020-2021学年高一上学期期中考试化学试题(已下线)【浙江新东方】61河南省许昌市建安区第一高级中学2020-2021学年高一上学期阶段性测试(12月)化学试题吉林省通化市职教中心高中部2020-2021学年高一12月月考化学试题河北深州市长江中学2020-2021学年高一上学期第三次月考化学试题(已下线)【浙江新东方】在线化学 (17)(已下线)【浙江新东方】在线化学35湖南省武冈市第二中学2020-2021学年高一上学期第一次月考化学试题第1课时 氧化还原反应(课后)——课前、课中、课后同步专题精编(人教版2019必修第一册)辽宁省丹东市凤城市第一中学2021-2022学年高一上学期第一次月考化学试题贵州省毕节市威宁第四中学2021-2022学年高一上学期第一次月考化学试题浙江省绍兴鲁迅中学2021-2022学年高一上学期第一次限时训练化学试题江西省抚州市临川第一中学2021-2022学年高一上学期第一次月考化学试题吉林省长春市十一高中2021-2022学年高一上学期第一学程考试化学试题河南省新乡县龙泉高级中学2021-2022学年高一上学期9月月考化学试题(已下线)必考点04 氧化还原反应的本质和相关概念-【对点变式题】2021-2022学年高一化学上学期期中期末必考题精准练(人教版2019)广东省东莞市新世纪英才学校2021-2022学年高一上学期第一次教学质量检测化学试题新疆生产建设兵团第十师北屯高级中学2021-2022学年高一上学期10月月考化学试卷黑龙江省饶河县高级中学2021-2022学年高一上学期第一次月考化学试题甘肃省庆阳市第六中学2021-2022学年高一上学期期中考试化学试题宁夏银川市景博中学2021-2022学年高一上学期期中考试化学试题山东省济南市天桥区黄河双语实验学校2021-2022学年高一上学期期中考试化学试题山西省运城市高中联合体2019-2020高一上学期12月月考化学试题广东省清远市大坪镇大坪中学2020-2021学年高二上学期期中考试化学试题北京师范大学附属中学2023-2024学年高一上学期10月月考化学试题天津市五十七中学2023-2024高一上学期第一次月考化学试题福建省福州外国语学校2023-2024学年高一上学期期中考试化学试题北京市第一六一中学2023-2024学年高一上学期期中考试化学试题
5 . 某反应可有效降低汽车尾气污染物的排放,其反应热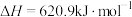 。一定条件下该反应经历三个基元反应阶段,反应历程如图所示(TS表示过渡态),下列说法正确的是( )
。一定条件下该反应经历三个基元反应阶段,反应历程如图所示(TS表示过渡态),下列说法正确的是( )
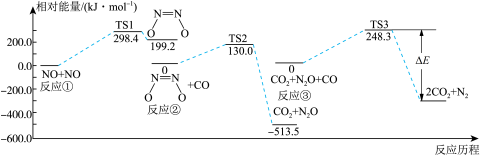
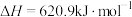 。一定条件下该反应经历三个基元反应阶段,反应历程如图所示(TS表示过渡态),下列说法正确的是( )
。一定条件下该反应经历三个基元反应阶段,反应历程如图所示(TS表示过渡态),下列说法正确的是( )
| A.三个基元反应中只有③是放热反应 |
| B.该化学反应的速率主要由反应②决定 |
C.该过程的总反应为 |
D. |
您最近一年使用:0次
2023-10-12更新
|
858次组卷
|
16卷引用:河南省平顶山市许昌市济源市2021-2022学年高三下学期3月第二次质量检测理科综合化学试题
河南省平顶山市许昌市济源市2021-2022学年高三下学期3月第二次质量检测理科综合化学试题(已下线)化学-2022年高考考前押题密卷(福建卷)河北省衡水中学2022-2023学年高三上学期四调考试化学试题(已下线)秘籍08 反应历程探究与催化原理图象分析-备战2022年高考化学抢分秘籍(全国通用)湖南省吉首市第一中学2022届高三下学期4月模拟预测考试化学试题(已下线)专项10 化学反应与能量-备战2022年高考化学阶段性新题精选专项特训(全国卷)(4月期)(已下线)专题07化学反应中的能量变化及反应机理-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题07化学反应中的能量变化及反应机理-五年(2018~2022)高考真题汇编(全国卷)(已下线)专题07化学反应中的能量变化及反应机理-2022年高考真题+模拟题汇编(全国卷)(已下线)专题07 化学反应中的能量变化及反应机理-三年(2020-2022)高考真题分项汇编(已下线)专题08 化学反应与能量-备战2023年高考化学母题题源解密(全国通用)福建省福州第三中学2022-2023学年高三第三次质量检测化学试题湖南省邵阳市第一中学2023届高三第七次月考化学试题陕西省西安市西北工业大学附属中学2023-2024学年高二上学期第一次月考化学试题广东省广州市第一一三中学2023-2024学年高二上学期第一次阶段性考试化学试题(已下线)题型10 反应微观机理分析 速率方程及其应用-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)
名校
解题方法
6 . NA表示阿伏加德罗常数的值。下列叙述正确的是
| A.标准状况下,11.2LCH3CH2OH中含有的分子数目为0.5NA |
| B.1molCl2通入足量水充分反应,转移的电子数为NA |
| C.1molHClO中所含H−Cl键为NA |
D.0.1L3mol⋅L﹣1NH4NO3溶液中含有的 数目小于0.3NA 数目小于0.3NA |
您最近一年使用:0次
2023-10-03更新
|
230次组卷
|
2卷引用:黑龙江省齐齐哈尔市2022届高三下学期三模考试化学试题
名校
7 . 铜是重要的过渡金属元素,铜被广泛应用于电子工业和航天领域中。回答下列问题:
(1)基态铜原子的核外电子排布式为___________ ,同周期与铜原子未成对电子数相同的p区元素原子为___________ (填符号)。
(2)向CuSO4溶液中滴加氨水可以得到1∶1型离子化合物,其阳离子结构如图所示,阴离子为正四面体结构。________ (填序号)。
A.离子键 B.极性键 C.非极性键 D.σ键 E.π键 F.配位键 G.氢键
②H2O与NH3中键角较大的是________ ,原因是________ 。
③该化合物加热时首先失去的组分是H2O,原因是________ 。
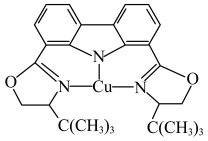
(3)我国科学家制取了一种铜的配合物如图所示,该配合物中四种非金属元素的第一电离能由大到小的顺序是_________ (填元素符号),配合物中sp2 杂化的碳原子与sp3 杂化的碳原子个数比为___________ 。___________ (用含r、ρ、NA的代数式表示)。
(1)基态铜原子的核外电子排布式为
(2)向CuSO4溶液中滴加氨水可以得到1∶1型离子化合物,其阳离子结构如图所示,阴离子为正四面体结构。

A.离子键 B.极性键 C.非极性键 D.σ键 E.π键 F.配位键 G.氢键
②H2O与NH3中键角较大的是
③该化合物加热时首先失去的组分是H2O,原因是
(3)我国科学家制取了一种铜的配合物如图所示,该配合物中四种非金属元素的第一电离能由大到小的顺序是

您最近一年使用:0次
名校
8 . 某小组利用含铅废料(主要含PbO、PbSO4和PbO2)制备化工产品三盐(PbSO4·3PbO·H2O)的工艺流程如图:
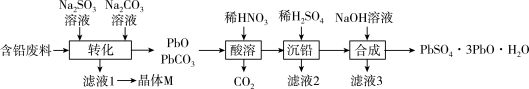
已知:Ksp(PbSO4)=1.82×10−8,Ksp(PbCO3)=1.46×10−13,Pb(OH)2具有两性,PbO2有强氧化性。请回答下列问题:
(1)结晶水合物M(M=322g/mol)的化学式为___________ 。
(2)“转化”中,加入Na2CO3目的是___________ ;Na2SO3溶液参加反应的离子反应方程式为___________ 。
(3)用一定浓度的稀硝酸进行“酸溶”时,金属离子浸出率与温度的关系如图所示。当温度为40℃,金属离子浸出率最高,其主要原因是___________ 。

(4)合成三盐的化学方程式为___________ ,解释“合成”需控制溶液的pH不能大于10的原因___________ 。
(5)取223 g含铅废料经上述“转化”,假设含铅废料中的PbO2和PbSO4全部转化成PbCO3,且PbO未发生反应,“酸溶”时共收集到4.48 L CO2(标准状况),“沉铅”完全时得到151.5 g PbSO4.则原含铅废料中PbO的质量分数为___________ 。
(6)工业上,可电解Pb(NO3)2溶液制备活性电极材料PbO2,其阳极的电极反应式为___________ 。

已知:Ksp(PbSO4)=1.82×10−8,Ksp(PbCO3)=1.46×10−13,Pb(OH)2具有两性,PbO2有强氧化性。请回答下列问题:
(1)结晶水合物M(M=322g/mol)的化学式为
(2)“转化”中,加入Na2CO3目的是
(3)用一定浓度的稀硝酸进行“酸溶”时,金属离子浸出率与温度的关系如图所示。当温度为40℃,金属离子浸出率最高,其主要原因是

(4)合成三盐的化学方程式为
(5)取223 g含铅废料经上述“转化”,假设含铅废料中的PbO2和PbSO4全部转化成PbCO3,且PbO未发生反应,“酸溶”时共收集到4.48 L CO2(标准状况),“沉铅”完全时得到151.5 g PbSO4.则原含铅废料中PbO的质量分数为
(6)工业上,可电解Pb(NO3)2溶液制备活性电极材料PbO2,其阳极的电极反应式为
您最近一年使用:0次
名校
9 . 2019年诺贝尔化学奖颁给在锂离子电池发展方面作出突出贡献的三位科学家。下面是最近研发的Ca-LiFePO4可充电电池的工作示意图,锂离子导体膜只允许Li+通过,电池反应为:xCa2++ 2LiFePO4  xCa + 2Li1-xFePO4+2x Li+下列说法正确的是
xCa + 2Li1-xFePO4+2x Li+下列说法正确的是
 xCa + 2Li1-xFePO4+2x Li+下列说法正确的是
xCa + 2Li1-xFePO4+2x Li+下列说法正确的是 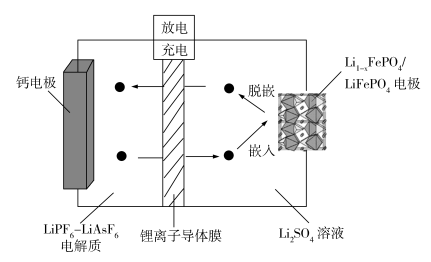
| A.放电时,负极反应为:LiFePO4-xe- =2Li1-xFePO4+xLi+ |
| B.充电时,Li1-xFePO/LiFePO4电极发生Li+嵌入,放电时发生Li+脱嵌 |
| C.放电时,当转移0.2 mol电子时,理论上左室中电解质的质量增重4.0 g |
| D.LiPF6-LiAsF6为非水电解质,其与Li2SO4溶液的主要作用都是传递离子 |
您最近一年使用:0次
名校
10 . 由下列实验及现象推出的相应结论正确的是
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 往Cu(OH)2沉淀中分别滴加盐酸和氨水 | 沉淀皆溶解 | Cu(OH)2为两性氢氧化物 |
| B | 将某气体通入品红溶液中 | 品红溶液褪色 | 该气体是SO2 |
| C | 相同温度下,同时往等体积的0.2 mol·L-1和0.05 mol·L-1的Na2S2O3溶液中滴加等浓度等体积的稀硫酸 | 0.2 mol·L-1的Na2S2O3溶液中先变浑浊 | 其他条件相同时,浓度越大,反应速率越快 |
| D | 将甲烷与氯气按体积比为1∶4混合于试管中,光照 | 反应后的混合气体能使湿润的石蕊试纸变红 | 生成的氯代甲烷有酸性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



