20-21高一·全国·课时练习
1 . 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系,下图是元素周期表的一部分, 回答下列问题:
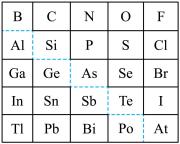
(1)元素Ga在元素周期表中的位置为:_______ ;
(2)Sn的最高正价为_______ ,Cl的最高价氧化物对应水化物的化学式为_______ ;
(3)根据元素周期律,推断
①阴影部分元素形成的氢化物中热稳定性最高的是_______ ;(写化学式)
②H3AsO4、H2SeO4的酸性强弱为:H3AsO4_______ H2SeO4 (填“>”、“<”、“=”或“无法比较”);
③氢化物的还原性:H2O_______ H2S (填“>”、“<”、“=”或“无法比较”);
④原子半径比较:N_______ Si (填“>”、“<”、“=”或“无法比较”)。

(1)元素Ga在元素周期表中的位置为:
(2)Sn的最高正价为
(3)根据元素周期律,推断
①阴影部分元素形成的氢化物中热稳定性最高的是
②H3AsO4、H2SeO4的酸性强弱为:H3AsO4
③氢化物的还原性:H2O
④原子半径比较:N
您最近一年使用:0次
2021-09-17更新
|
1208次组卷
|
5卷引用:人教必修第一册第4章第1节第4课时原子结构与元素的性质(课后)
(已下线)人教必修第一册第4章第1节第4课时原子结构与元素的性质(课后)(已下线)5.1.2 元素周期表 元素周期表的应用-2021-2022学年高一化学课后培优练(苏教版2019必修第一册)湖北省荆州市八县市2021-2022学年高一上学期期末质量检测化学试题(已下线)第四章 物质结构 元素周期律(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)(已下线)【知识图鉴】单元讲练测必修第一册第四单元02基础练
2 . X、Y、Z、M、Q、R是元素周期表前四周期的元素,且原子序数依次增大,其相关信息如表所示:
请回答下列问题。
(1)请写出元素Q的基态原子的价电子轨道表示式:______ 。
(2)X、Y、Z、M四种元素的原子半径由小到大的顺序是______ (用元素符号表示)。
(3)元素R可形成 和
和 ,其中较稳定的是
,其中较稳定的是 ,原因是
,原因是______ 。
(4)短周期元素T与元素M在周期表中的位置呈现对角线关系,则元素T为______ (填元素符号);已知元素T、Q的电负性分别为1.5和3.0,则它们形成的化合物是______ (填“离子化合物”或“共价化合物”)。
| 元素代号 | 相关信息 |
| X | 原子核外有6种不同运动状态的电子 |
| Y | 基态原子中s电子总数与p电子总数相等 |
| Z | 原子半径在同周期元素中最大 |
| M | 第一至第六电离能( )依次为578、1817、2745、11575、14830、18376 )依次为578、1817、2745、11575、14830、18376 |
| Q | 基态原子的最外层p轨道上有两个电子的自旋方向与其他电子的自旋方向相反 |
| R | 基态原子核外有7个能级上有电子且能量最高的能级上有6个电子 |
(1)请写出元素Q的基态原子的价电子轨道表示式:
(2)X、Y、Z、M四种元素的原子半径由小到大的顺序是
(3)元素R可形成
 和
和 ,其中较稳定的是
,其中较稳定的是 ,原因是
,原因是(4)短周期元素T与元素M在周期表中的位置呈现对角线关系,则元素T为
您最近一年使用:0次
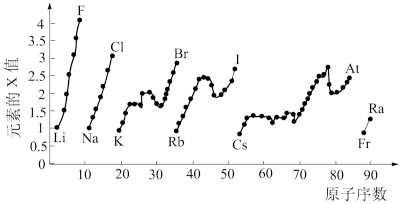
3 . 如图表示元素周期表中部分元素的某种性质(X值)随原子序数变化的关系示意图。______ (填元素符号)。
(2)同主族内不同元素的X值变化的特点是______ ;同周期内,随着原子序数的增大,X值的变化总趋势是______ 。元素周期表中X值的这种变化特点体现了元素性质的______ 变化规律。
(3)预测S元素与 元素x值的大小关系为
元素x值的大小关系为______ ,x值最小的元素在元素周期表中的位置是______ (放射性元素除外)。
(4)X值较小的元素集中在元素周期表的______ (填标号)。
a.左下角 b.右上角 c.分界线附近
(5)下列关于元素性质的说法正确的是______ (填标号)。
a.X值可反映元素最高正化合价的变化规律
b.X值可反映元素在化合物中吸引电子的能力
c.X值的大小可用来判断元素金属性和非金属性的强弱
(2)同主族内不同元素的X值变化的特点是
(3)预测S元素与
 元素x值的大小关系为
元素x值的大小关系为(4)X值较小的元素集中在元素周期表的
a.左下角 b.右上角 c.分界线附近
(5)下列关于元素性质的说法正确的是
a.X值可反映元素最高正化合价的变化规律
b.X值可反映元素在化合物中吸引电子的能力
c.X值的大小可用来判断元素金属性和非金属性的强弱
您最近一年使用:0次
2021-02-15更新
|
241次组卷
|
2卷引用:(鲁科版2019)选择性必修2 第1章 原子结构与元素性质 章末综合检测卷
解题方法
4 . 如图是原子序数为1~19的元素第一电离能的变化曲线(其中部分元素第一电离能已经标出数据)。结合元素在元素周期表中的位置,分析图中曲线的变化特点,并回答下列有关问题。
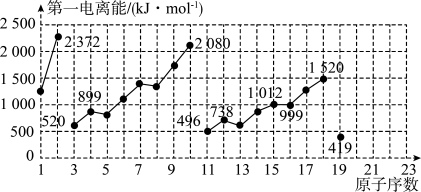
(1)碱金属元素中Li、Na、K的第一电离能分别为_____________  、
、 _____________  、
、 _____________  。
。
(2)同主族中不同元素的第一电离能变化的规律为:_____________ ,碱金属元素这一变化的规律与碱金属的活泼性的关系是 _____________ 。
(3)钙元素的第一电离能的数值范围为_____________ 。

(1)碱金属元素中Li、Na、K的第一电离能分别为
 、
、  、
、  。
。(2)同主族中不同元素的第一电离能变化的规律为:
(3)钙元素的第一电离能的数值范围为
您最近一年使用:0次
解题方法
5 . 如图是部分短周期元素的常见化合价与原子序数的关系:
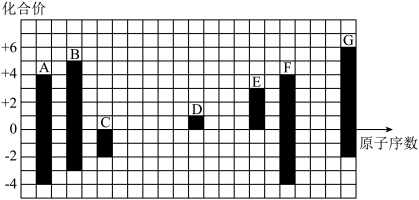
(1)元素 在元素周期表中的位置是
在元素周期表中的位置是__________________ 。
(2)其中金属性最强的元素是______ (用元素符号表示,下同),非金属性最强的元素是______ 。
(3)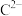 、
、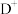 、
、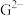 的半径由大到小的顺序是
的半径由大到小的顺序是__________ (用离子符号表示)。
(4)最简单氢化物的稳定性:
______  (填“
(填“ ”或“
”或“ ”)。
”)。
(5) 、
、 、
、 元素最高价氧化物对应水化物的酸性:
元素最高价氧化物对应水化物的酸性:_____ (用化学式表示,下同)
______ 
______ 。
(6) 与
与 形成的具有强氧化性的化合物为
形成的具有强氧化性的化合物为______ (填化学式),该化合物与 反应的化学方程式为
反应的化学方程式为________________________ ,其中氧化剂与还原剂的物质的量之比为____________ 。

(1)元素
 在元素周期表中的位置是
在元素周期表中的位置是(2)其中金属性最强的元素是
(3)
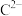 、
、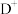 、
、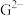 的半径由大到小的顺序是
的半径由大到小的顺序是(4)最简单氢化物的稳定性:

 (填“
(填“ ”或“
”或“ ”)。
”)。(5)
 、
、 、
、 元素最高价氧化物对应水化物的酸性:
元素最高价氧化物对应水化物的酸性:

(6)
 与
与 形成的具有强氧化性的化合物为
形成的具有强氧化性的化合物为 反应的化学方程式为
反应的化学方程式为
您最近一年使用:0次
2020-03-02更新
|
244次组卷
|
4卷引用:鲁科版(2019)必修第二册第一章 第3节 易错疑难集训
鲁科版(2019)必修第二册第一章 第3节 易错疑难集训高一必修第一册(苏教2019版)专题5 易错疑难集训(一)(已下线)4.2.1 元素性质的周期性变化规律(基础练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版2019必修第一册)第1章原子结构与元素周期律 易错疑难集训(二)
6 . 元素周期律(表)是认识元素化合物性质的重要理论。
(1)某学习小组研究了金属锂、钠、镁的性质后发现:
ⅰ.锂、镁和水反应均较为微弱,钠和水反应较为剧烈
ⅱ.锂和镁的氢氧化物均为中等强度的碱
ⅲ.锂、镁在空气中燃烧均生成氧化物,而钠在空气中燃烧生成过氧化物
根据以上事实,可知锂、钠、镁三种元素的金属性强弱关系是___________________ (用“>”“=”或“<”)。
(2)锶(38Sr)元素广泛存在于矿泉水中,是一种人体必需的微量元素,在元素周期表中与20Ca和56Ba同属于第ⅡA族。
①碱性:Sr(OH)2_____ Ba (OH)2(填“>”或“<”)。
②用原子结构的观点解释锶的化学性质与钡差异的原因:______________________________
(3)硒(Se)的部分信息如图,且知34Se、35Br位于同一周期。
①Se在元素周期表中的位置是_______________ 。
②H2Se的电子式是______________ 。
③Cl、Se、Br的非金属性强弱的顺序是__________________ ;能证明上述强弱关系的事实是____________________________ (写出一条即可)。
④某同学对SeO2(白色的挥发性固体,易溶于水)的各种不同化学性质进行推测,并用SO2水溶液、H2O2溶液、NaOH溶液、稀H2SO4等试剂进行实验,证明了推测是正确的。完成下表:
(1)某学习小组研究了金属锂、钠、镁的性质后发现:
ⅰ.锂、镁和水反应均较为微弱,钠和水反应较为剧烈
ⅱ.锂和镁的氢氧化物均为中等强度的碱
ⅲ.锂、镁在空气中燃烧均生成氧化物,而钠在空气中燃烧生成过氧化物
根据以上事实,可知锂、钠、镁三种元素的金属性强弱关系是
(2)锶(38Sr)元素广泛存在于矿泉水中,是一种人体必需的微量元素,在元素周期表中与20Ca和56Ba同属于第ⅡA族。
①碱性:Sr(OH)2
②用原子结构的观点解释锶的化学性质与钡差异的原因:
(3)硒(Se)的部分信息如图,且知34Se、35Br位于同一周期。
| O | |
| S | |
| Se | Br |
②H2Se的电子式是
③Cl、Se、Br的非金属性强弱的顺序是
④某同学对SeO2(白色的挥发性固体,易溶于水)的各种不同化学性质进行推测,并用SO2水溶液、H2O2溶液、NaOH溶液、稀H2SO4等试剂进行实验,证明了推测是正确的。完成下表:
| 编号 | 性质推测 | 化学方程式 |
| 1 | 氧化性 | SeO2+2SO2+2H2O=Se+2H2SO4 |
| 2 | ||
| 3 |
您最近一年使用:0次
2020-04-13更新
|
308次组卷
|
2卷引用:章末检测卷(四) 物质结构 元素周期律
解题方法
7 . a~n10中元素在周期表中的位置如图所示,请回答下列问题:
(1)m的阴离子的结构示意图为___ 。
(2)b的最高价氧化物的化学式为___ ;用化学方程式表示f、d的单质形成f2d2的过程___ 。
(3)d、g、n形成的简单离子的半径由大到小的顺序为___ (用离子符号表示)。
(4)以上元素组成的物质有下列框图中的转化关系,其中甲为10电子微粒。
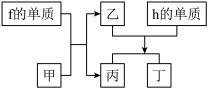
请写出h的单质与乙反应的化学方程式:___ 。
| a | ||||||||
| b | c | d | e | |||||
| f | g | h | m | n | ||||
| …… |
(2)b的最高价氧化物的化学式为
(3)d、g、n形成的简单离子的半径由大到小的顺序为
(4)以上元素组成的物质有下列框图中的转化关系,其中甲为10电子微粒。

请写出h的单质与乙反应的化学方程式:
您最近一年使用:0次
名校
解题方法
8 . 现有部分短周期元素的信息如表所示:
A、B、D三种单质(分别由X、Y、Z元素组成)和甲、乙、丙、丁、戊五种化合物之间的转化关系如图所示(某些条件已略去)。其中丁是一种筒能燃料,分子中含有18个电子,其组成元素与丙相同。
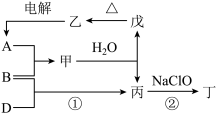
(1)元素X在周期表中的位置是______ ,其简单离子的结构示意图为______ 。
(2)单质B的电子式为______ 。
(3)丙中所含的化学键类型是______ (填序号)。
a.离子键 b.极性共价键 c.非极性共价键
(4)反应②中,0.5 mol 参加反应时转移1 mol电子,该反应的化学方程式为
参加反应时转移1 mol电子,该反应的化学方程式为______ 。
(5)一定条件下,A与 、C(石墨)反应只生成乙和碳化钛(
、C(石墨)反应只生成乙和碳化钛( ),二者均为某些高温结构陶瓷的主要成分,该反应的化学方程式为
),二者均为某些高温结构陶瓷的主要成分,该反应的化学方程式为______ 。
| 元素编号 | 元素性质或原子结构信息 |
| X | 第三周期元素中简单离子半径最小的元素 |
| Y | 其最简单氢化物丙的水溶液呈碱性 |
| Z | 原子核外电子数和所在周期数相等 |

(1)元素X在周期表中的位置是
(2)单质B的电子式为
(3)丙中所含的化学键类型是
a.离子键 b.极性共价键 c.非极性共价键
(4)反应②中,0.5 mol
 参加反应时转移1 mol电子,该反应的化学方程式为
参加反应时转移1 mol电子,该反应的化学方程式为(5)一定条件下,A与
 、C(石墨)反应只生成乙和碳化钛(
、C(石墨)反应只生成乙和碳化钛( ),二者均为某些高温结构陶瓷的主要成分,该反应的化学方程式为
),二者均为某些高温结构陶瓷的主要成分,该反应的化学方程式为
您最近一年使用:0次
2020-03-02更新
|
1108次组卷
|
7卷引用:人教版(2019)高一必修第一册第四章 物质结构 元素周期律 高考挑战区
10-11高三上·北京朝阳·期末
名校
9 . 已知烃B分子内C、H原子个数比为1︰2,相对分子质量为28,核磁共振氢谱显示分子中只有一种化学环境的氢原子,且有如下的转化关系:
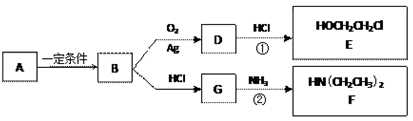
(1)B的结构简式是_________________
(2)A可能属于下列哪类物质___________
a.醇 b.卤代烃 c.酚 d.羧酸
(3)反应①是D与HCl按物质的量之比1︰1的加成反应,则D的分子式是___________ 。
反应②可表示为:G + NH3→ F + HCl (未配平),该反应配平后的化学方程式是(有机化合物均用结构简式表示):____________________________________
化合物E(HOCH2CH2Cl)和 F [ HN(CH2CH3)2 ]是药品普鲁卡因合成的重要中间体,普鲁卡因的合成路线如下:(已知: )
)
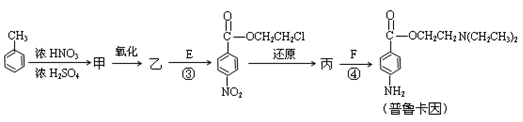
(4)甲的结构简式是_________________ 。
由甲苯生成甲的反应类型是_________________ 。
(5)乙中有两种含氧官能团,反应③的化学方程式是___________________________________
(6)丙中官能团的名称是_______________________________________ 。
(7)普鲁卡因有两种水解产物丁和戊。
① 戊与甲互为同分异构体,戊的结构简式是_____________________ 。
② 戊经聚合反应制成的高分子纤维广泛用于通讯、宇航等领域。该聚合反应的化学方程式是__________________________________________ 。
③ D的红外光谱表明分子内除C—H键、C—C键外还含有两个C—O单键。则D与F在一定条件下反应生成丁的化学方程式是________________________________ 。

(1)B的结构简式是
(2)A可能属于下列哪类物质
a.醇 b.卤代烃 c.酚 d.羧酸
(3)反应①是D与HCl按物质的量之比1︰1的加成反应,则D的分子式是
反应②可表示为:G + NH3→ F + HCl (未配平),该反应配平后的化学方程式是(有机化合物均用结构简式表示):
化合物E(HOCH2CH2Cl)和 F [ HN(CH2CH3)2 ]是药品普鲁卡因合成的重要中间体,普鲁卡因的合成路线如下:(已知:
 )
)
(4)甲的结构简式是
由甲苯生成甲的反应类型是
(5)乙中有两种含氧官能团,反应③的化学方程式是
(6)丙中官能团的名称是
(7)普鲁卡因有两种水解产物丁和戊。
① 戊与甲互为同分异构体,戊的结构简式是
② 戊经聚合反应制成的高分子纤维广泛用于通讯、宇航等领域。该聚合反应的化学方程式是
③ D的红外光谱表明分子内除C—H键、C—C键外还含有两个C—O单键。则D与F在一定条件下反应生成丁的化学方程式是
您最近一年使用:0次
2016-12-09更新
|
490次组卷
|
11卷引用:2011-2012学年河北省衡水中学高二下学期调考试化学试卷
(已下线)2011-2012学年河北省衡水中学高二下学期调考试化学试卷(已下线)北京朝阳区2010年第一学期期末考试高三理综试题(已下线)2011-2012学年山东东阿曹植培训学校高二下学期3月调研化学试卷(已下线)2012-2013学年江苏省淮安市涟水县涟西中学高一下期末考试化学试卷云南省河口县民中2017-2018学年高二下学期6月份考试化学试题云南省广南县第三中学校2019-2020学年高二上学期期末考试化学试题云南省广南县二中2019-2020学年高二上学期期末考试化学试题贵州省独山县第四中学2019-2020学年高二上学期期末考试化学试题贵州省黎平第二中学2019-2020学年高二上学期期末考试化学试题云南省曲靖市师宗县第二中学2019-2020学年高二上学期期末考试化学试题广西壮族自治区崇左市天等县民族高中2019-2020学年高二上学期期末考试化学试题



