名校
解题方法
1 .  是一种重要的化工产品。以菱锰矿(主要成分为
是一种重要的化工产品。以菱锰矿(主要成分为 ,还含有
,还含有 、FeO、CoO等)为原料制备
、FeO、CoO等)为原料制备 的工艺流程如下图。
的工艺流程如下图。
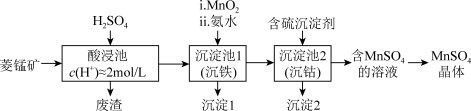
资料:金属离子沉淀的pH
(1)酸浸后所得溶液的金属阳离子包括 、
、 、
、_______ 。
(2)沉淀池1中,先加 充分反应后再加氨水,写出加
充分反应后再加氨水,写出加 时发生反应的离子方程式:
时发生反应的离子方程式:_______ 。
(3)沉淀池2中,不能用NaOH代替含硫沉淀剂,原因是_______ 。
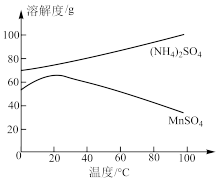
(4)图为 和
和 的溶解度曲线。从“含
的溶解度曲线。从“含 的溶液”中提取“
的溶液”中提取“ 晶体”的操作为
晶体”的操作为_______ 、洗涤、干燥。
(5)受实际条件限制,“酸浸池”所得的废渣中还含有锰元素,其含量测定方法如下。
i.称取a g废渣,加酸将锰元素全部溶出成 ,过滤,将滤液定容于100mL容量瓶中;
,过滤,将滤液定容于100mL容量瓶中;
ii.取25.00 mL溶液于锥形瓶中,加入少量催化剂和过量 溶液,加热、充分反应后,煮沸溶液使过量的
溶液,加热、充分反应后,煮沸溶液使过量的 分解。
分解。
iii.加入指示剂,用b mol/L 溶液滴定,滴定至终点时消耗
溶液滴定,滴定至终点时消耗 溶液的体积为c mL ,
溶液的体积为c mL , 重新变成
重新变成 。
。
①补全步骤ⅱ中反应的离子方程式:_______ 。
 +
+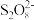 +_______
+_______
 +_______+_______
+_______+_______
②废渣中锰元素的质量分数为_______ 。
 是一种重要的化工产品。以菱锰矿(主要成分为
是一种重要的化工产品。以菱锰矿(主要成分为 ,还含有
,还含有 、FeO、CoO等)为原料制备
、FeO、CoO等)为原料制备 的工艺流程如下图。
的工艺流程如下图。
资料:金属离子沉淀的pH
| 金属离子 | Fe3+ | Fe2+ | Co2+ | Mn2+ |
| 开始沉淀 | 1.5 | 6.3 | 7.4 | 7.6 |
| 完全沉淀 | 2.8 | 8.3 | 9.4 | 10.2 |
 、
、 、
、(2)沉淀池1中,先加
 充分反应后再加氨水,写出加
充分反应后再加氨水,写出加 时发生反应的离子方程式:
时发生反应的离子方程式:(3)沉淀池2中,不能用NaOH代替含硫沉淀剂,原因是
(4)图为
 和
和 的溶解度曲线。从“含
的溶解度曲线。从“含 的溶液”中提取“
的溶液”中提取“ 晶体”的操作为
晶体”的操作为
(5)受实际条件限制,“酸浸池”所得的废渣中还含有锰元素,其含量测定方法如下。
i.称取a g废渣,加酸将锰元素全部溶出成
 ,过滤,将滤液定容于100mL容量瓶中;
,过滤,将滤液定容于100mL容量瓶中;ii.取25.00 mL溶液于锥形瓶中,加入少量催化剂和过量
 溶液,加热、充分反应后,煮沸溶液使过量的
溶液,加热、充分反应后,煮沸溶液使过量的 分解。
分解。iii.加入指示剂,用b mol/L
 溶液滴定,滴定至终点时消耗
溶液滴定,滴定至终点时消耗 溶液的体积为c mL ,
溶液的体积为c mL , 重新变成
重新变成 。
。①补全步骤ⅱ中反应的离子方程式:
 +
+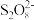 +_______
+_______
 +_______+_______
+_______+_______②废渣中锰元素的质量分数为
您最近一年使用:0次
2023-04-15更新
|
268次组卷
|
3卷引用:西藏自治区林芝市第二高级中学2023-2024学年高三上学期第三次月考理科综合试题
名校
解题方法
2 .  是制备某负载型活性铁催化剂 的主要原料,具有工业生产价值。某化学小组用如下方法制备
是制备某负载型活性铁催化剂 的主要原料,具有工业生产价值。某化学小组用如下方法制备 ,并测定产品中铁的含量。
,并测定产品中铁的含量。
I.制备晶体
i.称取 5 g 莫尔盐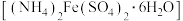 ,用 15 mL 水和几滴
,用 15 mL 水和几滴 溶液充分溶解,再加入25 mL饱和
溶液充分溶解,再加入25 mL饱和 溶液,加热至沸,生成黄色沉淀;
溶液,加热至沸,生成黄色沉淀;
ⅱ.将沉淀洗涤至中性,加入10 mL饱和 溶液,水浴加热至40℃,边搅拌边缓慢滴加
溶液,水浴加热至40℃,边搅拌边缓慢滴加 溶液,沉淀逐渐变为红褐色;
溶液,沉淀逐渐变为红褐色;
ⅲ.将混合物煮沸30 s,加入8 mL饱和 溶液,红褐色沉淀溶解,趁热过滤,滤液冷却后,析出翠绿色晶体,过滤、干燥。
溶液,红褐色沉淀溶解,趁热过滤,滤液冷却后,析出翠绿色晶体,过滤、干燥。
II.测定产品中铁的含量
ⅳ.称量 制得的样品,加水溶解,并加入稀
制得的样品,加水溶解,并加入稀 酸化,再滴入
酸化,再滴入 溶液使其恰好反应;
溶液使其恰好反应;
v.向ⅳ的溶液中加入过量Zn粉,反应完全后,弃去不溶物,向溶液中加入稀 酸化,用
酸化,用 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 。
。
已知: 为二元弱酸,具有较强的还原性
为二元弱酸,具有较强的还原性
(1)莫尔盐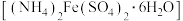 中铁元素的化合价是
中铁元素的化合价是_______ 。
(2)步骤ⅰ中黄色沉淀的化学式为 ,生成该沉淀的离子方程式是
,生成该沉淀的离子方程式是_______ 。
(3)步骤ⅱ中除了生成红褐色沉淀,另一部分铁元素转化为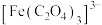 、将下述反应的离子方程式补充完整
、将下述反应的离子方程式补充完整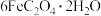 +____+____=
+____+____= ____
____ ,
,_____________ 。
(4)步骤ⅱ中水浴加热的温度不宜过高,原因是_______ 。
(5)步骤iv在铁的含量测定中所起的作用是_______ 。
(6)已知:ⅴ中Zn粉将铁元素全部还原为 ;反应中
;反应中 转化为
转化为 。则该样品中铁元素的质量分数是
。则该样品中铁元素的质量分数是_______ (用含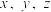 的代数式表示)。
的代数式表示)。
 是制备某负载型活性铁催化剂 的主要原料,具有工业生产价值。某化学小组用如下方法制备
是制备某负载型活性铁催化剂 的主要原料,具有工业生产价值。某化学小组用如下方法制备 ,并测定产品中铁的含量。
,并测定产品中铁的含量。I.制备晶体
i.称取 5 g 莫尔盐
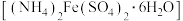 ,用 15 mL 水和几滴
,用 15 mL 水和几滴 溶液充分溶解,再加入25 mL饱和
溶液充分溶解,再加入25 mL饱和 溶液,加热至沸,生成黄色沉淀;
溶液,加热至沸,生成黄色沉淀;ⅱ.将沉淀洗涤至中性,加入10 mL饱和
 溶液,水浴加热至40℃,边搅拌边缓慢滴加
溶液,水浴加热至40℃,边搅拌边缓慢滴加 溶液,沉淀逐渐变为红褐色;
溶液,沉淀逐渐变为红褐色;ⅲ.将混合物煮沸30 s,加入8 mL饱和
 溶液,红褐色沉淀溶解,趁热过滤,滤液冷却后,析出翠绿色晶体,过滤、干燥。
溶液,红褐色沉淀溶解,趁热过滤,滤液冷却后,析出翠绿色晶体,过滤、干燥。II.测定产品中铁的含量
ⅳ.称量
 制得的样品,加水溶解,并加入稀
制得的样品,加水溶解,并加入稀 酸化,再滴入
酸化,再滴入 溶液使其恰好反应;
溶液使其恰好反应;v.向ⅳ的溶液中加入过量Zn粉,反应完全后,弃去不溶物,向溶液中加入稀
 酸化,用
酸化,用 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 。
。已知:
 为二元弱酸,具有较强的还原性
为二元弱酸,具有较强的还原性(1)莫尔盐
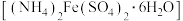 中铁元素的化合价是
中铁元素的化合价是(2)步骤ⅰ中黄色沉淀的化学式为
 ,生成该沉淀的离子方程式是
,生成该沉淀的离子方程式是(3)步骤ⅱ中除了生成红褐色沉淀,另一部分铁元素转化为
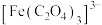 、将下述反应的离子方程式补充完整
、将下述反应的离子方程式补充完整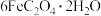 +____+____=
+____+____= ____
____ ,
,(4)步骤ⅱ中水浴加热的温度不宜过高,原因是
(5)步骤iv在铁的含量测定中所起的作用是
(6)已知:ⅴ中Zn粉将铁元素全部还原为
 ;反应中
;反应中 转化为
转化为 。则该样品中铁元素的质量分数是
。则该样品中铁元素的质量分数是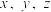 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2020-12-19更新
|
143次组卷
|
4卷引用:西藏拉萨中学2021届高三上学期第三次月考理综化学试题
名校
3 . 为测定某样品中氟元素的质量分数进行如下实验,利用高氯酸(高沸点酸)将样品中的氟元素转化为氟化氢(氢氟酸为低沸点酸,含量低,不考虑对玻璃仪器的腐蚀),用水蒸气蒸出,再通过滴定测量。实验装置如下图所示,加热装置省略。

(1)A的名称是___________ ,长导管用于平衡压强,实验过程中其下端___________ (填“能”或“不能”)在液面以上。
(2)仪器C是直形冷凝管,实验过程中,冷却水应从___________ 口出。(填“a”或“b")
(3)实验时,首先打开活塞K,待水沸腾时,关闭活塞K,开始蒸馏:若蒸馏时因反应装置局部堵塞造成长导管水位急剧上升,应立即______________________ 。
(4)连接水蒸气发生装置和反应装置之间的玻璃管常裹以石棉绳,其作用是___________ 。
(5)B中加入一定体积高氯酸和1.00g氟化稀土矿样,D中盛有滴加酚酞的NaOH溶液。加热A、B,使A中产生的水蒸气进入B。
①下列物质不可代替高氯酸的是___________ (填标号)
a.醋酸 b.硝酸 c.磷酸 d.硫酸
②D中主要反应的离子方程式为_________________________________ 。
(6)向馏出液中加入25.00mL0.100mol·L-1La(NO3)3溶液,得到LaF3沉淀,再用0.100 mol·L -1EDTA标准溶液滴定剩余La3+(La3+与EDTA按1︰1络合),消耗EDTA标准溶液20.00mL,则氟化稀土样品中氟的质量分数为______________________ 。

(1)A的名称是
(2)仪器C是直形冷凝管,实验过程中,冷却水应从
(3)实验时,首先打开活塞K,待水沸腾时,关闭活塞K,开始蒸馏:若蒸馏时因反应装置局部堵塞造成长导管水位急剧上升,应立即
(4)连接水蒸气发生装置和反应装置之间的玻璃管常裹以石棉绳,其作用是
(5)B中加入一定体积高氯酸和1.00g氟化稀土矿样,D中盛有滴加酚酞的NaOH溶液。加热A、B,使A中产生的水蒸气进入B。
①下列物质不可代替高氯酸的是
a.醋酸 b.硝酸 c.磷酸 d.硫酸
②D中主要反应的离子方程式为
(6)向馏出液中加入25.00mL0.100mol·L-1La(NO3)3溶液,得到LaF3沉淀,再用0.100 mol·L -1EDTA标准溶液滴定剩余La3+(La3+与EDTA按1︰1络合),消耗EDTA标准溶液20.00mL,则氟化稀土样品中氟的质量分数为
您最近一年使用:0次
2019-03-14更新
|
679次组卷
|
4卷引用:西藏自治区拉萨市拉萨中学2020届高三第六次月考理科化学试题
真题
名校
4 . 化学兴趣小组对某品牌牙膏中的摩擦剂成分及其含量进行以下探究:查得资料:该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸时无气体产生。
Ⅰ.摩擦剂中氢氧化铝的定性检验
取适量牙膏样品,加水充足搅拌、过滤。
(1)往滤渣中加入过量 NaOH溶液,过滤。氢氧化铝与NaOH溶液反应的离子方程式是_______ 。
(2)往(1)所得滤液中先通入过量二氧化碳,再加入过量稀盐酸。观察的现象是______ 。
Ⅱ.牙膏样品中碳酸钙的定量测定
利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO 沉淀质量,以确定碳酸钙的质量分数。
沉淀质量,以确定碳酸钙的质量分数。
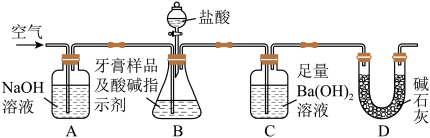
依据实验过程回答下列问题:
(3)实验过程中需持续缓缓通入空气。其作用除了可搅拌B、C中的反应物外,还有:________
(4)C中反应生成BaCO3的化学方程式是__________________ 。
(5)下列各项措施中,不能提高测定准确度的是_________ (填标号)。
a.在加入盐酸之前,应排净装置内的CO2气体
b.滴加盐酸不宜过快
c.在A-B之间增添盛有浓硫酸的洗气装置
d.在B-C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(6)实验中准确称取8.00 g样品三份,进行三次测定,测得BaCO3平均质量为3.94 g。则样品中碳酸钙的质量分数为__________ 。
(7)有人认为不必测定C中生成的BaCO3质量,只要测定装置C在吸收CO2前后的质量差,一样可以确定碳酸钙的质量分数。实验证明按此方法测定的结果明显偏高,原因是______ .
Ⅰ.摩擦剂中氢氧化铝的定性检验
取适量牙膏样品,加水充足搅拌、过滤。
(1)往滤渣中加入过量 NaOH溶液,过滤。氢氧化铝与NaOH溶液反应的离子方程式是
(2)往(1)所得滤液中先通入过量二氧化碳,再加入过量稀盐酸。观察的现象是
Ⅱ.牙膏样品中碳酸钙的定量测定
利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO
 沉淀质量,以确定碳酸钙的质量分数。
沉淀质量,以确定碳酸钙的质量分数。
依据实验过程回答下列问题:
(3)实验过程中需持续缓缓通入空气。其作用除了可搅拌B、C中的反应物外,还有:
(4)C中反应生成BaCO3的化学方程式是
(5)下列各项措施中,不能提高测定准确度的是
a.在加入盐酸之前,应排净装置内的CO2气体
b.滴加盐酸不宜过快
c.在A-B之间增添盛有浓硫酸的洗气装置
d.在B-C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(6)实验中准确称取8.00 g样品三份,进行三次测定,测得BaCO3平均质量为3.94 g。则样品中碳酸钙的质量分数为
(7)有人认为不必测定C中生成的BaCO3质量,只要测定装置C在吸收CO2前后的质量差,一样可以确定碳酸钙的质量分数。实验证明按此方法测定的结果明显偏高,原因是
您最近一年使用:0次
2019-01-30更新
|
1322次组卷
|
11卷引用:2017届西藏自治区拉萨中学高三上第一次月考化学卷
2017届西藏自治区拉萨中学高三上第一次月考化学卷(已下线)2012届山西省康杰中学高三9月份月考化学试卷【全国百强校】宁夏回族自治区银川一中2019届高三第二次月考理综化学试题新疆克拉玛依市第十三中学2018-2019学年高一上学期第二次月考化学试题河南省名校联盟2021-2022学年高三上学期第三次诊断考试化学试题2011年普通高等学校招生全国统一考试化学卷(福建)(已下线)2013-2014湖南省衡南县高二下学期期末考试化学试卷(已下线)解密12 实验化学(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)浙江省诸暨市第二高级中学2020-2021学年高二下学期期中考试化学试题江西省九校2021-2022学年高三上学期期中联考化学试题(已下线)解密13 实验化学(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)
5 . 已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:

(1)该“84消毒液”的物质的量浓度约为_________ mol·L-1(保留2位有效数字)
(2)某同学取100 mL 该“84消毒液”,按规定标准稀释后用于消毒,稀释后的溶液中:c(Na+)=__________ mol·L-1。
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液。下列说法正确的是__________ (填字母)。
A.如下图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器

B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
C.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低
D.需要称量NaClO固体的质量为143.0g
(4)如上面第(3)小题A选项所示,除了应该使用的仪器外,还需要的玻璃仪器是______________ 。
(5)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用18.4 mol·L-1的浓硫酸配制2000 mL 2.3 mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①所配制的稀硫酸中,H+的物质的量浓度为__________ mol·L-1。
②需用浓硫酸的体积为__________ mL。
(6)测定“84消毒液”中次氯酸钠含量的主要步骤:
a.取5.00mL“84消毒液”经稀释等步骤最后定容于250mL容量瓶中;
b.取稀释后的溶液25.00mL于锥形瓶中,加入足量硫酸酸化的KI溶液,在阴凉处静置5分钟;
c.加入5~10滴0.5%的淀粉溶液,溶液变蓝色,再用c mol·L-1Na2S2O3溶液滴定,当消耗的Na2S2O3溶液为VmL时,溶液的蓝色恰好退去,且半分钟内蓝色不再恢复。则“84消毒液”中NaClO的浓度为__________ g·L-1。(用c、V表示)
(已知:2KI + H2SO4 + NaClO = I2 + K2SO4 + NaCl + H2O;I2 + 2Na2S2O3 = 2NaI + Na2S4O6)

(1)该“84消毒液”的物质的量浓度约为
(2)某同学取100 mL 该“84消毒液”,按规定标准稀释后用于消毒,稀释后的溶液中:c(Na+)=
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液。下列说法正确的是
A.如下图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器

B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
C.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低
D.需要称量NaClO固体的质量为143.0g
(4)如上面第(3)小题A选项所示,除了应该使用的仪器外,还需要的玻璃仪器是
(5)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用18.4 mol·L-1的浓硫酸配制2000 mL 2.3 mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①所配制的稀硫酸中,H+的物质的量浓度为
②需用浓硫酸的体积为
(6)测定“84消毒液”中次氯酸钠含量的主要步骤:
a.取5.00mL“84消毒液”经稀释等步骤最后定容于250mL容量瓶中;
b.取稀释后的溶液25.00mL于锥形瓶中,加入足量硫酸酸化的KI溶液,在阴凉处静置5分钟;
c.加入5~10滴0.5%的淀粉溶液,溶液变蓝色,再用c mol·L-1Na2S2O3溶液滴定,当消耗的Na2S2O3溶液为VmL时,溶液的蓝色恰好退去,且半分钟内蓝色不再恢复。则“84消毒液”中NaClO的浓度为
(已知:2KI + H2SO4 + NaClO = I2 + K2SO4 + NaCl + H2O;I2 + 2Na2S2O3 = 2NaI + Na2S4O6)
您最近一年使用:0次
2018高三·全国·专题练习
名校
6 . 工业采用氯化铵焙烧菱锰矿制备高纯碳酸锰的流程如图所示:

已知:①菱锰矿的主要成分是MnCO3,其中含Fe、Ca、Mg、Al等元素。
②Al3+、Fe3+沉淀完全的pH分别为4.7、3.2,Mn2+、Mg2+开始沉淀的pH分别为8.1、9.1。
③焙烧过程中主要反应为MnCO3+2NH4Cl MnCl2+2NH3↑+CO2↑+H2O。
MnCl2+2NH3↑+CO2↑+H2O。
(1)结合图1、2、3,分析焙烧过程中最佳的焙烧温度、焙烧时间、 分别为
分别为_____ 、_____ 、_______ 。

(2)对浸出液净化除杂时,需先加入MnO2将Fe2+转化为Fe3+,再调节溶液pH的范围为_______ ,将Fe3+和Al3+变为沉淀而除去,然后加入NH4F将Ca2+、Mg2+变为氟化物沉淀除去。
(3)“碳化结晶”步骤中,加入碳酸氢铵时反应的离子方程式为______________ 。
(4)上述流程中可循环使用的物质是________ 。
(5)现用滴定法测定浸出液中Mn2+的含量。实验步骤:称取1.000 g试样,向其中加入稍过量的磷酸和硝酸,加热使反应2Mn2++ +4
+4 +2H+
+2H+ 2[Mn(PO4)2]3−+
2[Mn(PO4)2]3−+ +H2O充分进行;加入稍过量的硫酸铵,发生反应
+H2O充分进行;加入稍过量的硫酸铵,发生反应 +
+
 N2↑+2H2O以除去
N2↑+2H2O以除去 ;加入稀硫酸酸化,用2.00 mol·L−1 10.00 mL硫酸亚铁铵标准溶液进行滴定,发生的反应为[Mn(PO4)2]3−+Fe2+
;加入稀硫酸酸化,用2.00 mol·L−1 10.00 mL硫酸亚铁铵标准溶液进行滴定,发生的反应为[Mn(PO4)2]3−+Fe2+ Mn2++ Fe3++2
Mn2++ Fe3++2 ;用0.10 mol·L−110.00 mL酸性K2Cr2O7溶液恰好除去过量的Fe2+。
;用0.10 mol·L−110.00 mL酸性K2Cr2O7溶液恰好除去过量的Fe2+。
①酸性K2Cr2O7溶液与Fe2+反应的离子方程式为_____________ (还原产物是Cr3+)。
②试样中锰的质量分数为_______ 。

已知:①菱锰矿的主要成分是MnCO3,其中含Fe、Ca、Mg、Al等元素。
②Al3+、Fe3+沉淀完全的pH分别为4.7、3.2,Mn2+、Mg2+开始沉淀的pH分别为8.1、9.1。
③焙烧过程中主要反应为MnCO3+2NH4Cl
 MnCl2+2NH3↑+CO2↑+H2O。
MnCl2+2NH3↑+CO2↑+H2O。(1)结合图1、2、3,分析焙烧过程中最佳的焙烧温度、焙烧时间、
 分别为
分别为
(2)对浸出液净化除杂时,需先加入MnO2将Fe2+转化为Fe3+,再调节溶液pH的范围为
(3)“碳化结晶”步骤中,加入碳酸氢铵时反应的离子方程式为
(4)上述流程中可循环使用的物质是
(5)现用滴定法测定浸出液中Mn2+的含量。实验步骤:称取1.000 g试样,向其中加入稍过量的磷酸和硝酸,加热使反应2Mn2++
 +4
+4 +2H+
+2H+ 2[Mn(PO4)2]3−+
2[Mn(PO4)2]3−+ +H2O充分进行;加入稍过量的硫酸铵,发生反应
+H2O充分进行;加入稍过量的硫酸铵,发生反应 +
+
 N2↑+2H2O以除去
N2↑+2H2O以除去 ;加入稀硫酸酸化,用2.00 mol·L−1 10.00 mL硫酸亚铁铵标准溶液进行滴定,发生的反应为[Mn(PO4)2]3−+Fe2+
;加入稀硫酸酸化,用2.00 mol·L−1 10.00 mL硫酸亚铁铵标准溶液进行滴定,发生的反应为[Mn(PO4)2]3−+Fe2+ Mn2++ Fe3++2
Mn2++ Fe3++2 ;用0.10 mol·L−110.00 mL酸性K2Cr2O7溶液恰好除去过量的Fe2+。
;用0.10 mol·L−110.00 mL酸性K2Cr2O7溶液恰好除去过量的Fe2+。①酸性K2Cr2O7溶液与Fe2+反应的离子方程式为
②试样中锰的质量分数为
您最近一年使用:0次
真题
名校
7 . K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。回答下列问题:
(1)晒制蓝图时,用K3[Fe(C2O4)3]·3H2O作感光剂,以K3[Fe(CN)6]溶液为显色剂。其光解反应的化学方程式为:2K3[Fe(C2O4)3]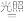 2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为
2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为______________ 。
(2)某小组为探究三草酸合铁酸钾的热分解产物,按下图所示装置进行实验。

①通入氮气的目的是________________________________________ 。
②实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有___________ 、___________ 。
③为防止倒吸,停止实验时应进行的操作是_____________________________ 。
④样品完全分解后,装置A中的残留物含有FeO和Fe2O3,检验Fe2O3存在的方法是:________________ 。
(3)测定三草酸合铁酸钾中铁的含量。
①称量m g样品于锥形瓶中,溶解后加稀H2SO4酸化,用c mol·L-1 KMnO4溶液滴定至终点。滴定终点的现象是___________________________ 。
②向上述溶液中加入过量锌粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。加稀H2SO4酸化,用c mol·L-1 KMnO4溶液滴定至终点,消耗KMnO4溶液V mL。该晶体中铁的质量分数的表达式为________________________________ 。
(1)晒制蓝图时,用K3[Fe(C2O4)3]·3H2O作感光剂,以K3[Fe(CN)6]溶液为显色剂。其光解反应的化学方程式为:2K3[Fe(C2O4)3]
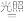 2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为
2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为(2)某小组为探究三草酸合铁酸钾的热分解产物,按下图所示装置进行实验。

①通入氮气的目的是
②实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有
③为防止倒吸,停止实验时应进行的操作是
④样品完全分解后,装置A中的残留物含有FeO和Fe2O3,检验Fe2O3存在的方法是:
(3)测定三草酸合铁酸钾中铁的含量。
①称量m g样品于锥形瓶中,溶解后加稀H2SO4酸化,用c mol·L-1 KMnO4溶液滴定至终点。滴定终点的现象是
②向上述溶液中加入过量锌粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。加稀H2SO4酸化,用c mol·L-1 KMnO4溶液滴定至终点,消耗KMnO4溶液V mL。该晶体中铁的质量分数的表达式为
您最近一年使用:0次
2018-06-09更新
|
13243次组卷
|
19卷引用:西藏自治区拉萨中学2022届高三第六次月考理综化学试题
西藏自治区拉萨中学2022届高三第六次月考理综化学试题西藏林芝市第二高级中学2022-2023学年高三上学期第二次月考化学试题四川省攀枝花市第十二中学2019届高三上学期10月月考化学试题云南省大理白族自治州漾濞二中2019—2020学年9月份高三化学考试试题黑龙江省大庆市第四中学2020届高三下学期4月月考理综化学试题山东省潍坊市诸城一中2021届高三11月份模拟化学试题重庆市开州中学高 2021-2022学年高三上学期10月月考化学试题2018年全国普通高等学校招生统一考试化学(新课标II卷)(已下线)2018年高考题及模拟题汇编 专题16 化学实验综合题广东省惠州市第一中学2019届高三上学期理科综合测试(二)化学试题云南省马关县二中2020届高三上学期开学考试化学试题云南省玉溪元江民中2020届高三开学考试化学试题云南省富宁县民族中学2020届高三上学期开学考试化学试题云南省富宁县第一中学2020届高三第一学期开学考试化学试题四川省自贡市田家炳中学2020届高三上学期期中考试化学试题(已下线)专题10.3 化学实验方案的设计与评价 (讲)-《2020年高考一轮复习讲练测》(已下线)考点32 化学实验方案设计与评价-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点35 化学实验方案的设计与评价-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)专题17化学实验综合题-五年(2018~2022)高考真题汇编(全国卷)
8 . 水泥是重要的建筑材料。水泥熟料的主要成分为CaO、SiO2,并含有一定量的铁、铝和镁等金属的氧化物。实验室测定水泥样品中钙含量的过程如图所示:
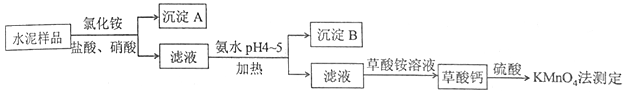
回答下列问题:
(1)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是________________________________________ ,还可使用___________ 代替硝酸。
(2)沉淀A的主要成分是_________ ,其不溶于强酸但可与一种弱酸反应,该反应的化学方程式为____________________________________ 。
(3)加氨水过程中加热的目的是______________________________________ 。沉淀B的主要成分为_____________ 、____________ (填化学式)。
(4)草酸钙沉淀经稀H2SO4处理后,用KMnO4标准溶液滴定,通过测定草酸的量可间接获知钙的含量,滴定反应为:MnO4-+H++H2C2O4→Mn2++CO2+H2O。实验中称取0.400 g水泥样品,滴定时消耗了0.0500 mol·L-1的KMnO4溶液36.00 mL,则该水泥样品中钙的质量分数为______________ 。

回答下列问题:
(1)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是
(2)沉淀A的主要成分是
(3)加氨水过程中加热的目的是
(4)草酸钙沉淀经稀H2SO4处理后,用KMnO4标准溶液滴定,通过测定草酸的量可间接获知钙的含量,滴定反应为:MnO4-+H++H2C2O4→Mn2++CO2+H2O。实验中称取0.400 g水泥样品,滴定时消耗了0.0500 mol·L-1的KMnO4溶液36.00 mL,则该水泥样品中钙的质量分数为
您最近一年使用:0次
2017-08-08更新
|
9846次组卷
|
25卷引用:西藏拉萨北京实验中学2018届高三第五次月考理科综合化学试题
西藏拉萨北京实验中学2018届高三第五次月考理科综合化学试题重庆市第二中学2018届高三3月测试化学试题【全国百强校】宁夏回族自治区吴忠中学2019届高三上学期第三次月考(期中)化学试题贵州省铜仁市思南中学2021届高三上学期第二次月考化学试题宁夏石嘴山市第三中学2021届高三上学期第二次月考化学试题福建省长泰县第一中学2021届高三上学期11月考试化学试题云南省保山第九中学2021届高三上学期开学考试化学试题广东省广州市禺山高级中学2020-2021学年高二下学期第一阶段考试化学试题黑龙江省哈尔滨市第三中学2021-2022学年上学期高三第三次验收考试化学试题广东省佛山市第一中学2021-2022学年高一下学期第一次段考(3月)化学试题2017年全国普通高等学校招生统一考试理综化学(新课标Ⅱ卷精编版)(已下线)《考前20天终极攻略》-5月28日 工艺流程分析(已下线)解密05 金属及其化合物(教师版)——备战2018年高考化学之高频考点解密(已下线)解密03 氧化还原反应——备战2018年高考化学之高频考点解密(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第5讲 无机框图题的解答策略【教学案】陕西省吴起高级中学2019届高三上学期期中考试化学试题安徽省亳州市第二中学2018-2019学年高二下学期期中考试化学试题百所名校联考-非金属及其化合物云南省漾濞二中2020届高三上学期开学考试化学试题(已下线)专题七 工艺流程题(真题汇编)-2020年高考二轮模块化复习之《元素化合物》名师讲案与提分特训福建省福州第一中学2021届高三上学期期中考试化学试题(已下线)专题四 能力提升检测卷 (测) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)考向10 碳、硅及其化合物-备战2022年高考化学一轮复习考点微专题(已下线)第11讲 碳、硅及无机非金属材料(练)-2023年高考化学一轮复习讲练测(全国通用)第四章 非金属及其化合物 第17讲 无机非金属材料
9 . 为了保护环境,充分利用资源,某研究小组通过如下简化流程,将工业制硫酸的硫铁矿烧渣(Fe主要以Fe2O3存在)转变成重要的化工原料FeSO4(反应条件略).
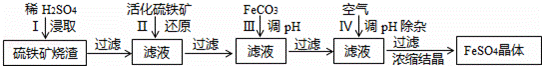
活化硫铁矿还原Fe3+的主要反应为:FeS2+7Fe2(S04)3+8H2O=15FeSO4+8H2SO4,不考虑其它反应,请回答下列问题:
(1)第Ⅰ步H2SO4与Fe2O3反应的离子方程式是_____________________ .
(2)检验第Ⅱ步中Fe3+是否完全被还原,应选择__________ (填字母编号).
A.KMnO4溶液 B.KCl溶液 C.KSCN 溶液
(3)第Ⅲ步加FeCO3调溶液pH到5.8左右,然后在第Ⅳ步通入空气使溶液pH到5.2,此时Fe2+不沉淀,滤液中铝、硅杂质被除尽,通入空气引起溶液pH降低的原因是_______________
(4)FeSO4可转化为FeCO3,FeCO3在空气中加热反应可制得铁系氧化物材料.
已知25℃,101kPa时:
4Fe(s)+3O2(g)═2Fe2O3(s)△H=﹣1648kJ/mol
C(s)+O2(g)═CO2(g)△H=﹣393kJ/mol
2Fe(s)+2C(s)+3O2(g)═2FeCO3(s)△H=﹣1480kJ/mol
FeCO3在空气中加热反应生成Fe2O3的热化学方程式是______________________
(5)FeSO4在一定条件下可制得FeS2(二硫化亚铁)纳米材料,该材料可用于制造高容量锂电池,电池放电时的总反应为4Li+FeS2=Fe+2Li2S,正极反应式是_________________________
(6)假如烧渣中的铁全部视为Fe2O3,其含量为50%,将a kg质量分数为b%的硫酸加入到c kg烧渣中浸取,铁的浸取率为96%,其它杂质浸出消耗的硫酸以及调pH后溶液呈微酸性,所残留的硫酸忽略不计,按上述流程,第Ⅲ步应加入FeCO3_________ kg.

活化硫铁矿还原Fe3+的主要反应为:FeS2+7Fe2(S04)3+8H2O=15FeSO4+8H2SO4,不考虑其它反应,请回答下列问题:
(1)第Ⅰ步H2SO4与Fe2O3反应的离子方程式是
(2)检验第Ⅱ步中Fe3+是否完全被还原,应选择
A.KMnO4溶液 B.KCl溶液 C.KSCN 溶液
(3)第Ⅲ步加FeCO3调溶液pH到5.8左右,然后在第Ⅳ步通入空气使溶液pH到5.2,此时Fe2+不沉淀,滤液中铝、硅杂质被除尽,通入空气引起溶液pH降低的原因是
(4)FeSO4可转化为FeCO3,FeCO3在空气中加热反应可制得铁系氧化物材料.
已知25℃,101kPa时:
4Fe(s)+3O2(g)═2Fe2O3(s)△H=﹣1648kJ/mol
C(s)+O2(g)═CO2(g)△H=﹣393kJ/mol
2Fe(s)+2C(s)+3O2(g)═2FeCO3(s)△H=﹣1480kJ/mol
FeCO3在空气中加热反应生成Fe2O3的热化学方程式是
(5)FeSO4在一定条件下可制得FeS2(二硫化亚铁)纳米材料,该材料可用于制造高容量锂电池,电池放电时的总反应为4Li+FeS2=Fe+2Li2S,正极反应式是
(6)假如烧渣中的铁全部视为Fe2O3,其含量为50%,将a kg质量分数为b%的硫酸加入到c kg烧渣中浸取,铁的浸取率为96%,其它杂质浸出消耗的硫酸以及调pH后溶液呈微酸性,所残留的硫酸忽略不计,按上述流程,第Ⅲ步应加入FeCO3
您最近一年使用:0次
2016-12-09更新
|
119次组卷
|
2卷引用:2016届西藏自治区拉萨中学高三上学期第四次月考化学试卷
23-24高三下·陕西西安·阶段练习
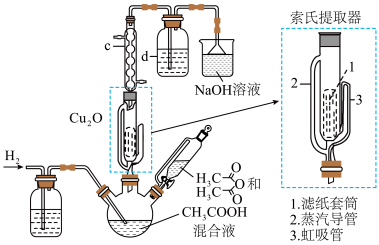
10 . 醋酸亚铜(CH3COOCu)为透明叶状晶体,难溶于乙醚,遇空气易水解或被氧化,可由氧化亚铜与醋酸酐的冰醋酸溶液在索氏提取器中制得。实验室利用Cu2O制备醋酸亚铜的装置如图所示(加热和夹持装置省略)。
已知:醋酸酐可吸水生成醋酸。
回答下列问题:
(1)仪器c的名称是_______ ,仪器d中的试剂和作用分别是_______ 。
(2)在氢气的氛围下,Cu2O和冰醋酸反应逐渐转化为醋酸亚铜,该过程中发生反应的化学方程式为_______ 。制备过程中醋酸酐的作用是_______ 。
(3)制备过程中不可选用明火直接加热,原因是_______ 。
(4)冷却三颈烧瓶中的提取液,有白色醋酸亚铜析出,经抽滤、无水乙醚迅速洗涤、_______ ,最终得到醋酸亚铜固体。
(5)产品纯度的测定:准确称取醋酸亚铜产品mg,迅速溶于过量的FeCl3溶液中得到V1mL待测液,从中量取V2mL溶液于锥形瓶中,加入2滴邻菲罗啉指示剂,立即用amol·L-1硫酸铈[Ce(SO4)2]标准溶液滴定至终点,消耗Ce(SO4)2标准溶液bmL(已知: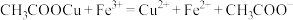 ,
, )。
)。
①产品中CH3COOCu的质量分数为_______ %(用代数式表示)。
②下列有关滴定的说法错误的是_______ (填标号)。
A.未用标准溶液润洗滴定管会使测定结果偏低
B.滴定时要适当控制滴定速度
C.在接近滴定终点时,使用“半滴操作”可提高滴定的准确度
D.滴定前滴定管尖嘴部分有气泡,滴定后无气泡,会使测定结果偏低
已知:醋酸酐可吸水生成醋酸。
回答下列问题:
(1)仪器c的名称是
(2)在氢气的氛围下,Cu2O和冰醋酸反应逐渐转化为醋酸亚铜,该过程中发生反应的化学方程式为
(3)制备过程中不可选用明火直接加热,原因是
(4)冷却三颈烧瓶中的提取液,有白色醋酸亚铜析出,经抽滤、无水乙醚迅速洗涤、
(5)产品纯度的测定:准确称取醋酸亚铜产品mg,迅速溶于过量的FeCl3溶液中得到V1mL待测液,从中量取V2mL溶液于锥形瓶中,加入2滴邻菲罗啉指示剂,立即用amol·L-1硫酸铈[Ce(SO4)2]标准溶液滴定至终点,消耗Ce(SO4)2标准溶液bmL(已知:
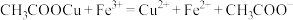 ,
, )。
)。①产品中CH3COOCu的质量分数为
②下列有关滴定的说法错误的是
A.未用标准溶液润洗滴定管会使测定结果偏低
B.滴定时要适当控制滴定速度
C.在接近滴定终点时,使用“半滴操作”可提高滴定的准确度
D.滴定前滴定管尖嘴部分有气泡,滴定后无气泡,会使测定结果偏低
您最近一年使用:0次



