名校
1 .  为阿伏加德罗常数的值下列说法正确的是
为阿伏加德罗常数的值下列说法正确的是
 为阿伏加德罗常数的值下列说法正确的是
为阿伏加德罗常数的值下列说法正确的是A.标准状况下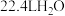 中含有的分子数为 中含有的分子数为 |
B.常温常压下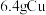 与足量 与足量 充分反应转移的电子数为 充分反应转移的电子数为 |
C.常温常压下 的 的 溶液中含有的 溶液中含有的 数目为 数目为 |
D.标准状况下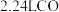 和 和 混合气体中含有的碳原子数为 混合气体中含有的碳原子数为 |
您最近一年使用:0次
2 . 铁元素在细菌的作用下可发生如图所示的转化。下列说法中正确的是

| A.反硝化过程均属于氮的固定 |
| B.硝化过程中,含氮物质均发生还原反应 |
C. 将 将 转化为 转化为 的离子方程式为 的离子方程式为 |
D.在氨氧化细菌作用下,水体中的铵态氮和硝态氮可转移到大气中,该反应中每产生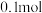 氮气时转移 氮气时转移 电子 电子 |
您最近一年使用:0次
3 . 下列有关化学反应速率的说法正确的是
A.用铁片与稀硫酸反应制取氢气时,改用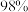 的浓硫酸可增大产生氢气的速率 的浓硫酸可增大产生氢气的速率 |
B. 的盐酸与锌片反应,加入适量的氯化钠溶液,化学反应速率不变 的盐酸与锌片反应,加入适量的氯化钠溶液,化学反应速率不变 |
C. 的催化氧化反应是一个放热反应,所以升高温度,化学反应速率减小 的催化氧化反应是一个放热反应,所以升高温度,化学反应速率减小 |
D.汽车尾气中的 与 与 可以缓慢反应生成 可以缓慢反应生成 和 和 ,增大压强,化学反应速率增大 ,增大压强,化学反应速率增大 |
您最近一年使用:0次
名校
4 . 请按要求完成下列方程式的书写。
(1) 与
与 反应的化学方程式:
反应的化学方程式:_______ 。
(2)金属钠投入氯化钠溶液_______ 。
(3)酸性条件下 与
与 溶液混合,反应的离子方程式:
溶液混合,反应的离子方程式:_______ 。
(4)氢氧化铁受热分解:_______ 。
(1)
 与
与 反应的化学方程式:
反应的化学方程式:(2)金属钠投入氯化钠溶液
(3)酸性条件下
 与
与 溶液混合,反应的离子方程式:
溶液混合,反应的离子方程式:(4)氢氧化铁受热分解:
您最近一年使用:0次
名校
5 . 物质的量是联系宏观和微观的桥梁:
(1) 个
个 气体分子的质量是
气体分子的质量是 ,则
,则 的摩尔质量是
的摩尔质量是_______ 。
(2) 氨气和
氨气和 二氧化碳,所含原子数
二氧化碳,所含原子数_______ (填“相等”或“不相等”)
(3)含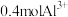 的
的 中所含的
中所含的 的个数是
的个数是_______ (用 表示),
表示), 的电离方程式是
的电离方程式是_______ 。
(4) 个
个 含
含_______ molO。
(1)
 个
个 气体分子的质量是
气体分子的质量是 ,则
,则 的摩尔质量是
的摩尔质量是(2)
 氨气和
氨气和 二氧化碳,所含原子数
二氧化碳,所含原子数(3)含
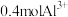 的
的 中所含的
中所含的 的个数是
的个数是 表示),
表示), 的电离方程式是
的电离方程式是(4)
 个
个 含
含
您最近一年使用:0次
6 . 下列实验中对应的操作、现象以及结论都正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 干燥氯气通入装有鲜花的集气瓶中 | 鲜花褪色 | 氯气有漂白性 |
| B | 将 溶液滴加到酸性 溶液滴加到酸性 溶液中,边加边振荡 溶液中,边加边振荡 | 溶液褪色 |  具有还原性 具有还原性 |
| C | 向某溶液中先加入 溶液,再加入稀硝酸 溶液,再加入稀硝酸 | 产生白色沉淀 | 该溶液中一定含有 |
| D | 向 溶液中加入一小块钠 溶液中加入一小块钠 | 有红色固体生成 |  与 与 发生了置换反应 发生了置换反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
7 .  常用作食盐中的补碘剂可用“氯酸钾氧化法”制备该方法的第一步反应为
常用作食盐中的补碘剂可用“氯酸钾氧化法”制备该方法的第一步反应为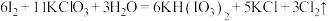 ,下列说法正确的是
,下列说法正确的是
 常用作食盐中的补碘剂可用“氯酸钾氧化法”制备该方法的第一步反应为
常用作食盐中的补碘剂可用“氯酸钾氧化法”制备该方法的第一步反应为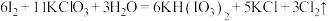 ,下列说法正确的是
,下列说法正确的是A.还原产物为 和 和 |
B.可用 与 与 燃烧后的产物溶于水制备盐酸 燃烧后的产物溶于水制备盐酸 |
C.还原剂和氧化剂的物质的量之比为 |
D.产生 时反应中转移 时反应中转移 |
您最近一年使用:0次
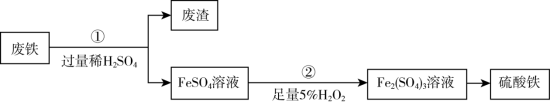
8 . 为充分利用资源,变废为宝,某研究小组采用废铁(主要成分为铁)制备硫酸铁,主要流程如下(部分 条件省略) :
(1)步骤①中主要反应的离子方程式是___________ 。
(2)分离废渣与FeSO4溶液的操作是___________ (选填“过滤”或“蒸发”)。
(3)步骤②中加入H2O2溶液发生的反应类型是___________ (选填“氧化还原反应”或“非氧化还原反应”);产生的现象是___________ 。
(4)检验SO42-的实验操作是___________ 。
(5)废铁中含有少量硫化物,反应产生的副产物与H2S,可用___________ 吸收(填选项代号)。
A.稀硫酸 B.氢氧化钠溶液 C.硫酸钠溶液
(1)步骤①中主要反应的离子方程式是
(2)分离废渣与FeSO4溶液的操作是
(3)步骤②中加入H2O2溶液发生的反应类型是
(4)检验SO42-的实验操作是
(5)废铁中含有少量硫化物,反应产生的副产物与H2S,可用
A.稀硫酸 B.氢氧化钠溶液 C.硫酸钠溶液
您最近一年使用:0次
名校
解题方法
9 . 下列反应的离子方程式正确的是
| A.氯化铜溶液与铁粉反应:Fe+Cu2+=Fe2++Cu |
B.氢氧化钡溶液和稀硫酸反应:Ba2++  =BaSO4↓ =BaSO4↓ |
| C.醋酸和氢氧化钠溶液反应:H++OH-=H2O |
| D.部分表面镀铜的铁片浸没在稀硫酸中制取氢气:Cu+2H+=Cu2++H2↑ |
您最近一年使用:0次
名校
解题方法
10 . 常温下,下列各组离子在指定溶液中一定能大量共存的是
A.澄清透明的溶液中:Na+、Fe2+、SO 、NO 、NO |
B.使石蕊变红的溶液中:Ca2+、NH 、CH3COO-、Cl- 、CH3COO-、Cl- |
C.0.1 mol·L-1 BaCl2溶液中:K+、Na+、SO 、NO 、NO |
D.碱性溶液中:Mg2+、K+、Br-、HCO |
您最近一年使用:0次



