1 . 下表列出9种元素在元素周期表(元素周期表只给出部分)中的位置
(1)考古工作者利用表中某元素的一种核素测定一些文物的年代,这种核素的原子符号是________ 。
(2)由元素②和元素④形成原子个数比为1:2的化合物的电子式为________ 。
(3)元素⑦的最高价氧化物与元素⑥的最高价氧化物的水化物的水溶液反应的离子方程式为________ 。
(4)③、④、⑤三种元素的简单氢化物稳定性顺序是________ (填化学式,用“>”连接)。
(5)元素④和⑥形成的淡黄色固体与元素①和④形成的常用化合物反应的离子方程式为________ 。
(6)将元素⑧的单质通入元素⑥和⑨形成的化合物水溶液中,观察到的现象是________ 。

(1)考古工作者利用表中某元素的一种核素测定一些文物的年代,这种核素的原子符号是
(2)由元素②和元素④形成原子个数比为1:2的化合物的电子式为
(3)元素⑦的最高价氧化物与元素⑥的最高价氧化物的水化物的水溶液反应的离子方程式为
(4)③、④、⑤三种元素的简单氢化物稳定性顺序是
(5)元素④和⑥形成的淡黄色固体与元素①和④形成的常用化合物反应的离子方程式为
(6)将元素⑧的单质通入元素⑥和⑨形成的化合物水溶液中,观察到的现象是
您最近一年使用:0次
解题方法
2 . 下列除杂的方法(括号里为少量杂质)中,所用试剂或操作不正确的是
| A.Fe2O3(Al2O3):加入足量NaOH溶液,过滤 |
| B.NaHCO3溶液(Na2CO3):通入足量的CO2 |
| C.FeCl3溶液(FeCl2):通入足量的氯气 |
| D.CO2(HCl):将气体通过盛有饱和Na2CO3溶液的洗气瓶 |
您最近一年使用:0次
3 . 与氮元素同主族的磷元素化合物有如下反应,其中反应物有:PH3、H2SO4、KClO3;生成物有:K2SO4、H3PO4、H2O和一种未知物质X。
(1)已知KClO3在反应中得到电子,则该反应的还原剂是___________ ,被氧化的元素是___________ 。
(2)已知0.2mol KClO3在反应中得到1mol电子生成X,则X的化学式为___________ 。
(3)完成并配平上述反应的化学方程式,标出电子转移方向和数目。___________
___________PH3+___________H2SO4+___________KClO3=___________K2SO4+___________H3PO4+___________H2O+___________
(4)根据上述反应可推知___________。
(5)在该反应中转移电子2mol时,生成H3PO4___________ mol。
(1)已知KClO3在反应中得到电子,则该反应的还原剂是
(2)已知0.2mol KClO3在反应中得到1mol电子生成X,则X的化学式为
(3)完成并配平上述反应的化学方程式,标出电子转移方向和数目。
___________PH3+___________H2SO4+___________KClO3=___________K2SO4+___________H3PO4+___________H2O+___________
(4)根据上述反应可推知___________。
| A.氧化性:KClO3 > H3PO4 | B.氧化性:KClO3 > H2O |
| C.还原性:PH3 > X | D.还原性:PH3 > K2SO4 |
您最近一年使用:0次
名校
4 . 现有4.1g含杂质的烧碱样品,某小组同学为测定其纯度,将其配制成250mL待测液,准确量取10.00mL待测液,并用0.2010 mol·L-1标准盐酸滴定待测烧碱溶液(假设烧碱中不含有与酸反应的杂质),试根据实验回答。
(1)在上述溶液配制与滴定过程中,不需要用到的实验仪器是___________。
(2)选用___________ 为指示剂,滴定终点的判断依据是___________ 。
(3)根据表中数据,计算样品烧碱的质量分数为___________ (结果保留两位有效数字)。
(4)滴定过程,下列情况会使测定结果偏高的是___________。
(1)在上述溶液配制与滴定过程中,不需要用到的实验仪器是___________。
A. | B. | C. | D. |
(3)根据表中数据,计算样品烧碱的质量分数为
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 10.00 | 0.50 | 20.40 |
| 第二次 | 10.00 | 4.00 | 24.10 |
| A.量取待测液的滴定管水洗后,直接用来量取待测液 |
| B.滴定前,滴定管有气泡,滴定后消失 |
| C.滴定过程中振荡锥形瓶时不慎有少量液体溅出 |
| D.盛装待测液的锥形瓶水洗后未烘干 |
您最近一年使用:0次
名校
解题方法
5 . 平衡思想是化学研究的一个重要观念,在电解质溶液中存在电离平衡、水解平衡、溶解平衡等多种平衡。
I.25℃时,三种弱酸的电离平衡常数如下:
回答下列问题:
(1)碳酸二级电离平衡常数的表达式为Ka2=___________ 。
(2)下列四种离子结合质子能力由大到小的顺序是___________ 。
A.CO B.ClO- C.CH3COO- D.HCO
B.ClO- C.CH3COO- D.HCO
(3)下列反应不能发生的是___________。
Ⅱ.体积均为10mL、pH均为2的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中pH变化如下图所示。___________ mol·L-1。
(5)用同浓度的NaOH溶液分别中和上述两种酸溶液,恰好中和时消耗NaOH溶液的体积:醋酸___________HX。
I.25℃时,三种弱酸的电离平衡常数如下:
| 弱酸 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10-5 | Ka1=4.2×10-7,Ka2=4.8×10-11 | 3.0×10-8 |
(1)碳酸二级电离平衡常数的表达式为Ka2=
(2)下列四种离子结合质子能力由大到小的顺序是
A.CO
 B.ClO- C.CH3COO- D.HCO
B.ClO- C.CH3COO- D.HCO
(3)下列反应不能发生的是___________。
A.CO +2CH3COOH=2CH3COO-+CO2↑+H2O +2CH3COOH=2CH3COO-+CO2↑+H2O |
| B.ClO-+CH3COOH=CH3COO-+HClO |
C.CO +2HClO=CO2↑+H2O+2ClO- +2HClO=CO2↑+H2O+2ClO- |
D.2ClO-+CO2+H2O=CO +2HClO +2HClO |
Ⅱ.体积均为10mL、pH均为2的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中pH变化如下图所示。
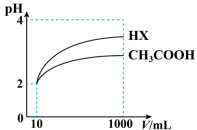
(5)用同浓度的NaOH溶液分别中和上述两种酸溶液,恰好中和时消耗NaOH溶液的体积:醋酸___________HX。
| A.大于 | B.等于 | C.小于 | D.无法比较 |
您最近一年使用:0次
解题方法
6 . 某城市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径≤2.5um的悬浮颗粒物,已知1μm=1×10-6m),其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。请回答下列问题:
(1)PM2.5分散在空气中形成的分散系___________ (填“属于"或“不属于)胶体。
(2)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据判断待测试样为___________ (填“酸”或“碱”)性。
(3)洗涤含SO2的烟气,以下物质可作洗涤剂的是___________ (填字母)
a.Ca(OH)2 b.CaCl2 c.Na2CO3 d.NaHSO3
(4)硫酸生产及煤燃烧产生的废气SO2等会对大气造成污染。
①为防止工业煤燃烧产生SO2,常向燃煤中加入CaCO3浆状物进行脱硫,脱硫的产品用于制造石膏。脱硫反应的化学方程式为___________ 。
②某硫酸化工厂,使用一种含杂质为25%的黄铁矿石(FeS2)为原料。若取2吨该矿石,可制得98%的浓硫酸___________ 吨(假设生产过程中96%SO2转化为SO3)。
(1)PM2.5分散在空气中形成的分散系
(2)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ | NH | SO | NO | Cl- |
| 浓度/mol/L | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
(3)洗涤含SO2的烟气,以下物质可作洗涤剂的是
a.Ca(OH)2 b.CaCl2 c.Na2CO3 d.NaHSO3
(4)硫酸生产及煤燃烧产生的废气SO2等会对大气造成污染。
①为防止工业煤燃烧产生SO2,常向燃煤中加入CaCO3浆状物进行脱硫,脱硫的产品用于制造石膏。脱硫反应的化学方程式为
②某硫酸化工厂,使用一种含杂质为25%的黄铁矿石(FeS2)为原料。若取2吨该矿石,可制得98%的浓硫酸
您最近一年使用:0次
解题方法
7 . 按要求回答下列问题:
(1)现有8种物质:A.稀硫酸;B.Fe2(SO4)3溶液;C.CO;D.熔融的NaNO3;E.SO2;F.Fe(OH)3胶体;G.NH4NO3固体;H.Na2CO3溶液。
①能导电的电解质有___________ (填字母,下同),属于酸性氧化物的有___________ 。
②Fe2(SO4)3溶于水的电离方程式为___________ 。
③写出实验室制取Fe(OH)3胶体的离子方程式:___________ 。
④写出H与足量A反应的离子方程式:___________ 。
(2)①甲烷(甲烷中C的化合价为-4)在厌氧氧化菌的作用下,可以和氢氧化铁发生如下反应,配平该离子方程式:___________ 。

②该反应中的还原剂为___________ (填化学式),被还原的物质与被氧化的物质的物质的量之比为___________ 。
(3)无氧条件下加热蓝铁矿(无杂质),发生反应的化学方程式为 ,蓝铁矿的质量由10.04g减小到7.16g,则n=
,蓝铁矿的质量由10.04g减小到7.16g,则n=___________ 。
(1)现有8种物质:A.稀硫酸;B.Fe2(SO4)3溶液;C.CO;D.熔融的NaNO3;E.SO2;F.Fe(OH)3胶体;G.NH4NO3固体;H.Na2CO3溶液。
①能导电的电解质有
②Fe2(SO4)3溶于水的电离方程式为
③写出实验室制取Fe(OH)3胶体的离子方程式:
④写出H与足量A反应的离子方程式:
(2)①甲烷(甲烷中C的化合价为-4)在厌氧氧化菌的作用下,可以和氢氧化铁发生如下反应,配平该离子方程式:

②该反应中的还原剂为
(3)无氧条件下加热蓝铁矿(无杂质),发生反应的化学方程式为
 ,蓝铁矿的质量由10.04g减小到7.16g,则n=
,蓝铁矿的质量由10.04g减小到7.16g,则n=
您最近一年使用:0次
8 . 氢能是极具发展潜力的清洁能源,以氢燃料为代表的燃料电池有良好的应用前景。
(1)298K时,1g 燃烧生成
燃烧生成 放热120.9kJ,1mol
放热120.9kJ,1mol 蒸发吸热44kJ,表示
蒸发吸热44kJ,表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为______ 。
(2)碱性(电解质为KOH溶液)氢氧燃料电池中负极电极反应式为______ 。
(3)工业上常用甲烷水蒸气重整制备氢气,体系中发生如下反应。
Ⅰ.
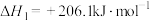
Ⅱ.

①下列措施中,不能提高 平衡转化率的是
平衡转化率的是______ (填标号)。
A.增加 用量 B.增加
用量 B.增加 用量
用量
C.恒温恒压下通入惰性气体 D.加入催化剂
②恒温恒压条件下,1mol 和1mol
和1mol 反应达平衡时,
反应达平衡时, 的转化率为
的转化率为 ,
, 的物质的量为b mol。其他条件不变,
的物质的量为b mol。其他条件不变, 起始量增加到4mol,达平衡时,
起始量增加到4mol,达平衡时,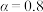 ,
,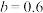 ,平衡体系中
,平衡体系中 的物质的量分数为
的物质的量分数为______ (结果保留3位有效数字,下同),该条件下,反应Ⅱ的化学平衡常数
______ 。
③“碳达峰·碳中和”是我国社会发展重大战略之一, 还原
还原 是实现“双碳”经济的有效途径之一,相关的主要反应为:
是实现“双碳”经济的有效途径之一,相关的主要反应为:

______ 。
(4)氢气还是合成氨工业的原料气,其反应为:

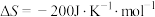 。该反应在常温下
。该反应在常温下______ (填“能”或“不能”)自发。
(1)298K时,1g
 燃烧生成
燃烧生成 放热120.9kJ,1mol
放热120.9kJ,1mol 蒸发吸热44kJ,表示
蒸发吸热44kJ,表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为(2)碱性(电解质为KOH溶液)氢氧燃料电池中负极电极反应式为
(3)工业上常用甲烷水蒸气重整制备氢气,体系中发生如下反应。
Ⅰ.

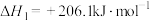
Ⅱ.


①下列措施中,不能提高
 平衡转化率的是
平衡转化率的是A.增加
 用量 B.增加
用量 B.增加 用量
用量C.恒温恒压下通入惰性气体 D.加入催化剂
②恒温恒压条件下,1mol
 和1mol
和1mol 反应达平衡时,
反应达平衡时, 的转化率为
的转化率为 ,
, 的物质的量为b mol。其他条件不变,
的物质的量为b mol。其他条件不变, 起始量增加到4mol,达平衡时,
起始量增加到4mol,达平衡时,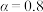 ,
,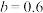 ,平衡体系中
,平衡体系中 的物质的量分数为
的物质的量分数为
③“碳达峰·碳中和”是我国社会发展重大战略之一,
 还原
还原 是实现“双碳”经济的有效途径之一,相关的主要反应为:
是实现“双碳”经济的有效途径之一,相关的主要反应为:

(4)氢气还是合成氨工业的原料气,其反应为:


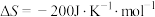 。该反应在常温下
。该反应在常温下
您最近一年使用:0次
名校
解题方法
9 . 下列离子反应方程式正确的是
A.氯气通入冷的石灰乳: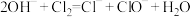 |
B.向NaHCO3溶液中滴入少量澄清石灰水: |
C.向明矾溶液中滴加Ba(OH)2溶液到 恰好完全沉淀时: 恰好完全沉淀时: |
| D.向FeI2溶液中通入少量氯气:Cl2 + 2I- = 2Cl- + I2 |
您最近一年使用:0次
解题方法
10 . 甲烷干重整(DRM)是利用 和
和 在催化剂的作用下制备合成气,作为可持续替代燃料。DRM的主要反应为:
在催化剂的作用下制备合成气,作为可持续替代燃料。DRM的主要反应为:
Ⅰ.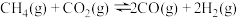
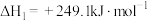
Ⅱ.
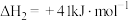
该过程中还伴随积碳反应的发生。
(1)一定压强下,由最稳定单质生成 化合物的焓变为该物质的摩尔生成焓。已知
化合物的焓变为该物质的摩尔生成焓。已知 、
、 的摩尔生成焓分别为
的摩尔生成焓分别为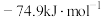 、
、 。则
。则 的摩尔生成焓为
的摩尔生成焓为_______  。
。
(2)甲烷和二氧化碳的起始物质的量均为 ,实验测得在
,实验测得在 下,平衡时各组分的量随温度变化如图所示。
下,平衡时各组分的量随温度变化如图所示。_______ mol,反应Ⅱ的压强平衡常数
_______ 。
②为了消除积碳带来的影响,反应选择在_______ (填“高温”或“低温”)下进行。
(3)在不同压强下,按照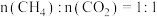 投料,假设只发生反应Ⅰ和Ⅱ。
投料,假设只发生反应Ⅰ和Ⅱ。 的平衡转化率随温度的变化关系如图所示。
的平衡转化率随温度的变化关系如图所示。 、
、 、
、 ,三者由大到小顺序为
,三者由大到小顺序为________ 。
②压强 、
、 、
、 、
、 由小到大的顺序为
由小到大的顺序为________ 。
③ ,四条曲线几乎交于一点的原因是
,四条曲线几乎交于一点的原因是________ 。
 和
和 在催化剂的作用下制备合成气,作为可持续替代燃料。DRM的主要反应为:
在催化剂的作用下制备合成气,作为可持续替代燃料。DRM的主要反应为:Ⅰ.
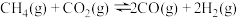
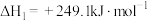
Ⅱ.

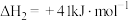
该过程中还伴随积碳反应的发生。
(1)一定压强下,由最稳定单质生成
 化合物的焓变为该物质的摩尔生成焓。已知
化合物的焓变为该物质的摩尔生成焓。已知 、
、 的摩尔生成焓分别为
的摩尔生成焓分别为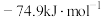 、
、 。则
。则 的摩尔生成焓为
的摩尔生成焓为 。
。(2)甲烷和二氧化碳的起始物质的量均为
 ,实验测得在
,实验测得在 下,平衡时各组分的量随温度变化如图所示。
下,平衡时各组分的量随温度变化如图所示。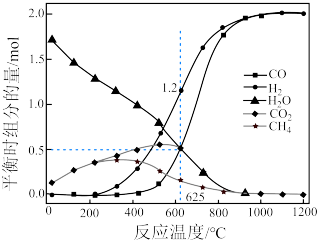

②为了消除积碳带来的影响,反应选择在
(3)在不同压强下,按照
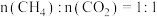 投料,假设只发生反应Ⅰ和Ⅱ。
投料,假设只发生反应Ⅰ和Ⅱ。 的平衡转化率随温度的变化关系如图所示。
的平衡转化率随温度的变化关系如图所示。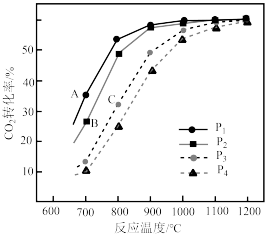
 、
、 、
、 ,三者由大到小顺序为
,三者由大到小顺序为②压强
 、
、 、
、 、
、 由小到大的顺序为
由小到大的顺序为③
 ,四条曲线几乎交于一点的原因是
,四条曲线几乎交于一点的原因是
您最近一年使用:0次



