名校
解题方法
1 . 标准状况下,1.5mol 的体积为
的体积为
 的体积为
的体积为| A.11.2L | B.22.4L | C.33.6L | D.67.2L |
您最近一年使用:0次
2024-05-22更新
|
78次组卷
|
5卷引用:贵州省长顺文博高级中学2020-2021学年高二上学期期中考试化学试题
贵州省长顺文博高级中学2020-2021学年高二上学期期中考试化学试题广西桂林市第十八中学2019-2020学年高二上学期期中考试化学(文)试题湖南省普通高中2024届高三学业水平合格性考试模拟试卷(二)化学试题(已下线)山东省青岛市2023-2024学年高三下学期第三次模拟考试化学试题(已下线)江苏省南京市第十三中学2024届高三下学期适应性考试化学试题
11-12高二上·河南郑州·阶段练习
名校
解题方法
2 .  是一种高效清洁的火箭燃料。
是一种高效清洁的火箭燃料。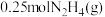 完全燃烧生成
完全燃烧生成 和
和 时,放出133.5 kJ热量。则下列热化学方程式正确的是
时,放出133.5 kJ热量。则下列热化学方程式正确的是
A.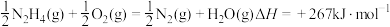 |
B. |
C. |
D.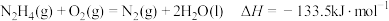 |
您最近一年使用:0次
2024-03-17更新
|
252次组卷
|
36卷引用:贵州省龙里中学2022-2023学年高二上学期11月期中考试化学试题
贵州省龙里中学2022-2023学年高二上学期11月期中考试化学试题(已下线)2011-2012学年辽宁省抚顺县高级中学高一下学期期中考试化学试卷江苏省清江中学2016-2017学年高一下学期期中考试化学试题【全国百强校】陕西省西安市长安区第一中学2018-2019学年高二上学期期中考试化学试题吉林省辽源市田家炳高级中学2019-2020学年高二上学期期中考试化学试题福建省宁德市高中同心顺联盟校2019-2020学年高二上学期期中考试化学试题江苏省无锡市江阴市高级中学2019-2020学年高一下学期期中考试化学试题陕西省榆林市绥德中学2021-2022学年高二下学期第一次阶段性测试化学试题江苏省宿迁市沭阳县2021-2022学年高一下学期期中调研测试化学试题西藏林芝市第二高级中学2021-2022学年高二上学期期中考试理综化学试题天津北京师范大学静海附属学校 (天津市静海区北师大实验学校)2023-2024学年高三上学期第二次阶段检测(期中)化学试题(已下线)2011-2012年河南省郑州四十七中高二上学期第一次月考化学试卷(已下线)2012届山东省枣庄十八中高三10月份质量检测化学试卷(已下线)2011-2012学年福建南平政和一中高二期末考试化学试卷(已下线)2011-2012学年浙江省嵊泗中学高二上学期第一次月考化学试卷一(已下线)2014届新疆乌鲁木齐市兵团二中高二(上)期末化学试卷2016-2017学年山东省德州市陵城一中高二上10月月考化学试卷山东省枣庄市第八中学南校区高二10月份月考化学试题山东省枣庄市第八中学东校区2017-2018学年高二10月月考化学试题广东省惠阳高级中学2017-2018学年高二上学期10月月考理科综合化学试题福建省惠安惠南中学2017-2018学年高二10月月考(理)化学试题山东省锦泽技工学校2017-2018学年高二10月月考化学试题河南省镇平县第一高级中学2018-2019学年高二上学期第一次月考化学试题高二人教版选修4 第一章 第一节 化学反应与能量的变化江西省南昌市第十中学2018-2019学年高一下学期期末考试化学试题人教版高中化学选修4第一章《化学反应与能量》测试卷鲁科版(2019)高二选择性必修第一册第1章 化学反应与能量变化 第1节 化学反应的热效应 课时2 热化学方程式人教版(2019)高二化学选择性必修1第一章 化学反应的热效应 第一节 反应热 课时2 热化学方程式 燃烧热云南省富宁县一中2020-2021学年高二下学期第一次月考化学试题陕西省咸阳市咸阳市实验中学2020-2021学年高二下学期第一次月考化学试题选择性必修1(SJ)专题1第一单元课时2 热化学方程式北京市首都师范大学附属密云中学2022-2023学年高二上学期10月阶段性练习化学试题西藏拉萨中学2022-2023学年高二上学期期末考试化学试题江苏省常州市联盟学校2022-2023学年高一下学期5月学情调研化学试题(已下线)BBWYhjhx1101河南省郑州市宇华实验学校2023-2024学年高二下学期开学考试化学试题
13-14高三下·山东青岛·阶段练习
名校
解题方法
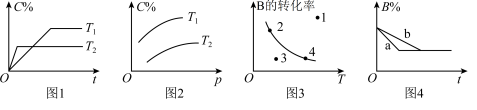
3 . 反应mA(g)+nB(g) pC(g)的速率和平衡图像如下,下列判断正确的是
pC(g)的速率和平衡图像如下,下列判断正确的是
 pC(g)的速率和平衡图像如下,下列判断正确的是
pC(g)的速率和平衡图像如下,下列判断正确的是
| A.图1中,T1<T2,该反应正反应为吸热反应 |
| B.图3中,表示反应速率v正>v逆的是点3 |
| C.图2中,该反应m+n<p |
| D.图4中,若m+n=p,则a曲线一定使用了催化剂 |
您最近一年使用:0次
2024-01-11更新
|
167次组卷
|
97卷引用:贵州省龙里中学2022-2023学年高二上学期11月期中考试化学试题
贵州省龙里中学2022-2023学年高二上学期11月期中考试化学试题2015-2016学年黑龙江大庆市铁人中学高一下期中化学试卷2016-2017学年陕西西安中学高二平行班上期中化学卷云南省玉溪市玉溪一中2017-2018学年高二上学期第二次月考化学试题【校级联考】江西省南昌市八一中学、洪都中学七校2018-2019学年高二上学期期中考试化学试题【全国百强校】山东省济南第一中学2018-2019学年高二上学期期中考试化学试题【全国百强校】四川省雅安市雅安中学2018-2019学年高二上学期期中考试化学试题辽宁省大连市第一〇三中学2018-2019学年高二上学期期中考试化学试题福建省福建师范大学附属中学2019-2020学年高二上学期期中考试化学(选考)试题广东省广州市2019-2020学年高二上学期期中模拟测试化学试题(二)山东省德州市陵城区第一中学2019-2020学年高二上学期期中考试化学试题山东省潍坊市安丘市实验中学2019-2020学年高一下学期期中考试化学试题河北省保定市2019-2020学年高二下学期期中考试化学试题云南省昆明师范专科学校附属中学2020-2021学年高二上学期期中考试化学试题福建省永安市第一中学2020-2021学年高二上学期期中考试化学试题江西省吉安市(吉安县三中、泰和二中、安福二中、井大附中 )2021-2022学年高二上学期期中考试化学试题陕西省泾阳县2020-2021学年高二上学期期中考试化学试题吉林省长春市希望高中2021-2022学年高二上学期期中考试化学试题吉林省长春市十一高中2021-2022学年高二上学期期中考试化学试题吉林省吉林市第一中学2021-2022学年高一下学期(平行班)期中考试化学试题广东省江门市新会华侨中学2022-2023学年高二上学期期中考试化学试题四川省成都外国语学校2022-2023学年高二上学期期中考试化学试题广东省珠海市斗门第一中学2022-2023学年高二上学期期中考试化学试题广东省深圳市第七高级中学2021-2022学年高二上学期期中考试化学试题新疆乌鲁木齐市第四中学2022-2023学年高二下学期期中阶段诊断测试化学试题广东省深圳市盐田高级中学2023-2024高二上学期期中考试化学试题山东省青岛第三中学2023-2024学年高二上学期期中考试化学试卷北京市第一七一中学2022-2023学年高二上学期期中考试化学试题(已下线)2014届山东省青岛市高三3月统一质量检测理综化学试卷2016届辽宁省五校协作体高三上学期期初考试化学试卷2015-2016学年安徽省六安一中高二上第一阶段测化学试卷2015-2016学年辽宁葫芦岛一中等五校高二6月联考化学卷2015-2016学年辽宁庄河高中高二下期末化学试卷2017届辽宁省铁岭市协作体高三第三次联考化学试卷江西省宜春市上高二中2017-2018学年高二第一次月考化学试题河南省滑县第二高级中学2017-2018学年高二12月月考化学试题河南省中原名校(即豫南九校)2017-2018学年高二上学期第三次联考化学试题宁夏银川一中2017-2018学年高二上学期期末考试化学试题辽宁省大连市普兰店区第二中学2017-2018学年高二上学期期末考试化学试题黑龙江省伊春中学2017-2018学年高二化学上学期期末考试试题高二人教版选修4 期末学业测评(二)【全国百强校】福建省三明市第一中学2019届高三上学期第二次月考化学试题江西省奉新县第一中学2019-2020学年高二上学期第一次月考化学试题安徽省青阳县第一中学2019-2020学年高二10月月考化学试题内蒙古第一机械制造(集团)有限公司第一中学2019-2020学年高二10月月考化学试题四川省蓬溪县蓬南中学2019-2020学年高二上学期第四次月考化学试题2019年秋高三化学复习强化练习—— 化学反应速率及化学平衡新疆昌吉市教育共同体2019-2020学年高二年级上学期期末考试化学试题夯基提能2020届高三化学选择题对题专练——选修4化学反应原理—— 化学平衡移动及其影响因素(强化练习)甘肃省张掖市2019—2020学年高二上学期期末学业水平质量检测化学试题山东省滕州市第一中学2019-2020学年高一下学期第一次月考化学试题河北省承德市第一中学2019-2020学年高一下学期第4次周测化学试题江西省宜春市樟树市滨江中学2018-2019学年高二上学期第一次月考化学试题云南省昆明市官渡区第一中学2019-2020学年高二下学期开学考试化学试题河北省石家庄市第二中学2019-2020学年高一7月期末考试百分练习化学试题河北省石家庄市第二中学2019-2020高一下期末考试化学模拟试题(三)吉林省东北师范大学附属中学2020届高三上学期第二次模拟考试化学试题江西省赣州市赣县区第三中学2020-2021学年高二上学期强化训练(一)化学试题广东省广州市广东实验中学2020-2021学年高二上学期月考化学试题江西省靖安中学2020-2021学年高二上学期第一次月考化学试题四川省广安友谊中学2021-2022学年上学期高二10月月考化学试题山东省济南市历城第一中学2021-2022学年高二上学期10月月考化学试题(已下线)第七单元 化学反应速率与化学平衡(A卷 新题基础练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)江西省丰城中学 2021-2022 学年高三上学期第四次段考化学试题(尖子重点班)新疆昌吉州2021-2022学年高二上学期期末考试化学试题福建省南平高级中学2021-2022学年高三上学期12月月考化学试题河北省盐山中学2021-2022学年高二12月月考化学试题安徽省亳州市第一中学2021-2022学年高二上学期第二次月考化学试题甘肃省永昌县第一高级中学2021-2022学年高二上学期期末考试化学试题江西省山江湖协作体2021-2022学年高二上学期联考(统招班)化学试题陕西省西安市西航一中2021-2022学年高二上学期期末考试化学试题浙江省杭州市浙江大学附属中学2021-2022学年高二上学期期末考试化学试题天津市汇文中学2022-2023学年高二上学期第二次阶段性测试化学试题广东省珠海市斗门区第一中学2022-2023学年高二上学期第一次考试化学试题山东省青岛第二中学2022-2023学年高二上学期10月月考化学试题陕西省咸阳市实验中学2021-2022学年高二上学期第二次月考化学试题河南郑州外国语学校2022-2023学年高三上学期调研考试2化学试题重庆市南川中学2022-2023学年高二上学期第一学月考试化学试题广东省梅州市兴宁市沐彬中学2022-2023学年高二上学期第二次月考化学试题吉林省乾安县第七中学2021-2022学年高二上学期第一次质量检测化学试题吉林省四平市第一高级中学2022-2023学年高三上学期第三次月考化学试题内蒙古自治区包头市第九中学2022-2023学年高二上学期期末考试化学试题河北省唐山市开滦第一中学2022-2023学年高二上学期期末考试化学试题甘肃天祝藏族自治县第一中学2022-2023学年高二上学期1月期末考试化学试题广东省大湾区2022-2023学年高二上学期期末联考化学试题四川省内江市第六中学2022-2023学年高二下学期入学考试化学试题 (已下线)第七章 化学反应速率与化学平衡 第44练 化学反应速率、平衡的常规图像湖北省十堰市部分重点中学2022-2023学年高二下学期3月联考化学试题河南省郑州外国语学校2022-2023学年高三上学期12月月考化学试题四川省双流中学2023-2024学年高二上学期10月月考化学试题广东省广州市第八十九中学2023-2024学年高二上学期10月月考化学试题四川省仪陇中学校2023-2024学年高二上学期10月月考化学试题四川省成都列五中学2023-2024学年高二上学期10月月考化学试题云南省昭通市盐津县第二中学2023-2024学年高二上学期期末考试化学试题(已下线)广西“贵百河”2023-2024学年高二上学期12月份联考化学试题山东省泰安市2023-2024学年高二上学期第四次调研测试化学试题山西省运城市河津中学2023-2024学年高二下学期开学考试化学试题
4 . 完成下列填空
(1)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较时间保持稳定的放电电压。
高铁电池的总反应为: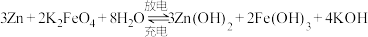
请回答下列问题:
①高铁电池放电时,负极发生___________ (填“氧化”或“还原”)反应,则正极电极反应式为___________ 。
②放电时,___________ (填“正极”或“负极”)附近溶液的碱性减弱。
(2)某种燃料电池的工作原理如图所示,a、b均为惰性电极。
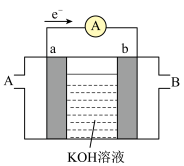
①使用时,空气从___________ 口通入(填“A”或“B”);
②假设使用的“燃料”是甲烷,a极的电极反应式为___________
③假设使用的“燃料”是水煤气(成分为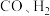 ),如用这种电池在待镀金属表面镀银,待镀金属的质量增加
),如用这种电池在待镀金属表面镀银,待镀金属的质量增加 ,则至少消耗标准状况下水煤气的体积为
,则至少消耗标准状况下水煤气的体积为___________ L。
(1)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较时间保持稳定的放电电压。
高铁电池的总反应为:
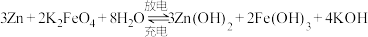
请回答下列问题:
①高铁电池放电时,负极发生
②放电时,
(2)某种燃料电池的工作原理如图所示,a、b均为惰性电极。

①使用时,空气从
②假设使用的“燃料”是甲烷,a极的电极反应式为
③假设使用的“燃料”是水煤气(成分为
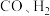 ),如用这种电池在待镀金属表面镀银,待镀金属的质量增加
),如用这种电池在待镀金属表面镀银,待镀金属的质量增加 ,则至少消耗标准状况下水煤气的体积为
,则至少消耗标准状况下水煤气的体积为
您最近一年使用:0次
名校
5 . 回答下列问题
(1)甲醇是一种可再生能源,由 制备甲醇可能涉及的反应如下:
制备甲醇可能涉及的反应如下:
反应Ⅰ: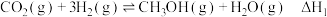
反应Ⅱ: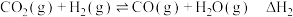
反应Ⅲ: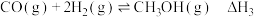
反应Ⅰ、Ⅱ、Ⅲ平衡常数分别为 ,则
,则
___________ (用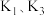 表示)。
表示)。
(2)某探究小组用 与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用
与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用 浓度为
浓度为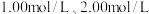 ,大理石有细颗粒和粗颗粒两种规格,实验温度为
,大理石有细颗粒和粗颗粒两种规格,实验温度为 、
、 ,每次实验
,每次实验 的用量为
的用量为 ,大理石用量为
,大理石用量为 。
。
请完成实验设计表,其中a为___________ ,e为___________ 。
(3)①氯气是制备系列含氯化合物的主要原料,可采用如图A所示的装置来制取氯气。装置中的离子膜只允许___________ (填“ ”或“
”或“ ”)通过,氯气的逸出口是
”)通过,氯气的逸出口是___________ (填标号“ ”或“b”)。
”或“b”)。

② 和
和 都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图B所示:阴极上的反应式为
都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图B所示:阴极上的反应式为___________ 。

(1)甲醇是一种可再生能源,由
 制备甲醇可能涉及的反应如下:
制备甲醇可能涉及的反应如下:反应Ⅰ:
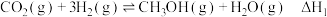
反应Ⅱ:
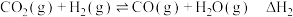
反应Ⅲ:
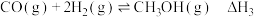
反应Ⅰ、Ⅱ、Ⅲ平衡常数分别为
 ,则
,则
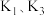 表示)。
表示)。(2)某探究小组用
 与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用
与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用 浓度为
浓度为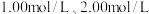 ,大理石有细颗粒和粗颗粒两种规格,实验温度为
,大理石有细颗粒和粗颗粒两种规格,实验温度为 、
、 ,每次实验
,每次实验 的用量为
的用量为 ,大理石用量为
,大理石用量为 。
。| 实验编号 | 温度( ) ) | 大理石规格 |  (浓度) (浓度)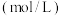 | 实验目的 |
| ① | 25 | 粗颗粒 | 2.00 | (Ⅰ)实验①和②探究浓度对反应速率的影响; (Ⅱ)实验①和③探究温度对反应速率的影响; (Ⅲ)实验①和④探究e___________对反应速率的影响 |
| ② | 25 | 粗颗粒 | a___________ | |
| ③ | b___________ | 粗颗粒 | 2.00 | |
| ④ | c___________ | 细颗粒 | d___________ |
(3)①氯气是制备系列含氯化合物的主要原料,可采用如图A所示的装置来制取氯气。装置中的离子膜只允许
 ”或“
”或“ ”)通过,氯气的逸出口是
”)通过,氯气的逸出口是 ”或“b”)。
”或“b”)。
②
 和
和 都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图B所示:阴极上的反应式为
都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图B所示:阴极上的反应式为
您最近一年使用:0次
名校
6 . 将气体 置于固定容积为2L的密闭容器中,发生如下反应:
置于固定容积为2L的密闭容器中,发生如下反应: ,反应进行到10s末,达到平衡,测得
,反应进行到10s末,达到平衡,测得 的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为
的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为 。
。
(1)用 表示
表示 内反应的平均反应速率为
内反应的平均反应速率为___________ 。
(2)反应前B的物质的量浓度是___________ 。
(3)平衡后,若改变下列条件,生成D的速率如何变化(填“增大”、“减小”或“不变”):
①增大压强___________ ;
②降低温度___________ 。
(4)下列叙述能说明该反应已达到化学平衡状态的是___________ (填标号)。
A.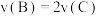
B. 的体积分数不再变化
的体积分数不再变化
C.容器内气体密度不再发生变化
D.容器内压强不再发生变化
E.相同时间内生成 的B的同时生成
的B的同时生成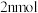 的D
的D
(5)向平衡后的容器中继续充入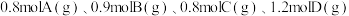 ,此时,v(正)
,此时,v(正)___________ v(逆)。(填“>”、“=”或“<”)
 置于固定容积为2L的密闭容器中,发生如下反应:
置于固定容积为2L的密闭容器中,发生如下反应: ,反应进行到10s末,达到平衡,测得
,反应进行到10s末,达到平衡,测得 的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为
的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为 。
。(1)用
 表示
表示 内反应的平均反应速率为
内反应的平均反应速率为(2)反应前B的物质的量浓度是
(3)平衡后,若改变下列条件,生成D的速率如何变化(填“增大”、“减小”或“不变”):
①增大压强
②降低温度
(4)下列叙述能说明该反应已达到化学平衡状态的是
A.
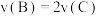
B.
 的体积分数不再变化
的体积分数不再变化C.容器内气体密度不再发生变化
D.容器内压强不再发生变化
E.相同时间内生成
 的B的同时生成
的B的同时生成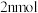 的D
的D(5)向平衡后的容器中继续充入
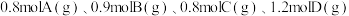 ,此时,v(正)
,此时,v(正)
您最近一年使用:0次
名校
解题方法
7 . 回答下列问题
(1)已知:

则
___________ (填“>”或“<”) 。
。
(2)已知在 时:
时:
①
②
写出 与
与 反应生成
反应生成 的热化学方程式
的热化学方程式___________ 。
(3)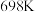 时,向VL的密闭容器中充入
时,向VL的密闭容器中充入 和
和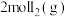 ,发生反应:
,发生反应: ,测得各物质的物质的量浓度与时间变化的关系如图所示。
,测得各物质的物质的量浓度与时间变化的关系如图所示。
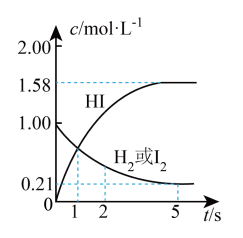
请回答下列问题:
①
___________ 。
②该反应达到最大限度的时间是___________ ,该时间内平均反应速率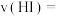
___________ 。
③该反应达到平衡状态时,放出的热量为___________ 。
(1)已知:


则

 。
。(2)已知在
 时:
时:①

②

写出
 与
与 反应生成
反应生成 的热化学方程式
的热化学方程式(3)
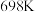 时,向VL的密闭容器中充入
时,向VL的密闭容器中充入 和
和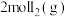 ,发生反应:
,发生反应: ,测得各物质的物质的量浓度与时间变化的关系如图所示。
,测得各物质的物质的量浓度与时间变化的关系如图所示。
请回答下列问题:
①

②该反应达到最大限度的时间是
③该反应达到平衡状态时,放出的热量为
您最近一年使用:0次
名校
8 . 我国提出努力争取2060年前实现碳中和目标,通过反应将 转化为
转化为 是实现该目标的一种方式。回答下列问题:
是实现该目标的一种方式。回答下列问题:
(1)向 恒容密闭容器中充入
恒容密闭容器中充入 和
和 ,发生反应
,发生反应 测定不同温度下
测定不同温度下 的平衡转化率如表所示。
的平衡转化率如表所示。
①该反应的
___________ (填“>”或“<”)0
已知: ,
,
则反应

___________ (用 和
和 表示)。
表示)。
②下列有利于增大 的平衡转化率的措施为
的平衡转化率的措施为___________ (填标号)。
a.增大反应体系的压强 b.增大
c.降低反应温度 d.移出
(3)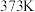 下,该反应的平衡常数
下,该反应的平衡常数
___________ (用含 的代数式表示)。
的代数式表示)。
(2)浙江大学某实验室用水热法还原 转化为
转化为 ,探究了不同条件下
,探究了不同条件下 的转化率,数据如图所示。
的转化率,数据如图所示。
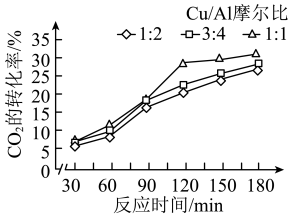
根据以上数据,最佳的Cu/Al摩尔比和反应时间分别是___________ 、___________ 。
 转化为
转化为 是实现该目标的一种方式。回答下列问题:
是实现该目标的一种方式。回答下列问题:(1)向
 恒容密闭容器中充入
恒容密闭容器中充入 和
和 ,发生反应
,发生反应 测定不同温度下
测定不同温度下 的平衡转化率如表所示。
的平衡转化率如表所示。 | 373 | 473 | 573 | 673 |
 的平衡转化率 的平衡转化率 |  | 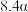 | 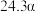 | 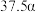 |

已知:
 ,
,则反应


 和
和 表示)。
表示)。②下列有利于增大
 的平衡转化率的措施为
的平衡转化率的措施为a.增大反应体系的压强 b.增大

c.降低反应温度 d.移出

(3)
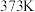 下,该反应的平衡常数
下,该反应的平衡常数
 的代数式表示)。
的代数式表示)。(2)浙江大学某实验室用水热法还原
 转化为
转化为 ,探究了不同条件下
,探究了不同条件下 的转化率,数据如图所示。
的转化率,数据如图所示。
根据以上数据,最佳的Cu/Al摩尔比和反应时间分别是
您最近一年使用:0次
名校
解题方法
9 . 银锌纽扣电池放电时反应为 。下列说法错误的是
。下列说法错误的是
 。下列说法错误的是
。下列说法错误的是A.电池工作时,电子从 极经过电解质溶液流到Zn极 极经过电解质溶液流到Zn极 |
| B.该电池的电解质溶液呈碱性 |
| C.Zn是电池的负极,发生氧化反应 |
D.正极的电极反应式: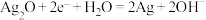 |
您最近一年使用:0次
2023-09-25更新
|
256次组卷
|
2卷引用:贵州省龙里中学2022-2023学年高二上学期11月期中考试化学试题
10 . 下列有关电解原理的应用的说法正确的是
| A.氯化铝是一种电解质,可用于电解法制铝 |
| B.在铁制品上镀银时,铁制品与电源正极相连 |
| C.电解法精炼铜时,以粗铜作阴极,纯铜作阳极 |
D.电解饱和食盐水时,阴极反应式为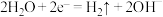 |
您最近一年使用:0次



