1 . 实验室用浓盐酸、二氧化锰共热制氯气,并用氯气和Ca(OH)2制取少量漂白粉,制备漂白粉的反应是放热反应,温度稍高即发生副反应:6Cl2+6Ca(OH)2=Ca(ClO3)2+5CaCl2+6H2O。
(1)请写出化学实验室制备氯气的离子反应方程式___________ 。
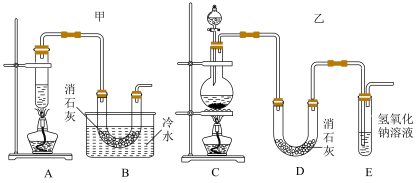
(2)现有两个同学分别设计的两套实验制备漂白粉,实验装置如图:___________ ,同学们发现制备出的产品中氯化钙含量比预期高,推断该组合中还缺少的装置是___________ 。
(3)此实验所得Ca(ClO)2产率太低。如图为反应后溶液中ClO-、 离子的物质的量n与反应时间t的关系曲线(不考虑氯气和水的反应)。
离子的物质的量n与反应时间t的关系曲线(不考虑氯气和水的反应)。___________ 离子的物质的量随反应时间变化的关系,该石灰乳中Ca(OH)2物质的量为___________ mol
②另取一份含有等物质的量Ca(OH)2的石灰乳,以较大的速率通入足量氯气,充分反应后测得产物中Cl-的物质的量为0.39mol,则产物中n(ClO-):n( )=
)=___________ 。
(4)漂白粉长时间暴露在空气中容易发生变质,为了判断一份久置的漂白粉是否变质及变质程度,甲、乙两位同学分别设计实验进行验证:甲同学取适量漂白粉样品,滴加浓盐酸,将产生的气体直接通入澄清石灰水中,没有发现石灰水变浑浊。乙同学改用滴加稀盐酸,发现产生大量气泡,将气体通入澄清石灰水中,石灰水变浑浊:他又取少量漂白粉样品配成溶液,滴在pH试纸上,最终试纸变白。
已知:Ca(ClO)2溶液呈碱性:
①漂白粉中的Ca(ClO)2能与空气中的CO2和水蒸气反应,写出该反应的化学方程式___________ 。
②乙同学认为甲同学的实验无法证明漂白粉是否变质,原因是___________ 。
(1)请写出化学实验室制备氯气的离子反应方程式
(2)现有两个同学分别设计的两套实验制备漂白粉,实验装置如图:
(3)此实验所得Ca(ClO)2产率太低。如图为反应后溶液中ClO-、
 离子的物质的量n与反应时间t的关系曲线(不考虑氯气和水的反应)。
离子的物质的量n与反应时间t的关系曲线(不考虑氯气和水的反应)。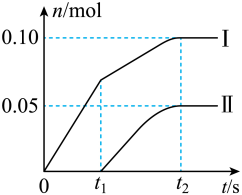
②另取一份含有等物质的量Ca(OH)2的石灰乳,以较大的速率通入足量氯气,充分反应后测得产物中Cl-的物质的量为0.39mol,则产物中n(ClO-):n(
 )=
)=(4)漂白粉长时间暴露在空气中容易发生变质,为了判断一份久置的漂白粉是否变质及变质程度,甲、乙两位同学分别设计实验进行验证:甲同学取适量漂白粉样品,滴加浓盐酸,将产生的气体直接通入澄清石灰水中,没有发现石灰水变浑浊。乙同学改用滴加稀盐酸,发现产生大量气泡,将气体通入澄清石灰水中,石灰水变浑浊:他又取少量漂白粉样品配成溶液,滴在pH试纸上,最终试纸变白。
已知:Ca(ClO)2溶液呈碱性:
①漂白粉中的Ca(ClO)2能与空气中的CO2和水蒸气反应,写出该反应的化学方程式
②乙同学认为甲同学的实验无法证明漂白粉是否变质,原因是
您最近一年使用:0次
名校
解题方法
2 . 钛在医疗领域的使用非常广泛,如制人造关节、头盖、主动心瓣等。 是制备金属钛的重要中间体。某小组同学利用如下装置在实验室制备
是制备金属钛的重要中间体。某小组同学利用如下装置在实验室制备 (夹持装置略去)。
(夹持装置略去)。
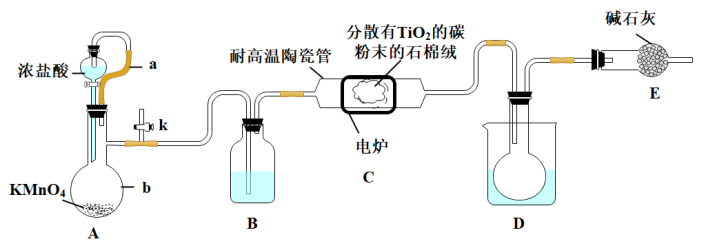
已知:HCl与 不发生反应;装置C中除生成
不发生反应;装置C中除生成 外,同时还生成一种有毒气态氧化物和少量
外,同时还生成一种有毒气态氧化物和少量 。其它相关信息如下表所示:
。其它相关信息如下表所示:
请回答下列问题:
(1)装置A中导管a的作用为___________ ,装置B中所盛试剂为___________ ,装置A中发生反应的离子方程式为___________ (反应后Mn元素以 形式存在)。
形式存在)。
(2)组装好仪器后,部分实验步骤如下:
a.装入药品 b.打开分液漏斗活塞 c.检查装置气密性 d.关闭分液漏斗活塞 e.停止加热,充分冷却 f.加热装置C中陶瓷管
从上述选项选择合适操作(不重复使用)并排序:___________→___________→b→___________→___________→d。__________
(3)下列说法不正确 的是___________ 。
A.通入氯气之前,最好先从k处通入氮气,否则实验会失败
B.石棉绒载体是为了增大气体与 、碳粉的接触面积,以加快反应速率
、碳粉的接触面积,以加快反应速率
C.装置D中的烧杯中可加入冰水,便于收集到纯的液态
D.装置E可防止空气中的水蒸气进入装置D的圆底烧瓶中使 变质
变质
E.该装置有缺陷,通过装置E后的气体不可直接排放到空气中
(4) 可制备纳米
可制备纳米 :以
:以 为载体,用
为载体,用 和水蒸气反应生成
和水蒸气反应生成 。再控制温度生成纳米
。再控制温度生成纳米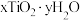 。测定产物
。测定产物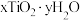 组成的方法如下:
组成的方法如下:
步骤一:取样品2.100g用稀硫酸充分溶解得到 ,再用足量铝将
,再用足量铝将 还原为
还原为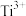 ,过滤并洗涤,将所得滤液和洗涤液合并注入250mL容量瓶,定容得到待测液。
,过滤并洗涤,将所得滤液和洗涤液合并注入250mL容量瓶,定容得到待测液。
步骤二:取待测液25.00mL于锥形瓶中,加几滴KSCN溶液作指示剂,用 的
的 标准溶液滴定,将
标准溶液滴定,将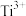 氧化为
氧化为 ,三次滴定消耗标准溶液的平均值为24.00mL。
,三次滴定消耗标准溶液的平均值为24.00mL。
①滴定终点的判断方法是___________ 。
②通过分析、计算,该样品的组成为___________ 。
 是制备金属钛的重要中间体。某小组同学利用如下装置在实验室制备
是制备金属钛的重要中间体。某小组同学利用如下装置在实验室制备 (夹持装置略去)。
(夹持装置略去)。
已知:HCl与
 不发生反应;装置C中除生成
不发生反应;装置C中除生成 外,同时还生成一种有毒气态氧化物和少量
外,同时还生成一种有毒气态氧化物和少量 。其它相关信息如下表所示:
。其它相关信息如下表所示:| 熔点/℃ | 沸点/℃ | 密度/(g/cm3) | 水溶性 | |
 | -24 | 136.4 | 1.7 | 易水解生成白色沉淀,能溶于有机溶剂 |
 | -23 | 76.8 | 1.6 | 难溶于水 |
(1)装置A中导管a的作用为
 形式存在)。
形式存在)。(2)组装好仪器后,部分实验步骤如下:
a.装入药品 b.打开分液漏斗活塞 c.检查装置气密性 d.关闭分液漏斗活塞 e.停止加热,充分冷却 f.加热装置C中陶瓷管
从上述选项选择合适操作(不重复使用)并排序:___________→___________→b→___________→___________→d。
(3)下列说法
A.通入氯气之前,最好先从k处通入氮气,否则实验会失败
B.石棉绒载体是为了增大气体与
 、碳粉的接触面积,以加快反应速率
、碳粉的接触面积,以加快反应速率C.装置D中的烧杯中可加入冰水,便于收集到纯的液态

D.装置E可防止空气中的水蒸气进入装置D的圆底烧瓶中使
 变质
变质E.该装置有缺陷,通过装置E后的气体不可直接排放到空气中
(4)
 可制备纳米
可制备纳米 :以
:以 为载体,用
为载体,用 和水蒸气反应生成
和水蒸气反应生成 。再控制温度生成纳米
。再控制温度生成纳米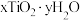 。测定产物
。测定产物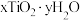 组成的方法如下:
组成的方法如下:步骤一:取样品2.100g用稀硫酸充分溶解得到
 ,再用足量铝将
,再用足量铝将 还原为
还原为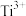 ,过滤并洗涤,将所得滤液和洗涤液合并注入250mL容量瓶,定容得到待测液。
,过滤并洗涤,将所得滤液和洗涤液合并注入250mL容量瓶,定容得到待测液。步骤二:取待测液25.00mL于锥形瓶中,加几滴KSCN溶液作指示剂,用
 的
的 标准溶液滴定,将
标准溶液滴定,将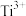 氧化为
氧化为 ,三次滴定消耗标准溶液的平均值为24.00mL。
,三次滴定消耗标准溶液的平均值为24.00mL。①滴定终点的判断方法是
②通过分析、计算,该样品的组成为
您最近一年使用:0次
2022-01-27更新
|
463次组卷
|
3卷引用:浙江省金衢六校联盟2021-2022学年高二上学期期末联考化学试题
3 . 某 样品露置在空气中部分变质生成
样品露置在空气中部分变质生成 ,为确定其中
,为确定其中 和
和 的含量,称取四份该样品溶于水后,分别逐滴加入相同浓度盐酸
的含量,称取四份该样品溶于水后,分别逐滴加入相同浓度盐酸 ,充分反应,产生气体的总体积(已折算成标准状况下的体积,不考虑气体在水中的溶解)如下表:
,充分反应,产生气体的总体积(已折算成标准状况下的体积,不考虑气体在水中的溶解)如下表:
(1)样品中物质的量之比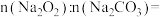
___________ 。
(2)盐酸的物质的量浓度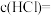
___________ 。
 样品露置在空气中部分变质生成
样品露置在空气中部分变质生成 ,为确定其中
,为确定其中 和
和 的含量,称取四份该样品溶于水后,分别逐滴加入相同浓度盐酸
的含量,称取四份该样品溶于水后,分别逐滴加入相同浓度盐酸 ,充分反应,产生气体的总体积(已折算成标准状况下的体积,不考虑气体在水中的溶解)如下表:
,充分反应,产生气体的总体积(已折算成标准状况下的体积,不考虑气体在水中的溶解)如下表:| 实验序号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 盐酸体积/mL | 100.0 | 100.0 | 100.0 | 100.0 |
| 样品质量/g | 2.62 | 3.93 | 5.24 | 6.55 |
| 气体总体积/mL | 448 | 560 | 448 | 560 |
(1)样品中物质的量之比
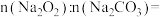
(2)盐酸的物质的量浓度
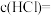
您最近一年使用:0次
解题方法
4 . 下列方案设计、现象和结论都正确的是
| A | 探究 固体样品是否变质 固体样品是否变质 | 取少量待测样品溶于蒸馏水,加入足量稀盐酸,再加入足量 溶液 溶液 | 若有白色沉淀产生,则样品已经变质 |
| B | 探究KI与 反应的限度 反应的限度 | 取1mL KI溶液于试管中,加入3mL KI溶液于试管中,加入3mL  溶液,充分反应后滴入5滴15%KSCN溶液 溶液,充分反应后滴入5滴15%KSCN溶液 | 若溶液变血红色,则KI与 的反应有一定限度 的反应有一定限度 |
| C | 验证 分子中的碳碳双键 分子中的碳碳双键 | 取样与适量溴水混合,充分反应,观察现象 | 溴水褪色,说明样品分子中含有碳碳双键 |
| D | 检验淀粉水解是否完全 | 将适量样品与稀硫酸反应,加入足量NaOH溶液后加入碘水,观察现象 | 无明显现象,说明淀粉水解完全 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 根据实验操作和现象得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 在稀盐酸中加入少量可能变质的碳酸钠样品,立即有气体产生 | Na2CO3已经变质,有一部分转化为NaHCO3 |
| B | 取少量可能被氧化的还原铁粉,加稀盐酸溶解,滴入5滴15%KSCN溶液,溶液不显血红色 | 还原铁粉未变质 |
| C | 取少量可能变质的Na2SO3样品加水溶解,加入BaCl2溶液,产生白色沉淀,过滤所得固体加足量稀盐酸,白色沉淀部分溶解 | Na2SO3样品已经变质,有一部分被氧化为Na2SO4 |
| D | 将表面已经变质的钠投入水中,产生无色无味的气体 | 钠已经变质,有一部分被氧化为Na2O2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
6 . 下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 检验淀粉是否已经发生水解 | 将淀粉和稀硫酸混合加热,再加入少量新制的Cu(OH)2,加热,没有砖红色沉淀产生 | 淀粉未发生水解 |
| B | 探究KI与FeCl3反应的限度 | 取5mL0.1mol·L-1KI溶液于试管中,加入1mL0.1mol·L-1FeCl3溶液,充分反应后滴入5滴15%KSCN溶液 | 若溶液变血红色,则KI与FeCl3的反应有一定限度 |
| C | 探究Na2SO3固体样品是否变质 | 取少量待测样品溶于蒸馏水,加入足量稀硫酸,再加入足量BaCl2溶液 | 若有白色沉淀产生, 则样品已经变质 |
| D | 检验气体Y | 用湿润的淀粉碘化钾试纸检验气体Y, | 试纸变蓝色,Y一定是Cl2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-11-19更新
|
353次组卷
|
3卷引用:浙江省金衢六校联盟2021-2022学年高二上学期期末联考化学试题
7 . 根据下列实验操作和现象所得到的结论正确 的是。
| 选项 | 实验操作和现象 | 结论 |
| A | 向试管中加入2mL 5%  溶液,再滴加数滴10% NaOH溶液,振荡后加入某物质,加热,没有砖红色沉淀生成。 溶液,再滴加数滴10% NaOH溶液,振荡后加入某物质,加热,没有砖红色沉淀生成。 | 该物质中不存在醛基 |
| B | 向淀粉溶液中加适量20%  溶液,加热,冷却后加NaOH溶液至中性,再滴加少量碘水,溶液变蓝 溶液,加热,冷却后加NaOH溶液至中性,再滴加少量碘水,溶液变蓝 | 淀粉未水解 |
| C | 取少量 样品溶于蒸馏水,加入足量稀盐酸,再加入足量 样品溶于蒸馏水,加入足量稀盐酸,再加入足量 溶液,若有白色沉淀产生。 溶液,若有白色沉淀产生。 | 则该 样品已经变质 样品已经变质 |
| D | 向 溶液中滴加 溶液中滴加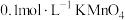 溶液,溶液褪色 溶液,溶液褪色 |  具有氧化性 具有氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-06-27更新
|
190次组卷
|
2卷引用:浙江省温州新力量联盟2021-2022学年高二下学期期末联考化学试题
名校
8 . 下列实验操作、现象和所得到的结论均正确的是
| 选项 | 实验内容 | 实验结论 |
| A | 将Fe(NO3)2样品溶于稀HNO3溶液中,加入KSCN溶液,显红色 | Fe(NO3)2已经氧化变质 |
| B | 用pH试纸测定同浓度的NaCl和NaF溶液的pH,pH(NaCl)<pH(NaF) | 结合H+能力:Cl-<F- |
| C | 取1mL0.1mol/LKI溶液于试管中,加入5mL0.1mol/LFeCl3,充分反应后滴入5滴15%KSCN溶液 | 若溶液变血红色,则KI和FeCl3反应有一定限度 |
| D | 向2支盛有5mL不同浓度NaHSO3溶液的试管中,同时加入2mL5%H2O2溶液,观察并比较实验现象 | 探究浓度对反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-02-23更新
|
220次组卷
|
3卷引用:浙江省宁波市奉化区2021-2022学年高二上学期期末联考化学试题
解题方法
9 . 下列实验方案设计、现象和结论都正确的是
| 实验目的 | 方案设计 | 现象和结论 | |
| A | 检验CH3CH2Br在NaOH溶液中是否发生水解 | 将CH3CH2Br与NaOH溶液共热,冷却后,取少量溶液,加入AgNO3溶液 | 若有沉淀产生,则CH3CH2Br发生水解 |
| B | 比较Br2和I2的氧化性强弱 | 将少量溴水加入KI溶液中,再加入CCl4,振荡,静置 | 若下层液体呈紫红色,则Br2的氧化性强于I2 |
| C | 检验Fe(NO3)2晶体是否氧化变质 | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液 | 若溶液变红,则Fe(NO3)2晶体已氧化变质 |
| D | 比较HNO2和CH3COOH电离出H+的能力 | 用pH试纸分别测CH3COONa溶液和NaNO2溶液的pH | 若CH3COONa溶液的pH比NaNO2溶液的pH大,则HNO2电离出H+的能力比CH3COOH的强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
20-21高一下·浙江·阶段练习
名校
10 . 实验室中有一瓶碳酸氢钠固体,因受热而部分变质(杂质为Na2CO3,假设杂质分布均匀)。为测定其组成,称取1.892g样品溶于水,配成500mL溶液。取出25.00mL该溶液,加入0.050mol·L-1Ba(OH)2溶液至22.00mL时沉淀量达到最大。请计算:
(1)25℃时,0.050mol·L-1Ba(OH)2溶液中的氢氧根离子浓度是_______ mol/L
(2)样品中n(NaHCO3)∶n(Na2CO3)=_______ 。
(1)25℃时,0.050mol·L-1Ba(OH)2溶液中的氢氧根离子浓度是
(2)样品中n(NaHCO3)∶n(Na2CO3)=
您最近一年使用:0次



