名校
解题方法
1 . 下列物质的检验中,其结论一定正确的是
A.向某溶液中加入 溶液,产生白色沉淀,加入稀 溶液,产生白色沉淀,加入稀 后,白色沉淀不溶解,也无其他现象,说明原溶液中一定含有 后,白色沉淀不溶解,也无其他现象,说明原溶液中一定含有 |
B.向某溶液中加入盐酸产生无色气体,该气体能使澄清的石灰水变浑浊,说明该溶液中一定含有 或 或 |
C.取少量久置的 样品于试管中加水溶解,若加足量盐酸时有气体产生,再加 样品于试管中加水溶解,若加足量盐酸时有气体产生,再加 溶液时有白色沉淀产生,则说明 溶液时有白色沉淀产生,则说明 样品已部分被氧化 样品已部分被氧化 |
D.将某气体通入品红溶液中,品红溶液褪色,该气体一定是 |
您最近一年使用:0次
2024-01-15更新
|
365次组卷
|
20卷引用:江西省丰城市第九中学2022-2023学年高三上学期入学考化学试题
江西省丰城市第九中学2022-2023学年高三上学期入学考化学试题2016届甘肃省兰州第一中学高三9月月考化学试卷2017届河北省望都中学高三8月月考化学试卷2017届天津一中高三上第一次月考化学试卷2017届甘肃省兰州一中高三上学期9月月考化学试卷上海市十二校2016届高三3月联考化学试题甘肃省兰州市第二十七中学2022届高三上学期8月月考化学试题陕西省西安高级中学2021-2022学年高三第一次适应性考试化学试题陕西省西安高级中学2021-2022学年高三第一次适应性考试化学试题(已下线)第四章 非金属及其化合物 第21练 硫酸 含硫物质的转化江西省宜春市宜丰中学2022-2023学年高一下学期3月月考化学试题(已下线)5.1.2 硫酸、含硫化合物的相互转化——同步学习必备知识西安市第八十三中学2022-2023学年高一下学期第一次月考化学试题(已下线)专题01 硫及其化合物的性质及转化(专题过关)-2022-2023学年高一化学下学期期中期末考点大串讲(人教版2019必修第二册)四川省达州市达川区2022-2023学年高一下学期4月期中考试化学试题上海市上海中学2023-2024学年高一上学期期末考试化学试卷湖北省襄阳市第一中学2023-2024学年高一下学期3月月考化学试题天津市滨海新区田家炳中学2023-2024学年高一下学期第一次月考化学试题山东省济宁市微山县第二中学2023-2024学年高一下学期第一次月考化学试题河南省焦作市博爱县第一中学2023-2024学年高一下学期4月期中考试化学试题
名校
2 . 四川含有非常丰富的矿产资源。以川西铝土矿(主要成分为Al2O3、Fe2O3、SiO2、少量FeS2)为原料,生产Fe3O4的部分工艺流程如下:
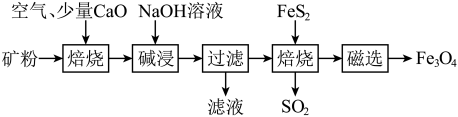
(1)Fe3O4_____ (填“属于”或“不属于”)碱性氧化物。
(2)已知上述流程中两次焙烧均会产生SO2,滤渣中含大量的Fe2O3。
①矿粉焙烧过程中还原剂和氧化剂物质的量之比为_____ ,过程加入少量CaO的目的是_____ ,用NaOH溶液吸收SO2离子方程式为________________
②“过滤”得到的滤液中含有的阴离子有OH-、___________ 。
③Fe2O3与FeS2混合后焙烧(缺氧条件下)反应的化学方程式为_________________ 。

(1)Fe3O4
(2)已知上述流程中两次焙烧均会产生SO2,滤渣中含大量的Fe2O3。
①矿粉焙烧过程中还原剂和氧化剂物质的量之比为
②“过滤”得到的滤液中含有的阴离子有OH-、
③Fe2O3与FeS2混合后焙烧(缺氧条件下)反应的化学方程式为
您最近一年使用:0次
名校
3 . 氧化钴常用作超耐热合金和磁性材料及化学工业的催化剂。一种以 -萘酚钴渣(含有
-萘酚钴渣(含有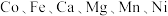 等元素的化合物及
等元素的化合物及 )制备氧化钴的工艺流程如下。
)制备氧化钴的工艺流程如下。
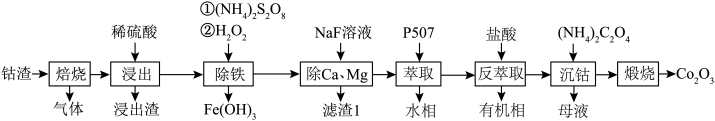
已知:① -萘酚钴渣焙烧浸出后溶液中金属元素主要以
-萘酚钴渣焙烧浸出后溶液中金属元素主要以 价离子形式存在。
价离子形式存在。
②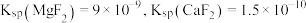 ;
;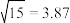 。
。
③溶液的氧化还原电势(E)为正,表示该溶液显示出一定的氧化性。氧化还原电势越高,氧化性越强;电势越低,氧化性越弱。
回答下列问题:
(1)“焙烧”过程中的主要气体产物为___________ (填化学式)。
(2)“除铁”过程中, 参与反应的离子方程式为
参与反应的离子方程式为___________ 。
(3)“除铁”后滤液中 浓度分别为
浓度分别为 和
和 ,若取
,若取 该废液,则至少需加入
该废液,则至少需加入___________ 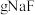 才能使该废液中
才能使该废液中 沉淀完全(当离子浓度
沉淀完全(当离子浓度 可认为沉淀完全)。
可认为沉淀完全)。
(4)用萃取剂P507“萃取”后所得水相中主要含有的金属离子为___________ (填离子符号)。“煅烧”时主要反应的化学方程式为___________ 。
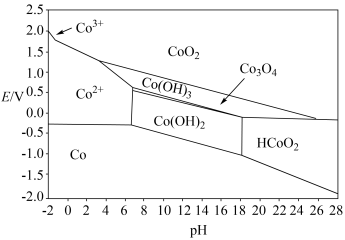
(5)钴元素的存在形式的稳定区域与溶液 的关系如图(
的关系如图(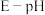 图)所示,在溶液
图)所示,在溶液 时,
时, 能将
能将 氧化,写出该反应的离子方程式:
氧化,写出该反应的离子方程式:___________ ;以1吨 -萘酚钴渣(
-萘酚钴渣( 的质量分数为
的质量分数为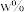 )为原料提取出
)为原料提取出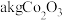 ,在提取过程中钴的损失率为
,在提取过程中钴的损失率为___________  (填含
(填含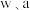 的表达式)。
的表达式)。
 -萘酚钴渣(含有
-萘酚钴渣(含有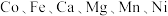 等元素的化合物及
等元素的化合物及 )制备氧化钴的工艺流程如下。
)制备氧化钴的工艺流程如下。
已知:①
 -萘酚钴渣焙烧浸出后溶液中金属元素主要以
-萘酚钴渣焙烧浸出后溶液中金属元素主要以 价离子形式存在。
价离子形式存在。②
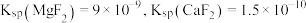 ;
;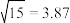 。
。③溶液的氧化还原电势(E)为正,表示该溶液显示出一定的氧化性。氧化还原电势越高,氧化性越强;电势越低,氧化性越弱。
回答下列问题:
(1)“焙烧”过程中的主要气体产物为
(2)“除铁”过程中,
 参与反应的离子方程式为
参与反应的离子方程式为(3)“除铁”后滤液中
 浓度分别为
浓度分别为 和
和 ,若取
,若取 该废液,则至少需加入
该废液,则至少需加入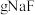 才能使该废液中
才能使该废液中 沉淀完全(当离子浓度
沉淀完全(当离子浓度 可认为沉淀完全)。
可认为沉淀完全)。(4)用萃取剂P507“萃取”后所得水相中主要含有的金属离子为
(5)钴元素的存在形式的稳定区域与溶液
 的关系如图(
的关系如图(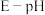 图)所示,在溶液
图)所示,在溶液 时,
时, 能将
能将 氧化,写出该反应的离子方程式:
氧化,写出该反应的离子方程式: -萘酚钴渣(
-萘酚钴渣( 的质量分数为
的质量分数为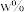 )为原料提取出
)为原料提取出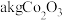 ,在提取过程中钴的损失率为
,在提取过程中钴的损失率为 (填含
(填含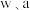 的表达式)。
的表达式)。
您最近一年使用:0次
2023-10-04更新
|
188次组卷
|
3卷引用:江西省百师联盟2023-2024学年高三开学考试化学试题
名校
4 . 甲烷是重要的气体燃料和化工原料,可将甲烷催化裂解以制取乙烯、乙炔。主要反应如下:
反应ⅰ: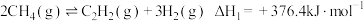
反应ⅱ:
反应ⅲ: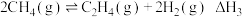
(1)反应ⅲ的焓变
___________ 。
(2)① 温度下,反应ⅰ的
温度下,反应ⅰ的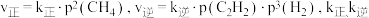 分别为正、逆反应速率常数,部分数据如表所示。
分别为正、逆反应速率常数,部分数据如表所示。
表中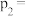
___________ ,该温度下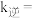
___________ MPa-3∙min-1。
②反应ⅰ达平衡后,温度由 降到
降到 ,再达平衡,
,再达平衡,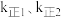 和
和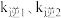 分别代表
分别代表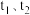 时的正、逆反应速率常数,则
时的正、逆反应速率常数,则
___________ 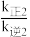 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
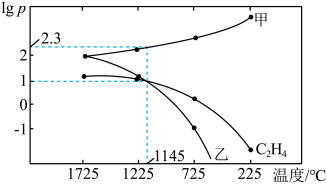
(3)一定温度下,向恒容密闭容器中充入一定量 发生反应,初始压强为
发生反应,初始压强为 ,体系中含碳元素气体平衡分压的对数与温度的关系如图所示(已知:
,体系中含碳元素气体平衡分压的对数与温度的关系如图所示(已知: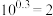 )。曲线乙表示物质为
)。曲线乙表示物质为___________ (填化学式),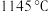 时
时 的平衡转化率为
的平衡转化率为___________ (保留1位小数),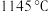 时反应ⅲ的
时反应ⅲ的
___________ 。
反应ⅰ:
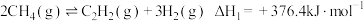
反应ⅱ:

反应ⅲ:
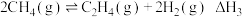
(1)反应ⅲ的焓变

(2)①
 温度下,反应ⅰ的
温度下,反应ⅰ的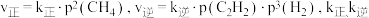 分别为正、逆反应速率常数,部分数据如表所示。
分别为正、逆反应速率常数,部分数据如表所示。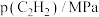 | 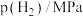 | 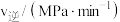 |
| 0.05 |  | 4 |
 | 1 | 2.4 |
 |  | 16 |
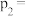
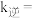
②反应ⅰ达平衡后,温度由
 降到
降到 ,再达平衡,
,再达平衡,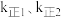 和
和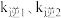 分别代表
分别代表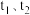 时的正、逆反应速率常数,则
时的正、逆反应速率常数,则
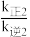 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(3)一定温度下,向恒容密闭容器中充入一定量
 发生反应,初始压强为
发生反应,初始压强为 ,体系中含碳元素气体平衡分压的对数与温度的关系如图所示(已知:
,体系中含碳元素气体平衡分压的对数与温度的关系如图所示(已知: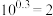 )。曲线乙表示物质为
)。曲线乙表示物质为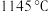 时
时 的平衡转化率为
的平衡转化率为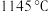 时反应ⅲ的
时反应ⅲ的

您最近一年使用:0次
2023-10-04更新
|
94次组卷
|
2卷引用:江西省百师联盟2023-2024学年高三开学考试化学试题
名校
5 . “点击化学”是指快速、高效连接分子的一类反应,例如铜催化的Huisgen环加成反应:

我国科研人员利用该反应设计、合成了具有特殊结构的聚合物F并研究其水解反应。合成线路如图所示:

已知: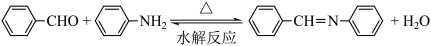
(1)化合物A的官能团名称是_____ ;反应①的反应类型是_____ 。
(2)关于B和C,下列说法正确的是_____ (填字母序号)。
a.利用质谱法可以鉴别B和C
b.B可以发生氧化、取代、消去反应
c.可用酸性高锰酸钾溶液检验C中含有碳碳三键
(3)B生成C的过程中还有另一种生成物X,分子式为C3H6O,核磁共振氢谱显示只有一组峰,X的结构简式为_____ 。
(4)反应②的化学方程式为_____ 。
(5)E的结构简式为_____ ;聚合物F的结构简式为_____ 。
(6)已知化合物M是比物质B多一个碳原子的同系物,则M满足下列条件的同分异构体共有_____ 种(不考虑立体异构)。
①属于芳香族化合物;
②苯环上只有两个对位的取代基,且其中一个取代基为乙烯基(CH2=CH一)
③只有两种官能团,且1mol该物质与足量银氨溶液发生银镜反应生成4molAg

我国科研人员利用该反应设计、合成了具有特殊结构的聚合物F并研究其水解反应。合成线路如图所示:

已知:

(1)化合物A的官能团名称是
(2)关于B和C,下列说法正确的是
a.利用质谱法可以鉴别B和C
b.B可以发生氧化、取代、消去反应
c.可用酸性高锰酸钾溶液检验C中含有碳碳三键
(3)B生成C的过程中还有另一种生成物X,分子式为C3H6O,核磁共振氢谱显示只有一组峰,X的结构简式为
(4)反应②的化学方程式为
(5)E的结构简式为
(6)已知化合物M是比物质B多一个碳原子的同系物,则M满足下列条件的同分异构体共有
①属于芳香族化合物;
②苯环上只有两个对位的取代基,且其中一个取代基为乙烯基(CH2=CH一)
③只有两种官能团,且1mol该物质与足量银氨溶液发生银镜反应生成4molAg
您最近一年使用:0次
6 . 工业上以锂辉石为原料生产碳酸锂的部分工业流程如图所示:

已知:(1)锂辉石的主要成分为Li2O·Al2O3·4SiO2,其中含少量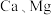 元素。
元素。
(2)Li2O·Al2O3·4SiO2+H2SO4(浓) Li2SO4+Al2O3·4SiO2·H2O
Li2SO4+Al2O3·4SiO2·H2O
(3)某些物质的溶解度(S)如下表所示:
回答下列问题:
(1)从滤渣1中分离出 的流程如图所示:
的流程如图所示:

写出生成沉淀的离子方程式:_____ 。
(2)已知滤渣2的主要成分有_____ 。
(3)最后一个步骤中,用“热水洗涤”的目的是_____ 。
(4)工业上,将 粗品制备成高纯
粗品制备成高纯 的部分工艺如下:
的部分工艺如下:
a.将 溶于盐酸作电解槽的阳极液,
溶于盐酸作电解槽的阳极液, 溶液作阴极液,两者用离子选择性透过膜隔开,用惰性电极电解。
溶液作阴极液,两者用离子选择性透过膜隔开,用惰性电极电解。
b.电解后向 溶液中加入少量
溶液中加入少量 溶液并共热,过滤、烘干得高纯
溶液并共热,过滤、烘干得高纯 。
。
①a中电解时所用的是_____ (填“阳离子交换膜”或“阴离子交换膜”)。
②电解后, 溶液浓度增大的原因是
溶液浓度增大的原因是_____ , 中生成
中生成 反应的化学方程式是
反应的化学方程式是_____
(5)磷酸亚铁锂电池总反应为FePO4+Li LiFePO4,电池中的固体电解质可传导
LiFePO4,电池中的固体电解质可传导 ,写出该电池放电时的正极反应:
,写出该电池放电时的正极反应:_____ 。
(6)铬与铁为同周期元素,某含铬化合物立方晶胞如图所示。Ca和Cr的最近距离为anm,设NA为阿伏加德罗常数的值,则该晶体密度为_____ (填含a、NA的表达式)g·cm-3。


已知:(1)锂辉石的主要成分为Li2O·Al2O3·4SiO2,其中含少量
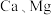 元素。
元素。(2)Li2O·Al2O3·4SiO2+H2SO4(浓)
 Li2SO4+Al2O3·4SiO2·H2O
Li2SO4+Al2O3·4SiO2·H2O(3)某些物质的溶解度(S)如下表所示:
| T/℃ | 20 | 40 | 60 | 80 |
| S(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0 .85 .85 |
| S(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
(1)从滤渣1中分离出
 的流程如图所示:
的流程如图所示:
写出生成沉淀的离子方程式:
(2)已知滤渣2的主要成分有
(3)最后一个步骤中,用“热水洗涤”的目的是
(4)工业上,将
 粗品制备成高纯
粗品制备成高纯 的部分工艺如下:
的部分工艺如下:a.将
 溶于盐酸作电解槽的阳极液,
溶于盐酸作电解槽的阳极液, 溶液作阴极液,两者用离子选择性透过膜隔开,用惰性电极电解。
溶液作阴极液,两者用离子选择性透过膜隔开,用惰性电极电解。b.电解后向
 溶液中加入少量
溶液中加入少量 溶液并共热,过滤、烘干得高纯
溶液并共热,过滤、烘干得高纯 。
。①a中电解时所用的是
②电解后,
 溶液浓度增大的原因是
溶液浓度增大的原因是 中生成
中生成 反应的化学方程式是
反应的化学方程式是(5)磷酸亚铁锂电池总反应为FePO4+Li
 LiFePO4,电池中的固体电解质可传导
LiFePO4,电池中的固体电解质可传导 ,写出该电池放电时的正极反应:
,写出该电池放电时的正极反应:(6)铬与铁为同周期元素,某含铬化合物立方晶胞如图所示。Ca和Cr的最近距离为anm,设NA为阿伏加德罗常数的值,则该晶体密度为

您最近一年使用:0次
2023-10-03更新
|
73次组卷
|
2卷引用:江西省新余市第一中学2023-2024学年高三上学期开学考试化学试题
名校
解题方法
7 .  的晶胞结构如图甲所示,将Mn掺杂到
的晶胞结构如图甲所示,将Mn掺杂到 的晶体中得到稀磁性半导体材料,其结构如图乙所示。a、b点的原子分数坐标分别为(0,0,0)和(1,1,0)。下列说法错误的是
的晶体中得到稀磁性半导体材料,其结构如图乙所示。a、b点的原子分数坐标分别为(0,0,0)和(1,1,0)。下列说法错误的是
 的晶胞结构如图甲所示,将Mn掺杂到
的晶胞结构如图甲所示,将Mn掺杂到 的晶体中得到稀磁性半导体材料,其结构如图乙所示。a、b点的原子分数坐标分别为(0,0,0)和(1,1,0)。下列说法错误的是
的晶体中得到稀磁性半导体材料,其结构如图乙所示。a、b点的原子分数坐标分别为(0,0,0)和(1,1,0)。下列说法错误的是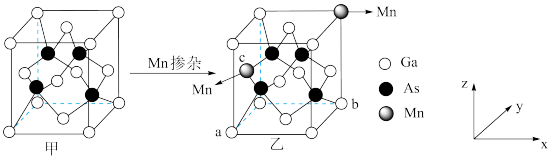
A.c点Mn的原子分数坐标为(0, , , ) ) |
B.晶体乙中 的原子个数比为5∶27∶32 的原子个数比为5∶27∶32 |
| C.基态Ga原子未成对电子数为3 |
D.若GaAs晶胞参数为anm,则Ga和As之间的最短距离为 anm anm |
您最近一年使用:0次
2023-10-03更新
|
188次组卷
|
7卷引用:江西省新余市第一中学2023-2024学年高三上学期开学考试化学试题
江西省新余市第一中学2023-2024学年高三上学期开学考试化学试题湖北省武汉市华中师范大学附属中学2022届高三高考押题化学试题(已下线)考点48 晶体结构与性质-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点43 晶体结构与性质(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)选择题11-15广东省广州市黄广中学2023届高三阶段训练考化学科试卷 安徽省阜阳市第三中学2023-2024学年高二上学期1月期末化学试题
名校
8 . 磷有多种同素异形体,其中白磷和黑磷的结构如图所示,设NA为阿伏加德罗常数的值。下列说法正确的是


| A.6.2g³1P4中含有的中子数为12.8NA |
| B.将白磷转化为黑磷属于物理变化 |
| C.12.4g白磷与0.6molH₂在密闭容器中充分反应,生成的PH3分子数为0.4NA |
| D.6.82g白磷发生反应:11P4+60CuSO4+96H2O=20CuP+24H3PO₄+60H2SO4,转移的电子数为0.6NA |
您最近一年使用:0次
9 . 利用稀硫酸酸化的软锰矿浆(主要成分为 ,另含有少量铁、铝、铜、镍等金属的化合物)脱除废气中的
,另含有少量铁、铝、铜、镍等金属的化合物)脱除废气中的 ,同时经过以下流程制备
,同时经过以下流程制备 。回答下列问题:
。回答下列问题:

(1)氨水中,有_____ 种氢键,任意表示出其中一种氢键:_____ 。
(2)滤渣a的主要成分为_____ (写化学式),证明“除铁铝”时 沉淀完全:取少量滤液,滴加
沉淀完全:取少量滤液,滴加_____ (填试剂),观察到_____ (填现象)。
(3)已知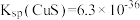 ,
,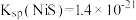 。在除铜镍的过程中,当
。在除铜镍的过程中,当 沉淀完全(溶液中的离子浓度小于或等于
沉淀完全(溶液中的离子浓度小于或等于 )时,此时溶液中
)时,此时溶液中 的浓度为
的浓度为_____  。
。
(4)写出用石灰乳从滤液a中回收 的化学方程式:
的化学方程式:_____ 。
(5)写出“氧化”过程中生成 的化学方程式:
的化学方程式:_____ 。
(6)工业上用碘-淀粉溶液测定燃煤尾气中 的含量。现有
的含量。现有 浓度为
浓度为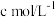 的碘-淀粉溶液,当通入尾气体积为
的碘-淀粉溶液,当通入尾气体积为 (已折算为标准状况)时,溶液蓝色消失。尾气中
(已折算为标准状况)时,溶液蓝色消失。尾气中 的体积分数为
的体积分数为_____ 。
 ,另含有少量铁、铝、铜、镍等金属的化合物)脱除废气中的
,另含有少量铁、铝、铜、镍等金属的化合物)脱除废气中的 ,同时经过以下流程制备
,同时经过以下流程制备 。回答下列问题:
。回答下列问题:
(1)氨水中,有
(2)滤渣a的主要成分为
 沉淀完全:取少量滤液,滴加
沉淀完全:取少量滤液,滴加(3)已知
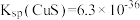 ,
,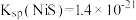 。在除铜镍的过程中,当
。在除铜镍的过程中,当 沉淀完全(溶液中的离子浓度小于或等于
沉淀完全(溶液中的离子浓度小于或等于 )时,此时溶液中
)时,此时溶液中 的浓度为
的浓度为 。
。(4)写出用石灰乳从滤液a中回收
 的化学方程式:
的化学方程式:(5)写出“氧化”过程中生成
 的化学方程式:
的化学方程式:(6)工业上用碘-淀粉溶液测定燃煤尾气中
 的含量。现有
的含量。现有 浓度为
浓度为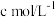 的碘-淀粉溶液,当通入尾气体积为
的碘-淀粉溶液,当通入尾气体积为 (已折算为标准状况)时,溶液蓝色消失。尾气中
(已折算为标准状况)时,溶液蓝色消失。尾气中 的体积分数为
的体积分数为
您最近一年使用:0次
2023-09-29更新
|
128次组卷
|
2卷引用:江西省南昌市等5地2022-2023学年高三上学期开学考试化学试题
名校
解题方法
10 . 铁(Fe)是第四周期第Ⅷ族元素,有多种化合价,铁及其化合物在工农业生产中具有重要作用。回答下列问题:
(1)在铁制品上镀银时,铁制品与电源_____ (填“正极”或“负极”)相连。
(2)已知下列热化学方程式:
①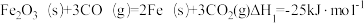
②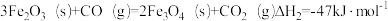
③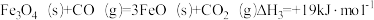
则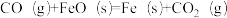 的△H
的△H_____ kJ·mol-1.
(3)高铁酸钾是一种新型非氯高效消毒剂,常用于饮用水处理。将一定量的高铁酸钾在不同温度下配制成1L 浓度为1.0mo1·L-1的溶液,存在反应:
浓度为1.0mo1·L-1的溶液,存在反应: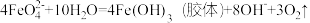 ,溶液中c(
,溶液中c( )随温度及时间的变化关系如图1所示。
)随温度及时间的变化关系如图1所示。
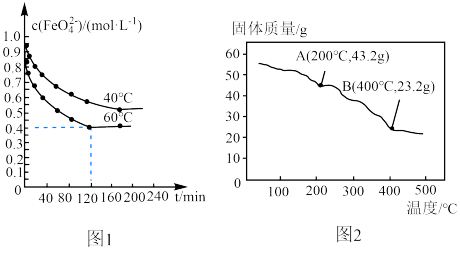
①下列说法正确的是_____ (填标号)。
A.该反应为放热反应
B.增大溶液的c(OH-)可使FeO 的水解程度减小
的水解程度减小
C.60℃、120min时,用物质的量表示的
②常温下,溶液中H2FeO4发生电离: ,溶液pH=3.32时,溶液中c(H2FeO4)=c(
,溶液pH=3.32时,溶液中c(H2FeO4)=c(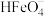 ),则Ka1(
),则Ka1(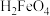 )=
)=_____ (100.68≈4.8)。
(4)常温下FeCO3的溶度积常数为Ksp(FeCO3),H2CO3的一级电离常数和二级电离常数分别为Ka1和Ka2。已知菱铁矿的主要成分是FeCO3,实验室中可以通过FeSO4与足量NaHCO3溶液混合制得FeCO3,常温下该反应的平衡常数K=_____ 。【用含有Ksp(FeCO3)、Ka1和Ka的代数式表示】。
(5)将54.0g草酸亚铁晶体(FeC2O4·2H2O)在氮气的氛围中加热分解,得到分解产物的热重曲线(固体质量随温度的变化情况)如图2所示。
①A点时,固体物质的化学式为_____ 。
②B点时,固体只含有一种铁的氧化物,则AB段反应的化学方程式为_____ 。
(1)在铁制品上镀银时,铁制品与电源
(2)已知下列热化学方程式:
①
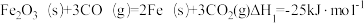
②
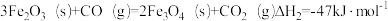
③
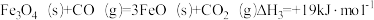
则
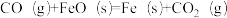 的△H
的△H(3)高铁酸钾是一种新型非氯高效消毒剂,常用于饮用水处理。将一定量的高铁酸钾在不同温度下配制成1L
 浓度为1.0mo1·L-1的溶液,存在反应:
浓度为1.0mo1·L-1的溶液,存在反应: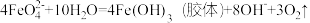 ,溶液中c(
,溶液中c( )随温度及时间的变化关系如图1所示。
)随温度及时间的变化关系如图1所示。
①下列说法正确的是
A.该反应为放热反应
B.增大溶液的c(OH-)可使FeO
 的水解程度减小
的水解程度减小C.60℃、120min时,用物质的量表示的

②常温下,溶液中H2FeO4发生电离:
 ,溶液pH=3.32时,溶液中c(H2FeO4)=c(
,溶液pH=3.32时,溶液中c(H2FeO4)=c(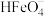 ),则Ka1(
),则Ka1(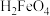 )=
)=(4)常温下FeCO3的溶度积常数为Ksp(FeCO3),H2CO3的一级电离常数和二级电离常数分别为Ka1和Ka2。已知菱铁矿的主要成分是FeCO3,实验室中可以通过FeSO4与足量NaHCO3溶液混合制得FeCO3,常温下该反应的平衡常数K=
(5)将54.0g草酸亚铁晶体(FeC2O4·2H2O)在氮气的氛围中加热分解,得到分解产物的热重曲线(固体质量随温度的变化情况)如图2所示。
①A点时,固体物质的化学式为
②B点时,固体只含有一种铁的氧化物,则AB段反应的化学方程式为
您最近一年使用:0次



