名校
1 . 瑞舒伐他汀钙是治疗高血脂的常用药物,其中间体H的合成路线如下。
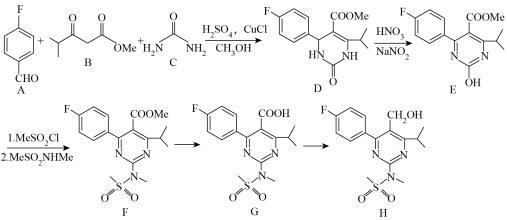
注:Me表示甲基
回答下列问题:
(1)D的分子式为___________ ,B中含有的官能团名称是___________ 。
(2)A+B+C→D的化学方程式是___________ 。
(3)E→F的反应类型为___________ 。实验室中完成F→G中官能团是转化需要的反应条件是___________ 。
(4)实现反应G→H,需要加入的反应试剂必须具有的性质是___________ 。
(5)X是A的一种同系物,X的相对分子质量比A大14,符合条件的X有___________ 种。
(6)用甲苯和适当的无机试剂(任选)合成对溴苯甲醛的流程如下:

①其中M和N的名称分别是___________ 、___________ 。
②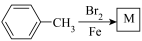 步骤中主要副产物的结构简式是
步骤中主要副产物的结构简式是___________ 。

注:Me表示甲基
回答下列问题:
(1)D的分子式为
(2)A+B+C→D的化学方程式是
(3)E→F的反应类型为
(4)实现反应G→H,需要加入的反应试剂必须具有的性质是
(5)X是A的一种同系物,X的相对分子质量比A大14,符合条件的X有
(6)用甲苯和适当的无机试剂(任选)合成对溴苯甲醛的流程如下:

①其中M和N的名称分别是
②
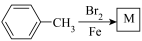 步骤中主要副产物的结构简式是
步骤中主要副产物的结构简式是
您最近一年使用:0次
名校
解题方法
2 . 由下列实验方案、现象得出的结论正确的是
| 实验方案 | 现象 | 结论 | |
| A | 向溴水中加入植物油,振荡后静置 | 水层颜色变浅 | 植物油可用于萃取溴水中的溴 |
| B | 向 溶液中加入乙醇 溶液中加入乙醇 | 析出深蓝色固体 |  在乙醇中溶解度小 在乙醇中溶解度小 |
| C | 用毛皮摩擦过的带电橡胶靠近CF2Cl2液流 | 液流方向改变 | CF2Cl2为四面体结构 |
| D | 将氯气通入盛有鲜花的集气瓶中 | 鲜花褪色 | 氯气具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-29更新
|
592次组卷
|
2卷引用:山西省晋城市第一中学校2023-2024学年高三下学期开学考试理综化学试题
名校
解题方法
3 . 以湿法炼锌厂所产的钴锰渣(主要成分为CO2O3、CoO、NiO、MnO2,含少量Fe2O3、ZnO、CuO、CaO等)为原料回收制备CoC2O4的工艺如下:

已知:常温下,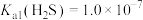 ,
,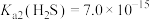 ;
;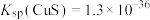 ,
,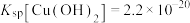 ,
, 。当平衡常数大于
。当平衡常数大于 ,反应进行彻底。
,反应进行彻底。
回答下列问题:
(1)“酸浸”时可能产生有毒气体___________ ,说出该气体的一种用途___________ 。
(2)“氧化调pH”过程中得到KFe3(SO4)2(OH)₆的离子方程式为___________ 。
(3)若K2S溶液的pH=13,则该溶液中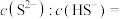
___________ ,试分析Cu2+主要以CuS形式除去,写出你的理由___________ 。
(4)“滤渣3”中含有a mol S、b mol MnO2,则理论上需要 的物质的量为
的物质的量为___________ mol(用含a、b的式子表示)。
(5)P204、P507对金属离子的萃取率与pH的关系如下图所示。

①直接用于分离钴镍的萃取剂是___________ 。
②指出分离钴镍的合适pH范围为___________ (填标号)。
A.3~4 B.4~5 C.5~6 D.6~7

已知:常温下,
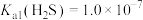 ,
, ;
; ,
,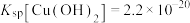 ,
, 。当平衡常数大于
。当平衡常数大于 ,反应进行彻底。
,反应进行彻底。回答下列问题:
(1)“酸浸”时可能产生有毒气体
(2)“氧化调pH”过程中得到KFe3(SO4)2(OH)₆的离子方程式为
(3)若K2S溶液的pH=13,则该溶液中
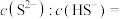
(4)“滤渣3”中含有a mol S、b mol MnO2,则理论上需要
 的物质的量为
的物质的量为(5)P204、P507对金属离子的萃取率与pH的关系如下图所示。

①直接用于分离钴镍的萃取剂是
②指出分离钴镍的合适pH范围为
A.3~4 B.4~5 C.5~6 D.6~7
您最近一年使用:0次
名校
解题方法
4 . H3X为一种三元弱酸,常温下,向一定浓度的H3X溶液中滴加同浓度的NaOH溶液,混合液中lga[a表示为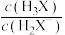 、
、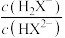 或
或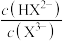 ]随
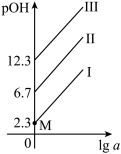
]随 的变化如图所示。下列说法正确的是
的变化如图所示。下列说法正确的是
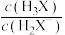 、
、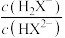 或
或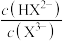 ]随
]随 的变化如图所示。下列说法正确的是
的变化如图所示。下列说法正确的是
A.曲线Ⅰ表示 随pOH的变化关系 随pOH的变化关系 |
B.反应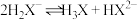 的平衡常数的数量级为 的平衡常数的数量级为 |
C.当溶液pOH=7时, |
D.M点时,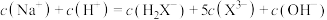 |
您最近一年使用:0次
名校
解题方法
5 . 有机电化学合成是一种有前景的绿色合成技术,利用电化学合成1,2-二氯乙烷的装置如图所示。若该装置工作时中间室NaCl溶液的浓度不变,电解时阴极生成气体的速率为xmol·h-1,下列说法错误的是
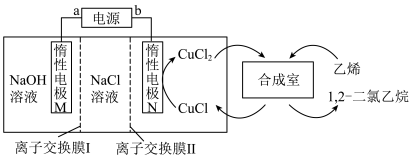

| A.惰性电极M为阴极 |
| B.离子交换膜Ⅰ为阳离子交换膜,离子交换膜Ⅱ为阴离子交换膜 |
C.合成室内发生的反应为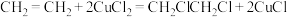 |
| D.中间室补充NaCl的速率为x mol⋅h-1 |
您最近一年使用:0次
名校
解题方法
6 . 阿司匹林是一种重要的合成药物,化学名称为乙酰水杨酸,具有解热镇痛作用,其合成原理如图。下列说法正确的是


| A.m分子中所有原子不可能处在同一平面 |
| B.m、n、p、q均能够与H2发生加成反应 |
| C.1mol p与NaOH溶液反应最多消耗2mol NaOH |
| D.m能形成分子内氢键和分子间氢键 |
您最近一年使用:0次
名校
解题方法
7 . 化学与生产、生活、科技息息相关。下列说法错误的是
| A.臭氧是替代氯气的净水剂,为弱极性分子,在水中的溶解度小于在四氯化碳中的溶解度 |
| B.聚四氟乙烯树脂可用于制印刷电路板的底板,聚四氟乙烯是有机高分子材料 |
| C.通过清洁煤技术可减少煤燃烧造成的污染,有利于促进碳中和 |
| D.“北斗三星”采用星载氢原子钟,通过电子跃迁产生的电磁波校准时钟 |
您最近一年使用:0次
名校
解题方法
8 . 探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
Ⅰ.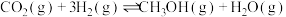

Ⅱ.

Ⅲ.

回答下列问题:
(1)
___________ kJ⋅mol-1。
(2)一定条件下,向体积为VL的恒容密闭容器中通入1molCO2和3molH2发生上述反应,达到平衡时,容器中 为a mol,CO为b mol,此时
为a mol,CO为b mol,此时 的浓度为
的浓度为___________ mol/L(用含a、b、V的代数式表示,下同),反应Ⅲ的平衡常数为___________ 。
(3)不同压强下,按照 投料,实验测定CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如下图所示。
投料,实验测定CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如下图所示。
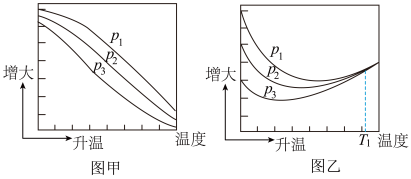
已知: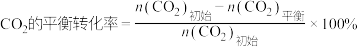
CH3OH的平衡产率=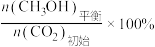
其中纵坐标表示CO2平衡转化率的是图___________ (填“甲”或“乙”);压强p1、p2、p3由大到小的顺序为___________ ;图乙中T1温度时,三条曲线几乎交于一点的原因是___________ 。
(4)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为___________(填标号)。
(5)甲醇燃料电池中甲醇在___________ (填“正”或“负”)极发生反应,酸性条件下其正极的电极反应式为___________ 。
(6)在允许O2-自由迁移的固体电解质燃料电池中,CnH2n+2放电的电极反应式为___________ 。
Ⅰ.
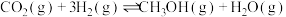

Ⅱ.


Ⅲ.


回答下列问题:
(1)

(2)一定条件下,向体积为VL的恒容密闭容器中通入1molCO2和3molH2发生上述反应,达到平衡时,容器中
 为a mol,CO为b mol,此时
为a mol,CO为b mol,此时 的浓度为
的浓度为(3)不同压强下,按照
 投料,实验测定CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如下图所示。
投料,实验测定CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如下图所示。
已知:
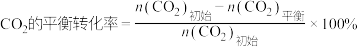
CH3OH的平衡产率=
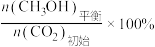
其中纵坐标表示CO2平衡转化率的是图
(4)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为___________(填标号)。
| A.低温、高压 | B.高温、低压 | C.低温、低压 | D.高温、高压 |
(5)甲醇燃料电池中甲醇在
(6)在允许O2-自由迁移的固体电解质燃料电池中,CnH2n+2放电的电极反应式为
您最近一年使用:0次
2024-03-16更新
|
240次组卷
|
2卷引用:山西省晋城市第一中学校2023-2024学年高三下学期开学考试理综化学试题
名校
解题方法
9 . 自分子识别兴起以来,冠醚、杯酚烃等的合成引起了研究者的广泛关注。硫代杯[4]芳烃已被应用于许多方面,如监测和分离一些阳离子、阴离子等。合成对叔丁基硫代杯[4]芳烃(M=720.0g⋅mol-1)的原理表示如下:
利用如图所示装置(加热、搅拌、夹持等装置省略),将60.00g对叔丁基苯酚、25.60gS8、8g氢氧化钠和40mL二苯醚加入500mL三颈烧瓶中,在N2气氛下磁力加热搅拌,逐步升温到230℃,温度保持在230℃反应4小时。停止加热并冷却至100℃以下后,加入40mL 6mol·L-1的盐酸和400mL乙醇的混合溶液,搅拌,抽滤,用乙醇和蒸馏水交替洗涤固体,得到粗产物。将粗产物在氯仿/乙醇中重结晶,得到30.24g纯化的对叔丁基硫代杯[4]芳烃。回答下列问题:
(1)仪器A的名称是___________ ,其作用是___________ 。
(2)对叔丁基邻苯二酚(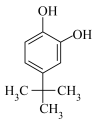 )的沸点小于2-叔丁基对苯二酚(
)的沸点小于2-叔丁基对苯二酚(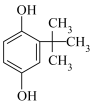 )的原因是
)的原因是___________ 。
(3)加热过程中要不断通入氮气,目的是___________ 。
(4)停止加热后,向反应器中加入盐酸和乙醇混合溶液的目的是___________ 。
(5)实验过程中会产生一种有毒气体,尾气吸收装置中应用___________ (填试剂名称)将该气体除去。
(6)在重结晶过程中,需要用到如图所示仪器中的___________ (填字母)___________ (计算结果精确到0.1%)。
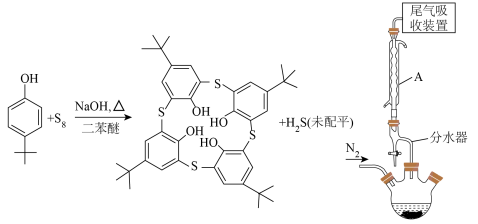
利用如图所示装置(加热、搅拌、夹持等装置省略),将60.00g对叔丁基苯酚、25.60gS8、8g氢氧化钠和40mL二苯醚加入500mL三颈烧瓶中,在N2气氛下磁力加热搅拌,逐步升温到230℃,温度保持在230℃反应4小时。停止加热并冷却至100℃以下后,加入40mL 6mol·L-1的盐酸和400mL乙醇的混合溶液,搅拌,抽滤,用乙醇和蒸馏水交替洗涤固体,得到粗产物。将粗产物在氯仿/乙醇中重结晶,得到30.24g纯化的对叔丁基硫代杯[4]芳烃。回答下列问题:
(1)仪器A的名称是
(2)对叔丁基邻苯二酚(
 )的沸点小于2-叔丁基对苯二酚(
)的沸点小于2-叔丁基对苯二酚( )的原因是
)的原因是(3)加热过程中要不断通入氮气,目的是
(4)停止加热后,向反应器中加入盐酸和乙醇混合溶液的目的是
(5)实验过程中会产生一种有毒气体,尾气吸收装置中应用
(6)在重结晶过程中,需要用到如图所示仪器中的
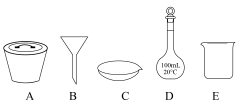
您最近一年使用:0次
2024-03-10更新
|
631次组卷
|
2卷引用:山西省晋城市第一中学校2023-2024学年高三下学期开学考试理综化学试题
10 . ZnO是一种光电材料,其立方晶体的晶胞结构如图1,图2是沿着立方格子对角面取得的截图。已知Zn、O原子半径分别为a pm、b pm,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,原子1的分数坐标为(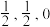 )。下列说法正确的是
)。下列说法正确的是
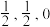 )。下列说法正确的是
)。下列说法正确的是
| A.基态Zn2+占据的最高能级共有3个原子轨道 |
B.晶胞边长为 |
C.原子2的分数坐标为(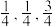 ) ) |
| D.晶体中与Zn2+距离最近且相等的O2-数目为8 |
您最近一年使用:0次
2024-03-10更新
|
292次组卷
|
2卷引用:山西省晋城市第一中学校2023-2024学年高三下学期开学考试理综化学试题



