名校
解题方法
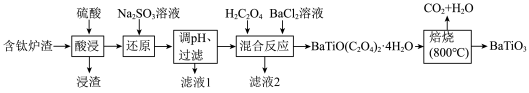
1 . BaTiO3,被用作陶瓷电容器的介电材料、麦克风和其他传感器的压电材料。以含钛炉渣(主要成分是TiO2,含少量Fe2O3、CaO、SiO2等)为原料制备BaTiO3的流程如下:
回答下列问题:
(1)下列为Ba粒子简化电子排布式,其中能量最高的是 (填字母)。
(2)“还原”中发生反应的离子方程式为________ 。若省去“还原”工艺,则________ 。
(3)设计实验检验滤液1中是否含有Fe2+:________ 。
(4)BaTiO(C2O4)2·4H2O中Ti的化合价为________ ,“焙烧”发生反应的化学方程式为________ 。
(5)经X射线分析鉴定,钛酸钡(BaTiO3)的晶胞结构如下图所示(Ti4+、Ba2+均与O2-相接触),已知晶胞边长为 pm,O2-的半径为
pm,O2-的半径为 pm,则Ti4+、Ba2+的半径分别为
pm,则Ti4+、Ba2+的半径分别为______ pm、______ pm。(用含 、
、 的代数式表示)
的代数式表示)
| 金属离子 | TiO2+ | Fe2+ | Fe3+ |
| 开始沉淀的pH | 0.5 | 6.3 | 1.5 |
| 完全沉淀的pH | 2.5 | 8.3 | 2.8 |
(1)下列为Ba粒子简化电子排布式,其中能量最高的是 (填字母)。
| A.[Xe]6s2 | B.[Xe]6s1 | C.[Xe]6s16p1 | D.[Xe]6s0p2 |
(2)“还原”中发生反应的离子方程式为
(3)设计实验检验滤液1中是否含有Fe2+:
(4)BaTiO(C2O4)2·4H2O中Ti的化合价为
(5)经X射线分析鉴定,钛酸钡(BaTiO3)的晶胞结构如下图所示(Ti4+、Ba2+均与O2-相接触),已知晶胞边长为
 pm,O2-的半径为
pm,O2-的半径为 pm,则Ti4+、Ba2+的半径分别为
pm,则Ti4+、Ba2+的半径分别为 、
、 的代数式表示)
的代数式表示)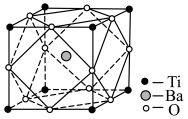
您最近一年使用:0次
名校
解题方法
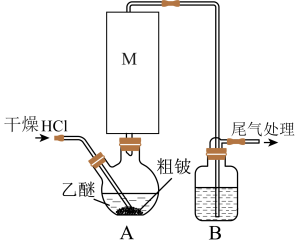
2 . 某实验小组以粗铍(含少量的Mg、Fe、Al、Cu、Si等)为原料制备、提纯BeCl2,并测定产品中BeCl2的含量。利用如图所示装置(夹持装置略)制BeCl2,实验开始前先通入一段时间的氩气。
②BeCl2溶于乙醚,不溶于苯,易发生水解;
③AlCl3溶于乙醚且溶于苯,FeCl2、MgCl2不溶于乙醚和苯;
④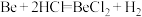 为放热反应。
为放热反应。
请回答下列问题:
(1)装置A中方框内的仪器M应为________ (填“直形冷凝管”或“球形冷凝管”),实验中装置A需置于温度15℃左右的水浴中,其主要目的是________ 。
(2)装置B中盛放的试剂为________ 。
(3)反应后,装置A中BeCl2的乙醚溶液先经过滤除去杂质________ ,再蒸馏滤液将乙醚蒸出得“固体”。为了除去“固体”中的其余杂质,可采取的操作为________ 。
(4)取 g产品溶于盐酸配成100 mL溶液;每次取20.00 mL溶液,加入EDTA掩蔽杂质离子,调节pH,过滤、洗涤,得Be(OH)2固体,加入40 mL30% KF溶液溶解固体,滴加酚酞作指示剂,用
g产品溶于盐酸配成100 mL溶液;每次取20.00 mL溶液,加入EDTA掩蔽杂质离子,调节pH,过滤、洗涤,得Be(OH)2固体,加入40 mL30% KF溶液溶解固体,滴加酚酞作指示剂,用 mol · L-1盐酸溶液滴定其中的KOH,重复三次平均消耗盐酸
mol · L-1盐酸溶液滴定其中的KOH,重复三次平均消耗盐酸 mL(已知:
mL(已知: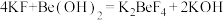 ;滴定过程中KF、K2BeF4不与盐酸反应),BeCl2的纯度为
;滴定过程中KF、K2BeF4不与盐酸反应),BeCl2的纯度为________ %(用含 、
、 和
和 的字母表示)。
的字母表示)。
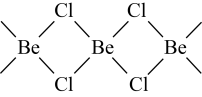
(5)氯化铍在气态时存在BeCl2分子(a)和二聚分子[(BeCl2)2](b),固态时则具有如下图所示的链状结构(c)。____ 。
②BeCl2溶于乙醚,不溶于苯,易发生水解;
③AlCl3溶于乙醚且溶于苯,FeCl2、MgCl2不溶于乙醚和苯;
④
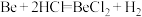 为放热反应。
为放热反应。请回答下列问题:
(1)装置A中方框内的仪器M应为
(2)装置B中盛放的试剂为
(3)反应后,装置A中BeCl2的乙醚溶液先经过滤除去杂质
(4)取
 g产品溶于盐酸配成100 mL溶液;每次取20.00 mL溶液,加入EDTA掩蔽杂质离子,调节pH,过滤、洗涤,得Be(OH)2固体,加入40 mL30% KF溶液溶解固体,滴加酚酞作指示剂,用
g产品溶于盐酸配成100 mL溶液;每次取20.00 mL溶液,加入EDTA掩蔽杂质离子,调节pH,过滤、洗涤,得Be(OH)2固体,加入40 mL30% KF溶液溶解固体,滴加酚酞作指示剂,用 mol · L-1盐酸溶液滴定其中的KOH,重复三次平均消耗盐酸
mol · L-1盐酸溶液滴定其中的KOH,重复三次平均消耗盐酸 mL(已知:
mL(已知: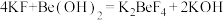 ;滴定过程中KF、K2BeF4不与盐酸反应),BeCl2的纯度为
;滴定过程中KF、K2BeF4不与盐酸反应),BeCl2的纯度为 、
、 和
和 的字母表示)。
的字母表示)。(5)氯化铍在气态时存在BeCl2分子(a)和二聚分子[(BeCl2)2](b),固态时则具有如下图所示的链状结构(c)。
您最近一年使用:0次
名校
解题方法
3 . 丙烷的价格低廉且产量大,而丙烯及其衍生物具有较高的经济附加值,因此丙烷脱氢制丙烯具有重要的价值。回答下列问题:
(1)已知下列反应的热化学方程式:
直接脱氢
反应①: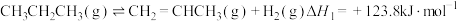
反应②: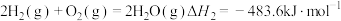
计算 氧化丙烷脱氢反应③:
氧化丙烷脱氢反应③: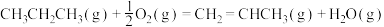 的
的
___________  。
。
(2)已知下列键能数据,结合反应①数据,计算 的键能是
的键能是___________  。
。
(3)一定温度下,向密闭容器中充入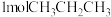 ,发生反应①。
,发生反应①。
①若该反应在恒压环境中进行,常通过向体系中通入稀有气体Ar的方式来提高CH3CH2CH3的平衡转化率,原因是___________ 。
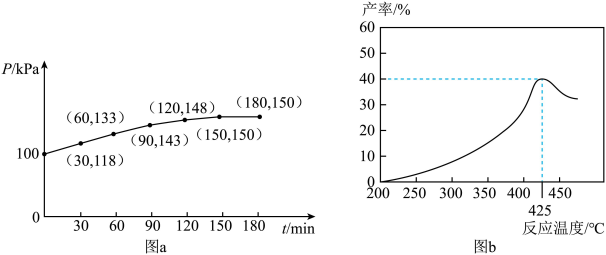
②若该反应在恒容环境中进行,用压强传感器测出容器内体系压强随时间的变化关系如图a所示,计算该温度下反应①的平衡常数Kp=___________ kPa(KP为用平衡时各气体分压代替气体的浓度表示的平衡常数,分压=总压×物质的量分数)。若保持相同反应时间,在不同温度下,丙烯产率如图b所示,丙烯产率在425℃之前随温度升高而增大的原因可能是___________ 和___________ ,随着温度继续升高,丙烷可能分解为其他产物。 作催化剂,对反应③的机理展开研究。以
作催化剂,对反应③的机理展开研究。以 和
和 为原料,初期产物中没有检测到
为原料,初期产物中没有检测到 ;以含有
;以含有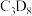 的
的 为
为 和
和 为原料,反应过程中没有检测到
为原料,反应过程中没有检测到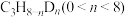 。下列推断合理的是
。下列推断合理的是___________ (填标号)。
A.V2O5先吸附氧气,吸附的氧气直接与吸附的丙烷反应
B.V2O5直接氧化吸附的丙烷,吸附的氧气补充V2O5中反应掉的氧
C.V2O5催化丙烷脱氢过程中,碳氢键的断裂是可逆的
(1)已知下列反应的热化学方程式:
直接脱氢
反应①:
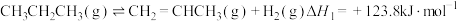
反应②:
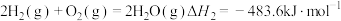
计算
 氧化丙烷脱氢反应③:
氧化丙烷脱氢反应③: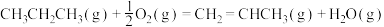 的
的
 。
。(2)已知下列键能数据,结合反应①数据,计算
 的键能是
的键能是 。
。| 化学键 |  |  |  |
键能 | 347.7 | 413.4 | 436.0 |
(3)一定温度下,向密闭容器中充入
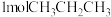 ,发生反应①。
,发生反应①。①若该反应在恒压环境中进行,常通过向体系中通入稀有气体Ar的方式来提高CH3CH2CH3的平衡转化率,原因是
②若该反应在恒容环境中进行,用压强传感器测出容器内体系压强随时间的变化关系如图a所示,计算该温度下反应①的平衡常数Kp=
 作催化剂,对反应③的机理展开研究。以
作催化剂,对反应③的机理展开研究。以 和
和 为原料,初期产物中没有检测到
为原料,初期产物中没有检测到 ;以含有
;以含有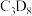 的
的 为
为 和
和 为原料,反应过程中没有检测到
为原料,反应过程中没有检测到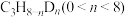 。下列推断合理的是
。下列推断合理的是A.V2O5先吸附氧气,吸附的氧气直接与吸附的丙烷反应
B.V2O5直接氧化吸附的丙烷,吸附的氧气补充V2O5中反应掉的氧
C.V2O5催化丙烷脱氢过程中,碳氢键的断裂是可逆的
您最近一年使用:0次
名校
4 . 超导现象一直吸引着广大科学家的关注。某超导材料的晶体结构属于四方晶系,其晶胞如图所示。下列说法错误的是
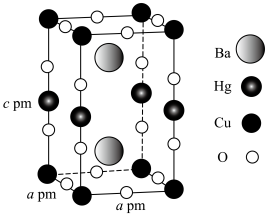
A. 位于元素周期表的第四周期第IB族 位于元素周期表的第四周期第IB族 |
B.与 等距且最近的 等距且最近的 有12个 有12个 |
C.该超导材料的化学式为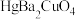 |
D.该晶体的密度为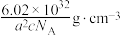 |
您最近一年使用:0次
名校
5 .  原子序数依次增大
原子序数依次增大 为同一短周期相邻元素,
为同一短周期相邻元素, 组成的
组成的 结构如图,其环上所有原子共平面。下列说法错误的是
结构如图,其环上所有原子共平面。下列说法错误的是
 原子序数依次增大
原子序数依次增大 为同一短周期相邻元素,
为同一短周期相邻元素, 组成的
组成的 结构如图,其环上所有原子共平面。下列说法错误的是
结构如图,其环上所有原子共平面。下列说法错误的是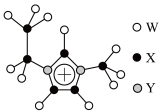
A.第一电离能: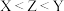 |
B. 的基态原子价层电子排布图 的基态原子价层电子排布图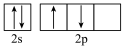 |
C.简单氢化物沸点: |
D. 中大 中大 键应表示为 键应表示为 |
您最近一年使用:0次
名校
6 . 有机化合物G(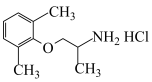 )是一种用于治疗功能性消化不良的药物。一种制备G的合成路线如图所示:
)是一种用于治疗功能性消化不良的药物。一种制备G的合成路线如图所示:
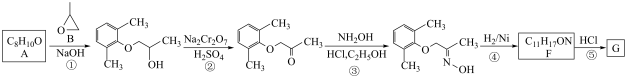
(1)A的化学名称为
(2)F的结构简式为
(3)A~G中含手性碳的有机物有
(4)反应①的化学方程式为
(5)满足下列条件的D的同分异构体有
a.苯环上连有一个取代基。
b.可发生银镜反应。
c.可发生水解反应。
(6)参考上述合成路线和信息,以
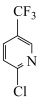 和
和 为原料(其他试剂任选),设计制备
为原料(其他试剂任选),设计制备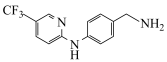 的合成路线:
的合成路线:
您最近一年使用:0次
名校
7 . 乙炔是有机合成的重要原料之一,可由块状的电石和水反应制备。电石(主要成分为CaC2,还含有CaS)能与水反应生成大量溶解度较小的胶态 ,其被乙炔气体冲鼓会产生大量泡沫。某兴趣小组探究实验室制备乙炔的条件及测定乙炔中杂质气体含量的相关实验装置和仪器如图所示,其中如图1所示装置为常用的制备乙炔的发生装置,如图2所示为备选的制备实验仪器。
,其被乙炔气体冲鼓会产生大量泡沫。某兴趣小组探究实验室制备乙炔的条件及测定乙炔中杂质气体含量的相关实验装置和仪器如图所示,其中如图1所示装置为常用的制备乙炔的发生装置,如图2所示为备选的制备实验仪器。
(1)仪器x的名称为___________ ,生成乙炔的化学方程式为___________ 。
(2)为寻找制备乙炔的合适试剂X并消除制备时产生的泡沫,兴趣小组进行了四组探究实验。
①以图1装置进行实验,若试剂X为纯水或饱和食盐水,实验中可能造成的不良后果为___________ 。
②查阅资料知,醇羟基不能与CaC2发生反应,若试剂X为50%酒精,泡沫消除可能与乙醇___________ (填选项字母)有关。
a.可燃性 b.与水任意比互溶 c.挥发性
③结合文字与化学方程式分析试剂X为稀盐酸时,不产生泡沫的原因:___________ 。
④若试剂X为50%酒精,选用图2中仪器___________ (填字母标号)组装装置可达到随时开始和关停实验的效果。
(3)测定VL(标准状况)乙炔中H2S的含量。以足量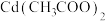 溶液作为吸收液,在酸性条件下,加入
溶液作为吸收液,在酸性条件下,加入
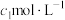 碘标准溶液和指示剂,再用Na2S2O3标准溶液滴定所得溶液,消耗
碘标准溶液和指示剂,再用Na2S2O3标准溶液滴定所得溶液,消耗
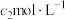 Na2S2O3标准溶液,已知:
Na2S2O3标准溶液,已知: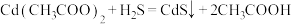 ;
; ;
;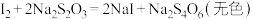 。
。
该气体样品中,H2S体积百分含量为___________ %(用含 、
、 、
、 、
、 、V的代数式表示);若滴定结束后仰视读数,会导致所得H2S体积百分含量
、V的代数式表示);若滴定结束后仰视读数,会导致所得H2S体积百分含量___________ (填“偏高”“偏低”或“无影响”)。
 ,其被乙炔气体冲鼓会产生大量泡沫。某兴趣小组探究实验室制备乙炔的条件及测定乙炔中杂质气体含量的相关实验装置和仪器如图所示,其中如图1所示装置为常用的制备乙炔的发生装置,如图2所示为备选的制备实验仪器。
,其被乙炔气体冲鼓会产生大量泡沫。某兴趣小组探究实验室制备乙炔的条件及测定乙炔中杂质气体含量的相关实验装置和仪器如图所示,其中如图1所示装置为常用的制备乙炔的发生装置,如图2所示为备选的制备实验仪器。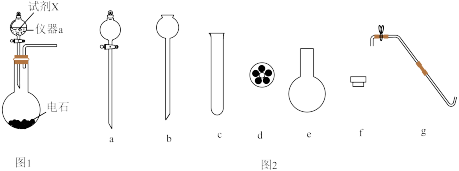
(1)仪器x的名称为
(2)为寻找制备乙炔的合适试剂X并消除制备时产生的泡沫,兴趣小组进行了四组探究实验。
| 序号 | 反应液体 | 反应现象 |
| 1 | 纯水 | 反应剧烈,产气快,有大量灰白色沉淀物[ ]和泡沫 ]和泡沫 |
| 2 | 饱和食盐水 | 反应稍慢,产气稍慢,有大量灰白色沉淀物[ ]和泡沫 ]和泡沫 |
| 3 | 50%酒精 | 反应慢,很适宜气体收集,有沉淀物生成,泡沫很少 |
| 4 | 稀盐酸 | 产气快,但没有沉淀和泡沫产生 |
②查阅资料知,醇羟基不能与CaC2发生反应,若试剂X为50%酒精,泡沫消除可能与乙醇
a.可燃性 b.与水任意比互溶 c.挥发性
③结合文字与化学方程式分析试剂X为稀盐酸时,不产生泡沫的原因:
④若试剂X为50%酒精,选用图2中仪器
(3)测定VL(标准状况)乙炔中H2S的含量。以足量
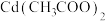 溶液作为吸收液,在酸性条件下,加入
溶液作为吸收液,在酸性条件下,加入
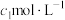 碘标准溶液和指示剂,再用Na2S2O3标准溶液滴定所得溶液,消耗
碘标准溶液和指示剂,再用Na2S2O3标准溶液滴定所得溶液,消耗
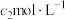 Na2S2O3标准溶液,已知:
Na2S2O3标准溶液,已知: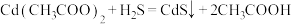 ;
; ;
;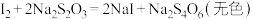 。
。该气体样品中,H2S体积百分含量为
 、
、 、
、 、
、 、V的代数式表示);若滴定结束后仰视读数,会导致所得H2S体积百分含量
、V的代数式表示);若滴定结束后仰视读数,会导致所得H2S体积百分含量
您最近一年使用:0次
名校
8 . 碳排放进入平台期后,进入平稳下降阶段称为“碳达峰”,与“碳中和”一起,简称“双碳”。以CO2为原料合成CH3OH依然是“双碳”环境下的科研热点,相关反应如下:
主反应:
 ;
;
副反应1:
 ;
;
副反应2:
 。
。
回答下列问题:
(1)部分键能的数据如下表所示,则主反应的
___________ ;
___________ (填“>”或“<”)0,原因为___________ 。
(2)化合物M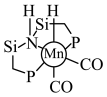 [
[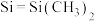 ,
,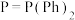 ,Ph代表苯基]可作为CO2合成甲醇的催化剂。化合物M使反应
,Ph代表苯基]可作为CO2合成甲醇的催化剂。化合物M使反应 的速率大大提高,对其逆反应活化能的影响为
的速率大大提高,对其逆反应活化能的影响为___________ 。
(3)某工厂控制条件,建立了存在上述主反应和副反应1的体系,保持其他条件不变,测定温度对合成甲醇过程的影响所得曲线如图1、图2所示(甲醇选择性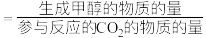 ,CO2转化率在指定时间段内测得),结合图1曲线变化趋势分析图2中温度对甲醇产率的影响:
,CO2转化率在指定时间段内测得),结合图1曲线变化趋势分析图2中温度对甲醇产率的影响:___________ ,242℃时甲醇产率为___________ %(保留三位有效数字)。 ,
, ,达到平衡时CH3OH产率为50%,总压强为p kPa,
,达到平衡时CH3OH产率为50%,总压强为p kPa, ,主反应的平衡常数
,主反应的平衡常数
___________ (保留两位有效数字);达到平衡用时5 min,则0~5 min内,用CH3OH分压表示的平均反应速率为___________ 。
主反应:

 ;
;副反应1:

 ;
;副反应2:

 。
。回答下列问题:
(1)部分键能的数据如下表所示,则主反应的


| 共价键 | H-H | C=O | C-H | C-O | O-H |
键能/( ) ) | 436 | 803 | 414 | 326 | 464 |
(2)化合物M
 [
[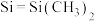 ,
,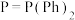 ,Ph代表苯基]可作为CO2合成甲醇的催化剂。化合物M使反应
,Ph代表苯基]可作为CO2合成甲醇的催化剂。化合物M使反应 的速率大大提高,对其逆反应活化能的影响为
的速率大大提高,对其逆反应活化能的影响为(3)某工厂控制条件,建立了存在上述主反应和副反应1的体系,保持其他条件不变,测定温度对合成甲醇过程的影响所得曲线如图1、图2所示(甲醇选择性
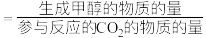 ,CO2转化率在指定时间段内测得),结合图1曲线变化趋势分析图2中温度对甲醇产率的影响:
,CO2转化率在指定时间段内测得),结合图1曲线变化趋势分析图2中温度对甲醇产率的影响: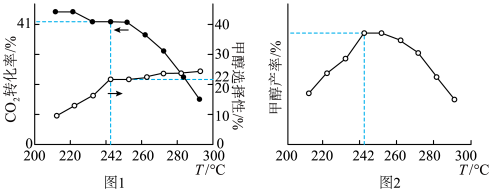
 ,
, ,达到平衡时CH3OH产率为50%,总压强为p kPa,
,达到平衡时CH3OH产率为50%,总压强为p kPa, ,主反应的平衡常数
,主反应的平衡常数
您最近一年使用:0次
名校
9 . 反应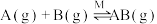 的反应机理为①
的反应机理为①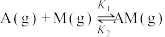
 ;②
;②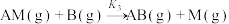
 ,反应过程中的能量变化如图所示。已知反应①:
,反应过程中的能量变化如图所示。已知反应①: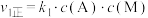 ,
,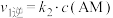 ;反应②:
;反应②: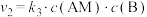 ;总反应
;总反应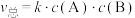 。下列说法错误的是
。下列说法错误的是
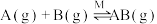 的反应机理为①
的反应机理为①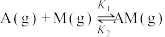
 ;②
;②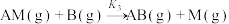
 ,反应过程中的能量变化如图所示。已知反应①:
,反应过程中的能量变化如图所示。已知反应①: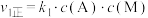 ,
,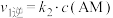 ;反应②:
;反应②: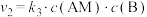 ;总反应
;总反应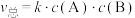 。下列说法错误的是
。下列说法错误的是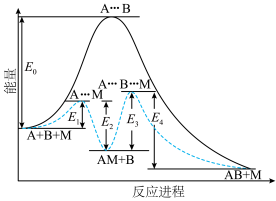
A. , , |
B.反应①先达到平衡状态,平衡时存在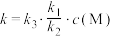 |
C.M为反应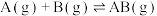 的催化剂 的催化剂 |
| D.反应体系达到平衡后,升高温度,AB浓度增大 |
您最近一年使用:0次
名校
10 . 化合物M是一种合成新型除草剂的中间体,其结构简式如图所示。已知: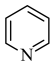 、
、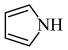 环上的碳原子和氮原子均以sp2杂化轨道相互重叠形成σ键。下列关于M的说法错误的是
环上的碳原子和氮原子均以sp2杂化轨道相互重叠形成σ键。下列关于M的说法错误的是
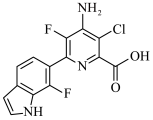
| A.能发生加成反应 |
| B.能发生缩聚反应 |
| C.分子式为C14H9ClN3O2F2 |
| D.所有N原子和C原子可能处于同一平面 |
您最近一年使用:0次



