名校
解题方法
1 . 某实验小组探究用银氨溶液检验醛基适宜的条件。
资料:i. 、
、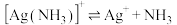
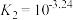 。
。
ii. 不稳定,极易分解为黑色
不稳定,极易分解为黑色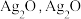 溶于氨水。
溶于氨水。
(1)实验发现:乙醛和 溶液水浴加热无明显现象;银氨溶液水浴加热无明显现象;滴加乙醛的银氨溶液水浴加热,试管壁逐渐出现一层光亮的银镜。
溶液水浴加热无明显现象;银氨溶液水浴加热无明显现象;滴加乙醛的银氨溶液水浴加热,试管壁逐渐出现一层光亮的银镜。
①有研究表明:配制银氨溶液时, 和氨水生成
和氨水生成 ,写出生成
,写出生成 的化学方程式
的化学方程式___________ 。
②从氧化还原角度分析:发生银镜反应时,氧化性微粒可能是 、
、___________ 。
(2)甲同学查阅资料:银镜反应时, 被还原成
被还原成 。
。
①电极反应式:
i.还原反应: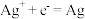
ii.氧化反应:___________ 。(碱性条件下)
②从电极反应角度分析物质氧化性和还原性的变化:
i.随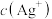 降低,
降低, 氧化性减弱。
氧化性减弱。
ii.随 增大,乙醛还原性增强。
增大,乙醛还原性增强。
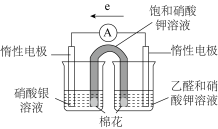
③补充实验验证②中的分析。实验操作及现象:
实验I:插入“饱和 溶液”盐桥,电流表指针偏转;
溶液”盐桥,电流表指针偏转;
实验II:电流稳定后向右侧烧杯滴加 溶液,指针偏转幅度增大;
溶液,指针偏转幅度增大;
实验III:电流再次稳定后向左侧烧杯滴加氨水,指针偏转幅度减小
乙同学认为实验III不能证明“随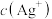 降低,
降低, 氧化性减弱”,理由是
氧化性减弱”,理由是___________ 。
(3)设计实验进一步验证。
①乙同学认为通过实验IV能证明“随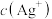 降低,
降低, 氧化性减弱”,你认为是否合理并说明原因
氧化性减弱”,你认为是否合理并说明原因___________ 。
②分析实验V中“立即出现银镜的原因”,提出假设:随 增大,可能是
增大,可能是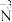 也参与了还原
也参与了还原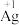 。经检验该假设成立,实验方案及现象是
。经检验该假设成立,实验方案及现象是___________ 。
(4)综上所述,银氨溶液检验醛基时,做氧化剂的粒子是___________ ;为观察到银镜的生成,银氨溶液中加入较浓的 溶液,该方案是否合理,说明理由:
溶液,该方案是否合理,说明理由:___________ 。
资料:i.
 、
、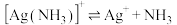
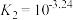 。
。ii.
 不稳定,极易分解为黑色
不稳定,极易分解为黑色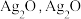 溶于氨水。
溶于氨水。
(1)实验发现:乙醛和
 溶液水浴加热无明显现象;银氨溶液水浴加热无明显现象;滴加乙醛的银氨溶液水浴加热,试管壁逐渐出现一层光亮的银镜。
溶液水浴加热无明显现象;银氨溶液水浴加热无明显现象;滴加乙醛的银氨溶液水浴加热,试管壁逐渐出现一层光亮的银镜。①有研究表明:配制银氨溶液时,
 和氨水生成
和氨水生成 ,写出生成
,写出生成 的化学方程式
的化学方程式②从氧化还原角度分析:发生银镜反应时,氧化性微粒可能是
 、
、(2)甲同学查阅资料:银镜反应时,
 被还原成
被还原成 。
。①电极反应式:
i.还原反应:
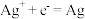
ii.氧化反应:
②从电极反应角度分析物质氧化性和还原性的变化:
i.随
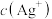 降低,
降低, 氧化性减弱。
氧化性减弱。 ii.随
 增大,乙醛还原性增强。
增大,乙醛还原性增强。③补充实验验证②中的分析。实验操作及现象:
实验I:插入“饱和
 溶液”盐桥,电流表指针偏转;
溶液”盐桥,电流表指针偏转;实验II:电流稳定后向右侧烧杯滴加
 溶液,指针偏转幅度增大;
溶液,指针偏转幅度增大;实验III:电流再次稳定后向左侧烧杯滴加氨水,指针偏转幅度减小
乙同学认为实验III不能证明“随
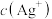 降低,
降低, 氧化性减弱”,理由是
氧化性减弱”,理由是(3)设计实验进一步验证。
| 实验 | 实验操作 | 实验现象 |
| IV | 往盛有银氨溶液的试管中滴加浓氨水,无明显现象,加入3滴乙醛,振荡,水浴加热 | 闻到刺激性气味,溶液略显灰色,试管壁未见银镜 |
| V | 往盛有银氨溶液的试管中滴加较浓的 溶液至 溶液至 与实验IV相同,振荡,溶液变浑浊,加入3滴乙醛,振荡,水浴加热 与实验IV相同,振荡,溶液变浑浊,加入3滴乙醛,振荡,水浴加热 | 试管壁 |
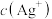 降低,
降低, 氧化性减弱”,你认为是否合理并说明原因
氧化性减弱”,你认为是否合理并说明原因②分析实验V中“立即出现银镜的原因”,提出假设:随
 增大,可能是
增大,可能是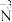 也参与了还原
也参与了还原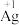 。经检验该假设成立,实验方案及现象是
。经检验该假设成立,实验方案及现象是(4)综上所述,银氨溶液检验醛基时,做氧化剂的粒子是
 溶液,该方案是否合理,说明理由:
溶液,该方案是否合理,说明理由:
您最近一年使用:0次
2 . Ⅰ.高铁酸钾(K2FeO4) 是一种高效、无毒的强氧化剂,常温下为紫色固体,微溶于浓KOH溶液,能溶于水,且能与水反应放出氧气,并生成Fe(OH)3胶体。稳定性随pH的下降而减弱,酸性条件下易分解。
(1)下列有关铁及其化合物的性质与用途具有对应关系的是___________
Ⅱ.K2FeO4的净水原理如图所示:
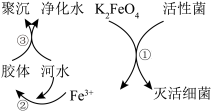
(2)下列说法错误的是___________
(3)写出K2FeO4与水反应的化学方程式___________ 。
Ⅲ.已知可用Cl2与Fe(NO3)3制备K2FeO4(含副产品KCl、KNO3),查阅资料得知高铁酸盐在水溶液中有四种含铁形体。25℃时,它们的物质的量分数随pH的变化如图所示:
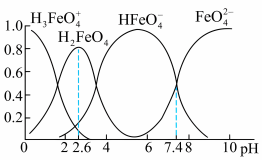
(4)①为获得尽可能纯净的高铁酸盐,pH应控制在___________ 。
②写出在此条件下,反应的离子方程式:___________ ;每生成39.6g K2FeO4,转移的电子数目为___________ ;
(5)已知溶液的酸碱性及离子浓度会对反应试剂的氧化性、还原性产生影响。
某实验小组研究不同反应试剂对K2FeO4产率的影响,对比实验如下:
注:上述实验中,溶液总体积、FeCl3和Fe(NO3)3的物质的量、Cl2的通入量均相同。
①由实验I、II的现象可知,Fe3+的还原性随溶液碱性的增强而___________ (填“增强”、“减弱”或“不变”);
②实验II中K2FeO4的产率比实验III低,试解释其可能的原因:___________ ;
③向实验II所得紫色溶液中继续通入Cl2,观察到溶液紫色变浅,试解释其可能的原因:___________ 。
(6)实验室测定含少量杂质的K2FeO4样品的纯度:称取0.1500g K2FeO4样品溶于碱性KI溶液中,调节pH至弱酸性使混合液充分反应。用0.1000 mol·L−1的Na2S2O3标准溶液进行滴定,消耗Na2S2O3标准溶液25.00 mL。滴定时,发生反应的离子方程式:FeO + 4I−+ 8H+= Fe2+ + 2I2+ 4H2O;I2 + 2S2O
+ 4I−+ 8H+= Fe2+ + 2I2+ 4H2O;I2 + 2S2O = S4O
= S4O + 2I−。已知:M(K2FeO4) =198g·mol−1,试计算K2FeO4样品的纯度:
+ 2I−。已知:M(K2FeO4) =198g·mol−1,试计算K2FeO4样品的纯度:___________ (写出计算过程)。
(1)下列有关铁及其化合物的性质与用途具有对应关系的是___________
| A.铁粉具有还原性,可防止食物氧化变质 | B.高铁酸钾能溶于水,可作氧化剂 |
| C.氢氧化铁胶体具有碱性,可用于净水 | D.纯铁无杂质,可用作建筑材料 |
Ⅱ.K2FeO4的净水原理如图所示:

(2)下列说法错误的是___________
| A.K2FeO4中铁元素显+6价 |
| B.过程①中K2FeO4被细菌还原 |
| C.过程②中的Fe(OH)3胶体粒子带正电荷 |
| D.过程③中聚沉是由于胶体发生了渗析 |
(3)写出K2FeO4与水反应的化学方程式
Ⅲ.已知可用Cl2与Fe(NO3)3制备K2FeO4(含副产品KCl、KNO3),查阅资料得知高铁酸盐在水溶液中有四种含铁形体。25℃时,它们的物质的量分数随pH的变化如图所示:

(4)①为获得尽可能纯净的高铁酸盐,pH应控制在
②写出在此条件下,反应的离子方程式:
(5)已知溶液的酸碱性及离子浓度会对反应试剂的氧化性、还原性产生影响。
某实验小组研究不同反应试剂对K2FeO4产率的影响,对比实验如下:
| 实验编号 | 反应试剂 | 实验现象 |
| Ⅰ | Cl2、FeCl3和少量KOH | 无明显现象 |
| Ⅱ | Cl2、FeCl3和过量KOH | 得到紫色溶液,无紫色固体 |
| Ⅲ | Cl2、Fe(NO3)3和过量KOH | 得到紫色溶液(颜色比Ⅱ深),有紫色固体 |
①由实验I、II的现象可知,Fe3+的还原性随溶液碱性的增强而
②实验II中K2FeO4的产率比实验III低,试解释其可能的原因:
③向实验II所得紫色溶液中继续通入Cl2,观察到溶液紫色变浅,试解释其可能的原因:
(6)实验室测定含少量杂质的K2FeO4样品的纯度:称取0.1500g K2FeO4样品溶于碱性KI溶液中,调节pH至弱酸性使混合液充分反应。用0.1000 mol·L−1的Na2S2O3标准溶液进行滴定,消耗Na2S2O3标准溶液25.00 mL。滴定时,发生反应的离子方程式:FeO
 + 4I−+ 8H+= Fe2+ + 2I2+ 4H2O;I2 + 2S2O
+ 4I−+ 8H+= Fe2+ + 2I2+ 4H2O;I2 + 2S2O = S4O
= S4O + 2I−。已知:M(K2FeO4) =198g·mol−1,试计算K2FeO4样品的纯度:
+ 2I−。已知:M(K2FeO4) =198g·mol−1,试计算K2FeO4样品的纯度:
您最近一年使用:0次
3 . FeSO4溶液放置在空气中容易变质,因此为了方便使用Fe2+,实验室中常保存硫酸亚铁铵晶体[俗称“摩尔盐”,化学式为(NH4)2Fe(SO4)2•6H2O],它比绿矾或绿矾溶液更稳定。
I.某兴趣小组设计实验制备硫酸亚铁铵晶体。
本实验中,配制溶液以及后续使用到的蒸馏水都经过煮沸、冷却后再使用。向FeSO4溶液中加入饱和(NH4)2SO4溶液,经过操作_______ 、冷却结晶、过滤、洗涤和干燥后得到一种浅蓝绿色的晶体。
II.实验探究影响溶液中Fe2+稳定性的因素
(1)配制0.8 mol/L的FeSO4溶液(pH=4.5)和0.8 mol/L的(NH4)2Fe(SO4)2溶液(pH=4.0),各取2 mL上述溶液于两支试管中,刚开始两种溶液都是浅绿色,分别同时滴加2滴0.01mol/L的KSCN溶液,15min后观察可见:(NH4)2Fe(SO4)2溶液仍然为浅绿色透明澄清溶液,FeSO4溶液则出现淡黄色浑浊。
【资料1】
①请用离子方程式解释FeSO4溶液产生淡黄色浑浊的原因___________________ 。
②讨论影响Fe2+稳定性的因素,小组同学提出以下3种假设:
假设1:其他条件相同时,NH4+的存在使(NH4)2Fe(SO4)2溶液中Fe2+稳定性较好。
假设2:其他条件相同时,在一定 pH范围内,溶液 pH越小Fe2+稳定性越好。
假设3:__________________________________________________ 。
(2)小组同学用如图装置(G为灵敏电流计),滴入适量的硫酸溶液分别控制溶液A(0.2 mol/L NaCl)和溶液B(0.1mol/L FeSO4)为不同的 pH,观察记录电流计读数,对假设2进行实验研究,实验结果如下表所示。
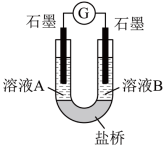
【资料2】原电池装置中,其他条件相同时,负极反应物的还原性越强或正极反应物的氧化性越强,该原电池的电流越大。
【资料3】常温下,0.1mol/LpH=1的FeSO4溶液比pH=5的FeSO4溶液稳定性更好。
根据以上实验结果和资料信息,经小组讨论可以得出以下结论:
①U型管中左池的电极反应式_________________ 。
②对比实验1和2(或3和4),在一定pH范围内,可得出的结论为______ 。
③对比实验_____ 和_____ 还可得出在一定 pH范围内,溶液酸碱性变化是对O2氧化性强弱的影响因素。
④对【资料3】实验事实的解释为____________________ 。
I.某兴趣小组设计实验制备硫酸亚铁铵晶体。
本实验中,配制溶液以及后续使用到的蒸馏水都经过煮沸、冷却后再使用。向FeSO4溶液中加入饱和(NH4)2SO4溶液,经过操作
II.实验探究影响溶液中Fe2+稳定性的因素
(1)配制0.8 mol/L的FeSO4溶液(pH=4.5)和0.8 mol/L的(NH4)2Fe(SO4)2溶液(pH=4.0),各取2 mL上述溶液于两支试管中,刚开始两种溶液都是浅绿色,分别同时滴加2滴0.01mol/L的KSCN溶液,15min后观察可见:(NH4)2Fe(SO4)2溶液仍然为浅绿色透明澄清溶液,FeSO4溶液则出现淡黄色浑浊。
【资料1】
| 沉淀 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀 pH | 7.6 | 2.7 |
| 完全沉淀 pH | 9.6 | 3.7 |
②讨论影响Fe2+稳定性的因素,小组同学提出以下3种假设:
假设1:其他条件相同时,NH4+的存在使(NH4)2Fe(SO4)2溶液中Fe2+稳定性较好。
假设2:其他条件相同时,在一定 pH范围内,溶液 pH越小Fe2+稳定性越好。
假设3:
(2)小组同学用如图装置(G为灵敏电流计),滴入适量的硫酸溶液分别控制溶液A(0.2 mol/L NaCl)和溶液B(0.1mol/L FeSO4)为不同的 pH,观察记录电流计读数,对假设2进行实验研究,实验结果如下表所示。
| 序号 | A 0.2mol/LNaCl | B 0.1mol/LFeSO4 | 电流计读数 |
| 实验1 | pH=1 | pH=5 | 8.4 |
| 实验2 | pH=1 | pH=1 | 6.5 |
| 实验3 | pH=6 | pH=5 | 7.8 |
| 实验4 | pH=6 | pH=1 | 5.5 |

【资料2】原电池装置中,其他条件相同时,负极反应物的还原性越强或正极反应物的氧化性越强,该原电池的电流越大。
【资料3】常温下,0.1mol/LpH=1的FeSO4溶液比pH=5的FeSO4溶液稳定性更好。
根据以上实验结果和资料信息,经小组讨论可以得出以下结论:
①U型管中左池的电极反应式
②对比实验1和2(或3和4),在一定pH范围内,可得出的结论为
③对比实验
④对【资料3】实验事实的解释为
您最近一年使用:0次
2020-04-02更新
|
346次组卷
|
4卷引用:北京市门头沟区2020届高三3月综合练习化学试题
北京市门头沟区2020届高三3月综合练习化学试题山东省2020届高三模拟考试化学试题(已下线)北京市2019-2020学年高三各区一模化学考试分类汇编:科学探究江苏省昆山中学2022-2023学年高一下学期期中考试化学试题
名校
4 . 某兴趣小组为探究浓硫酸与铜的反应,设计了如下装置。_______ 。
(2)为验证品红被 漂白的产物不稳定,简述操作步骤及现象
漂白的产物不稳定,简述操作步骤及现象_______ 。
(3)浸NaOH溶液的棉团作用是_______ 。
(4)为进一步探究 的还原性,将过量的
的还原性,将过量的 通入到200mL1.0mol/L的
通入到200mL1.0mol/L的 和过量
和过量 混合溶液中,观察到装置中产生了白色沉淀。装置如图所示。
混合溶液中,观察到装置中产生了白色沉淀。装置如图所示。 产生的原因进行探究(不考虑溶液中
产生的原因进行探究(不考虑溶液中 的影响)
的影响)
①查阅资料 不同浓度的 被还原的产物不同且产物不单一、不同pH时,
被还原的产物不同且产物不单一、不同pH时, 的氧化性不同。1.0mol/L的
的氧化性不同。1.0mol/L的 的
的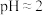 。
。
②提出猜想 猜想1: 被
被 氧化
氧化
猜想2: 在酸性条件下被
在酸性条件下被 氧化
氧化
猜想3:_______
③设计实验、验证猜想
限选实验试剂:0.01mol/LHCl、0.02mol/LHCl、3.0mol/LHNO3、6.0mol/LHNO3、3.0mol/LNaNO3、6.0mol/LNaNO3、0.1mol/LKSCN、 和
和 固体
固体
④交流讨论 小组同学认为,综合上述两个实验不足以证明猜想3成立。
⑤优化实验 若要证明猜想3成立,还要进行实验3。
实验3:_______ (只需提供设计思路,不需要写出具体操作步骤)。

(2)为验证品红被
 漂白的产物不稳定,简述操作步骤及现象
漂白的产物不稳定,简述操作步骤及现象(3)浸NaOH溶液的棉团作用是
(4)为进一步探究
 的还原性,将过量的
的还原性,将过量的 通入到200mL1.0mol/L的
通入到200mL1.0mol/L的 和过量
和过量 混合溶液中,观察到装置中产生了白色沉淀。装置如图所示。
混合溶液中,观察到装置中产生了白色沉淀。装置如图所示。
 产生的原因进行探究(不考虑溶液中
产生的原因进行探究(不考虑溶液中 的影响)
的影响)①查阅资料 不同浓度的
 被还原的产物不同且产物不单一、不同pH时,
被还原的产物不同且产物不单一、不同pH时, 的氧化性不同。1.0mol/L的
的氧化性不同。1.0mol/L的 的
的 。
。②提出猜想 猜想1:
 被
被 氧化
氧化猜想2:
 在酸性条件下被
在酸性条件下被 氧化
氧化猜想3:
③设计实验、验证猜想
限选实验试剂:0.01mol/LHCl、0.02mol/LHCl、3.0mol/LHNO3、6.0mol/LHNO3、3.0mol/LNaNO3、6.0mol/LNaNO3、0.1mol/LKSCN、
 和
和 固体
固体| 实验步骤 | 实验现象和结论 |
| 实验1:取少量反应后的上层清液于试管中,滴入少量 | 出现 与 与 发生的离子方程式为 发生的离子方程式为 |
实验2:往图中的装置中加入100mL 固体,再通入过量 固体,再通入过量 。 。 | 出现白色沉淀,说明猜想2成立。 |
⑤优化实验 若要证明猜想3成立,还要进行实验3。
实验3:
您最近一年使用:0次
2022-04-29更新
|
1051次组卷
|
7卷引用:广东省粤港澳大湾区普通高中2022届高三第二次模拟考试化学试题
广东省粤港澳大湾区普通高中2022届高三第二次模拟考试化学试题(已下线)化学-2023年高考押题预测卷03(广东卷)(含考试版、全解全析、参考答案、答题卡)(已下线)专项14 化学实验综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(5月期)湖南省郴州市永兴县第一中学2021-2022学年高三下学期期中考试化学试题热点1实验方案设计四川省泸州市古蔺县金兰高级中学校2022-2023学年高二下学期第一次月考化学试题2024届四川省攀枝花市第十五中学校高三上学期12月第7次半月考理科综合试题-高中化学
名校
解题方法
5 . 某研究性学习小组对亚硫酸钠的组成及性质进行探究。
(1)向Na2SO3溶液中滴加少量Na2S溶液无明显现象,继续滴加适量稀硫酸,有沉淀生成。
①该反应说明Na2SO3具有_______ (填“氧化性”或“还原性”),反应的离子方程式为_______ 。
②查资料知H2SO3是二元弱酸,Ka1=1.2×10-2,Ka2=6.3×10-8.判断NaHSO3溶液显_______ (填“酸性”、“碱性”或“中性”)。
(2)经分析,Na2SO3溶液在存放过程中有可能变质。甲同学设计了如下两种方案来检验Na2SO3溶液是否变质。
方案1:取样,加入稀盐酸有气泡生成,认为Na2SO3溶液没有变质。
方案2:取样,加入BaCl2溶液有白色沉淀生成,认为Na2SO3溶液完全变质。
乙同学认为上述两种方案均不合理。乙同学对方案2作出判断的依据是_______ 。
(3)丙同学设计了下图所示的实验装置(夹持装置已略去),测定Na2SO3溶液变质的百分率(变质的百分率=已变质的亚硫酸钠质量/溶液中亚硫酸钠的总质量×100%)。
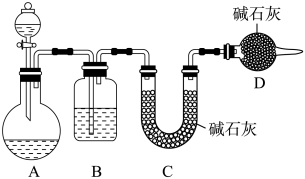
量取60mL标签上注明为1.0mol·L-1的Na2SO3溶液放入A装置中,进行实验。
①D装置的作用是_______ ;缺少B装置,测定的变质的百分率将会_______ (填“偏高”、“偏低”或“不变”)。
②该实验装置中存在的明显缺陷是_______ 。改进缺陷后再进行实验,若实验前后测得C装置增重3.2g,则Na2SO3变质的百分率为_______ 。
(1)向Na2SO3溶液中滴加少量Na2S溶液无明显现象,继续滴加适量稀硫酸,有沉淀生成。
①该反应说明Na2SO3具有
②查资料知H2SO3是二元弱酸,Ka1=1.2×10-2,Ka2=6.3×10-8.判断NaHSO3溶液显
(2)经分析,Na2SO3溶液在存放过程中有可能变质。甲同学设计了如下两种方案来检验Na2SO3溶液是否变质。
方案1:取样,加入稀盐酸有气泡生成,认为Na2SO3溶液没有变质。
方案2:取样,加入BaCl2溶液有白色沉淀生成,认为Na2SO3溶液完全变质。
乙同学认为上述两种方案均不合理。乙同学对方案2作出判断的依据是
(3)丙同学设计了下图所示的实验装置(夹持装置已略去),测定Na2SO3溶液变质的百分率(变质的百分率=已变质的亚硫酸钠质量/溶液中亚硫酸钠的总质量×100%)。

量取60mL标签上注明为1.0mol·L-1的Na2SO3溶液放入A装置中,进行实验。
①D装置的作用是
②该实验装置中存在的明显缺陷是
您最近一年使用:0次
6 . 某研究性学习小组学生根据氧化还原反应规律,探究NO2、NO与Na2O2反应的情况,提出假设并进行相关实验。
Ⅰ.从理论上分析Na2O2和NO2都既有氧化性又有还原性,于是提出如下假设:
假设1:Na2O2氧化NO2;假设2:NO2氧化Na2O2。
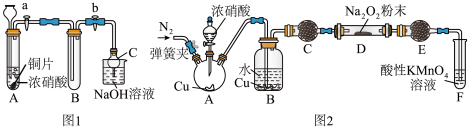
(1)甲同学设计如图1装置进行实验:
①试管A 中反应的离子方程式是____________________________ 。
②待试管B 中充满红棕色气体,关闭旋塞a和b;取下试管B;向其中加入适量Na2O2粉末,塞上塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的木条迅速伸进试管内,木条复燃。
③仪器C兼有防倒吸的作用,仪器C的名称为___________________ 。
结论:甲同学认为假设2 正确。
(2)乙同学认为甲同学设计的实验存在缺陷,为达到实验目的,在A、B之间应增加一个装置,该装置的作用是________________________ 。乙同学用改进后的装置,重复了甲同学的实验操作,观察到红棕色气体迅速消失;带火星的木条未复燃,得出结论:假设1正确,则NO2和Na2O2反应的化学方程式是_______________________ 。
Ⅱ.该研究性学习小组同学还认为NO 易与O2发生反应,应该更易被Na2O2氧化。查阅资料:2NO+Na2O2=2NaNO2;2NaNO2+2HCl=2NaCl+NO2↑+NO↑+H2O; 酸性条件下,NO 能与MnO 反应生成NO
反应生成NO 和Mn2+。
和Mn2+。
(3)丙同学用图2所示装置(部分夹持装置略)探究NO与Na2O2的反应。
①在反应前,打开弹簧夹,通入一段时间N2,目的是_________________ 。
②B 中观察到的主要现象是____________ (填字母编号)。
a.铜片逐渐溶解,溶液变为蓝色 b.有红棕色气泡产生 C.有无色气泡产生
③C、E 中所盛装的试剂不能是________ (填字母编号)。
a.无水硫酸铜 b.无水氯化钙 c.碱石灰 d.生石灰
④F 中发生反应的氧化剂与还原剂的物质的量之比为_____________ 。
⑤充分反应后,检验D装置中产物的方法是:______________ ,则产物是NaNO2。

Ⅰ.从理论上分析Na2O2和NO2都既有氧化性又有还原性,于是提出如下假设:
假设1:Na2O2氧化NO2;假设2:NO2氧化Na2O2。
(1)甲同学设计如图1装置进行实验:
①试管A 中反应的离子方程式是
②待试管B 中充满红棕色气体,关闭旋塞a和b;取下试管B;向其中加入适量Na2O2粉末,塞上塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的木条迅速伸进试管内,木条复燃。
③仪器C兼有防倒吸的作用,仪器C的名称为
结论:甲同学认为假设2 正确。
(2)乙同学认为甲同学设计的实验存在缺陷,为达到实验目的,在A、B之间应增加一个装置,该装置的作用是
Ⅱ.该研究性学习小组同学还认为NO 易与O2发生反应,应该更易被Na2O2氧化。查阅资料:2NO+Na2O2=2NaNO2;2NaNO2+2HCl=2NaCl+NO2↑+NO↑+H2O; 酸性条件下,NO 能与MnO
 反应生成NO
反应生成NO 和Mn2+。
和Mn2+。(3)丙同学用图2所示装置(部分夹持装置略)探究NO与Na2O2的反应。
①在反应前,打开弹簧夹,通入一段时间N2,目的是
②B 中观察到的主要现象是
a.铜片逐渐溶解,溶液变为蓝色 b.有红棕色气泡产生 C.有无色气泡产生
③C、E 中所盛装的试剂不能是
a.无水硫酸铜 b.无水氯化钙 c.碱石灰 d.生石灰
④F 中发生反应的氧化剂与还原剂的物质的量之比为
⑤充分反应后,检验D装置中产物的方法是:
您最近一年使用:0次
解题方法
7 . 某化学小组探究硫酸铁铵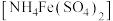 与
与 、
、 的反应。
的反应。
已知: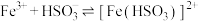 (棕红)
(棕红)
(1)①实验Ⅰ中产生红褐色沉淀与气泡的离子方程式为___________ 。
②由实验Ⅰ可得出与 结合的能力:
结合的能力:
___________  (填“>”、“<”、“=”)。
(填“>”、“<”、“=”)。
(2)资料显示, 可以氧化
可以氧化 。针对实验Ⅱ中的现象,小组同学又设计并实施了如下实验。
。针对实验Ⅱ中的现象,小组同学又设计并实施了如下实验。
①实验Ⅲ中 与
与 反应生成
反应生成 的离子方程式为
的离子方程式为___________ 。
②结合化学反应原理解释实验Ⅱ、Ⅳ中现象存在差异的可能原因___________ 。
(3)针对实验Ⅲ、Ⅳ的现象差异,小组同学提出猜想:pH影响了 的氧化性或
的氧化性或 的还原性,并实施实验。
的还原性,并实施实验。
①a、b分别是___________ 。
②结合电极反应解释步骤3中电压表示数减小的原因___________ 。
③补充实验Ⅵ:向实验Ⅱ得到的棕红色液体中加入3滴10%稀硫酸,棕红色迅速变黄,检测到 。结合化学用语解释实验Ⅵ中氧化还原反应明显加快的可能原因
。结合化学用语解释实验Ⅵ中氧化还原反应明显加快的可能原因___________ 。
(4)综合以上实验,盐溶液间反应的多样性与___________ 有关。
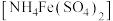 与
与 、
、 的反应。
的反应。| 实验 | 操作 | 现象 |
| Ⅰ | 向2mL 溶液(pH=2.03)中逐滴加入 溶液(pH=2.03)中逐滴加入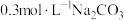 溶液 溶液 | 迅速产生大量红褐色沉淀和大量气泡;继续滴加,当气泡量明显减少时,试管口的湿润红色石蕊试纸开始逐渐变蓝 |
| Ⅱ | 向2mL 溶液(pH=2.03)中逐滴加入 溶液(pH=2.03)中逐滴加入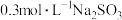 溶液 溶液 | 溶液立即变棕红(无丁达尔现象),继续滴加 溶液至过量,溶液依然为棕红色,放置两天无明显变化 溶液至过量,溶液依然为棕红色,放置两天无明显变化 |
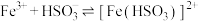 (棕红)
(棕红)(1)①实验Ⅰ中产生红褐色沉淀与气泡的离子方程式为
②由实验Ⅰ可得出与
 结合的能力:
结合的能力:
 (填“>”、“<”、“=”)。
(填“>”、“<”、“=”)。(2)资料显示,
 可以氧化
可以氧化 。针对实验Ⅱ中的现象,小组同学又设计并实施了如下实验。
。针对实验Ⅱ中的现象,小组同学又设计并实施了如下实验。| 实验 | 操作 | 现象 |
| Ⅲ | 向2mL 溶液(pH=1.78)中加入0.5mL 溶液(pH=1.78)中加入0.5mL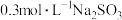 溶液 溶液 | 溶液立即变棕红色,约2小时后,棕红色变为黄色,检测到 |
| Ⅳ | 向2mL 溶液(pH=2.03)中加入0.5mL 溶液(pH=2.03)中加入0.5mL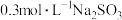 溶液 溶液 | 溶液立即变棕红色,约5小时后,棕红色变为黄色,检测到 |
 与
与 反应生成
反应生成 的离子方程式为
的离子方程式为②结合化学反应原理解释实验Ⅱ、Ⅳ中现象存在差异的可能原因
(3)针对实验Ⅲ、Ⅳ的现象差异,小组同学提出猜想:pH影响了
 的氧化性或
的氧化性或 的还原性,并实施实验。
的还原性,并实施实验。| 实验 | 实验装置 | 实验步骤及现象 |
| Ⅴ |
| 1.按如图搭好装置,接通电路,电压表读数为0.6V; 2.向a电极附近滴加3滴10%稀硫酸,电压表读数不变; 3.向石墨电极附近滴加3滴10%稀硫酸,电压表读数变为0.5V。 |
②结合电极反应解释步骤3中电压表示数减小的原因
③补充实验Ⅵ:向实验Ⅱ得到的棕红色液体中加入3滴10%稀硫酸,棕红色迅速变黄,检测到
 。结合化学用语解释实验Ⅵ中氧化还原反应明显加快的可能原因
。结合化学用语解释实验Ⅵ中氧化还原反应明显加快的可能原因(4)综合以上实验,盐溶液间反应的多样性与
您最近一年使用:0次
名校
解题方法
8 . 硫代硫酸银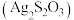 为白色固体,受热易分解且具有还原性,可用作乙烯抑制剂。某课外小组向
为白色固体,受热易分解且具有还原性,可用作乙烯抑制剂。某课外小组向 溶液中逐滴滴加
溶液中逐滴滴加 溶液制备
溶液制备 。实验记录如下。
。实验记录如下。
已知:Ⅰ.①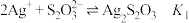
②
Ⅱ.相关物质的 :
:

(1) 中配位原子为
中配位原子为_______ ,配体阴离子的空间构型是_______ 。
(2)实验中沉淀溶解的总反应为: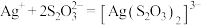 ,其平衡常数
,其平衡常数
_______ (用含 、
、 的代数式表示)。
的代数式表示)。
(3)用平衡移动原理解释实验中随 溶液滴入,又产生白色沉淀的原因是
溶液滴入,又产生白色沉淀的原因是_______ 。
(4)设计如下实验证明实验过程中产生的沉淀除了含有 外,还含有S和
外,还含有S和 。
。
取少量沉淀,加入足量_______ (填标号),充分振荡,过滤得滤液a和固体b。
A.乙醇 B.乙醚 C.丙酮 D.
i.取滤液a蒸馏可得黄色物质,证明沉淀中含有S。
ii.取固体b,_______ ,证明沉淀中含有 。(可供选择的试剂:稀硫酸、稀盐酸、稀硝酸、
。(可供选择的试剂:稀硫酸、稀盐酸、稀硝酸、 溶液)
溶液)
(5)查阅资料可知: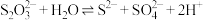 。实验证明:实验中S产生的主要原因是
。实验证明:实验中S产生的主要原因是 被
被 氧化而非被
氧化而非被 氧化。从反应速率的角度解释其原因:i.等浓度
氧化。从反应速率的角度解释其原因:i.等浓度 的氧化性大于
的氧化性大于 ,氧化
,氧化 的速率更快;ii.
的速率更快;ii._______ 。
(6)制备 时需及时分离出白色沉淀的原因是
时需及时分离出白色沉淀的原因是_______ 。
(7) 中的银元素在乙烯抑制剂中发挥重要的作用。该小组同学测定制得的白色固体中银的质量分数,具体实验过程如下。取
中的银元素在乙烯抑制剂中发挥重要的作用。该小组同学测定制得的白色固体中银的质量分数,具体实验过程如下。取 白色固体,加入适量硝酸充分反应,所得溶液加水稀释至
白色固体,加入适量硝酸充分反应,所得溶液加水稀释至 。再取
。再取 稀溶液于锥形瓶中,加入指示剂用
稀溶液于锥形瓶中,加入指示剂用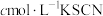 溶液进行滴定,重复滴定2~3次,平均消耗
溶液进行滴定,重复滴定2~3次,平均消耗 溶液的体积为
溶液的体积为 。已知:
。已知:
①选用的指示剂是_______ (填标号)。
A. B.
B. C.
C. D.
D.
②若未加入适量硝酸充分反应,会导致测量结果_______ (填“偏高”、“偏低”或“无影响”)。
③白色固体中银的质量分数为_______ %。
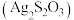 为白色固体,受热易分解且具有还原性,可用作乙烯抑制剂。某课外小组向
为白色固体,受热易分解且具有还原性,可用作乙烯抑制剂。某课外小组向 溶液中逐滴滴加
溶液中逐滴滴加 溶液制备
溶液制备 。实验记录如下。
。实验记录如下。| 操作 | 试剂a | 试剂b | 实验现象 |
 |  溶液 溶液 | 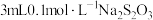 溶液 溶液 | 开始有白色沉淀,振荡后溶解,随 溶液滴入,又产生白色沉淀,而后沉淀逐渐变成黄色,最终变成黑色 溶液滴入,又产生白色沉淀,而后沉淀逐渐变成黄色,最终变成黑色 |
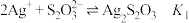
②

Ⅱ.相关物质的
 :
:| 物质 |  |  |  |
 | 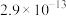 | 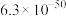 |  |

(1)
 中配位原子为
中配位原子为(2)实验中沉淀溶解的总反应为:
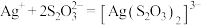 ,其平衡常数
,其平衡常数
 、
、 的代数式表示)。
的代数式表示)。(3)用平衡移动原理解释实验中随
 溶液滴入,又产生白色沉淀的原因是
溶液滴入,又产生白色沉淀的原因是(4)设计如下实验证明实验过程中产生的沉淀除了含有
 外,还含有S和
外,还含有S和 。
。取少量沉淀,加入足量
A.乙醇 B.乙醚 C.丙酮 D.

i.取滤液a蒸馏可得黄色物质,证明沉淀中含有S。
ii.取固体b,
 。(可供选择的试剂:稀硫酸、稀盐酸、稀硝酸、
。(可供选择的试剂:稀硫酸、稀盐酸、稀硝酸、 溶液)
溶液)(5)查阅资料可知:
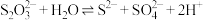 。实验证明:实验中S产生的主要原因是
。实验证明:实验中S产生的主要原因是 被
被 氧化而非被
氧化而非被 氧化。从反应速率的角度解释其原因:i.等浓度
氧化。从反应速率的角度解释其原因:i.等浓度 的氧化性大于
的氧化性大于 ,氧化
,氧化 的速率更快;ii.
的速率更快;ii.(6)制备
 时需及时分离出白色沉淀的原因是
时需及时分离出白色沉淀的原因是(7)
 中的银元素在乙烯抑制剂中发挥重要的作用。该小组同学测定制得的白色固体中银的质量分数,具体实验过程如下。取
中的银元素在乙烯抑制剂中发挥重要的作用。该小组同学测定制得的白色固体中银的质量分数,具体实验过程如下。取 白色固体,加入适量硝酸充分反应,所得溶液加水稀释至
白色固体,加入适量硝酸充分反应,所得溶液加水稀释至 。再取
。再取 稀溶液于锥形瓶中,加入指示剂用
稀溶液于锥形瓶中,加入指示剂用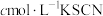 溶液进行滴定,重复滴定2~3次,平均消耗
溶液进行滴定,重复滴定2~3次,平均消耗 溶液的体积为
溶液的体积为 。已知:
。已知:
①选用的指示剂是
A.
 B.
B. C.
C. D.
D.
②若未加入适量硝酸充分反应,会导致测量结果
③白色固体中银的质量分数为
您最近一年使用:0次
解题方法
9 . 某校化学研究性学习小组查阅资料了解到以下内容:
乙二酸(HOOC—COOH,可简写为H2C2O4)俗称草酸,易溶于水,属于二元中强酸(为弱电解质),且酸性强于碳酸,其熔点为101.5℃,在157℃升华.为探究草酸的部分化学性质,进行了如下实验:
(1)向盛有1mL饱和NaHCO3溶液的试管中加入足量乙二酸溶液,观察到有无色气泡产生.该反应的离子方程式为____________________ 。
(2)向盛有乙二酸饱和溶液的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现紫红色逐渐褪去,说明乙二酸具有_______ (填:“氧化性”、“还原性”或“酸性”),请配平该反应的离子方程式:__ MnO +
+__ H2C2O4+__ H+=__ Mn2++__ CO2↑+__ H2O
(3)将一定量的乙二酸放于试管中,按下图所示装置进行实验(夹持装置未标出):

实验发现:装置C、G中澄清石灰水变浑浊,B中CuSO4粉末变蓝,F中CuO粉末变红。据此回答:上述装置中,D的作用是____________________ 。乙二酸分解的化学方程式为________________ 。
(4)该小组同学将2.52g草酸晶体(H2C2O4·2H2O)加入到100mL 0.2mol·L-1的NaOH溶液中充分反应,测得反应后溶液呈酸性,其原因是___________________ 。
(5)Na2C2O4溶液中离子的浓度由大到小的顺序为:__________________ 。
(6)设计实验证明草酸的酸性比碳酸强:__________________ 。
乙二酸(HOOC—COOH,可简写为H2C2O4)俗称草酸,易溶于水,属于二元中强酸(为弱电解质),且酸性强于碳酸,其熔点为101.5℃,在157℃升华.为探究草酸的部分化学性质,进行了如下实验:
(1)向盛有1mL饱和NaHCO3溶液的试管中加入足量乙二酸溶液,观察到有无色气泡产生.该反应的离子方程式为
(2)向盛有乙二酸饱和溶液的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现紫红色逐渐褪去,说明乙二酸具有
 +
+(3)将一定量的乙二酸放于试管中,按下图所示装置进行实验(夹持装置未标出):

实验发现:装置C、G中澄清石灰水变浑浊,B中CuSO4粉末变蓝,F中CuO粉末变红。据此回答:上述装置中,D的作用是
(4)该小组同学将2.52g草酸晶体(H2C2O4·2H2O)加入到100mL 0.2mol·L-1的NaOH溶液中充分反应,测得反应后溶液呈酸性,其原因是
(5)Na2C2O4溶液中离子的浓度由大到小的顺序为:
(6)设计实验证明草酸的酸性比碳酸强:
您最近一年使用:0次
名校
解题方法
10 . 次氯酸盐是常用的水处理剂。有效氯含量(COAC)指与含氯消毒剂氧化能力相当的氯气量,单位为 mol/L;物质氧化性越强,氧化还原电位(ORP)越高;相同条件下,次氯酸的氧化性大于次氯酸盐。温度及pH对Ca(ClO)2溶液有效氯含量(COAC)及氧化还原电位的影响。
(1)在不同温度下,用0.2 mol/L乙酸溶液调节pH得到Ca(ClO)2溶液COAC、ORP的关系如图1室温(25 ℃)、图2(70 ℃)所示。___________ (填“增大”或“减小”)。
②Ca(ClO)2溶液用于消毒时适宜的条件:温度为___________ (填字母,下同)、pH为___________ 。
A. 25 ℃ B. 70 ℃ C. 5.75 D. 6.85
(2)某小组探究70 ℃时,pH及稳定剂对NaClO溶液有效氯含量的影响。甲同学设计实验方案如下:
①设计实验1和2的目的是___________ 。
②实验5中的a___________ 0.935(填“大于”“小于”或“等于”)。
③根据实验3~5,可得出的结论是___________ 。
④下列物质中最适宜作为NaClO溶液稳定剂的是___________ (填字母)。
A. MgCl2 B. NaCl C. Na2S D. CH3COONa
资料:ⅰ.Mn2+在一定条件下被ClO-氧化成MnO2(棕黑色)、 (绿色)、
(绿色)、 (紫色)。
(紫色)。
ⅱ.浓碱条件下, 可被OH-还原为
可被OH-还原为 。
。
ⅲ.NaClO的氧化性随碱性增强而减弱。
实验记录如下:
(3)根据资料ⅱ,Ⅲ中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的原因。
原因一:可能是通入Cl2导致溶液的碱性减弱。
原因二:可能是氧化剂过量,氧化剂将 氧化为
氧化为 。
。
①离子方程式表示可能导致溶液碱性减弱的原因:_______________ ,但通过实验测定溶液的碱性变化很小。
②取Ⅲ中放置后的1 mL悬浊液,加入4 mL 40% NaOH溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶液紫色变为绿色的离子方程式为___________ ,溶液绿色缓慢加深,原因是MnO2被___________ (填化学式)氧化,可证明Ⅲ的悬浊液中氧化剂过量。
③从反应速率的角度,分析实验Ⅲ未得到绿色溶液的可能原因:___________ 。
(1)在不同温度下,用0.2 mol/L乙酸溶液调节pH得到Ca(ClO)2溶液COAC、ORP的关系如图1室温(25 ℃)、图2(70 ℃)所示。
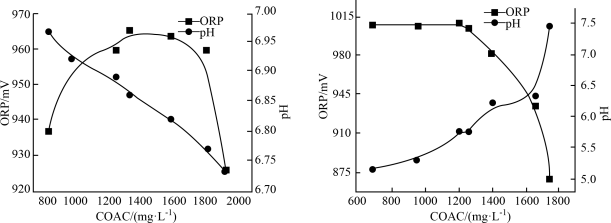
图1 图2
①由图1可知,随着少量乙酸的滴入,Ca(ClO)2溶液的pH在②Ca(ClO)2溶液用于消毒时适宜的条件:温度为
A. 25 ℃ B. 70 ℃ C. 5.75 D. 6.85
(2)某小组探究70 ℃时,pH及稳定剂对NaClO溶液有效氯含量的影响。甲同学设计实验方案如下:
| 序号 | 硅酸钠的质量分数 | 碳酸钠的质量分数 | 初始COAC | pH | 12 h后COAC | 12 h后COAC/初始COAC |
| 1 | 0 | 0 | 1 794 | 8.53 | 1 218 | 0.679 |
| 2 | 0 | 0 | 1 794 | 8.63 | 1 288 | 0.718 |
| 3 | 0.9% | 0.6% | 1 794 | 13.44 | 1 676 | 0.935 |
| 4 | 1.5% | 0 | 1 834 | 13.76 | 1 597 | 0.871 |
| 5 | 0 | 1.5% | 1 834 | 13.66 | - | a |
②实验5中的a
③根据实验3~5,可得出的结论是
④下列物质中最适宜作为NaClO溶液稳定剂的是
A. MgCl2 B. NaCl C. Na2S D. CH3COONa
资料:ⅰ.Mn2+在一定条件下被ClO-氧化成MnO2(棕黑色)、
 (绿色)、
(绿色)、 (紫色)。
(紫色)。ⅱ.浓碱条件下,
 可被OH-还原为
可被OH-还原为 。
。ⅲ.NaClO的氧化性随碱性增强而减弱。
实验记录如下:
| 序号 | Cl2的吸收液 | C中实验现象 | |
| 通入Cl2前 | 通入Cl2后 | ||
| Ⅰ | 10mL水+5滴0.1mol/L MnSO4溶液 | 得到无色溶液 | 产生棕黑色沉淀,且放置后不发生变化 |
| Ⅱ | 10mL5% NaOH溶液+5滴0.1mol/L MnSO4溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
| Ⅲ | 10mL40% NaOH溶液+5滴0.1mol/L MnSO4溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
(3)根据资料ⅱ,Ⅲ中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的原因。
原因一:可能是通入Cl2导致溶液的碱性减弱。
原因二:可能是氧化剂过量,氧化剂将
 氧化为
氧化为 。
。①离子方程式表示可能导致溶液碱性减弱的原因:
②取Ⅲ中放置后的1 mL悬浊液,加入4 mL 40% NaOH溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶液紫色变为绿色的离子方程式为
③从反应速率的角度,分析实验Ⅲ未得到绿色溶液的可能原因:
您最近一年使用:0次