解题方法
1 . 铝、铁是常见的两种金属,它们的单质及化合物在生活生产中处处可见。
(1)过量的铁和稀硝酸发生反应,产物是Fe(NO3)2和NO,写出该反应的化学方程式___________ 。
(2)实验室配制FeSO4溶液时,如果没有隔绝空气,FeSO4会被氧化为_______ (填写化学式)。在该溶液中加入___________ 试剂,看到_____________________ 现象,证明溶液变质。
(3)KAl(SO4)2·12H2O俗称明矾,常用作净水剂,请述其原因并写出有关的离子方程式____________________ 。
(4)已知Ba(AlO2)2可溶于水,下图表示的是向Al2(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系。

由图可知c点的沉淀是________ (填化学式),已知a-b时存在的沉淀是Al(OH)3和BaSO4,两者的物质的量:________ 比________ 多。
(1)过量的铁和稀硝酸发生反应,产物是Fe(NO3)2和NO,写出该反应的化学方程式
(2)实验室配制FeSO4溶液时,如果没有隔绝空气,FeSO4会被氧化为
(3)KAl(SO4)2·12H2O俗称明矾,常用作净水剂,请述其原因并写出有关的离子方程式
(4)已知Ba(AlO2)2可溶于水,下图表示的是向Al2(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系。

由图可知c点的沉淀是
您最近一年使用:0次
2 . 早在1000多年前,我国就已采用加热胆矾(CuSO4∙5H2O)的方法制取硫酸。某同学设计实验加热胆矾获取硫酸。称取样品37.50 g,经完全分解后,得硫酸溶液、Cu2O、CuO、SO2、O2。经分析:气体产物的质量为2.88 g;残留的固体产物质量为11.52 g。
已知: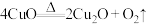 。计算:
。计算:
(1)固体产物中的m(Cu2O)=___________ g。
(2)生成的n(H2SO4)=___________ mol。(写出计算过程)
已知:
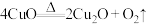 。计算:
。计算:(1)固体产物中的m(Cu2O)=
(2)生成的n(H2SO4)=
您最近一年使用:0次
2022-03-26更新
|
606次组卷
|
4卷引用:浙江省温州市2022届高三高考适应性测试(二模)化学试题
浙江省温州市2022届高三高考适应性测试(二模)化学试题(已下线)化学-2022年高考押题预测卷03(浙江卷)浙江省温州市2022届高三选考二模化学试题浙江省宁波市咸祥中学2021-2022学年高一下学期期末考试化学试题
3 . 某同学设计实验确定CaC2O4•xH2O的结晶水数目。称取样品9.84g,经热分解测得气体产物中有CO、CO2、H2O,其中H2O的质量为2.16g;残留的固体产物是CaO和CaCO3的混合物,质量为5.34g。计算:
(1)x=____ (写出计算过程)。
(2)n(CO)=____ mol。
(1)x=
(2)n(CO)=
您最近一年使用:0次
解题方法
4 . 镁及其化合物在工业上有广泛的应用。
完成下列计算:
(1)称取某镁铝合金10g,放入100mL3mol/L的NaOH溶液中,完全反应收集到6.72L的H2(标准状况)。该合金中镁的质量分数为___ 。
(2)将镁条在空气中燃烧后的产物溶解在50mL1.6mol/L的盐酸中恰好完全反应,再加入过量NaOH把NH3全部蒸发出来,经测定NH3为0.102g,则镁条在空气中燃烧的产物及质量为___ 。
(3)Mg(HCO3)2溶液加热分解,得到产品轻质碳酸镁。18.2g轻质碳酸镁样品经高温完全分解后得8.0g氧化镁固体,放出3.36L二氧化碳(标准状况),求轻质碳酸镁的化学式___ 。
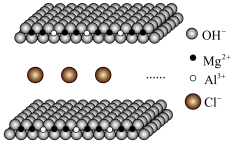
(4)氯离子插层的镁铝水滑石(Mg-Al-ClLDHs)是一种新型的阴离子交换材料。其结构示意图如图所示(每一层可视作平面无限延伸结构)。该离子交换原理是将插层离子与其它阴离子进行等电荷交换。取镁铝水滑石10.66g与0.02molNa2CO3发生完全交换,产物在高温下完全分解,得到金属氧化物和气体。将金属氧化物加入稀硝酸完全溶解后,再加入NaOH溶液直至过量,最终得到4.64g白色沉淀。求Mg-Al-ClLDHs的化学式___ 。
完成下列计算:
(1)称取某镁铝合金10g,放入100mL3mol/L的NaOH溶液中,完全反应收集到6.72L的H2(标准状况)。该合金中镁的质量分数为
(2)将镁条在空气中燃烧后的产物溶解在50mL1.6mol/L的盐酸中恰好完全反应,再加入过量NaOH把NH3全部蒸发出来,经测定NH3为0.102g,则镁条在空气中燃烧的产物及质量为
(3)Mg(HCO3)2溶液加热分解,得到产品轻质碳酸镁。18.2g轻质碳酸镁样品经高温完全分解后得8.0g氧化镁固体,放出3.36L二氧化碳(标准状况),求轻质碳酸镁的化学式
(4)氯离子插层的镁铝水滑石(Mg-Al-ClLDHs)是一种新型的阴离子交换材料。其结构示意图如图所示(每一层可视作平面无限延伸结构)。该离子交换原理是将插层离子与其它阴离子进行等电荷交换。取镁铝水滑石10.66g与0.02molNa2CO3发生完全交换,产物在高温下完全分解,得到金属氧化物和气体。将金属氧化物加入稀硝酸完全溶解后,再加入NaOH溶液直至过量,最终得到4.64g白色沉淀。求Mg-Al-ClLDHs的化学式

您最近一年使用:0次
名校
解题方法
5 . 硫的含氧钠盐有许多,现有Na2SO3、Na2S2O3、Na2S2O4(连二亚硫酸钠),其热稳定性比相应的酸强。
已知:2Na2S2O4 =Na2S2O3+Na2SO3+SO2↑
4H++ 2S2O42- = 3SO2↑+ S↓ + 2H2O
完成下列计算:
(1)用Na2S2O3溶液与不同浓度的硫酸反应,可以研究浓度对化学反应速率的影响。现有98%的浓硫酸(密度为1.84g·cm-3)来配制500mL1mol·L(密度为1.06g·cm-3)的稀硫酸,则需要浓硫酸___________ mL;加水_______ g;
(2)称取部分氧化的亚硫酸钠样品10.16克溶于水,加入稍过量的盐酸酸化了的氯化钡溶液,过滤,洗涤,干燥,所得沉淀质量为2.33克,则该亚硫酸钠中已有_______ %(质量分数)的亚硫酸钠被氧化。
(3)现有8.70g的无水Na2S2O4,吸水后得到10.50g Na2S2O4·nH2O,则水合物中n的值是______ ;
(4)Na2S2O4在500℃时部分分解得产物A,将9.16g产物A中加入足量的稀硫酸中,生成SO21.568L(标准状况),试确定残留物中钠、硫和氧的原子个数比_______ ;若取另一份Na2S2O4部分分解得到的产物B,则ag产物B中钠、硫和氧的原子个数比为__________ (范围)。
已知:2Na2S2O4 =Na2S2O3+Na2SO3+SO2↑
4H++ 2S2O42- = 3SO2↑+ S↓ + 2H2O
完成下列计算:
(1)用Na2S2O3溶液与不同浓度的硫酸反应,可以研究浓度对化学反应速率的影响。现有98%的浓硫酸(密度为1.84g·cm-3)来配制500mL1mol·L(密度为1.06g·cm-3)的稀硫酸,则需要浓硫酸
(2)称取部分氧化的亚硫酸钠样品10.16克溶于水,加入稍过量的盐酸酸化了的氯化钡溶液,过滤,洗涤,干燥,所得沉淀质量为2.33克,则该亚硫酸钠中已有
(3)现有8.70g的无水Na2S2O4,吸水后得到10.50g Na2S2O4·nH2O,则水合物中n的值是
(4)Na2S2O4在500℃时部分分解得产物A,将9.16g产物A中加入足量的稀硫酸中,生成SO21.568L(标准状况),试确定残留物中钠、硫和氧的原子个数比
您最近一年使用:0次
2013·上海奉贤·二模
6 . 硫化钠是用于皮革鞣制的重要化学试剂,可用无水芒硝(Na2SO4)与炭粉在高温下反应而制得,反应方程式如下:Na2SO4+4C Na2S+4CO Na2SO4+4CO
Na2S+4CO Na2SO4+4CO Na2S+4CO2
Na2S+4CO2
(1)现要制取Na2S11.70 g,若生成过程中无水芒硝的利用率为90%,则理论上需要无水芒硝_________ g(精确到0.01)。
(2)若在反应过程中生成的Na2S物质的量为3 mol,则消耗的碳单质的物质的量 n的范围是______ mol≤n≤_____ mol。若产生的气体最终只有CO2,则消耗的碳的物质的量为________ mol;若生成等物质的量CO和CO2,则消耗的碳的物质的量为________ mol;
(3)若在上述反应中消耗的碳单质为1 mol,生成 Na2S的物质的量为y mol,生成的CO和 CO2的物质的量之比为x,则x与y的关系为y=_________ 。
(4)Na2S放置在空气中,会被缓慢氧化成Na2SO4及Na2SO3,现称取已经部分氧化的硫化钠样品78.40 g溶于水中,加入足量盐酸,充分反应后过滤得沉淀19.20 g,放出H2S气体2.24 L(标准状况)。请计算:78.40 g样品中各氧化产物的物质的量_________ (写出必要的计算过程)。
 Na2S+4CO Na2SO4+4CO
Na2S+4CO Na2SO4+4CO Na2S+4CO2
Na2S+4CO2(1)现要制取Na2S11.70 g,若生成过程中无水芒硝的利用率为90%,则理论上需要无水芒硝
(2)若在反应过程中生成的Na2S物质的量为3 mol,则消耗的碳单质的物质的量 n的范围是
(3)若在上述反应中消耗的碳单质为1 mol,生成 Na2S的物质的量为y mol,生成的CO和 CO2的物质的量之比为x,则x与y的关系为y=
(4)Na2S放置在空气中,会被缓慢氧化成Na2SO4及Na2SO3,现称取已经部分氧化的硫化钠样品78.40 g溶于水中,加入足量盐酸,充分反应后过滤得沉淀19.20 g,放出H2S气体2.24 L(标准状况)。请计算:78.40 g样品中各氧化产物的物质的量
您最近一年使用:0次
7 . 硫化钠是用于皮革鞣制的重要化学试剂,可用无水芒硝(Na2SO4)与炭粉在高温下反应而制得,反应方程式如下:Na2SO4+4C →Na2S+ 4CO,Na2SO4+4CO→Na2S+4CO2
(1)现有无水芒硝17.75g,若生成过程中无水芒硝的利用率为80%,则理论上可得到Na2S_____ g,最多生成标况下的CO_____ L。
(2)若在反应过程中生成的Na2S3mol,则消耗的碳单质的物质的量 n的范围是____ mol≤n≤___ mol,若生成等物质的量CO和CO2,则消耗的碳的物质的量为____ mol。
(3)Na2S放置在空气中,会被缓慢氧化成Na2SO4及 Na2SO3,现称取已经部分氧化的硫化钠样品78.40g溶于水中,加入足量盐酸,充分反应后过滤得沉淀19.20g,放出H2S气体2.24L(标准状况)。请计算:78.40g样品中各氧化产物的物质的量(写出必要的计算过程)。_____
(1)现有无水芒硝17.75g,若生成过程中无水芒硝的利用率为80%,则理论上可得到Na2S
(2)若在反应过程中生成的Na2S3mol,则消耗的碳单质的物质的量 n的范围是
(3)Na2S放置在空气中,会被缓慢氧化成Na2SO4及 Na2SO3,现称取已经部分氧化的硫化钠样品78.40g溶于水中,加入足量盐酸,充分反应后过滤得沉淀19.20g,放出H2S气体2.24L(标准状况)。请计算:78.40g样品中各氧化产物的物质的量(写出必要的计算过程)。
您最近一年使用:0次
2014·上海松江·三模
解题方法
8 . 有三份不同质量的硫化铜与硫化亚铜的混合物样品①②③。甲、乙、丙三同学各取一种样品,加强热充分反应,测定各样品中硫化铜的量。
(1)甲取2.56克样品①,置于空气中加强热,产物为氧化铜和二氧化硫。若产生0.448 L气体(标准状况),该气体被30 mL一定浓度氢氧化钠恰好完全吸收,将所得溶液小心低温蒸干得固体2.3克。则样品①中硫化铜的质量为_____ g,氢氧化钠浓度_______ mol·L-1;
(2)乙取3.52克样品②,投入过量的浓硝酸中加热,充分反应后,样品全部参与反应,溶液失重8.44克。样品②中硫化铜的物质的量为____ mol;若浓硝酸的浓度为14.2 mol·L-1,则反应消耗浓硝酸____ mL。(已知:Cu2S+14HNO3→2Cu(NO3)2+10NO2↑+H2SO4+6H2O)
(3)丙称量样品③强热后剩余的固体质量比原样品减小了a g,若该固体为氧化铜,则样品③中硫化铜物质的量(n)为_________ mol。若要计算硫化亚铜的质量,则缺少_____________ 数据,若设该数据为b克,则硫化亚铜的质量为___________ 。
(1)甲取2.56克样品①,置于空气中加强热,产物为氧化铜和二氧化硫。若产生0.448 L气体(标准状况),该气体被30 mL一定浓度氢氧化钠恰好完全吸收,将所得溶液小心低温蒸干得固体2.3克。则样品①中硫化铜的质量为
(2)乙取3.52克样品②,投入过量的浓硝酸中加热,充分反应后,样品全部参与反应,溶液失重8.44克。样品②中硫化铜的物质的量为
(3)丙称量样品③强热后剩余的固体质量比原样品减小了a g,若该固体为氧化铜,则样品③中硫化铜物质的量(n)为
您最近一年使用:0次
9 . 蛋氨酸铜[Cux(Met)y,Met表示蛋氨酸根离子]是一种新型饲料添加剂。为确定蛋氨酸铜[Cux(Met)y]的组成,进行如下实验:
(1)称取一定质量的样品于锥形瓶中,加入适量的蒸馏水和稀盐酸,加热至全部溶解,冷却后将溶液分成两等份。
②取其中一份溶液,调节溶液pH在6~8之间。加入0.1000 mol/LI2的标准溶液25.00 mL,充分反应后滴入2~3滴指示剂X,用0.1000 mol/LNa2S2O3标准溶液滴定至蓝色恰好褪去,发生反应: 。消耗Na2S2O3标准溶液22.00 mL(蛋氨酸与I2反应时物质的量之比为1:1,产物不与Na2S2O3发生反应)。
。消耗Na2S2O3标准溶液22.00 mL(蛋氨酸与I2反应时物质的量之比为1:1,产物不与Na2S2O3发生反应)。
③向另一份溶液中加入NH3·H2O-NH4Cl缓冲溶液,加热至70℃左右,滴入2-3滴指示剂PAN,用0.02500 mol/LEDTA (Na2H2Y)标准溶液滴定其中Cu2+(离子方程式为Cu2++H2Y2--=CuY2-+2H+),消耗EDTA标准溶液28.00 mL。
(1)指示剂X为____ 。
(2)用Na2S2O3标准液滴定时,若pH过小,会有S和SO2生成。写出S2O32-与H+反应的离子方程式___________ 。
(3)若滴定管水洗后未用EDTA标准溶液润洗,测得Cu2+的物质的量将____ (填“偏大”、“偏小”或“不变”)。
(4)通过计算确定蛋氨酸铜[Cux(Met)y]的化学式(写出计算过程)________ 。
(1)称取一定质量的样品于锥形瓶中,加入适量的蒸馏水和稀盐酸,加热至全部溶解,冷却后将溶液分成两等份。
②取其中一份溶液,调节溶液pH在6~8之间。加入0.1000 mol/LI2的标准溶液25.00 mL,充分反应后滴入2~3滴指示剂X,用0.1000 mol/LNa2S2O3标准溶液滴定至蓝色恰好褪去,发生反应:
 。消耗Na2S2O3标准溶液22.00 mL(蛋氨酸与I2反应时物质的量之比为1:1,产物不与Na2S2O3发生反应)。
。消耗Na2S2O3标准溶液22.00 mL(蛋氨酸与I2反应时物质的量之比为1:1,产物不与Na2S2O3发生反应)。③向另一份溶液中加入NH3·H2O-NH4Cl缓冲溶液,加热至70℃左右,滴入2-3滴指示剂PAN,用0.02500 mol/LEDTA (Na2H2Y)标准溶液滴定其中Cu2+(离子方程式为Cu2++H2Y2--=CuY2-+2H+),消耗EDTA标准溶液28.00 mL。
(1)指示剂X为
(2)用Na2S2O3标准液滴定时,若pH过小,会有S和SO2生成。写出S2O32-与H+反应的离子方程式
(3)若滴定管水洗后未用EDTA标准溶液润洗,测得Cu2+的物质的量将
(4)通过计算确定蛋氨酸铜[Cux(Met)y]的化学式(写出计算过程)
您最近一年使用:0次
2020-04-04更新
|
304次组卷
|
2卷引用:江苏省七市(南通、泰州、扬州、徐州、淮安、连云港、宿迁)2020届高三第二次调研考试化学试题
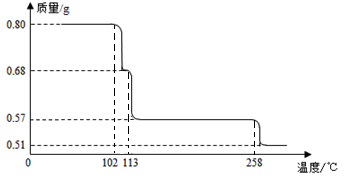
10 . 0.80gCuSO4•5H2O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如下图所示。
请回答下列问题:
(1)试确定200℃时固体物质的化学式______________ (要求写出推断过程);
(2)取270℃所得样品,于570℃灼烧得到的主要产物是黑色粉末和一种氧化性气体,该反应的化学方程式为______________ 。把该黑色粉末溶解于稀硫酸中,经浓缩、冷却,有晶体析出,该晶体的化学式为_________ ,其存在的最高温度是_____________ ;
(3)上述氧化性气体与水反应生成一种化合物,该化合物的浓溶液与Cu在加热时发生反应的化学方程式为________________ ;
(4)在0.10mol·L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=________________ mol·L-1(Ksp[Cu(OH)2]=2.2×10-20)。若在0.1mol·L-1硫酸铜溶液中通入过量H2S气体,使Cu2+完全沉淀为CuS,此时溶液中的H+浓度是_______________ mol·L-1。

请回答下列问题:
(1)试确定200℃时固体物质的化学式
(2)取270℃所得样品,于570℃灼烧得到的主要产物是黑色粉末和一种氧化性气体,该反应的化学方程式为
(3)上述氧化性气体与水反应生成一种化合物,该化合物的浓溶液与Cu在加热时发生反应的化学方程式为
(4)在0.10mol·L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=
您最近一年使用:0次
2019-01-30更新
|
1964次组卷
|
5卷引用:2014陕西省西安铁一中、铁一中国际校高三下一模化学试卷
(已下线)2014陕西省西安铁一中、铁一中国际校高三下一模化学试卷2011年普通高等学校招生全国统一考试化学卷(新课标)(已下线)2012届陕西省兴平市秦岭中学高三上学期期末练习化学试卷2017届广东省华侨中学高三上学期摸底考试理综化学试卷黑龙江嫩江市高级中学2021届高三上学期第二次月考化学试题



