1 .  具有氧化性、还原性和漂白性,某同学在实验室利用
具有氧化性、还原性和漂白性,某同学在实验室利用 做相关验证和探究实验。回答下列问题:
做相关验证和探究实验。回答下列问题:
(1)用如图1装置(夹持仪器已省略)验证 具有氧化性。
具有氧化性。 的名称为
的名称为___________ 。
②装置甲试管中反应的离子方程式为___________ 。
③说明 具有氧化性的现象为
具有氧化性的现象为___________ 。
(2)该同学设计如图2所示装置(夹持仪器已省略)制备 (难溶解于水中)。
(难溶解于水中)。 的作用是
的作用是___________ 。
②三颈烧瓶中反应的化学方程式为___________ 。
(3)该实验体现了 的性质是
的性质是___________ 。
(4)实验表明,将纯净的 缓缓地通入到
缓缓地通入到 溶液中,得到
溶液中,得到 沉淀。为了探究该反应中的氧化剂,该同学提出以下假设:
沉淀。为了探究该反应中的氧化剂,该同学提出以下假设:
假设Ⅰ:溶液中的 ;
;
假设Ⅱ:溶解在水中的氧气。
①验证假设Ⅰ(配制溶液前已将蒸馏水煮沸并密封冷却)。
实验i现象为___________ ,实验ii的现象为___________ 。
②验证假设Ⅱ。请完成下列表格:
实验iv的步骤为___________ ,实验目的是___________ 。
 具有氧化性、还原性和漂白性,某同学在实验室利用
具有氧化性、还原性和漂白性,某同学在实验室利用 做相关验证和探究实验。回答下列问题:
做相关验证和探究实验。回答下列问题:(1)用如图1装置(夹持仪器已省略)验证
 具有氧化性。
具有氧化性。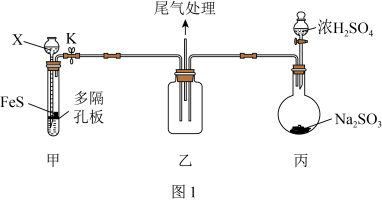
 的名称为
的名称为②装置甲试管中反应的离子方程式为
③说明
 具有氧化性的现象为
具有氧化性的现象为(2)该同学设计如图2所示装置(夹持仪器已省略)制备
 (难溶解于水中)。
(难溶解于水中)。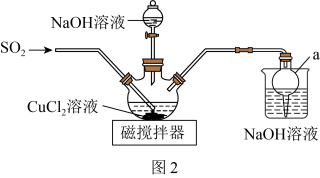
 的作用是
的作用是②三颈烧瓶中反应的化学方程式为
(3)该实验体现了
 的性质是
的性质是(4)实验表明,将纯净的
 缓缓地通入到
缓缓地通入到 溶液中,得到
溶液中,得到 沉淀。为了探究该反应中的氧化剂,该同学提出以下假设:
沉淀。为了探究该反应中的氧化剂,该同学提出以下假设:假设Ⅰ:溶液中的
 ;
;假设Ⅱ:溶解在水中的氧气。
①验证假设Ⅰ(配制溶液前已将蒸馏水煮沸并密封冷却)。
| 实验步骤 | 实验操作 | 实验现象 | 结论 |
实验 | 向 溶液中缓慢通入纯净的 溶液中缓慢通入纯净的 气体 气体 | 假设I成立 | |
实验 | 向 溶液的烧杯中缓慢通入纯净的 溶液的烧杯中缓慢通入纯净的 气体 气体 |
②验证假设Ⅱ。请完成下列表格:
| 实验步骤 | 实验现象 | 实验目的 | |
| 实验iii | 同实验 步骤 步骤 | 同实验 的相关现象 的相关现象 | 作对照实验 |
| 实验iv | 产生白色沉淀 | ||
您最近一年使用:0次
2024-02-23更新
|
669次组卷
|
8卷引用:专题03 常见气体的实验室制取(考题猜想)(6大题型)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)
(已下线)专题03 常见气体的实验室制取(考题猜想)(6大题型)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)四川省绵阳中学2023-2024学年高三下学期2月开学考理科综合-高中化学(已下线)大题02 化学实验综合题(分类过关)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)2024届内蒙古自治区乌海市第六中学高三下学期第三次模拟考试理综试题-高中化学河南省郑州市第五高级中学2023-2024学年高三2月开学考理综试题-高中化学四川省广元市川师大万达中学2023-2024学年高一下学期3月月考化学试题黑龙江省牡丹江市第一高级中学2023-2024学年高一下学期5月期中考试化学试题江西省部分学校2023-2024学年高三上学期2月月考化学试题
名校
解题方法
2 . 科学探究要实事求是、严谨细致。某化学兴趣小组设计实验进行有关氯化物的探究实验,回答下列问题:
I.制备FeCl2。装置如图所示(夹持装置省略),已知FeCl3极易水解。

(1)仪器a的名称是______________ 。
(2)装置II中制备FeCl2的化学方程式为__________________________________________ 。
(3)该装置存在的缺陷是:①__________________________________ ;②缺少氢气的尾气处理装置。
II.利用惰性电极电解0.1 mol•L-1FeCl2溶液,探究外界条件对电极反应(离子放电顺序)的影响。
(4)实验数据如表所示:
①由实验1、2现象可以得出结论:增大电压,________ 优先于________ 放电;
②若由实验1、4现象可以得出结论:_________________________________________________ 。
II.为了探究外界条件对氯化铵水解平衡的影响,兴趣小组设计了如下实验方案:
(5)该实验限选药品和仪器:恒温水浴、pH传感器、烧杯、0.1mol.L-1硝酸银溶液、蒸馏水和各种浓度的NH4Cl溶液。
①实验中,“待测物理量”是________________ ;
②实验目的ii是_________________ ;
③上述表格中,b____ d(填“>”、“<”或“=”)。
I.制备FeCl2。装置如图所示(夹持装置省略),已知FeCl3极易水解。

(1)仪器a的名称是
(2)装置II中制备FeCl2的化学方程式为
(3)该装置存在的缺陷是:①
II.利用惰性电极电解0.1 mol•L-1FeCl2溶液,探究外界条件对电极反应(离子放电顺序)的影响。
(4)实验数据如表所示:
实验编号 | 电压/V | pH | 阳极现象 | 阴极现象 |
1 | 1.5 | 5.52 | 无气泡,滴加KSCN显红色 | 无气泡,银白色金属析出 |
2 | 3.0 | 5.52 | 少量气泡,滴加KSCN显红色 | 无气泡,银白色金属析出 |
3 | 4.5 | 5.52 | 大量气泡,滴加KSCN显红色 | 较多气泡,极少量金属析出 |
4 | 1.5 | 1.00 | 无气泡,滴加KSCN显红色 | 较多气泡,极少量金属析出 |
②若由实验1、4现象可以得出结论:
II.为了探究外界条件对氯化铵水解平衡的影响,兴趣小组设计了如下实验方案:
实验编号 | c(NH4Cl)/mol·L-1 | 温度/℃ | 待测物理量 | 实验目的 |
5 | 0.5 | 30 | a | —— |
6 | 1.5 | i | b | 探究浓度对氯化铵水解平衡的影响 |
7 | 0.5 | 35 | c | ii |
8 | 2.0 | 40 | d | 探究温度、浓度同时对氯化铵水解平衡的影响 |
①实验中,“待测物理量”是
②实验目的ii是
③上述表格中,b
您最近一年使用:0次
名校
解题方法
3 . 某化学兴趣小组为探究Cl2的性质并制备氯水,用如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
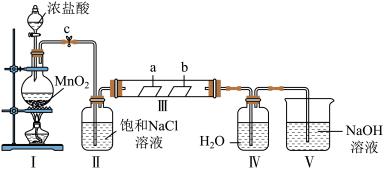
回答下列问题:
(1)加入药品前,必须先___________ 。
(2)装置Ⅰ中发生反应的化学方程式为___________ 。
(3)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为应在___________ 和___________ (填装置序号)之间添加洗气装置,该装置的作用是___________ 。
(4)装置Ⅴ中NaOH溶液的作用是___________ ,相关反应的化学方程式为___________ 。
(5)反应完毕,为探究装置Ⅳ中溶质的成分,需要的试剂主要有___________ 。

回答下列问题:
(1)加入药品前,必须先
(2)装置Ⅰ中发生反应的化学方程式为
(3)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为应在
(4)装置Ⅴ中NaOH溶液的作用是
(5)反应完毕,为探究装置Ⅳ中溶质的成分,需要的试剂主要有
您最近一年使用:0次
22-23高二下·全国·课时练习
解题方法
4 . 实验室可用酒精、浓硫酸作试剂来制取乙烯,但实验表明,还有许多副反应发生,如反应中会生成SO2、CO2、水蒸气等无机物。某研究性学习小组欲用如图所示的装置制备纯净的乙烯并探究乙烯与单质溴能否反应及反应类型。回答下列问题:
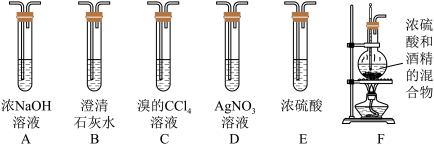
(1)实验中,混合浓硫酸与乙醇的方法是将_______ 慢慢加入另一种物质中;加热F装置时必须使液体温度_______ 。
(2)写出浓硫酸与酒精直接反应生成上述无机副产物的化学方程式:_______ 。
(3)为实现上述实验目的,装置的连接顺序为F→_______ →D(各装置限用一次)。
(4)当C中观察到_______ 时,表明单质溴能与乙烯反应;当D中_______ 时,表明C中发生的是取代反应;若D中没有出现前面所描述的现象时,表明C中发生的是_______ 反应。
(5)关于浓硫酸和乙醇混合加热制取乙烯的实验装置F中,下列说法正确的个数有_______ 个。
①浓硫酸的作用是作催化剂
②在反应容器中放入几片碎瓷片防止混合液暴沸
③圆底烧瓶中装的是乙醇和3mol·L-1H2SO4的混合液
④温度计应插入反应溶液液面下,以便控制温度
⑤若出口出来的气体能使酸性KMnO4溶液褪色,说明有乙烯生成
⑥反应过程中溶液的颜色会逐渐变黑
⑦生成的乙烯气体中混有带刺激性气味的气体

(1)实验中,混合浓硫酸与乙醇的方法是将
(2)写出浓硫酸与酒精直接反应生成上述无机副产物的化学方程式:
(3)为实现上述实验目的,装置的连接顺序为F→
(4)当C中观察到
(5)关于浓硫酸和乙醇混合加热制取乙烯的实验装置F中,下列说法正确的个数有
①浓硫酸的作用是作催化剂
②在反应容器中放入几片碎瓷片防止混合液暴沸
③圆底烧瓶中装的是乙醇和3mol·L-1H2SO4的混合液
④温度计应插入反应溶液液面下,以便控制温度
⑤若出口出来的气体能使酸性KMnO4溶液褪色,说明有乙烯生成
⑥反应过程中溶液的颜色会逐渐变黑
⑦生成的乙烯气体中混有带刺激性气味的气体
您最近一年使用:0次
名校
解题方法
5 . 某校化学兴趣小组为研究Cl2的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
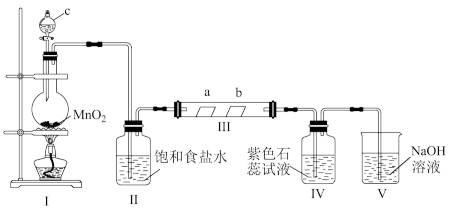
(1)装置Ⅰ中仪器c的名称是___ ,实验室以二氧化锰和浓盐酸制备氯气的化学方程式为___ 。
(2)装置Ⅱ的作用是___
(3)若产生Cl2足量,实验过程中装置Ⅳ中的实验现象___ 。
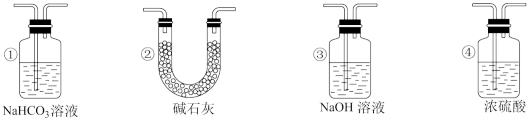
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的___ 装置(填序号)。
(5)有一种“地康法”制取氯气的反应原理如图所示:
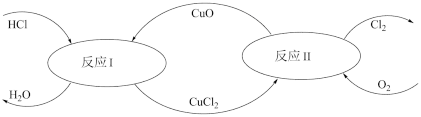
①反应Ⅰ属于___ 反应。(填四种基本反应类型之一)
②在450℃条件下,反应Ⅱ的化学方程式为____ 。
③工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟生成(为NH4Cl固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:___ 。

(1)装置Ⅰ中仪器c的名称是
(2)装置Ⅱ的作用是
(3)若产生Cl2足量,实验过程中装置Ⅳ中的实验现象
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的

(5)有一种“地康法”制取氯气的反应原理如图所示:

①反应Ⅰ属于
②在450℃条件下,反应Ⅱ的化学方程式为
③工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟生成(为NH4Cl固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:
您最近一年使用:0次
2021-09-24更新
|
796次组卷
|
6卷引用:辽宁省营口市第二高级中学2021-2022学年高三上学期第一次月考化学试题
辽宁省营口市第二高级中学2021-2022学年高三上学期第一次月考化学试题(已下线)必考点09 氯气的制取 氯离子的检验-【对点变式题】2021-2022学年高一化学上学期期中期末必考题精准练(人教版2019)(已下线)衔接点16 氯气的性质-2022年初升高化学无忧衔接?陕西省榆林市府谷县第一中学2023-2024学年高一上学期12月月考化学试题福建省泉州市第五中学2020-2021学年高一上学期期中考化学试题广东省佛山市第一中学2021-2022学年高一上学期期中考试化学试题
解题方法
6 . 某化学小组对铁及其化合物的性质、制备进行如下探究。请按要求回答下列问题。
(一) 与
与 性质探究。供选试剂:
性质探究。供选试剂: 溶液、
溶液、 溶液、
溶液、 片、
片、 粉、
粉、 溶液
溶液
(1)同学甲探究铁具有还原性,可选择试剂: 粉、
粉、 溶液、
溶液、_______ 。
(2)同学乙为探究 的还原性,取2 mL
的还原性,取2 mL  溶液,向其中滴加少量氯水,观察现象不太明显,其原因可能是
溶液,向其中滴加少量氯水,观察现象不太明显,其原因可能是_______ ;欲获得更充分证据,此实验操作应该完善为_______ 。
(3)同学丙欲探究 具有氧化性,其方案涉及反应的离子方程式为
具有氧化性,其方案涉及反应的离子方程式为_______ 。
(二) 的制备同学丁设计如图所示装置,气密性已查完好。
的制备同学丁设计如图所示装置,气密性已查完好。
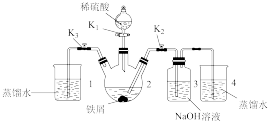
(4)为达到实验目的,需进行的操作:先打开 ,关闭
,关闭 ,打开
,打开 ,反应片刻后,再
,反应片刻后,再_______ ,_______ ,发现溶液从装置2进入装置3中,关闭 。
。
(5)从实验操作过程分析装置3中有灰绿色沉淀产生而没有产生白色沉淀的原因:_______ 。
(三)出土铁器修复部分过程的分析与探究
(6)腐蚀原理分析:一般认为,铁经过了如下腐蚀循环:Ⅰ. 转化为
转化为 ;Ⅱ.
;Ⅱ. 在自然环境中形成
在自然环境中形成 ;Ⅲ.
;Ⅲ. 和
和 反应形成致密的
反应形成致密的 保护层;Ⅳ.
保护层;Ⅳ. 保护层再转化为
保护层再转化为 。如此往复腐蚀。
。如此往复腐蚀。
①从原子结构解释步骤I很容易发生的原因:_______ 。
②上述过程属于氧化还原反应的步骤为_______ (填序号)。
(7)化学修复过程探究:研究发现, 对铁的腐蚀会造成严重影响,铁器表面会产生
对铁的腐蚀会造成严重影响,铁器表面会产生 。将铁器浸没在盛有
。将铁器浸没在盛有
 、
、
 的溶液的容器中,缓慢加热至60~90℃。一段时间后,取出器物,用
的溶液的容器中,缓慢加热至60~90℃。一段时间后,取出器物,用 溶液洗涤,至无
溶液洗涤,至无 。
。
①加热目的是_______ 。
②检测 洗涤干净与否的操作:
洗涤干净与否的操作:_______ 。
③铁器表面的 脱氯生成
脱氯生成 。写出该反应的离子方程式:
。写出该反应的离子方程式:_______ 。
④修复中 变成
变成 。写出该反应的化学方程式:
。写出该反应的化学方程式:_______ 。
(一)
 与
与 性质探究。供选试剂:
性质探究。供选试剂: 溶液、
溶液、 溶液、
溶液、 片、
片、 粉、
粉、 溶液
溶液(1)同学甲探究铁具有还原性,可选择试剂:
 粉、
粉、 溶液、
溶液、(2)同学乙为探究
 的还原性,取2 mL
的还原性,取2 mL  溶液,向其中滴加少量氯水,观察现象不太明显,其原因可能是
溶液,向其中滴加少量氯水,观察现象不太明显,其原因可能是(3)同学丙欲探究
 具有氧化性,其方案涉及反应的离子方程式为
具有氧化性,其方案涉及反应的离子方程式为(二)
 的制备同学丁设计如图所示装置,气密性已查完好。
的制备同学丁设计如图所示装置,气密性已查完好。
(4)为达到实验目的,需进行的操作:先打开
 ,关闭
,关闭 ,打开
,打开 ,反应片刻后,再
,反应片刻后,再 。
。(5)从实验操作过程分析装置3中有灰绿色沉淀产生而没有产生白色沉淀的原因:
(三)出土铁器修复部分过程的分析与探究
(6)腐蚀原理分析:一般认为,铁经过了如下腐蚀循环:Ⅰ.
 转化为
转化为 ;Ⅱ.
;Ⅱ. 在自然环境中形成
在自然环境中形成 ;Ⅲ.
;Ⅲ. 和
和 反应形成致密的
反应形成致密的 保护层;Ⅳ.
保护层;Ⅳ. 保护层再转化为
保护层再转化为 。如此往复腐蚀。
。如此往复腐蚀。①从原子结构解释步骤I很容易发生的原因:
②上述过程属于氧化还原反应的步骤为
(7)化学修复过程探究:研究发现,
 对铁的腐蚀会造成严重影响,铁器表面会产生
对铁的腐蚀会造成严重影响,铁器表面会产生 。将铁器浸没在盛有
。将铁器浸没在盛有
 、
、
 的溶液的容器中,缓慢加热至60~90℃。一段时间后,取出器物,用
的溶液的容器中,缓慢加热至60~90℃。一段时间后,取出器物,用 溶液洗涤,至无
溶液洗涤,至无 。
。①加热目的是
②检测
 洗涤干净与否的操作:
洗涤干净与否的操作:③铁器表面的
 脱氯生成
脱氯生成 。写出该反应的离子方程式:
。写出该反应的离子方程式:④修复中
 变成
变成 。写出该反应的化学方程式:
。写出该反应的化学方程式:
您最近一年使用:0次
解题方法
7 . 某校化学兴趣小组为研究 的性质,设计如图1所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
的性质,设计如图1所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。

(1)实验室用 和浓盐酸制备
和浓盐酸制备 的离子方程式为
的离子方程式为__________________________________ 。
(2)实验过程中装置Ⅳ中的实验现象为__________________________________ 。
(3)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在装置Ⅱ与Ⅲ之间添加如图2中的________ (填序号)装置。
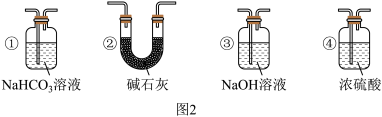
(4)装置Ⅴ的目的是防止尾气污染空气,写出装置Ⅴ中发生反应的离子方程式__________________ 。
 的性质,设计如图1所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
的性质,设计如图1所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
(1)实验室用
 和浓盐酸制备
和浓盐酸制备 的离子方程式为
的离子方程式为(2)实验过程中装置Ⅳ中的实验现象为
(3)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在装置Ⅱ与Ⅲ之间添加如图2中的

(4)装置Ⅴ的目的是防止尾气污染空气,写出装置Ⅴ中发生反应的离子方程式
您最近一年使用:0次
解题方法
8 . 某化学小组拟设计实验探究SO2与钙盐溶液的反应情况。
【文献资料】
①CaSO3是难溶于水、易溶于盐酸的白色固体;
②实验室用Na2SO3粉末和70%硫酸反应制备SO2;
③浓硫酸与水混合时放出大量的热,产生大量“酸雾”。
【设计实验】
实验Ⅰ:探究二氧化硫与氯化钙溶液的反应。
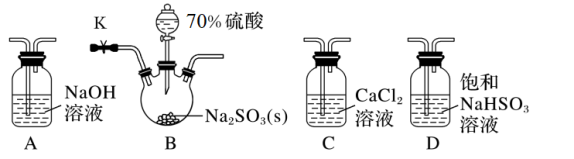
(1)若气体从左至右流动,选择装置并排序为___________ (填字母)。
(2)D装置的作用是___________ (用离子方程式表示)。
(3)连接装置进行实验,发现C装置中产生白色沉淀。
①甲同学对白色沉淀成分提出如下假设:
假设1:白色沉淀是CaSO3;
假设2:白色沉淀是CaSO4;
假设3:白色沉淀是CaSO4和CaSO3。
②乙同学设计实验证明白色沉淀是CaSO4,他的实验方法和现象是___________ 。
③丙同学认为C中生成硫酸钙的原因是装置内O2氧化了SO2。
排除装置内O2干扰采取的措施是:在启动B中反应之前,___________ (填实验步骤),重新实验,C中无明显现象,所以SO2和CaCl2溶液不反应。
实验Ⅱ:探究SO2和Ca(ClO)2溶液的反应。
丁同学仅将上述实验C装置中氯化钙溶液换成漂白精溶液,进行实验时产生了大量白色沉淀。
(4)化学反应有两种情况。
①若SO2过量,则发生的反应为Ca(ClO)2+2SO2+2H2O=CaSO4↓+2HCl+H2SO4;
②若SO2少量,则发生的反应为___________ 。
(5)为了探究C中SO2是否过量,戊同学取少量C中上层清液于试管中,加入下列物质可以达到实验目的的是___________ (填字母)。
a.NaHCO3溶液
b.品红溶液
c.AgNO3溶液
d.紫色石蕊溶液
【文献资料】
①CaSO3是难溶于水、易溶于盐酸的白色固体;
②实验室用Na2SO3粉末和70%硫酸反应制备SO2;
③浓硫酸与水混合时放出大量的热,产生大量“酸雾”。
【设计实验】
实验Ⅰ:探究二氧化硫与氯化钙溶液的反应。

(1)若气体从左至右流动,选择装置并排序为
(2)D装置的作用是
(3)连接装置进行实验,发现C装置中产生白色沉淀。
①甲同学对白色沉淀成分提出如下假设:
假设1:白色沉淀是CaSO3;
假设2:白色沉淀是CaSO4;
假设3:白色沉淀是CaSO4和CaSO3。
②乙同学设计实验证明白色沉淀是CaSO4,他的实验方法和现象是
③丙同学认为C中生成硫酸钙的原因是装置内O2氧化了SO2。
排除装置内O2干扰采取的措施是:在启动B中反应之前,
实验Ⅱ:探究SO2和Ca(ClO)2溶液的反应。
丁同学仅将上述实验C装置中氯化钙溶液换成漂白精溶液,进行实验时产生了大量白色沉淀。
(4)化学反应有两种情况。
①若SO2过量,则发生的反应为Ca(ClO)2+2SO2+2H2O=CaSO4↓+2HCl+H2SO4;
②若SO2少量,则发生的反应为
(5)为了探究C中SO2是否过量,戊同学取少量C中上层清液于试管中,加入下列物质可以达到实验目的的是
a.NaHCO3溶液
b.品红溶液
c.AgNO3溶液
d.紫色石蕊溶液
您最近一年使用:0次
解题方法
9 . 某校化学兴趣小组为研究Cl2的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的有色布条,b为湿润的有色布条。

(1)A装置的名称是______________ ,实验室以二氧化锰和浓盐酸制备氯气的离子方程式是______________ 。
(2)装置Ⅱ的作用是______________ 。
(3)实验过程中,装置Ⅳ中的实验现象为______________ ;发生反应的化学方程式为______________ 。
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在上图装置Ⅱ与Ⅲ之间添加如图中的______________ (填序号)装置。
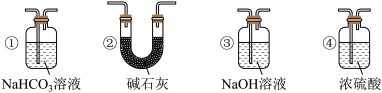
(5)装置Ⅴ的目的是防止尾气污染,写出装置Ⅴ中发生反应的离子方程式:______________ 。

(1)A装置的名称是
(2)装置Ⅱ的作用是
(3)实验过程中,装置Ⅳ中的实验现象为
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在上图装置Ⅱ与Ⅲ之间添加如图中的

(5)装置Ⅴ的目的是防止尾气污染,写出装置Ⅴ中发生反应的离子方程式:
您最近一年使用:0次
10 . 某校化学兴趣小组为研究Cl2的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。

(1)实验室用MnO2和浓盐酸制备Cl2的化学方程式为______________________________________ 。
(2)实验过程中装置Ⅳ中的实验现象为_____________________________________ 。
(3)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在装置Ⅱ与Ⅲ之间添加如图中的_________________ (填序号)装置。
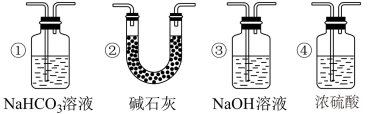
(4)装置V的作用是防止尾气污染空气,写出装置V中发生反应的化学方程式:_________________________________________________________ 。

(1)实验室用MnO2和浓盐酸制备Cl2的化学方程式为
(2)实验过程中装置Ⅳ中的实验现象为
(3)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在装置Ⅱ与Ⅲ之间添加如图中的

(4)装置V的作用是防止尾气污染空气,写出装置V中发生反应的化学方程式:
您最近一年使用:0次



