名校
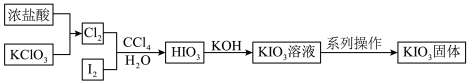
1 . 碘酸钾(KIO3)是重要的食品添加剂,某化学兴趣小组查阅资料得知,HIO3与KIO3均为白色固体,能溶于水,难溶于部分有机溶剂,且KIO3在碱性条件下易被ClO 氧化为KIO4,于是设计了以下路线制备碘酸钾。下列有关说法正确的是
氧化为KIO4,于是设计了以下路线制备碘酸钾。下列有关说法正确的是
 氧化为KIO4,于是设计了以下路线制备碘酸钾。下列有关说法正确的是
氧化为KIO4,于是设计了以下路线制备碘酸钾。下列有关说法正确的是
| A.浓盐酸在反应中体现了氧化性 |
| B.加入CCl4目的是萃取I2 |
| C.加入KOH前,应先对原溶液加热煮沸 |
| D.系列操作包括:加入乙醇溶液、搅拌、静置、过滤、洗涤、干燥 |
您最近一年使用:0次
2020-11-26更新
|
622次组卷
|
2卷引用:江苏省启东市2021届高三上学期期中考试化学试题
名校
2 . 除第一周期外,关于同周期主族元素的下列变化规律的叙述中不正确的是
| A.从左到右,原子半径逐渐减小 |
| B.从左到右,元素原子的氧化性减弱,还原性增强 |
| C.从左到右,元素最高正价数从+1递增到+7,负价由-4递变到-1 |
| D.从左到右,元素最高价氧化物对应水化物碱性减弱,酸性增强 |
您最近一年使用:0次
2018-05-06更新
|
277次组卷
|
6卷引用:【全国百强校】贵州省铜仁市第一中学2017-2018学年高一下学期期中考试化学试题
【全国百强校】贵州省铜仁市第一中学2017-2018学年高一下学期期中考试化学试题黑龙江省绥滨县第一中学2018-2019学年高一(理)下学期期中考试化学试题(已下线)【全国百强校】贵州省思南中学2018-2019学年2018-2019学年高一下学期期中考试化学试题湖南省常德市2019-2020学年高一上学期第一次月考化学试题四川省内江市市中区天立学校2019-2020学年高一下学期第二次月考化学试题贵州省铜仁市思南中学2019-2020学年高一下学期5月月考化学试题
名校
3 . 查阅资料可知:Bi位于周期表的第VA族, 是浅黄色固体;溶液中
是浅黄色固体;溶液中 较稳定呈无色。某实验小组依次进行以下实验操作:
较稳定呈无色。某实验小组依次进行以下实验操作:
①向稀硫酸酸化的 溶液中加入适量
溶液中加入适量 ,溶液变为紫红色。
,溶液变为紫红色。
②继续滴加适量草酸 溶液,溶液紫红色褪去,并有
溶液,溶液紫红色褪去,并有 产生。
产生。
下列说法正确的是
 是浅黄色固体;溶液中
是浅黄色固体;溶液中 较稳定呈无色。某实验小组依次进行以下实验操作:
较稳定呈无色。某实验小组依次进行以下实验操作:①向稀硫酸酸化的
 溶液中加入适量
溶液中加入适量 ,溶液变为紫红色。
,溶液变为紫红色。②继续滴加适量草酸
 溶液,溶液紫红色褪去,并有
溶液,溶液紫红色褪去,并有 产生。
产生。下列说法正确的是
| A.Bi的基态原子中只含一个未成对电子 |
B.由操作①现象可知酸性条件下氧化性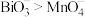 |
C.操作②中每生成标准状况下 ,反应转移1mol电子 ,反应转移1mol电子 |
D.向稀硫酸酸化的 中加入草酸,溶液会变为紫红色 中加入草酸,溶液会变为紫红色 |
您最近一年使用:0次
昨日更新
|
4次组卷
|
2卷引用:江苏省如皋市第一中学 南京市第九中学2023-2024学年高一下学期教学质量调研(二)化学试题
解题方法
4 . ①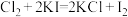 ②
②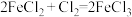 ③
③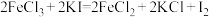 ④
④ ,根据上述化学方程式,下列说法错误的是
,根据上述化学方程式,下列说法错误的是
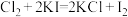 ②
②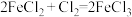 ③
③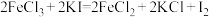 ④
④ ,根据上述化学方程式,下列说法错误的是
,根据上述化学方程式,下列说法错误的是A.氧化性由强到弱的顺序为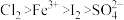 |
B.还原性由强到弱的顺序为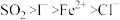 |
C. 气体能使湿润的KI-淀粉试纸变蓝 气体能使湿润的KI-淀粉试纸变蓝 |
| D.预测新制氯水和二氧化硫的水溶液反应后溶液的酸性减弱 |
您最近一年使用:0次
2022-11-01更新
|
146次组卷
|
2卷引用:河北省唐山市十县一中联盟2022-2023学年高一上学期期中考试化学试题
解题方法
5 . 已知还原性:I->Fe2+>Br-,且有下列三个反应:①Cl2(少量)+FeI2=FeCl2+I2②2Fe2++Br2=2Fe3++2Br-③Co2O3+6HCl=2CoCl2+Cl2↑+3H2O。下列说法正确的是
| A.①②③中的氧化产物分别是I2、Fe3+、Cl2 |
| B.根据以上方程式可以得到氧化性Cl2>Fe3+>Co2O3 |
| C.可以推理得到Cl2(少量)+FeBr2=FeCl2+Br2 |
| D.在反应③中HCl体现了酸性和还原性 |
您最近一年使用:0次
2021-12-04更新
|
189次组卷
|
2卷引用:江西省九校2021-2022学年高一上学期期中联考化学试题
名校
6 . 如图是实验室进行二氧化硫制备与性质探究实验的组合装置,部分固定装置未画出。下列有关说法正确的是
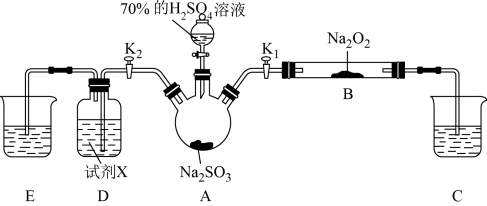

| A.关闭K1,打开K2,试剂X是酸性KMnO4或H2O2溶液,均可证明SO2有还原性 |
| B.关闭K2,打开K1,滴加H2SO4溶液,则装置B中每消耗1.5molNa2O2,转移电子数为3NA |
| C.为防止环境污染,装置C和E中的试剂均取用氢氧化钠溶液 |
| D.实验过程中体现了H2SO4的酸性、难挥发性、强氧化性 |
您最近一年使用:0次
2021-11-03更新
|
324次组卷
|
5卷引用:江西省乐安县第二中学2022-2023学年高一下学期5月期中考试化学试题
名校
7 . 学习硫及其化合物,可运用物质类别和元素价态二维视角模型对硫及其化合物的性质进行推测验证。以下说法中不正确的是


| A.H2S能与a反应生成硫 |
| B.a有还原性,能使酸性KMnO4溶液褪色 |
| C.c能与水剧烈反应生成d |
| D.b的浓溶液具有吸水性、脱水性和强氧化性 |
您最近一年使用:0次
2021-07-11更新
|
505次组卷
|
6卷引用:云南省蒙自市第一高级中学2022-2023学年高一下学期5月期中考试化学试题
名校
解题方法
8 . 下列实验结论不正确 的是
| 实验操作 | 现象 | 结论 | |
| A | 食醋浸泡水垢 | 产生无色气体 | 乙酸的酸性比碳酸强 |
| B | 乙醇与橙色酸性重铬酸钾溶液混合 | 橙色溶液变为绿色 | 乙醇具有还原性 |
| C | 碘酒滴到土豆片上 | 土豆片变蓝 | 淀粉遇碘元素变蓝 |
| D | 新制Cu(OH)2与葡萄糖溶液混合加热 | 产生砖红色沉淀 | 葡萄糖具有氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 下列对浓硫酸的叙述正确的是( )
| A.常温下,浓硫酸与铁、铝不反应,所以铁质、铝质容器能盛放浓硫酸 |
B.浓硫酸具有强氧化性, 、 、 、 、 具有还原性,故浓硫酸不能干燥 具有还原性,故浓硫酸不能干燥 、 、 、 、 |
| C.浓硫酸和铜片加热既表现出酸性,又表现出氧化性 |
D.浓硫酸与亚硫酸钠反应制取 时,浓硫酸表现出酸性 时,浓硫酸表现出酸性 |
您最近一年使用:0次
2020-09-10更新
|
323次组卷
|
9卷引用:安徽省阜阳市第十一中学2019-2020学年高一下学期期中考试化学试题
安徽省阜阳市第十一中学2019-2020学年高一下学期期中考试化学试题贵州省安顺市普定县第一中学2018-2019学年高一上学期12月份考试化学试题【全国百强校】内蒙古自治区杭锦后旗奋斗中学2018-2019学年高一下学期第一次月考化学试题云南省临沧市双江县第一中学2019-2020学年高一上学期12月月考化学试题安徽省六安市第一中学2019-2020学年高一下学期延期开学期间辅导作业专题卷(一)化学试题苏教版(2020)高一必修第一册专题4第一单元课时2 硫酸鲁科版(2019)高一必修第一册第3章 物质的性质与转化 第2节 硫的转化 课时2 硫酸高一必修第二册(人教2019版)第五章 第一节 硫及其化合物 课时2 硫酸及硫酸根离子的检验江苏省盐城市华东师范大学盐城实验中学2020-2021学年高一上学期第二次质量监控化学试题
10 . 如图所示的实验,发现烧杯中酸性KMnO4溶液褪色。若将烧杯中的溶液换成含有少量KSCN的FeSO4溶液,溶液呈血红色。判断下列说法中不正确的是
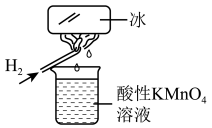

| A.该条件下H2燃烧生成了既具有氧化性又具有还原性的物质 |
| B.该条件下H2燃烧的产物中可能含有一定量的H2O2 |
| C.酸性FeSO4溶液中加入双氧水的离子反应为:Fe2++H2O2+2H+=Fe3++2H2O |
| D.将烧杯中溶液换成KI淀粉溶液也能验证生成物具有还原性 |
您最近一年使用:0次
2020-08-20更新
|
548次组卷
|
11卷引用:福建省南安市侨光中学2020-2021学年高一下学期期中阶段考试化学试题
福建省南安市侨光中学2020-2021学年高一下学期期中阶段考试化学试题2016届河北省衡水中学高三上学期二调化学试卷2016届四川省眉山中学高三上学期10月月考化学试卷2017届福建省柘荣一中、宁德中学高三上联考一化学卷河北省衡水中学2018届高三上学期二调考试化学试题云南省临沧市第一中学2018届高三上学期第七次月考化学试题山东省潍坊市奎文区潍坊中学2019—2020学年高一下学期开学考试化学试题山东省山东师范大学附属中学2019-2020学年高一上学期12月份月考化学试题(已下线)小题必刷08 氧化还原反应的规律及应用——2021年高考化学一轮复习小题必刷(通用版)河南省安阳市第一中学2019-2020学年高一上学期期末考试化学试题江西省宜春市奉新县第一中学2020-2021学年高一下学期第一次月考化学试题



