名校
1 . 百里酚蓝(以下记为 )是一种有机弱酸,结构如图1所示,其电离平衡可表示为:
)是一种有机弱酸,结构如图1所示,其电离平衡可表示为: 、
、 ,
, 时
时 溶液中,
溶液中, 的分布分数
的分布分数 与pH的变化关系如图2所示。已知:
与pH的变化关系如图2所示。已知: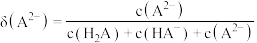 ,下列说法不正确的是
,下列说法不正确的是

 )是一种有机弱酸,结构如图1所示,其电离平衡可表示为:
)是一种有机弱酸,结构如图1所示,其电离平衡可表示为: 、
、 ,
, 时
时 溶液中,
溶液中, 的分布分数
的分布分数 与pH的变化关系如图2所示。已知:
与pH的变化关系如图2所示。已知: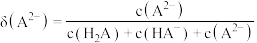 ,下列说法不正确的是
,下列说法不正确的是
| A.溶液由黄色变为蓝色原因是酚羟基发生了变化 |
B. |
C. 时 时 |
D.NaOH滴定 ,可用 ,可用 作指示剂,溶液由红色变为橙色且半分钟内不复原即为滴定终点 作指示剂,溶液由红色变为橙色且半分钟内不复原即为滴定终点 |
您最近一年使用:0次
解题方法
2 .  易水解,是常见的抗氧化剂。实验室以
易水解,是常见的抗氧化剂。实验室以 为原料制备
为原料制备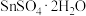 的流程如下,下列说法正确的是
的流程如下,下列说法正确的是

 易水解,是常见的抗氧化剂。实验室以
易水解,是常见的抗氧化剂。实验室以 为原料制备
为原料制备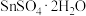 的流程如下,下列说法正确的是
的流程如下,下列说法正确的是
A.气体为 |
| B.反应1只发生复分解反应 |
| C.溶解时,再加入适量Sn粉可以提高产品纯度 |
| D.操作I为蒸发浓缩、降温结晶、过滤、洗涤、干燥 |
您最近一年使用:0次
名校
解题方法
3 . SO2易溶于水,光谱研究表明,SO2的水溶液中存在下列平衡:

其中K1、K2、K3为各步的平衡常数,且K1= [p(SO2)表示SO2的平衡压强]
[p(SO2)表示SO2的平衡压强]
下列说法正确的是

其中K1、K2、K3为各步的平衡常数,且K1=
 [p(SO2)表示SO2的平衡压强]
[p(SO2)表示SO2的平衡压强]下列说法正确的是
A.SO2(g) SO2(aq)的焓变△H<0 SO2(aq)的焓变△H<0 |
| B.SO2在水中的溶解度(以物质的量浓度表示)为c,则c=K1p(SO2) |
C.若pH=6.2时,溶液中 = =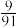 ,则pH=9.2时,溶液中 ,则pH=9.2时,溶液中 = =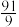 |
D.当SO2的平衡压强为p时,测得c(SO )=amol·L-1,则溶液c(H+)= )=amol·L-1,则溶液c(H+)=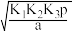 |
您最近一年使用:0次
2022-03-03更新
|
530次组卷
|
2卷引用:福建省龙岩市第一中学2022届高考考前模拟化学试题
名校
4 . 中国科学院化学研究所报道了化合物1催化CO2氢化机理。其机理中化合物1(催化剂,固态)→化合物2(中间产物,固态)的过程和其相对能量曲线如下图所示。下列说法错误的是
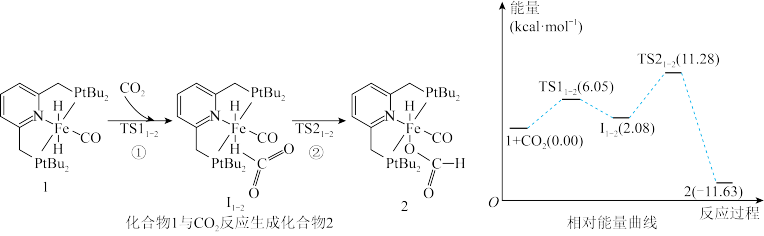

A.化合物1与CO2反应生成化合物2的过程中有两个过渡态TS11-2、TS21-2,说明这一过程包含两个基元反应 |
| B.图中Ⅰl-2与化合物2互为同分异构体 |
| C.过程①的活化能高于过程②的活化能 |
| D.过程①的热化学方程式为:I(s)+CO2(g)=I1-2 (s) △H=2.08 kJ·mol-1 |
您最近一年使用:0次
2021-05-14更新
|
972次组卷
|
10卷引用:福建省厦门外国语学校2021届高三5月高考适应性考试化学试题
福建省厦门外国语学校2021届高三5月高考适应性考试化学试题山东省日照市2021届高三下学期第三次模拟考试化学试题河北省秦皇岛市青龙一中2021届高三高考适应性考试化学试题湖南省岳阳市平江县2022届高三下学期教学质量监测(三)化学试题山东省泰安第二中学2021-2022学年高二上学期期中考试化学试题湖南省娄底市第五中学2021-2022学年高三下学期期中考试化学试题河北省衡水中学2021-2022学年高三下学期二调考试化学试题河北省邯郸市大名县第一中学2022-2023学年高三上学期第一次月考化学试题湖南省长郡中学2022-2023学年高二上学期第一次月考化学试题辽宁省东北育才学校高中部2023-2024学年高二上学期第一次月考化学试题
名校
5 . 向等体积pH不同的盐酸和NH4Cl溶液中加入过量镁条,溶液pH和温度随时间变化曲线如图。下列有关说法错误的是
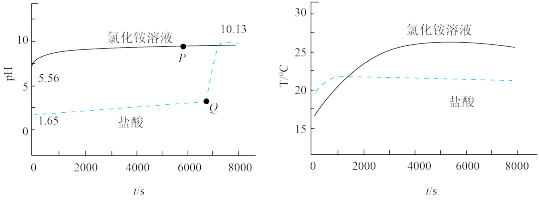

A.在NH4Cl溶液中,P点存在:2c(Mg2+)+c(NH )>c(Cl-) )>c(Cl-) |
| B.Ksp[Mg(OH)2]=5×10-12.61 |
| C.在NH4Cl溶液中,2000~4000温度上升是因为Mg与H2O发生反应 |
| D.在盐酸中,Q点后pH上升是因为Mg与HCl发生反应 |
您最近一年使用:0次
2021-04-11更新
|
547次组卷
|
2卷引用:福建省部分地区(南平、龙岩、三明、宁德、厦门)2021届高中毕业班4月质量检测化学试题
名校
6 . 短周期元素X、Y、Z、Q、R的原子序数依次增大,且X、Y、Q、R的原子的最外层电子数之和为12.X与R同主族,Q是地壳中含量最高的元素。下列说法不正确的是
| A.简单离子半径: Z>Q>R |
| B.最简单氢化物的沸点:Y>Z>Q |
| C.R的最高价氧化物对应的水化物为强碱 |
| D.X、Z、Q三种元素可形成离子化合物和共价化合物 |
您最近一年使用:0次
2021-03-11更新
|
538次组卷
|
3卷引用:福建省厦门市2021届高三下学期第一次质量检测化学试题
福建省厦门市2021届高三下学期第一次质量检测化学试题山东省泰安市宁阳一中2020-2021学年高二下学期期中考试化学试题(已下线)专题17 化学键(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练
解题方法
7 . 室温下,Ka1(H2S)=1.3×10-7,Ka2(H2S)=7.1×10-15。不考虑溶液混合引起的体积变化和H2S的挥发,室温时下列指定溶液中微粒物质的量浓度关系正确的是( )
| A.0.1mol·L-1NaHS溶液:c(Na+)>c(HS-)>c(H2S)>c(S2-) |
| B.0.1mol·L-1Na2S溶液:c(OH-)=c(H+)+c(HS-)+c(H2S) |
| C.0.2mol·L-1NaHS溶液和0.1mol·L-1NaOH溶液等体积混合:c(HS-)+3c(H2S)>c(S2-) |
| D.向0.1mol·L-1NaOH溶液中通入H2S至溶液呈中性:c(Na+)=c(HS-)+c(S2-) |
您最近一年使用:0次
2020-05-19更新
|
203次组卷
|
2卷引用:福建省莆田二中、泉州一中、南安一中三校2020-2021学年高三下学期联考化学试题
2010·浙江·二模
名校
解题方法
8 . 化学中常用图像直观地描述化学反应的进程或结果。下列图像描述正确的是()
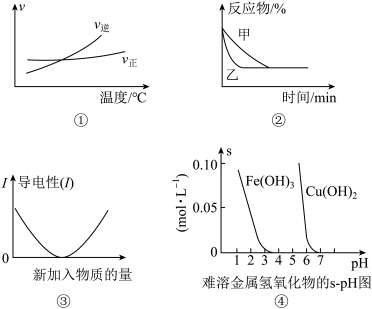

A.根据图①可判断可逆反应“A2(g)+3B2(g) 2AB3(g)+Q的Q﹤0 2AB3(g)+Q的Q﹤0 |
B.图②表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强大 3C(g)+D(s)的影响,乙的压强大 |
| C.图③可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化 |
| D.根据图④,若除去CuSO4溶液中的Fe3+可采用向溶液中加入适量CuO,至pH在4左右 |
您最近一年使用:0次
2020-03-31更新
|
214次组卷
|
26卷引用:2012届福建省漳州市芗城中学高三适应性检测化学试卷
(已下线)2012届福建省漳州市芗城中学高三适应性检测化学试卷(已下线)2010年浙江省第二次五校联考理科综合试题卷(已下线)2010年四川省绵阳市南山中学高三考前模拟考试(理科综合)化学部分(已下线)2010届江苏启东中学高三考前辅导训练化学试题(已下线)2011届山东省济宁一中高三第一次模拟测试试题理综化学试卷(已下线)2011届吉林省长春市高三第二次模拟考试(理综)化学部分(已下线)2011届山东省潍坊市三县最后一次模拟联考(理综)化学部分(已下线)2011届广东省深圳高级中学高三高考前最后模拟试卷(理综)化学部分2016届山东省济南外国语学校高三上学期1月模拟测试理综化学试卷湖南省五市十校教研教改共同体2018届高三12月联考化学试题(已下线)上海市2011届高三六校联考化学试题(已下线)2012届浙江省杭州市学军中学高三上学期第一次月考化学试卷(已下线)2012届江苏省启东中学高三上学期第二次月考化学试卷(已下线)2014届河北省正定中学高三上学期第四次月考化学试卷2016届黑龙江省牡丹江高级中学高三上学期期末理综化学试卷2015-2016学年四川成都石室中学高二4月月考化学试卷2017届陕西省师范大学附属中学高三上学期第二次模考化学试卷(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第5讲 数形结合思想的应用【押题专练】重庆市綦江中学2018-2019学年高二上学期第三次月考化学试题山西省长治市城区第二中学校2018-2019学年高二上学期期末考试化学试题山西省吕梁市汾阳中学2018-2019学年高二下学期期中考试化学试题2020届高三化学二轮冲刺新题专练——化学反应速率的图像分析夯基提能2020届高三化学选择题对题专练——选修4化学反应原理—— 沉淀溶解平衡及其影响因素新疆和田地区第二中学2020届高三上学期12月月考化学试题(重点普通班)广东实验中学2021-2022学年高二上学期期中考试化学试题湖南省长沙市雅礼中学2022-2023学年高二上学期期中考试化学试题
9 . 25℃时,将浓度均为0.1mol·L-1HX溶液和HY溶液分别与等浓度的NaHCO3溶液等体积混合,实验测得产生的气体体积(V)随时间(t)变化的示意图如图所示:下列说法正确的是


| A.相同浓度的HX和HY溶液中水的电离程度:HX﹥HY |
| B.相同体积相同浓度的HX和HY溶液中阴离子数目前者大于后者 |
| C.向10 mL 0.1 mol·L -1的Na2CO3溶液中缓慢滴加10 mL 0.1 mol·L -1的HY,混合后的离子浓度大小关系:c(Na+)﹥c(Y-)﹥c(HCO3-)﹥c(OH-)﹥c(H+) |
| D.将等体积等浓度的HX和HY溶液分别用相同浓度的氢氧化钠溶液滴定,至中性时,消耗的氢氧化钠溶液体积前者大于后者 |
您最近一年使用:0次



