解题方法
1 . N元素的单质及其化合物之间的转化关系如图所示:
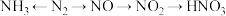
回答下列问题:
(1)N元素在元素周期表中的位置为__________ ,画出N原子结构示意图_________ 。
(2)工业上用氮气和氢气合成氨气,请写出NH3的电子式_____________ 。
(3)实验室可以利用氢氧化钙固体和氯化铵固体制备氨气,请写出该反应的化学方程式___________
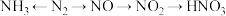
回答下列问题:
(1)N元素在元素周期表中的位置为
(2)工业上用氮气和氢气合成氨气,请写出NH3的电子式
(3)实验室可以利用氢氧化钙固体和氯化铵固体制备氨气,请写出该反应的化学方程式
您最近一年使用:0次
名校
解题方法
2 . N元素的单质及其化合物之间的转化关系:NH3N2NO NO2HNO3。回答下列问题:
(1)N元素在元素周期表中的位置为_______ ;
(2)上述四种气体只能用排水法收集的是_______ (填化学式,下同),只能用排空气法收集的是______ ;
(3)氮的氧化物是空气的主要污染物,下列环境问题与氮的氧化物排放有关的是_____ ;
A. 酸雨 B. 光化学烟雾 C. 白色污染 D. 臭氧层空洞
(4)NO2形成酸雨的化学方程式为______ ;
(5)Ertl(获2007年诺贝尔化学奖)对合成氨机理进行深入研究,并将研究成果用于汽车尾气处理中,在催化剂存在下可将NO和CO反应转化为两种无色无毒气体,用化学反应方程式表示这个过程______ ;
(6)若将12.8 g铜与 50 mL一定浓度的浓硝酸反应,两者恰好完全反应共产生气体5.6 L(标准状况),计算此浓硝酸的物质的量浓度_______ (写出解题过程)。
(1)N元素在元素周期表中的位置为
(2)上述四种气体只能用排水法收集的是
(3)氮的氧化物是空气的主要污染物,下列环境问题与氮的氧化物排放有关的是
A. 酸雨 B. 光化学烟雾 C. 白色污染 D. 臭氧层空洞
(4)NO2形成酸雨的化学方程式为
(5)Ertl(获2007年诺贝尔化学奖)对合成氨机理进行深入研究,并将研究成果用于汽车尾气处理中,在催化剂存在下可将NO和CO反应转化为两种无色无毒气体,用化学反应方程式表示这个过程
(6)若将12.8 g铜与 50 mL一定浓度的浓硝酸反应,两者恰好完全反应共产生气体5.6 L(标准状况),计算此浓硝酸的物质的量浓度
您最近一年使用:0次
2010·江苏南京·一模
3 . 有机物A只含碳、氢、氧三种元素,分子中碳、氢、氧原子个数比为7:10:3,A具有酸性;1molA需要1mol氢氧化钠完全中和;1molA可以和1molBr2加成,已测定A的相对分子质量不大于150。各有机物的转化关系如图所示。

已知:①R—CH=CH—R1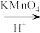 RCOOH+R1COOH
RCOOH+R1COOH
②
回答下列问题:
(1)写出A的结构简式________________________________ 。
(2)反应③的反应类型是_____________ 。
(3)A—F六种物质中含有手性碳原子的是_____________ (用字母填写)。
(4)写出一种符合下列条件的D的同分异构体的结构简式__________________ 。
①能发生银镜反应 ②能发生水解反应 ③结构中无和 环状结构
环状结构
(5)写出一定条件下F生成高分子化合物的反应方程式______________________ 。
(6)丙酮酸 是E的最简单的同系物。
是E的最简单的同系物。
试以丙酮酸为原料合成乙二酸(用合成路线流程图表示,并注明反应条件)_____________ 。
提示:①合成过程中无机试剂任选;②合成路线流程图示例如下:

已知:①R—CH=CH—R1
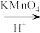 RCOOH+R1COOH
RCOOH+R1COOH②

回答下列问题:
(1)写出A的结构简式
(2)反应③的反应类型是
(3)A—F六种物质中含有手性碳原子的是
(4)写出一种符合下列条件的D的同分异构体的结构简式
①能发生银镜反应 ②能发生水解反应 ③结构中无和
 环状结构
环状结构(5)写出一定条件下F生成高分子化合物的反应方程式
(6)丙酮酸
 是E的最简单的同系物。
是E的最简单的同系物。试以丙酮酸为原料合成乙二酸(用合成路线流程图表示,并注明反应条件)
提示:①合成过程中无机试剂任选;②合成路线流程图示例如下:

您最近一年使用:0次
解题方法
4 . X、Y、Z、Q、W、R是常见的短周期主族元素,其相关信息如下表:
(1)元素X在元素周期表中的位置是_______ 。
(2)上述六种元素中有2种元素能形成一种淡黄色的固体化合物,该化合物的电子式是_________ ,所含化学键的类型有离子键、____
(3)Y、Q、R三种元素的简单氢化物中,稳定性最强的化合物的结构式为________
(4)上述六种元素原子半径与主要化合价的关系如图,其中④对应的元素为_______

(5)将RQ2通入BaCl2溶液中,没有明显变化,再向其中加入Z的最高价氧化物的水化物,可观察到的现象是_____ ,发生反应的离子方程式是_____________
| 元素 | 相关信息 |
| X | 它的一种同位素被用作相对原子质量的标准 |
| Y | 常温下单质为双原子分子,分子中含有3对共用电子对 |
| Z | 是短周期中(除稀有气体外)原子半径最大的元素 |
| Q | 最外层电子数是次外层电子数的3倍 |
| W | 原子序数等于X、Y原子序数之和 |
| R | 与Q同族,且最高价氧化物的水化物的浓溶液常温下使W单质钝化 |
(1)元素X在元素周期表中的位置是
(2)上述六种元素中有2种元素能形成一种淡黄色的固体化合物,该化合物的电子式是
(3)Y、Q、R三种元素的简单氢化物中,稳定性最强的化合物的结构式为
(4)上述六种元素原子半径与主要化合价的关系如图,其中④对应的元素为

(5)将RQ2通入BaCl2溶液中,没有明显变化,再向其中加入Z的最高价氧化物的水化物,可观察到的现象是
您最近一年使用:0次
9-10高二下·江苏·期末
5 . 下图为一些常见物质的转化关系图(部分反应物与生成物未标出)。A、C、E、G为单质,其中A、C、G为金属,E为气体。B为常见无色液体,L为红褐色固体,I的焰色反应呈紫色。常温下A、G投入J的浓溶液无明显现象,K是反应①所得溶液中的唯一溶质。
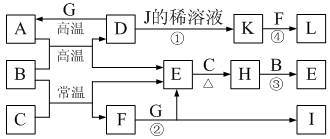
⑴A在元素周期表中的位置为_______ ,H的电子式为________ 。
⑵写出有关反应的离子方程式:
反应①的离子方程式为__________ 。
反应②的离子方程式为__________ 。
⑶反应③中每生成1 mol E,转移电子的物质的量为__________ 。

⑴A在元素周期表中的位置为
⑵写出有关反应的离子方程式:
反应①的离子方程式为
反应②的离子方程式为
⑶反应③中每生成1 mol E,转移电子的物质的量为
您最近一年使用:0次
解题方法
6 . (1)下面是 4 种粒子的结构示意图:
A.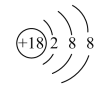 B.
B.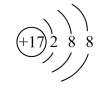 C.
C.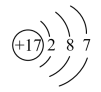 D.
D. 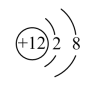
图中粒子共能表示________ 种元素,
图中表示的阳离子是________ (用离子符号表示),
图中B 所表示的元素在元素周期表中的位置________ 。
(2)在 1﹣18 号的短周期主族元素中,图中的字母代表一种元素,回答下列问题:
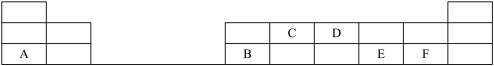
①写出 D 气态氢化物的电子式________ ;
②写出 C 的最高价氧化物的结构式________ ;
③E 和 F 分别形成的气态氢化物中较稳定的是(填写氢化物的化学式)_________ ;
④A 最高价氧化物的水化物所含化学键为____ ,其水溶液与 B 反应的离子方程式为________ ;
(3) X、Y、Z、M、N、Q 皆为短周期主族元素,其原子半径与主要化合价的关系如图所示。下列说法正确的是______

A.金属性:N>Q
B.简单离子半径:Q>N>X
C.最高价氧化物对应水化物的酸性:M>Y>N
D.原子序数:Z>M>X>Y
A.
 B.
B. C.
C. D.
D. 
图中粒子共能表示
图中表示的阳离子是
图中B 所表示的元素在元素周期表中的位置
(2)在 1﹣18 号的短周期主族元素中,图中的字母代表一种元素,回答下列问题:

①写出 D 气态氢化物的电子式
②写出 C 的最高价氧化物的结构式
③E 和 F 分别形成的气态氢化物中较稳定的是(填写氢化物的化学式)
④A 最高价氧化物的水化物所含化学键为
(3) X、Y、Z、M、N、Q 皆为短周期主族元素,其原子半径与主要化合价的关系如图所示。下列说法正确的是

A.金属性:N>Q
B.简单离子半径:Q>N>X
C.最高价氧化物对应水化物的酸性:M>Y>N
D.原子序数:Z>M>X>Y
您最近一年使用:0次
名校
解题方法
7 . A、B、C、D、E为原子序数依次增大的短周期主族元素,其原子半径与最外层电子数的关系如图。E原子最外层上的电子数是D原子最外层电子数的4倍,D离子核外电子排布与C2-相同。
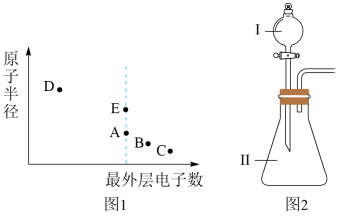
试回答:
(1)元素C在元素周期表中的位置是___________ 。
(2)D离子的离子结构示意图为__________ 。
(3)B和E最高价氧化物对应的水化物,酸性较弱的是_________ 。(用化学式作答)若用上如图中装置验证这两种酸的酸性强弱,则在装置中加入的试剂分别为:Ⅰ_______ Ⅱ_________ ,观察到的实验现象是______ 。

试回答:
(1)元素C在元素周期表中的位置是
(2)D离子的离子结构示意图为
(3)B和E最高价氧化物对应的水化物,酸性较弱的是
您最近一年使用:0次
9-10高一下·江苏连云港·期末
解题方法
8 . 现有A、B、C三种短周期元素,原子序数依次递增。A与C的质子数之和为27,最外层电子数之差为5;0.9g单质B与足量盐酸反应,收集到气体1.12L(标准状况)。请回答下列问题:
(1)B元素在元素周期表中的位置是___________ 。
(2)A、B、C三种元素最高价氧化物对应的水化物酸性渐强、碱性渐弱的顺序是(写化学式)___________________________________________ 。
(3)A、B两元素的最高价氧化物对应的水化物之间可以发生反应,其离子方程式_____________________________________________________ 。
(4)将B单质与石墨按如右图装置连接,石墨电极的名称为_________ ;该电极反应式为:_________________ 。

(5)C的一种氧化物是常见的大气污染物。为防止大气污染,某化工厂用NaOH溶液、石灰和O2处理含C的上述氧化物的尾气,使其转化为石膏(CaSO4·2H2O)。假设在转化过程中C元素不损失,每天处理1120 m3(标准状况下)含2%(体积分数)上述氧化物的尾气,理论上可以得到多少千克石膏(请写出简要的计算过程)。
________________
(1)B元素在元素周期表中的位置是
(2)A、B、C三种元素最高价氧化物对应的水化物酸性渐强、碱性渐弱的顺序是(写化学式)
(3)A、B两元素的最高价氧化物对应的水化物之间可以发生反应,其离子方程式
(4)将B单质与石墨按如右图装置连接,石墨电极的名称为

(5)C的一种氧化物是常见的大气污染物。为防止大气污染,某化工厂用NaOH溶液、石灰和O2处理含C的上述氧化物的尾气,使其转化为石膏(CaSO4·2H2O)。假设在转化过程中C元素不损失,每天处理1120 m3(标准状况下)含2%(体积分数)上述氧化物的尾气,理论上可以得到多少千克石膏(请写出简要的计算过程)。
您最近一年使用:0次
名校
9 . 相对分子质量为92的某芳香烃X是一种重要的有机化工原料,研究部门以它为初始原料设计出如图转化关系图(部分产物、合成路线、反应条件略去)。C是一种功能高分子,链节组成为C7H5NO。
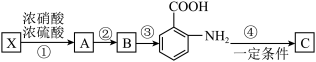
已知: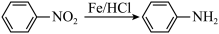 (苯胺,易被氧化)
(苯胺,易被氧化)
(1)C的结构简式是___ 。
(2)反应②、③的类型分别是:___ 反应、___ 反应;②、③两步能否互换?理由是____ 。

已知:
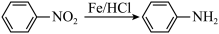 (苯胺,易被氧化)
(苯胺,易被氧化)(1)C的结构简式是
(2)反应②、③的类型分别是:
您最近一年使用:0次
名校
解题方法
10 . Ⅰ.元素化合物知识形散而神不散。含有相同元素的物质间在一定条件下是有规律转化的。某金属单质A及其化合物间的转化关系如图(某些产物和反应条件已略去),B的焰色反应为黄色。
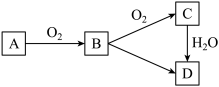
请写出下列物质转化的反应方程式:
(1)A与CuSO4溶液反应的总化学反应方程式___________ 。
(2)C与CO2反应的化学反应方程式___________ 。
(3)D与小苏打溶液反应的离子方程式___________ 。
Ⅱ.完成下列有关物质的量的相关计算:
(1)若1g N2中含有x个N原子,则阿伏加德罗常数为___________ 。
(2)3.4 gNH3 与标准状况下的___________ L的H2S含有相同数目的氢原子。
(3)一个密闭容器,中间有一可自由滑动的隔板(厚度可忽略)将容器分成两部分,当左边充入lmolN2,右边充入CO和CO2的混合气体共18g时,隔板处于如图位置(左、右两侧温度相同)。则右侧混合气体中碳原子与氧原子的个数比为___________ 。


请写出下列物质转化的反应方程式:
(1)A与CuSO4溶液反应的总化学反应方程式
(2)C与CO2反应的化学反应方程式
(3)D与小苏打溶液反应的离子方程式
Ⅱ.完成下列有关物质的量的相关计算:
(1)若1g N2中含有x个N原子,则阿伏加德罗常数为
(2)3.4 gNH3 与标准状况下的
(3)一个密闭容器,中间有一可自由滑动的隔板(厚度可忽略)将容器分成两部分,当左边充入lmolN2,右边充入CO和CO2的混合气体共18g时,隔板处于如图位置(左、右两侧温度相同)。则右侧混合气体中碳原子与氧原子的个数比为

您最近一年使用:0次



