名校
1 . 下列元素中,原子半径最小的是
A. | B. | C. | D. |
您最近一年使用:0次
2024-01-20更新
|
230次组卷
|
11卷引用:广西钦州市2020-2021学年高一下学期期末考试化学(文)试题
广西钦州市2020-2021学年高一下学期期末考试化学(文)试题宁夏海原第一中学2020-2021学年高一下学期期末考试化学试题北京市丰台区2019-2020学年高一下学期期末考试化学试题贵阳市第三十七中学2020-2021学年高一下学期期中考试化学试题北京市昌平区2022-2023学年高一下学期期末质量抽测化学试题北京市第二十中学2021-2022学年高一下学期期末考试化学试题北京市西城区2023-2024学年高一上学期期末考试化学试卷2014-2015辽宁省锦州市第一高级中学高一下学期期中化学试卷北京市第十一中学2021-2022学年高一下学期6月月考化学试题北京理工大学附属中学2023-2024学年高一下学期4月期中考试化学试题福建省德化第二中学2023-2024学年高一下学期3月月考化学试题
2 . 已知CaCO3的Ksp=2.8×10-9,现将浓度为2×10-4mol/L的Na2CO3溶液与CaCl2溶液等体积混合,若要产生沉淀,则所用CaCl2溶液的浓度至少应为
| A.2.8×10-2mol/L | B.1.4×10-5mol/L | C.5.6×10-5mol/L | D.2.8×10-5mol/L |
您最近一年使用:0次
2024-01-10更新
|
112次组卷
|
38卷引用:广西钦州市2020-2021学年高二下学期期末考试化学试题
广西钦州市2020-2021学年高二下学期期末考试化学试题吉林省公主岭市范家屯镇第一中学2020-2021学年高二上学期期末两校联考化学试题甘肃省天水市一中2020-2021学年高二上学期第二学段(期末)考试化学试题云南省中央民族大学附属中学芒市国际学校2017-2018学年高二上学期末考试化学试题吉林省白城市第一中学2020-2021学年高二下学期3月月考化学试题海南省北京师范大学万宁附属中学2021-2022学年高二上学期第一次月考化学试题 安徽省芜湖市第一中学2021-2022学年高二上学期第二次月末诊断测试化学试题(已下线)3.4.1 难溶电解质的沉淀溶解平衡(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)新疆昌吉州2021-2022学年高二上学期期末考试化学试题陕西省渭南市大荔县2021-2022学年高二上学期期末考试化学试题云南省文山州麻栗坡县2021-2022学年高二上学期期中测试化学试题江西省抚州市临川区第一中学2017-2018学年高二上学期期中考试化学试题湖南省衡阳县第四中学2018-2019学年高二第一学期实验班9月月考化学试题河北省沧州市盐山中学2018-2019学年高二上学期12月月考化学试题【全国百强校】河北省石家庄市第二中学2018-2019学年高二上学期期中考试化学试题陕西省吴起高级中学2019-2020学年高二上学期期中考试化学(能力卷)试题陕西省吴起高级中学2019-2020学年高二上学期期中考试化学(基础卷)试题(已下线)2019年11月13日 《每日一题》人教版(选修4)——溶度积的有关计算河北省邯郸市大名县第一中学2019-2020学年高二上学期12月月考化学试题(清北组)2020年春季人教版高中化学选修4第三章《水溶液中的离子平衡》测试卷鲁科版(2019)选择性必修1第3章 物质在水溶液中的行为 第3节 沉淀溶解平衡 课时1 沉淀溶解平衡及其应用高中必刷题高二选择性必修1第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡 课时1 溶解平衡及其应用(已下线)第3章 章末检测-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)(已下线)第三章 水溶液中的离子平衡(基础过关)-2020-2021学年高二化学单元测试定心卷(人教版选修4)(已下线)易错17 难溶电解质的溶解平衡及应用-备战2021年高考化学一轮复习易错题鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 第3节 沉淀溶解平衡(已下线)3.4 难溶电解质的溶解平衡(基础练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)安徽省阜阳市临泉县第一中学2021-2022学年高二下学期开学考试化学试题(已下线)3.4.1 沉淀溶解平衡-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)辽宁省重点高中沈阳市郊联体2022-2023学年高二上学期期中考试化学试题辽宁省沈阳市辽中区第二高级中学2022-2023学年高二上学期期中考试化学试题(已下线)专题突破卷09 水溶液中的离子反应与平衡 ?-2024年高考化学一轮复习考点通关卷(新教材新高考)作业(二十) 沉淀溶解平衡与溶度积第三章 第四节 沉淀溶解平衡 第1课时 沉淀溶解平衡与溶度积黑龙江省实验中学2023-2024学年高二上学期12月月考化学试题山西省朔州市怀仁县阳高一中2023-2024学年高二上学期11月化学试卷广东省湛江市雷州市第二中学2023-2024学年高二下学期开学化学试题陕西省 韩城市象山中学2023-2024学年高二上学期第三次月考化学试题
名校
3 . 硫的氧化物的排放是形成硫酸型酸雨的主要原因,含硫烟气(主要成分为SO2)的处理备受关注,主要有以下两种方法。请回答下列问题:
I.碱液吸收法
步骤1:用足量氨水吸收SO2。
步骤2:再加入熟石灰,发生反应2NH +Ca2++2OH-+SO
+Ca2++2OH-+SO ⇌CaSO3↓+2NH3•H2O。
⇌CaSO3↓+2NH3•H2O。
(1)已知:25℃时,Kb(NH3•H2O)=a;Ksp(CaSO3)=b。该温度下,步骤2中反应的平衡常数K=________ (用含a、b的代数式表示)。
Ⅱ.水煤气还原法
已知:
i.2CO(g)+SO2(g)⇌S(l)+2CO2(g)ΔH1═-37.0kJ•mol-1
ii.2H2(g)+SO2(g)⇌S(l)+2H2O(g)ΔH2=+45.4kJ•mol-1
(2)CO(g)与H2O(g)反应生成CO2(g)、H2(g)的热化学方程式为________ 。
(3)在一定压强下,发生反应ii。平衡时,SO2的转化率α(SO2)与原料气投料比[ ]和温度(T)的关系如图所示。
]和温度(T)的关系如图所示。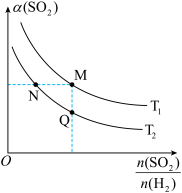 ①H2的转化率α(H2):M
①H2的转化率α(H2):M______ N(填“>”“<”或“=”)。
②逆反应速率:Q______ M(填“>”“<”或“=”)。
(4)T℃,向2L恒容密闭容器中充入2molCO(g)、2molSO2(g)和2molH2(g),发生反应i和反应ii。5min达到平衡时,CO2(g)和H2O(g)的物质的量分别为1.6mol、1.8mol。
①其他条件不变,6min时缩小容器容积,α(H2)________ (填“增大”“减小”或“不变)。
②该温度下,反应ii的平衡常数K=________ 。
I.碱液吸收法
步骤1:用足量氨水吸收SO2。
步骤2:再加入熟石灰,发生反应2NH
 +Ca2++2OH-+SO
+Ca2++2OH-+SO ⇌CaSO3↓+2NH3•H2O。
⇌CaSO3↓+2NH3•H2O。(1)已知:25℃时,Kb(NH3•H2O)=a;Ksp(CaSO3)=b。该温度下,步骤2中反应的平衡常数K=
Ⅱ.水煤气还原法
已知:
i.2CO(g)+SO2(g)⇌S(l)+2CO2(g)ΔH1═-37.0kJ•mol-1
ii.2H2(g)+SO2(g)⇌S(l)+2H2O(g)ΔH2=+45.4kJ•mol-1
(2)CO(g)与H2O(g)反应生成CO2(g)、H2(g)的热化学方程式为
(3)在一定压强下,发生反应ii。平衡时,SO2的转化率α(SO2)与原料气投料比[
 ]和温度(T)的关系如图所示。
]和温度(T)的关系如图所示。 ①H2的转化率α(H2):M
①H2的转化率α(H2):M②逆反应速率:Q
(4)T℃,向2L恒容密闭容器中充入2molCO(g)、2molSO2(g)和2molH2(g),发生反应i和反应ii。5min达到平衡时,CO2(g)和H2O(g)的物质的量分别为1.6mol、1.8mol。
①其他条件不变,6min时缩小容器容积,α(H2)
②该温度下,反应ii的平衡常数K=
您最近一年使用:0次
名校
解题方法
4 . NiCl2是一种重要催化剂。某科研小组以废弃催化剂含Ni2+、Cu2+、Fe3+、Ca2+、Mg2+等)为原料,按下列流程回收NiCl2:6H2O晶体,回答下列问题。

已知:Ksp(CaF2)=4×10-11,Ksp(MgF2)=9×10-9
(1)滤渣1的主要成分是S和_________ (写化学式),生成S的离子方程式为_____ 。
(2)若用H2O2代替Cl2,试剂Y的使用量会减少,原因是________ 。
(3)氟化除杂时要保证完全除去Ca2+和Mg2+(离子浓度<10-5mol/L),滤液3中F—的浓度不小___ mol/L。
(4)操作A为______ 、过滤、洗涤、干燥。
(5)二氯亚砜(SOCl2)是一种无色易挥发液体,遇水剧烈水解生成两种气体,常用作脱水剂将所得NiCl2•6H2O与SOCl2混合加热可制备无水NiCl2,反应的化学方程式为____ 。

已知:Ksp(CaF2)=4×10-11,Ksp(MgF2)=9×10-9
(1)滤渣1的主要成分是S和
(2)若用H2O2代替Cl2,试剂Y的使用量会减少,原因是
(3)氟化除杂时要保证完全除去Ca2+和Mg2+(离子浓度<10-5mol/L),滤液3中F—的浓度不小
(4)操作A为
(5)二氯亚砜(SOCl2)是一种无色易挥发液体,遇水剧烈水解生成两种气体,常用作脱水剂将所得NiCl2•6H2O与SOCl2混合加热可制备无水NiCl2,反应的化学方程式为
您最近一年使用:0次
名校
5 . 某同学利用Cl2氧化K2MnO4制备KMnO4的装置如图所示(夹持装置略):
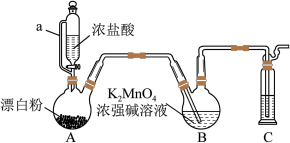
已知:锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:3MnO +2H2O═2MnO
+2H2O═2MnO +MnO2↓+4OH-
+MnO2↓+4OH-
回答下列问题:
(1)装置A中a的作用是_________ 装置C中的试剂为_________ ;装置A中制备Cl2的化学方程式为_________ 。
(2)上述装置存在一处缺陷,会导致KMnO4产率降低,改进的方法是_________ 。
(3)高锰酸钾还可以用电解法制备:
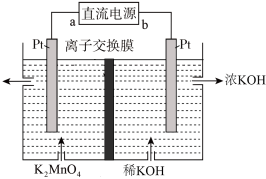
①电解时阳极的电极反应式是_________ 。
②该装置中的离子交换膜是_________ 离子交换膜(填“阴”或“阳”)。
(4)某化学学习小组测定某草酸溶液的浓度,并用所测草酸溶液测定某样品中高锰酸钾的纯度(已知:杂质不参与反应;KMnO4的摩尔质量为158g/mol),进行了如下实验:
步骤i.配制0.1000mol/L的标准氢氧化钠溶液;
步骤ii.取草酸溶液10.00mL,用0.1000mol/L的标准氢氧化钠溶液滴定,结果用去氢氧化钠溶液20.00mL;
步骤iii.取1.0g样品溶于水,滴入几滴稀硫酸酸化,用测定的草酸溶液进行滴定,达到滴定终点消耗草酸溶液50.00mL。
①步骤ii中应选择_________ 作指示剂。
②样品中高锰酸钾的纯度为_________ 。
③本实验中,若第一次滴定时盛装氢氧化钠溶液的滴定管未润洗,会测得高锰酸钾纯度_________ (填“偏大”、“偏小”或“无影响”)。

已知:锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:3MnO
 +2H2O═2MnO
+2H2O═2MnO +MnO2↓+4OH-
+MnO2↓+4OH-回答下列问题:
(1)装置A中a的作用是
(2)上述装置存在一处缺陷,会导致KMnO4产率降低,改进的方法是
(3)高锰酸钾还可以用电解法制备:

①电解时阳极的电极反应式是
②该装置中的离子交换膜是
(4)某化学学习小组测定某草酸溶液的浓度,并用所测草酸溶液测定某样品中高锰酸钾的纯度(已知:杂质不参与反应;KMnO4的摩尔质量为158g/mol),进行了如下实验:
步骤i.配制0.1000mol/L的标准氢氧化钠溶液;
步骤ii.取草酸溶液10.00mL,用0.1000mol/L的标准氢氧化钠溶液滴定,结果用去氢氧化钠溶液20.00mL;
步骤iii.取1.0g样品溶于水,滴入几滴稀硫酸酸化,用测定的草酸溶液进行滴定,达到滴定终点消耗草酸溶液50.00mL。
①步骤ii中应选择
②样品中高锰酸钾的纯度为
③本实验中,若第一次滴定时盛装氢氧化钠溶液的滴定管未润洗,会测得高锰酸钾纯度
您最近一年使用:0次
名校
解题方法
6 . 常温下,用NaOH溶液滴定NaH2PO4溶液,溶液pH与 的关系如图所示,下列关系正确的是
的关系如图所示,下列关系正确的是

 的关系如图所示,下列关系正确的是
的关系如图所示,下列关系正确的是
| A.常温下,Ka2(H3PO4)=10-6.8 |
| B.常温下,NaH2PO4溶液水解程度大于电离程度 |
C.向0.1mol/L的NaH2PO4溶液中滴加NaOH溶液至中性:c(Na+)>3c(HPO )+3c(PO )+3c(PO ) ) |
D.0.1mol/L的NaH2PO4溶液与0.1mol/L的Na3PO4溶液等体积混合:2c(H3PO4)+c(H2PO )+c(H+)=c(OH—)+c(PO )+c(H+)=c(OH—)+c(PO ) ) |
您最近一年使用:0次
名校
解题方法
7 . 液流电池是一种新型蓄电池,这种电池具有容量高、使用领域广、循环使用寿命长等特点。如图是设计的一种有机物液流电池原理图,充电时,聚对苯二酚( )被氧化,下列说法错误的是
)被氧化,下列说法错误的是

 )被氧化,下列说法错误的是
)被氧化,下列说法错误的是
| A.该电池使用一段时间后,理论上需再补充正负极的电解液 |
B.放电时,正极反应式: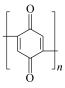 +2ne—+2nH+= +2ne—+2nH+=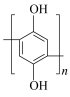 |
C.充电时,阴极反应式: +4ne—+4nH+= +4ne—+4nH+= |
| D.交换膜为质子交换膜,可防止两种有机物进入对方区域 |
您最近一年使用:0次
名校
解题方法
8 . 向两个体积可变的密闭容器中均充入1mol的A2和2mol的B2,发生反应:A2(g)+2B2(g)⇌2AB2(g)△H,维持两个容器的压强分别为P1和P2,在不同温度下达到平衡,测得平衡时AB的体积分数随温度的变化如图所示。已知:点Ⅱ时容器的体积为0L。下列叙述正确的是
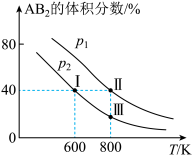

| A.由图象可知:P1<P2,△H<0 |
| B.点Ⅰ时A2的平衡转化率为40% |
| C.点Ⅲ所对应的反应平衡常数K=0.2 |
| D.将点Ⅱ所对应的容器冷却到600K即可变成点Ⅰ |
您最近一年使用:0次
名校
解题方法
9 . 根据下列实验操作和现象所得出的结论正确的是
| 实验内容 | 实验结论 | |
| A | 溴乙烷、乙醇及固体NaOH混合加热,产生的气态物质通入酸性高锰酸钾溶液,溶液褪色 | 溴乙烷发生消去反应生成了乙烯 |
| B | 向2支均盛有2mL 1.0mol/L的KOH溶液的试管中,分别加入2滴浓度均为0.1mol/L的AlCl3和FeCl3溶液,一支试管出现红褐色沉淀,另一支无明显现象 | 在相同温度下Ksp[Al(OH)3]>Ksp[Fe(OH)3] |
| C | 向含有酚酞的Na2CO3溶液中滴期少量BaCl2固体,溶液颜色变浅 | Na2CO3溶液中存在水解平衡 |
| D | 向某溶液中滴加少量稀NaOH溶液,将湿润的红色石蕊试纸置于试管口,试纸不变蓝 | 溶液中不含 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
10 . 己烷雌酚的一种合成路线如图:

下列叙述正确的是

下列叙述正确的是
| A.在NaOH水溶液中加热,化合物X可发生消去反应 |
| B.在一定条件,化合物Y可与HCHO发生缩聚反应 |
| C.用FeCl3溶液不可鉴别化合物X和Y |
| D.化合物X的一氯代物有4种 |
您最近一年使用:0次



