解题方法
1 . 碱式次氯酸镁[MgmClO(OH)n·H2O]微溶于水,不潮解,相对稳定,是一种有开发价值的无机抗菌剂,以菱镁矿(MgCO3,含少量FeCO3)为主要原料,制备碱式次氯酸镁的工艺流程如下,下列说法不正确的是
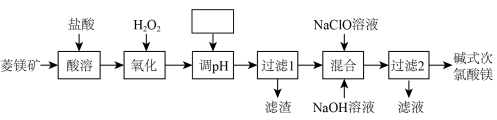
| A.流程中“酸溶”后溶液中含有Mg2+、Fe2+ |
| B.调pH时所选试剂可能是MgCO3 |
| C.“过滤1”所得的滤渣含有Fe(OH)3 |
| D.“混合”时反应的离子方程式只有Mg2++ClO-+OH-+H2O=MgClO(OH)·H2O↓ |
您最近一年使用:0次
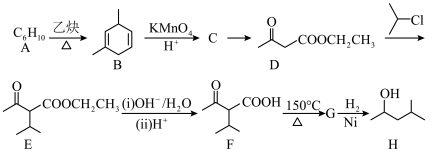
2 . 有机物H是优良的溶剂,在工业上可用作洗涤剂、润滑剂,其合成线路:
(1)H的名称为___________ 。A的结构简式为___________ 。
(2)C→D所需试剂及反应条件分别为___________ 。
(3)D→E的化学方程式为___________ 。
(4)F中含有官能团的名称为___________ 。G→H的反应类型为___________ 。
(5)符合下列条件的F的同分异构体的结构简式为___________ 。
①能与NaHCO3溶液反应放出CO2②能发生银镜反应
③核磁共振氢谱有4组峰且峰面积之比为9:1:1:1;
(6)请设计由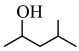 和乙烯(CH2=CH2)为起始原料,制备
和乙烯(CH2=CH2)为起始原料,制备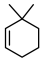 的合成路线
的合成路线___________ (无机试剂任选)。
合成路线流程图示例如下:
H2C=CH2 CH3CH2OH
CH3CH2OH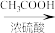 CH3COOC2H
CH3COOC2H
已知:①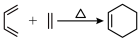 ;
;
②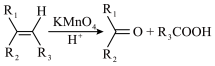
③
(1)H的名称为
(2)C→D所需试剂及反应条件分别为
(3)D→E的化学方程式为
(4)F中含有官能团的名称为
(5)符合下列条件的F的同分异构体的结构简式为
①能与NaHCO3溶液反应放出CO2②能发生银镜反应
③核磁共振氢谱有4组峰且峰面积之比为9:1:1:1;
(6)请设计由
 和乙烯(CH2=CH2)为起始原料,制备
和乙烯(CH2=CH2)为起始原料,制备 的合成路线
的合成路线合成路线流程图示例如下:
H2C=CH2
 CH3CH2OH
CH3CH2OH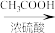 CH3COOC2H
CH3COOC2H
您最近一年使用:0次
3 . 设NA表示阿伏加德罗常数的值,下列说法正确的是
| A.78gNa2S和Na2O2的混合物中含有阴离子的数目为NA |
| B.标准状况下2.24LCl2完全溶于水时,转移电子数为0.1NA |
| C.46gC2H6O分子中含极性键数目一定是7NA |
| D.100g含甲酸46%的水溶液中含氧原子数为2NA |
您最近一年使用:0次
4 . 下列关于电解质溶液的说法中错误的是
| A.新制氯水中:c(ClO-)+c(HClO)=c(Cl-) |
| B.等浓度、等体积的HCOOH溶液与HCOONa溶液混合后pH<7:c(HCOO-)>c(Na+)>c(H+)>c(OH-) |
C.Na2CO3与NaHCO3的混合溶液中:c(Na+)+c(H+)=c(OH-)+c(HC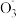 )+c(C )+c(C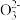 ) ) |
D.已知Ka(HF)> (H2S),则同浓度的NaHS和NaF溶液的pH:NaHS>NaF (H2S),则同浓度的NaHS和NaF溶液的pH:NaHS>NaF |
您最近一年使用:0次
5 . 某化学实验探究小组探究MnO2与某些盐溶液的反应,设计如图装置。左烧杯中加入50mL6mol·L-1硫酸,右烧杯中加入50mL6mol·L-1CaCl2溶液,盐桥选择氯化钾琼脂。当闭合开关K时,电流表中出现指针偏转,下列说法正确的是
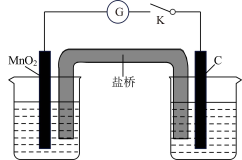
| A.该实验装置属于电解池 |
| B.左侧烧杯中的电极反应为MnO2+4H++2e-=Mn2++2H2O |
| C.右侧C电极上发生还原反应,产生的气体可使湿润的碘化钾淀粉试纸变蓝 |
| D.若将盐桥中氯化钾琼脂换成KNO3琼脂,则C电极上产生的气体的总量增加 |
您最近一年使用:0次
解题方法
6 . 下列离子方程式书写正确的是
| A.Na与水反应:Na+2H2O=Na++2OH-+H2↑ |
B.过量NaOH溶液与NH4HCO3溶液反应:HC +OH-=H2O+C +OH-=H2O+C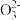 |
| C.FeO溶于稀硝酸:FeO+2H+=Fe2++H2O |
| D.向AgNO3溶液中滴加过量氨水:Ag++2NH3·H2O=[Ag(NH3)2]++2H2O |
您最近一年使用:0次
7 . 化学与生活密切相关,下列说法正确的是
| A.SO2有毒,严禁将其添加到任何食品和饮料中 |
| B.将豆浆煮沸的目的是将蛋白质转化为氨基酸便于人体吸收 |
| C.聚酯纤维、有机玻璃、酚醛树脂都属于有机高分子材料 |
| D.电热水器用镁棒防止金属内胆腐蚀,原理是外加电流保护法 |
您最近一年使用:0次
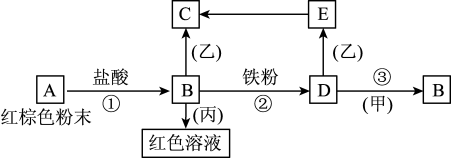
8 . 下列物质之间有如下反应关系:
(1)写出下列物质的化学式:
A___________ B___________ D___________ 甲___________ 乙___________ 丙___________ ;
(2)写出E→C反应的化学方程式:___________ ;
(3)写出B+丙反应的离子方程式:___________ 。
(1)写出下列物质的化学式:
A
(2)写出E→C反应的化学方程式:
(3)写出B+丙反应的离子方程式:
您最近一年使用:0次
9 . 用18mol·L-1浓硫酸配制100mL3.0mol·L-1稀硫酸的实验步骤如下:
①计算所用浓硫酸的体积②量取一定体积的浓硫酸③溶解④转移、洗涤⑤定容、摇匀
完成下列问题:
(1)所需浓硫酸的体积是___________ ,量取浓硫酸所用的量筒的规格是___________ (从下列中选用)。
A.10mL B.25mL C.50mL D.100mL
(2)第③步实验的操作是___________ 。
(3)下列情况对所配制的稀硫酸浓度有何影响?(用“偏大”“偏小”“无影响”填写)
A.所用的浓硫酸长时间放置在密封不好的容器中___________ ;
B.容量瓶用蒸馏洗涤后残留有少量的水___________ ;
C.所用过的烧杯、玻璃棒未洗涤___________ ;
D.定容时俯视刻度线___________ 。
①计算所用浓硫酸的体积②量取一定体积的浓硫酸③溶解④转移、洗涤⑤定容、摇匀
完成下列问题:
(1)所需浓硫酸的体积是
A.10mL B.25mL C.50mL D.100mL
(2)第③步实验的操作是
(3)下列情况对所配制的稀硫酸浓度有何影响?(用“偏大”“偏小”“无影响”填写)
A.所用的浓硫酸长时间放置在密封不好的容器中
B.容量瓶用蒸馏洗涤后残留有少量的水
C.所用过的烧杯、玻璃棒未洗涤
D.定容时俯视刻度线
您最近一年使用:0次
10 . (Ⅰ)有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示。E的单质可与酸反应,1molE单质与足量酸作用,在标准状况下能产生33.6LH2;E的阳离子与A的阴离子核外电子层结构完全相同。
(1)①A与E形成的化合物的化学式是___________ 。
②B的最高价氧化物化学式为___________ 。
③C元素的名称为___________ 。
(2)D的单质与水反应的化学方程式为:___________ 。
(3)向D与E形成的化合物的水溶液中滴入烧碱溶液直至过量,观察到的现象是___________ ,有关反应的离子方程式为:
___________ ,___________ 。
(Ⅱ) A、B、C、D、E分别代表5种微粒,每种微粒中都含有18个电子。其中A和C都是由单原子形成的阴离子,B、D和E都是分子;又知在水溶液中A跟B反应可生成C和D;常温下E是一种强氧化性气体。请回答:
(4)用化学符号表示上述5种微粒:A___________ ,B___________ ,C___________ ,D___________ ,E___________ 。
(5)在水溶液中A跟B反应的离子方程式是___________ 。
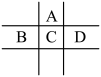
(1)①A与E形成的化合物的化学式是
②B的最高价氧化物化学式为
③C元素的名称为
(2)D的单质与水反应的化学方程式为:
(3)向D与E形成的化合物的水溶液中滴入烧碱溶液直至过量,观察到的现象是
(Ⅱ) A、B、C、D、E分别代表5种微粒,每种微粒中都含有18个电子。其中A和C都是由单原子形成的阴离子,B、D和E都是分子;又知在水溶液中A跟B反应可生成C和D;常温下E是一种强氧化性气体。请回答:
(4)用化学符号表示上述5种微粒:A
(5)在水溶液中A跟B反应的离子方程式是
您最近一年使用:0次



