1 . 常温下,向含 、
、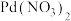 和
和 的溶液中滴加KSCN溶液,浊液中
的溶液中滴加KSCN溶液,浊液中 [
[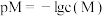 ,
,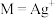 、
、 或
或 ]与
]与 的关系如图所示。已知:常温下,
的关系如图所示。已知:常温下,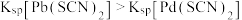 ,平衡常数K大于
,平衡常数K大于 时认为该反应能完全进行。
时认为该反应能完全进行。
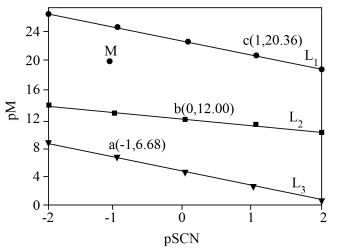
下列叙述错误的是
 、
、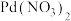 和
和 的溶液中滴加KSCN溶液,浊液中
的溶液中滴加KSCN溶液,浊液中 [
[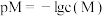 ,
,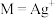 、
、 或
或 ]与
]与 的关系如图所示。已知:常温下,
的关系如图所示。已知:常温下,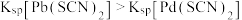 ,平衡常数K大于
,平衡常数K大于 时认为该反应能完全进行。
时认为该反应能完全进行。
下列叙述错误的是
A.直线 代表pPd与pSCN的关系 代表pPd与pSCN的关系 |
B.饱和AgSCN溶液中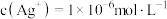 |
C.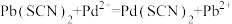 不可逆 不可逆 |
D.M点溶液可析出AgSCN和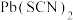 |
您最近一年使用:0次
2024-03-10更新
|
253次组卷
|
2卷引用:湖南省株洲市第一中学2021届高三第一次模拟检测化学试题
名校
2 .  为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.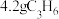 中含有 中含有 键数目可能为 键数目可能为 |
B. ( (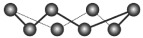 )分子中所含共价键数为 )分子中所含共价键数为 |
C. 质量分数为98%的 质量分数为98%的 ,用水稀释至 ,用水稀释至 的质量分数为9.8% 的质量分数为9.8% |
D.完全燃烧生成 和 和 物质的量之比为 物质的量之比为 的有机物一定为 的有机物一定为 |
您最近一年使用:0次
2024-03-09更新
|
567次组卷
|
2卷引用:湖南省株洲市第一中学2021届高三下学期第二次模拟检测化学试题
名校
3 . 某晶体立方晶胞如图所示。已知图中微粒1的分数坐标是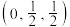 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。下列说法正确的是
。下列说法正确的是
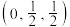 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。下列说法正确的是
。下列说法正确的是
A. 周围距离最近且相等的 周围距离最近且相等的 个数是6 个数是6 |
B.微粒2的分数坐标是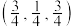 |
| C.已知银与铜位于同一族,银元素位于元素周期表的d区 |
D.若晶胞边长为a pm,则晶体密度为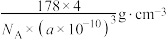 |
您最近一年使用:0次
2024-02-25更新
|
1308次组卷
|
7卷引用:湖南省株洲市第一中学2021届高三下学期第二次模拟检测化学试题
湖南省株洲市第一中学2021届高三下学期第二次模拟检测化学试题广西柳州高中、南宁三中名校联盟2023-2024学年高三一轮复习诊断联考化学试题(已下线)专题04 物质结构与性质 元素推断-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)江西省南昌市2024届高三下学期第三次模拟测试化学试题(已下线)选择题11-14安徽省蚌埠第二中学2023-2024学年高二下学期3月月考化学试题广西来宾市忻城县高级中2023-2024学年高二下学期期中考试化学试卷
4 . 某溶液 可能含有下列离子中的几种:
可能含有下列离子中的几种: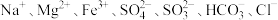 ,且所含离子的物质的量浓度均相等。为了确定该溶液的组成,某同学取适量上述溶液X,进行如下实验(所加试剂均足量),下列说法正确的是
,且所含离子的物质的量浓度均相等。为了确定该溶液的组成,某同学取适量上述溶液X,进行如下实验(所加试剂均足量),下列说法正确的是
 可能含有下列离子中的几种:
可能含有下列离子中的几种: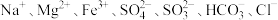 ,且所含离子的物质的量浓度均相等。为了确定该溶液的组成,某同学取适量上述溶液X,进行如下实验(所加试剂均足量),下列说法正确的是
,且所含离子的物质的量浓度均相等。为了确定该溶液的组成,某同学取适量上述溶液X,进行如下实验(所加试剂均足量),下列说法正确的是
A.溶液X中一定含有 |
B.溶液 中可能存在 中可能存在 |
C.无色气体 不含有 不含有 |
D.白色沉淀 一定含有 一定含有 ,可能含有 ,可能含有 |
您最近一年使用:0次
2024-02-20更新
|
139次组卷
|
3卷引用:湖南省长沙市宁乡市第一高级中学2021届高三新高考第一次模拟考试化学试卷
2024·广东·模拟预测
名校
解题方法
5 . 某小组利用如图所示装置制备并收集TiCl4(夹持装置略去),并测定由TiCl4制备的纳米xTiO2•yH2O的组成。
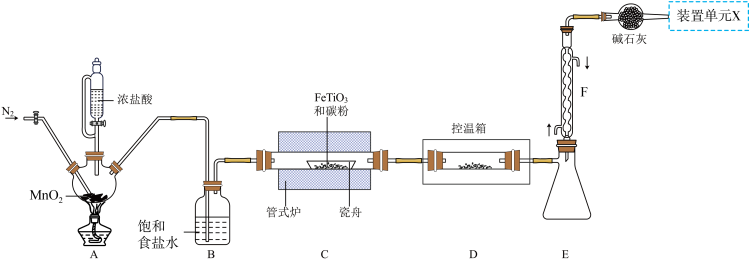
已知:
I. TiCl4高温时能与O2反应,极易水解,能溶于CCl4;
Ⅱ.瓷舟中主反应生成TiCl4、FeCl3(容易二聚成Fe2Cl6)和一种氧化物(有毒气体),还有少量副产物CCL4;
Ⅲ.相关物质的熔沸点如表:
(1)TiCl4摩尔质量大于FeCl3,但沸点却低于FeCl3的原因是_______ 。
(2)写出A中反应的化学方程式_______ ;上述装置存在一处缺陷,会导致TiCl4产率降低,改进的方法是_______ 。
(3)将管式炉加热至900℃时,瓷舟中主要反应的化学方程式为_______ 。
(4)装置E、F的作用为_______ 。
(5)设计实验测定纳米xTiO2•yH2O组成。
已知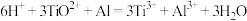 ,
,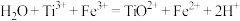
(可选试剂:水、稀硫酸、稀硝酸、氢氧化钠溶液、Al粉、0.1000 的NH4Fe(SO4)2标准溶液、硫氰化钾溶液、铁氰化钾溶液)
的NH4Fe(SO4)2标准溶液、硫氰化钾溶液、铁氰化钾溶液)
①取样称重:称取4.675g样品。②酸溶:用足量稀硫酸溶解。
③还原:加入过量Al粉还原至Al粉不再溶解,过滤取滤液定容。定容为500mL,取20.00mL。
④滴定:用0.1000 的NH4Fe(SO4)2标准溶液滴定,标准溶液装在
的NH4Fe(SO4)2标准溶液滴定,标准溶液装在_______ 滴定管(填“酸式”、“碱式”),用_______ 做指示剂,平均消耗标准溶液20.00mL,则xTiO2•yH2O的化学式为_______ 。

已知:
I. TiCl4高温时能与O2反应,极易水解,能溶于CCl4;
Ⅱ.瓷舟中主反应生成TiCl4、FeCl3(容易二聚成Fe2Cl6)和一种氧化物(有毒气体),还有少量副产物CCL4;
Ⅲ.相关物质的熔沸点如表:
TiCl4 | FeCl3 | CCl4 | |
熔点/℃ |
| 306 |
|
沸点/℃ | 136.4 | 315 | 76.8 |
(1)TiCl4摩尔质量大于FeCl3,但沸点却低于FeCl3的原因是
(2)写出A中反应的化学方程式
(3)将管式炉加热至900℃时,瓷舟中主要反应的化学方程式为
(4)装置E、F的作用为
(5)设计实验测定纳米xTiO2•yH2O组成。
已知
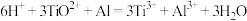 ,
,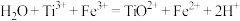
(可选试剂:水、稀硫酸、稀硝酸、氢氧化钠溶液、Al粉、0.1000
 的NH4Fe(SO4)2标准溶液、硫氰化钾溶液、铁氰化钾溶液)
的NH4Fe(SO4)2标准溶液、硫氰化钾溶液、铁氰化钾溶液)①取样称重:称取4.675g样品。②酸溶:用足量稀硫酸溶解。
③还原:加入过量Al粉还原至Al粉不再溶解,过滤取滤液定容。定容为500mL,取20.00mL。
④滴定:用0.1000
 的NH4Fe(SO4)2标准溶液滴定,标准溶液装在
的NH4Fe(SO4)2标准溶液滴定,标准溶液装在
您最近一年使用:0次
2024-02-19更新
|
921次组卷
|
3卷引用:湖南省株洲市第一中学2021届高三下学期第二次模拟检测化学试题
湖南省株洲市第一中学2021届高三下学期第二次模拟检测化学试题(已下线)2024届广东省华南师范大学附属中学 广雅中学 深圳中学 广东实验中学高三上学期四校联考化学试题广东省云浮市云安区云安中学2023-2024学年高三下学期3月考试化学试题
名校
解题方法
6 . NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等。已知:饱和NaClO2溶液在温度低于38℃时析出NaCO2•3H2O晶体,温度高于38℃时析出NaClO2晶体,温度高于60℃时,NaClO2分解生成NaClO3和NaCl。其生产工艺如图所示。
(1)NaClO2中氯元素的化合价为___________ 。
(2)“反应I”中氧化剂与还原剂的物质的量之比为___________ 。
(3)“反应Ⅱ”的离子方程式为___________ 。
(4)“反应”所用“食盐水”由粗盐水精制而成。精制时,为除去粗盐水中的Ca2+、Mg2+和 ,需要用到试剂:①NaOH溶液②Na2CO3溶液③BaCl2溶液④稀盐酸,所用试剂的加入顺序正确的是___________。(填标号)
,需要用到试剂:①NaOH溶液②Na2CO3溶液③BaCl2溶液④稀盐酸,所用试剂的加入顺序正确的是___________。(填标号)
(5)“一系列操作”为蒸发浓缩、趁热过滤、___________ 、干燥,其中“趁热过滤”应控制的温度范围是___________ 。
(6)“反应Ⅱ”产生的Cl2可用于制备含氯消毒剂。将Cl2通入足量NaOH溶液中,加热后得到NaCl、NaClO、NaClO3的混合液。经测定ClO-与 的物质的量浓度之比为3∶1,则Cl2与NaOH溶液反应时,被氧化的氯元素与被还原的氯元素的物质的量之比为
的物质的量浓度之比为3∶1,则Cl2与NaOH溶液反应时,被氧化的氯元素与被还原的氯元素的物质的量之比为___________ 。
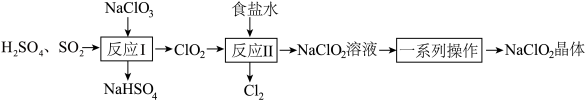
(1)NaClO2中氯元素的化合价为
(2)“反应I”中氧化剂与还原剂的物质的量之比为
(3)“反应Ⅱ”的离子方程式为
(4)“反应”所用“食盐水”由粗盐水精制而成。精制时,为除去粗盐水中的Ca2+、Mg2+和
 ,需要用到试剂:①NaOH溶液②Na2CO3溶液③BaCl2溶液④稀盐酸,所用试剂的加入顺序正确的是___________。(填标号)
,需要用到试剂:①NaOH溶液②Na2CO3溶液③BaCl2溶液④稀盐酸,所用试剂的加入顺序正确的是___________。(填标号)| A.①②③④ | B.②①③④ | C.③①②④ | D.③②①④ |
(5)“一系列操作”为蒸发浓缩、趁热过滤、
(6)“反应Ⅱ”产生的Cl2可用于制备含氯消毒剂。将Cl2通入足量NaOH溶液中,加热后得到NaCl、NaClO、NaClO3的混合液。经测定ClO-与
 的物质的量浓度之比为3∶1,则Cl2与NaOH溶液反应时,被氧化的氯元素与被还原的氯元素的物质的量之比为
的物质的量浓度之比为3∶1,则Cl2与NaOH溶液反应时,被氧化的氯元素与被还原的氯元素的物质的量之比为
您最近一年使用:0次
2024-02-11更新
|
628次组卷
|
6卷引用:湖南省宁乡市第一高级中学2021届高三第三次模拟考试化学试卷
名校
解题方法
7 . 下列装置与对应操作正确的是
 |  | 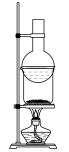 |  |
A.析出 晶体 晶体 | B.分离苯酚和水的混合物 | C.碘晶体(含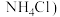 | D.测定 溶液的浓度 溶液的浓度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-10更新
|
449次组卷
|
3卷引用:湖南省宁乡市第一高级中学2021届高三第二次模拟考试化学试卷
名校
8 . 阿司匹林片的有效成分是乙酰水杨酸,辅助成分是淀粉。某实验小组设计实验方案如下:
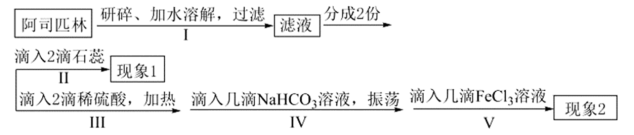
| A.操作Ⅰ研碎的目的为了增大接触面积,加快乙酰水杨酸的溶解 |
| B.操作Ⅱ可观察到溶液显红色,操作Ⅴ可观察到溶液显紫色 |
C.操作Ⅲ目的为了加快酯基的水解,可用足量 溶液替代,仍可显色 溶液替代,仍可显色 |
| D.操作Ⅳ为了中和过量硫酸,否则溶液酸性过强不易显色 |
您最近一年使用:0次
2024-02-03更新
|
297次组卷
|
4卷引用:湖南省长沙市宁乡市第一高级中学2021届高三新高考第一次模拟考试化学试卷
湖南省长沙市宁乡市第一高级中学2021届高三新高考第一次模拟考试化学试卷 浙江省义乌中学2024届高三上学期首考适应性考试化学试题(已下线)压轴题03 物质的制备检验分离与提纯(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)(已下线)选择题6-10
名校
解题方法
9 . 工业上常用碱性 废液吸收
废液吸收 ,反应原理为
,反应原理为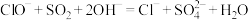 ,部分催化过程如图所示。下列说法正确的是
,部分催化过程如图所示。下列说法正确的是
 废液吸收
废液吸收 ,反应原理为
,反应原理为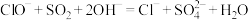 ,部分催化过程如图所示。下列说法正确的是
,部分催化过程如图所示。下列说法正确的是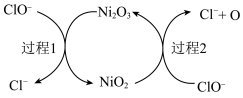
A.“过程1”中氧化产物与还原产物的物质的量之比为 |
B.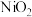 是该反应的催化剂 是该反应的催化剂 |
C.“过程2”可表示为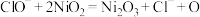 |
D.吸收过程中存在反应: |
您最近一年使用:0次
2024-02-03更新
|
516次组卷
|
4卷引用:湖南省宁乡市第一高级中学2021届高三第三次模拟考试化学试卷
湖南省宁乡市第一高级中学2021届高三第三次模拟考试化学试卷 浙江省义乌中学2024届高三上学期首考适应性考试化学试题(已下线)热点05 氧化还原反应的概念、规律、配平及计算(已下线)压轴题02 氧化还原反应的概念及规律(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)
名校
10 . 有机物M是一种用于治疗脑血管意外后遗症的药物。下列路线可用于合成该有机物,回答下列问题。 (乙酸酐)
(乙酸酐)
(1)B的化学名称为___________ 。
(2)I的结构简式为___________ ;F→H的反应类型为___________ 。
(3)F中含氧官能团的名称为___________ 。
(4)K→M的化学方程式为___________ 。
(5)符合下列条件D的同分异构体有___________ 种(不考虑立体异构)。
①属于芳香族化合物;②含有硝基;③含有手性碳原子。
(6)参照上述信息,写出以苯酚、1—溴丙烷为原料合成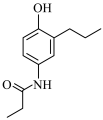 的路线
的路线_____ 。
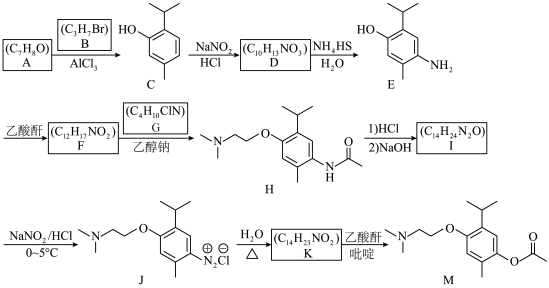
 (乙酸酐)
(乙酸酐)(1)B的化学名称为
(2)I的结构简式为
(3)F中含氧官能团的名称为
(4)K→M的化学方程式为
(5)符合下列条件D的同分异构体有
①属于芳香族化合物;②含有硝基;③含有手性碳原子。
(6)参照上述信息,写出以苯酚、1—溴丙烷为原料合成
 的路线
的路线
您最近一年使用:0次
2024-02-02更新
|
472次组卷
|
5卷引用:湖南省宁乡市第一高级中学2021届高三第三次模拟考试化学试卷

 23.2
23.2

